| SPECT/CT融合显像评价下肢骨折远期愈合的初步探讨 |
下肢骨折在临床上常见,大部分骨折根据临床标准可判断其愈合情况,但骨折的损伤修复受多种原因影响,部分骨折患者具有远期愈合的可能。X线、CT由于自身的局限性[1],无法判断骨折是否具有远期愈合的可能。SPECT/CT融合显像不仅能显示骨折部位的磷酸盐代谢情况、成骨细胞活跃程度及血液供应情况,还能显示骨折部位的解剖学影像[2]。本研究旨在探讨SPECT/CT融合显像对下肢骨折远期愈合能力的诊断价值。
1 资料与方法 1.1 一般资料收集2015年1月至2020年12月在我院接受治疗的下肢骨折患者59例,其中男39例,女20例;年龄11~74岁,平均(37.8±15.1)岁。骨折部位包括胫骨25例、股骨干17例、股骨颈9例、腓骨6例、髂骨2例。46例行手术治疗(39例钢板或髓内钉内固定,7例支架外固定);13例行非手术保守治疗。治疗后6~12个月行X线或CT检查显示骨折线清晰、骨折端无连续或少量骨痂。
1.2 仪器与方法采用Siemens Synbia-T6双探头SPECT/CT图像融合显像仪,配低能高分辨平行孔准直器和6层螺旋CT。钼-锝发生器由北京原子高科股份有限公司提供,MDP由江苏省原子医学研究所江原制药厂生产。扫描前2.5 h静脉注射99mTc-MDP 20~25 mCi,先对骨折部位行SPECT断层扫描,采集能峰140 keV,窗宽20%,矩阵128×128,放大倍数1,探头旋转轨迹为自动人体轨迹,360°采集,双探头各旋转180°,每旋转60°采集1帧图片,每帧采集时间为20 s,连续采集30帧;扫描完毕嘱患者保持体位不动,行CT扫描,110 keV,150 mA,层厚1 mm,螺距1,矩阵512×512。采用SPECT/CT Symbia True point自带软件进行图像融合。59例随访6~12个月,最终结果经手术或随访证实。
1.3 图像分析由2名高年资放射科医师和1名核医学医师共同阅片,意见分歧时经协商达成一致。分析SPECT骨显像、CT解剖图像及SPECT/CT融合图像,包括放射性浓聚、骨痂形成、骨质改变情况。
1.4 诊断标准① 骨折愈合的诊断标准:放射性核素聚集通过骨折线或跨越骨折两端,则处于愈合进程中,具有远期愈合的可能;反之则为骨折不愈合。②手术判断骨折不愈合标准:术中见骨折端存在异常活动,无连续骨痂形成,骨折端骨质硬化或明显骨吸收、缺损。③临床随访判断标准:X线或CT检查见骨折线模糊、骨折端有连续通过骨折线的新生骨痂形成为骨折愈合;骨折线清晰、骨折端未见连续通过骨折线的新生骨痂为骨折不愈合。
2 结果59例SPECT图像均可见骨折部位的放射性核素浓聚,但核素浓聚的准确部位和损伤程度无法判断。CT示35例骨折端周围可见少量骨痂形成,骨痂通过骨折线21例;24例骨折部位无骨痂形成,13例骨折部位无明显骨质吸收和硬化,8例部分骨质吸收硬化,3例骨密度减低。SPECT/CT融合显像示51例骨折部位放射性核素聚集连续性通过骨折线包含骨折两端(图 1,2),表明骨折具有远期愈合的可能,正处于骨折愈合期;其中44例随访X线片示骨折端有连续性骨痂通过骨折线,余7例手术治疗后X线未见明显骨痂形成,需再次手术治疗。8例SPECT/CT融合现象示骨折线无放射性核素聚集的连续通过(图 3),表明骨折不愈合,远期愈合的可能性不大;手术治疗中观察无骨痂形成且骨折端骨质明显硬化吸收,诊断为骨折不愈合。SPECT/CT融合显像判断骨折愈合的准确率为88.1%(52/59)。
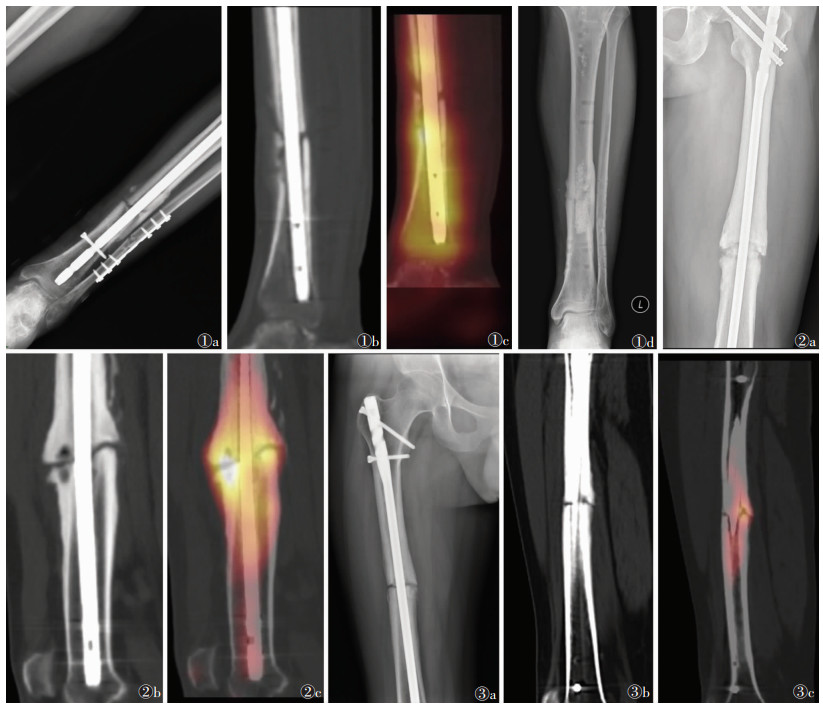 |
| 图 1 男,49岁,左胫骨下端粉碎性骨折术后 图 1a,1b 术后9个月X线正位片与CT冠状位MPR图像示骨折线清晰,无明显骨痂生成,提示骨折不愈合 图 1c SPECT/CT融合图像示连续性放射性核素通过骨折线并跨越两端,提示骨折具有远期愈合可能 图 1d 术后15个月胫骨X线正位片显示骨折线模糊,大量骨痂生成包围骨折部位,骨折愈合 图 2 男,47岁,左股骨中下段骨折术后 图 2a,2b 术后7个月X线正位片与CT冠状位MPR图像,可见骨折线清晰,骨折端骨质硬化,无明显骨痂形成,提示骨折不愈合 图 2c SPECT/CT融合显像显示放射性核素聚集,跨越骨折两端,提示具有远期愈合可能,后经临床随访证实骨折愈合 图 3 男,24岁,右股骨中端骨折术后 图 3a,3b 术后6个月X线正位片与CT冠状位MPR图像示骨折线清晰,无骨痂形成,骨折延迟愈合 图 3c SPECT/CT融合显像显示右股骨中段折端内后侧见片状明显放射性核素浓聚,其外侧放射性核素浓聚不明显,骨折远段髓内钉周围轻度放射性核素浓聚,提示骨折愈合不佳,后经二次手术证实骨折不愈合 |
3 讨论
无论是治疗方案的选择、患者内固定物的取出时间,以及是否需二次手术,还是患者功能锻炼的方式、时间,均与骨折愈合情况密切相关[3-5]。目前为止,临床判断骨折是否愈合多依靠X线或CT。X线或CT示骨折线模糊,骨折周围有连续性骨痂形成,则判断骨折可愈合;对于不符合上述诊断标准的患者无法准确判断愈合情况。对于无骨痂形成或仅少量骨痂形成的骨折患者,选择二次手术还是继续保守治疗较困难。X线与CT对骨折的诊断也有局限性,骨骼骨矿含量达到一定的程度才能分辨出是否有骨痂形成[6];当仅有少量骨痂形成时,可能漏诊。
SPECT骨显像需静脉注射99mTc-MDP,参与全身骨骼的代谢[7]。当存在骨质破坏时,病变区的血供、无机盐的代谢,以及成骨细胞的活跃程度均发生改变[8]。这时,骨折部位对99mTc-MDP的摄取量增加[9],当有连续性骨痂通过骨折线时,可见连续性放射性核素聚集通过骨折线。对比X线、CT,SPECT可较早发现骨质破坏,且准确率与敏感度高[10-11]。但SPECT显像空间分辨力较差,当患者存在创伤、炎症及一些骨代谢疾病时可能影响显像剂的分布。在骨折修复的过程中,骨折部位的一系列生理病理变化均表现为放射性核素浓聚,因此特异度较低。本研究中59例SPECT骨显像均表现为核素浓聚,但无法判断是否有连续性放射性核素聚集通过骨折线。
SPECT/CT融合显像集合了SPECT骨显像与CT图像优点,不仅在早期可发现病变部位的生理代谢变化,还可提供高分辨力的解剖图像,清楚显示骨折处放射性核素聚集的程度与范围[12]。当骨折部位有连续性放射性核素聚集通过骨折线时,即使无骨痂形成,也表明骨折处于损伤修复的阶段,具有远期愈合的可能。当骨折部位无连续性放射性核素聚集通过骨折线时,则表明该骨折处的血供、骨代谢及成骨细胞活跃度均很缺乏,无法完成完整骨折愈合,需再次手术干预。本研究59例中,SPECT/CT融合显像检查51例均具有远期愈合的可能,后经临床随访证实;8例不具有远期愈合能力,后经再次手术证实。SPECT/CT融合显像评价骨折远期愈合的准确率为88.1%(52/59)。
行SPECT/CT融合显像时的注意事项:①应尽量考虑影响诊断结果的因素,降低假阳性出现的概率;②SPECT/CT无法完全诊断骨折远期愈合,当有连续性放射核素聚集通过骨折线时,不表示一定能够愈合,只是具备远期愈合的基础条件。最终骨折能否愈合受多种因素的影响,治疗过程中应密切观察,定期随访才能保证治疗效果[13]。
综上所述,SPECT/CT融合显像集功能影像与解剖影像优势,虽然具有一定的局限性,但能为评价骨折远期愈合能力提供有效依据,具有重要的临床价值。
| [1] |
PRANDINI N, LAZZERI E, ROSSI B, et al. Nuclear medicine imaging of bone infections[J]. Nucl Med Commun, 2006, 27(8): 633-644. DOI:10.1097/00006231-200608000-00006 |
| [2] |
MOTOMURA G, YAMAMOTO T, KARASUYAMA K, et al. Bone SPECT/CT of femoral head subchondral insufficiency fracture[J]. Clin Nucl Med, 2015, 40(9): 752-754. DOI:10.1097/RLU.0000000000000886 |
| [3] |
EINHORN T A. New technologies for the enhancement of skeletal repair[J]. Injury Extra, 2009, 40(10): 195-198. |
| [4] |
TAORMINA D P, SHULMAN B S, KARIA R, et al. Older age does not affect healing time and functional outcomes after fracture nonunion surgery[J]. Geriatr Orthop Surg Rehabil, 2014, 5(3): 116-121. DOI:10.1177/2151458514532811 |
| [5] |
周本根, 罗筱玮. 两种植骨法治疗肱骨干骨折不愈合疗效的比较[J]. 实用医学杂志, 2016, 32(15): 2535-2538. |
| [6] |
张斌青, 宋青凤, 王军辉, 等. SPECT/CT显像对骨折延迟愈合的诊断价值[J]. 中华核医学与分子影像杂志, 2014, 34(4): 305-307. |
| [7] |
HIRSCHMANN M T, DAVDA K, RASCH H, et al. Clinical value of combined single photon emission computerized tomography and conventional computer tomography (SPECT/CT) in sports medicine[J]. Sports Med Arthrosc Rev, 2011, 19(2): 174-181. DOI:10.1097/JSA.0b013e3181ec8707 |
| [8] |
SARIKAYA I, SARIKAYA A, HOLDER L E. The role of single photon emission computed tomography in bone imaging[J]. Semin Nucl Med, 2001, 31(1): 3-16. |
| [9] |
CHICKLORE S, GNANASEGARAN G, VIJAYANATHAN S, et al. Potential role of multislice SPECT/CT in impingement syndrome and soft-tissue pathology of the ankle and foot[J]. Nucl Med Commun, 2013, 34(2): 130-139. DOI:10.1097/MNM.0b013e32835c0964 |
| [10] |
HAMANN M, ALDRIDGE M, DICKSON J, et al. Evaluation of a lowdose slow-rotating SPECT/CT system[J]. Phys Med Biol, 2008, 53(10): 2495-2508. DOI:10.1088/0031-9155/53/10/003 |
| [11] |
ZHAO Z, LI L, LI F, et al. Single photon emission computed tomography/spiral computed tomography fusion imaging for the diagnosis of bone metastasis in patients with known cancer[J]. Skeletal Radiol, 2010, 39(2): 147-153. DOI:10.1007/s00256-009-0764-0 |
| [12] |
AL-FAHAM Z, RYDBERG J N, OLIVER W. Use of SPECT/CT with 99mTc-MDP bone scintigraphy to diagnose sacral insufficiency fracture[J]. J Nucl Med Technol, 2014, 42(3): 240-241. DOI:10.2967/jnmt.114.137547 |
| [13] |
曹克勇, 方彩莲, 叶积飞. 不同强度的早期负重对股骨干骨折愈合的影响[J]. 中国康复, 2014, 29(6): 458-459. |
 2022, Vol. 20
2022, Vol. 20


