| 二维斑点追踪成像对术前左室射血分数正常的重度二尖瓣反流患者左室长轴纵向心肌分层应变的评价 |
部分重度二尖瓣反流患者能长时间承受大量反流容量而无明显临床症状,这是因其早期代偿期左室射血分数(left ventricular ejection fraction,LVEF)受容量负荷的影响维持在正常范围内,掩盖了术前受损的心功能,一旦通过手术解除过重的容量负荷,术前隐匿的左室收缩功能减低就会表现出来,有些患者甚至出现心衰,严重影响生活质量和远期生存率。而早期发现心肌损伤、及时手术能改善重度二尖瓣反流患者的临床转归。目前,国际上关于重度二尖瓣反流患者的手术指征均参考常规超声测值指标,即LVEF<60%和/或左心室收缩末期内径(left ventricular internal diameter at end-systole,LVIDs)≥40 mm[1],但该指标忽略了心室壁不同心肌层对心脏收缩功能影响的差异性。研究[2]表明,部分LVEF>60%且LVIDs<40 mm的患者,术后左室收缩功能亦降低。因此,早期发现重度二尖瓣反流患者术前左室功能障碍且行手术治疗,有利于术后左室功能的恢复和远期生存率的提高[3]。目前,应用二维斑点追踪成像技术(two-dimensional speckle tracking echocardiography,2D-STI)能早期检出术前已出现的亚临床左室收缩功能受损的重度二尖瓣反流患者[4-6]。本研究旨在应用2D-STI,评估LVEF正常的重度二尖瓣反流患者术前左心室长轴的纵向心肌分层应变,分析其左心室心肌有无受累及受累程度,为临床选择治疗方法提供参考。
1 资料与方法 1.1 一般资料选取2018年1月至2019年11月我院诊断为重度二尖瓣反流且准备择期行手术治疗的患者30例。诊断标准:根据指南[7]中二尖瓣反流程度分级的特异性,当有以下表现时诊断为重度二尖瓣反流,即反流颈宽度≥0.7 cm且呈大的中心性反流束(反流束面积>左房面积40%)或偏心性反流束在左房内形成涡流;大量血流汇聚;肺静脉收缩期血流反向;明显的腱索或乳头肌断裂。患者术前平均LVEF(60.60±3.62)%。依据术后1个月内复查LVEF是否出现左室收缩功能降低将30例分为A组(LVEF≥50%)18例和B组(LVEF<50%)12例。A组男6例,女12例;年龄9~67岁,平均(42.83±16.51)岁。B组男6例,女6例;年龄39~66岁,平均(49.92±8.67)岁。排除标准:术前左心室收缩功能降低、冠状动脉粥样硬化性心脏病、高血压性心脏病、先天性心脏病、心房颤动或出现频发早搏、常规超声心动图和心电图检查无明显异常、其他严重瓣膜病或二尖瓣轻度以上狭窄及心肌病等。
对照组选择年龄及性别与重度二尖瓣反流组相匹配的健康志愿者30例,其中男15例,女15例;年龄26~60岁,平均(44.37±8.40)岁。
1.2 仪器与方法3组均行超声心动图。选取GE Vivid E9超声诊断仪,M5S探头,频率1.5~4.5 MHz,帧频≥40帧/s。连接心电图后,嘱受试者取左侧卧位,在胸骨旁左心室长轴切面测量左心房收缩末期内径(left atrial end systolic diameter,LAD)、左心室舒张末期内径(left ventricular internal diameter at end-diastole,LVIDd)、LVIDs,用双平面Simpson法测量LVEF。存储左室心尖长轴切面至少连续3个心动周期原始二维动态图像,后期导入GE EchoPAC超声工作站进行脱机分析,分别测量3组心尖四腔、心尖两腔及心尖左室长轴水平左室分层应变值。所有图像由2位医师分别进行分析。
1.3 统计学方法使用SPSS 22.0统计软件进行数据分析。3组数据满足正态性检验和方差齐性检验,行单因素方差分析,以P<0.05为差异有统计学意义。2位医师一致性检验采用Bland-Altman统计分析图。
2 结果 2.1 3组超声心动图常规参数比较(表 1)| 表 1 3组超声心动图常规参数比较(x±s) |
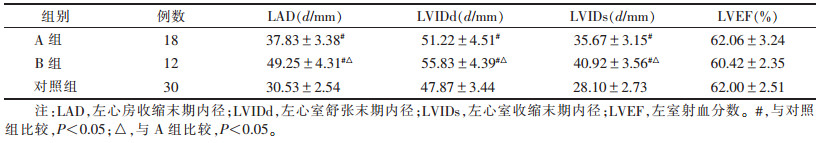 |
A、B组LAD、LVIDd及LVIDs较对照组均升高(均P<0.05);B组LAD、LVIDd及LVIDs较A组均升高(均P<0.05);3组间LVEF比较差异无统计学意义(P>0.05)。
2.2 3组左心室长轴纵向心肌分层应变值比较(表 2)| 表 2 3组左心室长轴纵向心肌分层应变值比较(%,x±s) |
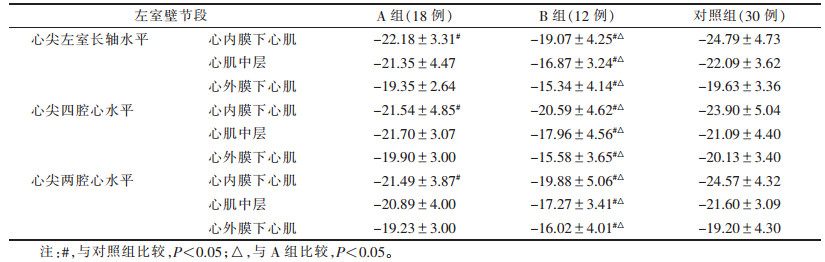 |
对照组及B组各心肌分层应变值/绝对值呈梯度特征,心内膜下心肌最高、中层心肌次之、心外膜下心肌最低。A组较对照组仅心内膜下心肌分层应变绝对值差异有统计学意义(P<0.05)。B组较对照组和A组心内膜下心肌、中层心肌、心外膜下心肌分层应变绝对值均降低(均P<0.05)(图 1,2)。
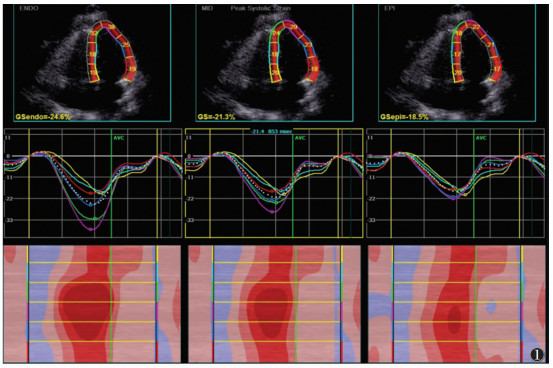 |
| 图 1 女,45岁,正常对照组。心尖四腔心切面心内膜下心肌、中层心肌、心外膜下心肌纵向收缩期峰值应变 |
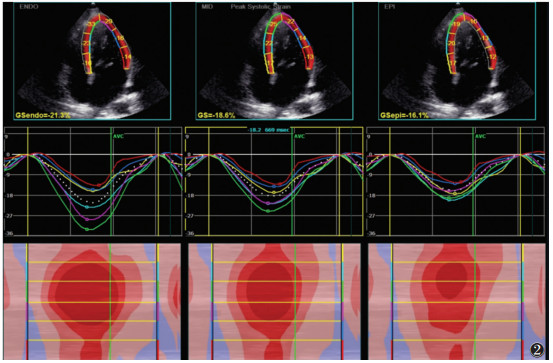 |
| 图 2 女,44岁,B组患者。心尖四腔心切面心内膜下心肌、中层心肌、心外膜下心肌纵向收缩期峰值应变,较正常对照组均降低 |
2.3 2位医师的一致性检验结果
Bland-Altman统计分析图显示,2位医师分析心内膜下、心肌中层、心外膜下心肌纵向应变平均偏倚分别是-0.23、0.01、0.14,95%置信区间(95%CI)分别是(-1.62,1.17)、(-1.26,1.28)、(-1.12,1.39),说明心肌各层纵向应变参数重复性较好(图 3~5)。
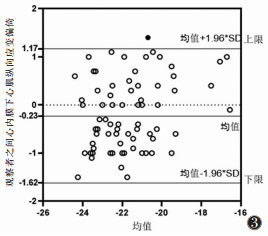 |
| 图 3 2位医师分析心内膜下心肌纵向应变的Bland-Altman统计分析图 |
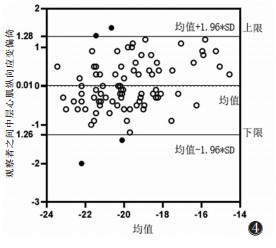 |
| 图 4 2位医师分析中层心肌纵向应变的Bland-Altman统计分析图 |
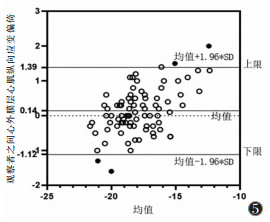 |
| 图 5 2位医师分析心外膜下心肌纵向应变的Bland-Altman统计分析图 |
3 讨论
某些疾病可能仅影响心肌壁的某一部分,或不同心肌层表现有所差异[8]。既往研究[9-10]多将左室心肌作为整体分析,忽视了左室心肌是复杂的多层非同质结构,因而无法切实反映重度二尖瓣反流对左室壁不同心肌层的影响。2D-STI技术可定量分析左室长轴和短轴方向的功能[11-12],测量纵向及环向分层应变值,能更加客观地评价心肌有无受累及受累程度[13]。研究[14]表明,左室长轴纵向应变值的临床诊断价值较左室短轴环向和径向应变值的诊断价值高。目前已有专家推荐将左室长轴应变指标加入临床应用指南[15]。
本研究结果显示,重度二尖瓣反流患者的LAD、LVIDd、LVIDs值均较对照组升高,且B组较A组升高更明显,差异均有统计学意义(均P<0.05)。这是由于重度二尖瓣反流患者因长期承受过重的容量负荷,左心为适应过重的容量负荷而代偿性增加,导致左心扩大及结构重塑;B组左心房、左心室较A组扩大更明显,可能原因是B组患者较A组患者处于疾病发生发展的更晚期阶段,受容量负荷影响的时间更长。本研究重度二尖瓣反流患者术前LVEF值均在正常范围内,这是由于左心室通过收缩末期将血液反流入低阻力的左心房,从而减小左室收缩末容积、使LVEF仍能维持在正常范围内。
本研究对照组左室长轴的分层应变值遵循一定规律:心内膜下心肌的收缩性最强,中层心肌次之,心外膜下心肌最弱,与既往研究[16-17]结果一致。本研究二尖瓣反流患者与对照组左室长轴分层应变值差异有统计学意义,表现为:A组较对照组心内膜下心肌分层应变绝对值降低(均P<0.05),B组较对照组和A组心内膜下心肌、中层心肌、心外膜下心肌应变绝对值均降低(均P<0.05)。说明在患者出现临床症状之前,重度二尖瓣反流患者左室心肌已出现不同程度损伤,LVEF是依靠左室射血能力评价左室心肌功能,而非心肌自身的功能。因此,仅依靠LVEF无法真实反映术前左室心肌功能状态,易将部分术前已出现心肌功能受损患者误诊为正常。本研究中重度二尖瓣反流患者,因受容量负荷影响,LVEF已无法准确反映左室收缩功能状态。2D-STI受容量负荷的影响较小,能早期发现重度二尖瓣反流患者术前左室收缩功能隐匿性降低[4-6]。
国内外研究对评价重度二尖瓣反流患者左室分层应变的报道少见,目前已有研究多是应用2D-STI评价重度二尖瓣反流患者左室整体纵向应变,但左室整体纵向应变值的正常值因受心肌测量位置、厂家及分析软件不同的影响,在文献报道[18-19]中差异较大。整体纵向应变值的正常值需大样本研究才能建立,目前认为纵向应变值在-20%左右视为正常,绝对值低于此值视为异常[20],但对于左室纵向分层应变还无确定的正常参考值。DE ISLA等[9]应用2D-STI评价慢性重度二尖瓣反流患者左室整体纵向应变值,结果表明该类患者术前在心功能正常时左心室整体纵向应变绝对值较正常对照组降低,且此指标比其他评估左室收缩功能的方法更准确。KIM等[10]发现,重度二尖瓣反流患者的左室短轴和长轴整体应变绝对值均较正常对照组降低,且长轴方向纵向应变绝对值的降低较径向应变值早。本研究结果与上述研究一致,A组和B组纵向应变绝对值均降低,心肌出现不同程度的损伤。重度二尖瓣反流患者左室心内膜下心肌受容量负荷影响应力最大,最易先发生损伤,中层、外膜层在病程较晚期阶段,才出现损伤。本研究中A组心肌损伤程度较轻,仅累及心内膜下心肌,术后心肌功能恢复尚可,而B组心肌损害程度较重,已累及心肌全层,术后心肌收缩功能恢复较差,出现左室收缩功能降低(LVEF<50%),故应尽早确诊并进行手术干预,最大限度地保护患者左室心肌功能。
本研究的局限性:仅从左室长轴纵向分层应变角度去分析重度二尖瓣反流患者术前心肌功能状态,未能从左室短轴的圆周、径向应变及扭转运动方面综合评估左室心肌功能情况。
综上所述,以LVEF评价重度二尖瓣反流患者左室心肌功能将被高估,而2D-STI通过评价心肌分层应变可定量评估术前LVEF正常的重度二尖瓣反流患者术前左心室心肌是否受累及受累程度,对指导临床选择合适的手术时机有一定意义。
| [1] |
NISHIMURA R A, OTTO C M, BONOW R O, et al. 2017 AHA/ACC focused update of the 2014 AHA/ACC guideline for the management of patients with valvular heart disease. a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines[J]. Circulation, 2017, 135(25): e1159-e1195. |
| [2] |
陈辉, 苏茂龙. 二维斑点追踪技术对二尖瓣反流术后左心室收缩功能改变的预测研究[J]. 中华超声影像学杂志, 2019, 28(6): 487-492. |
| [3] |
LING L H, ENRIQUEZ-SARANO M, SEWARD J B, et al. Early surgery in patients with mitral regurgitation due to flail leaflets:a long-term outcome study[J]. Circulation, 1997, 96: 1819-1825. DOI:10.1161/01.CIR.96.6.1819 |
| [4] |
王晓冰, 杨军, 陈昕, 等. 左心室纵向应变预测原发性二尖瓣反流术后左心室收缩功能减低[J]. 中国医科大学学报, 2017, 46(4): 353-356. |
| [5] |
WITKOWSKI T G, THOMAS J D, DEBONNAIRE P J, et al. Global longitudinal strain predicts left ventricular dysfunction after mitral valve repair[J]. Eur Heart J Cardiovasc Imaging, 2013, 14(1): 69-76. DOI:10.1093/ehjci/jes155 |
| [6] |
CHO E J, PARK S J, YUN H R, et al. Predicting left ventricular dysfunction after surgery in patients with chronic mitral regurgitation:assessment of myocardial deformation by 2-dimensional multilayer speckle tracking echocardiography[J]. Korean Circ J, 2016, 46(2): 213-221. DOI:10.4070/kcj.2016.46.2.213 |
| [7] |
CHEITLIN M D, ARMSTRONG W F. ACC/AHA/ASE 2003 guideline update for the clinical application of echocardiography:summary article. a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (ACC/AHA/ASE Committee to Update the 1997 Guidelines for the Clinical Application of Echocardiography)[J]. J Am Soc Echocardiogr, 2003, 16(10): 1091-1100. |
| [8] |
温晓娜, 武俊, 李洁明, 等. 二维斑点追踪技术评价主动脉瓣狭窄围手术期左室心肌分层应变[J]. 中国超声医学杂志, 2019, 35(6): 566-569. |
| [9] |
DE ISLA L P, AGUSTIN A, RODRIGO J L, et al. Chronic mitral regurgitation:a pilot study to assess preoperative left ventricular contractile function using speckle-tracking echocardiography[J]. J Am Soc Echocardiogr, 2009, 22(7): 831-838. DOI:10.1016/j.echo.2009.04.016 |
| [10] |
KIM M S, KIM Y J, KIM H K, et al. Evaluation of left ven tricular short-and long-axis function in severe mitral regurgita tion using 2-dimensional strain echocardiography[J]. Am Heart J, 2009, 157(2): 345-351. |
| [11] |
常荷.二维斑点追踪技术评价腹膜透析前后尿毒症患者左室心肌收缩功能[D].太原: 山西医科大学, 2016.
|
| [12] |
杨勇, 吕秀花, 王臻, 等. 二维斑点追踪技术在评价糖尿病患者左心室整体与节段长轴收缩功能[J]. 中国超声医学杂志, 2015, 31(3): 218-220. |
| [13] |
黄冬梅, 崔洪岩, 夏稻子, 等. 超声斑点追踪技术评价尿毒症患者左室心肌分层应变[J]. 中国超声医学杂志, 2016, 32(2): 143146. |
| [14] |
SCHWARZ K, AHEARN T, SRINIVASAN J, et al. Alterations in cardiac deformation, timing of contraction and relaxation, and early myocardial fibrosis accompany the apparent recovery of acute stress-induced (takotsubo) cardiomyopathy:an end to the concept of transience[J]. J Am Soc Echocardiogr, 2017, 30(8): 745-755. DOI:10.1016/j.echo.2017.03.016 |
| [15] |
HAUGAA K H, DEJGAARD L A. Global longitudinal strain:ready for clinical use and guideline implementation[J]. Am Coll Cardiol, 2018, 71(18): 1958-1959. DOI:10.1016/j.jacc.2018.03.015 |
| [16] |
邢雨蒙, 史静, 等. 二维斑点追踪成像技术评价冠状动脉慢血流患者左室心肌分层应变[J]. 复旦学报(医学版), 2018, 45(4): 467-472. |
| [17] |
SHI J, PAN C, et al. Left ventricular longitudinal and circum ferential layer-specific myocardial strains and their determinants in healthy subjects[J]. Echocardiography, 2016, 33(4): 510-518. |
| [18] |
KOCABAY G, MURARU D, PELUSO D, et al. Normal left ven tricular mechanics by two-dimensional speckle-tracking echo cardiography. Reference values in healthy adults[J]. Rev Esp Cardiol(Engl Ed), 2014, 67(8): 651-658. DOI:10.1016/j.recesp.2013.12.011 |
| [19] |
YINGCHONCHAROEN T, AGARWAL S, POPOVIC Z B, et al. Normal ranges of left ventricular strain:a meta-analysis[J]. Am Soc Echocardiogr, 2013, 26(2): 185-191. DOI:10.1016/j.echo.2012.10.008 |
| [20] |
LANG R M, BADANO L P, MOR-AVI V A, et al. Recommenda tions for cardiac chamber quantification by echocardiography in adults:an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging[J]. Eur Heart J Cardiovasc Imaging, 2015, 16(3): 233-270. DOI:10.1093/ehjci/jev014 |
 2020, Vol. 18
2020, Vol. 18


