| 3.0 T MRI鉴别乳腺良恶性病变的最佳ADC阈值分析 |
乳腺癌是女性最常见的癌症,2018年全球女性乳腺癌发病率为4.6‰、死亡率为1.3‰[1]。我国女性乳腺癌发病人数、死亡人数居世界首位,且呈逐年上升趋势[2]。如何准确鉴别女性乳腺病变良恶性是影像学研究的热点和难点问题。
目前,MRI是鉴别乳腺良恶性病变最准确的影像学检查方法。DWI是MRI检查乳腺病变的最重要序列之一,ADC值可定量分析病变,更准确地鉴别乳腺良恶性病变,但不同厂家设备的ADC测量值存在一定差异[3]。收集我院2018年11月至2021年2月经病理证实的56例乳腺病变患者,分析3.0 T MRI鉴别良恶性病变的ADC阈值,以提高对乳腺良恶性病变的鉴别诊断水平。
1 资料与方法 1.1 一般资料56例(56个病变)均为女性,年龄29~87岁,平均(53.23±11.86)岁;其中良性病变18例(良性组),平均年龄(51.83±12.27)岁;乳腺癌38例(恶性组),平均年龄(53.89±11.76)岁。多为偶然发现,少数触及乳房肿块,大多无疼痛。纳入标准:临床或其他检查发现乳腺病变,未行放化疗或手术治疗,病灶实性部分可测量ADC值。
1.2 仪器与方法尽量选择月经后第1周检查。采用联影uMR 770型3.0 T超导MRI扫描仪,10通道乳腺专用线圈,患者取俯卧位。扫描序列与参数:轴位快速脂肪抑制T2WI序列,TI 230 ms,TR 3 259 ms,TE 62.16 ms,翻转角150°,带宽320 Hz,层厚4.5 mm,层距1.1 mm,视野340 mm×340 mm,矩阵456×456;轴位梯度回波DWI序列,b值取50、400、800 s/mm2,TR 4 600 ms,TE 83 ms,翻转角90°,带宽1 750 Hz,层厚4.5 mm,层距1.1 mm,视野190 mm×350 mm,矩阵104×192;轴位T1WI动态增强扫描序列,t1_quick3d_tra_fs,在1个平扫序列后,注射对比剂,同时开始连续6个序列扫描(7 min 24 s),TR 4.87 ms,TE 2.2 ms,翻转角10°,带宽400 Hz,层厚1.0 mm,视野340 mm×340 mm,矩阵316×352。对比剂为Gd-DTPA,剂量0.1 mmol/kg体质量,经手背静脉注射,流率2.0 mL/s,注射后追加20 mL生理盐水冲管。
1.3 ADC值测量选择病灶内实性部分最低扩散率或最黑区域,同时避开坏死、囊变、出血区域,获取病灶内实性部分最低ADC值。
1.4 统计学分析采用SPSS 23.0软件进行数据分析。采用独立t检验及箱式图分析良恶性病变的ADC值差异,采用ROC曲线及散点图分析最佳ADC阈值,应用Excel表计算约登指数。AUC取值范围为0.5~1.0,≤0.5表示无诊断效能,0.5<AUC≤0.7为诊断效能较低,0.7<AUC≤0.9为诊断效能中等,AUC > 0.9为诊断效能较高。
2 结果恶性组38例中,非浸润性癌4例,均为导管原位癌4例;浸润性癌34例,其中WHO Ⅰ级1例,WHO Ⅱ级12例(图 1),WHO Ⅲ级7例,未分级14例。良性组18例中,纤维腺瘤8例(图 2),腺病/增生6例,导管内乳头瘤3例,肌上皮瘤1例。
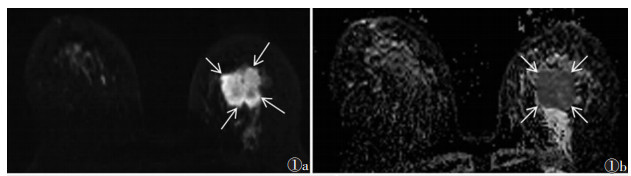 |
| 注:患者,女,68岁,病理结果为浸润性大汗腺乳腺癌,WHO Ⅱ级。图 1a为轴位DWI,示左乳腺中份肿块(白箭),呈高信号;图 1b为轴位ADC图,示左乳腺肿块呈低信号(白箭),ADC值为1.001×10-3 mm2/s 图 1 乳腺癌MRI图像 |
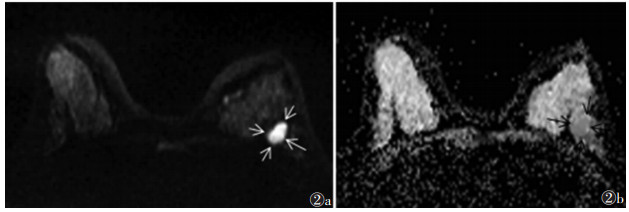 |
| 注:患者,女,46岁,病理结果为纤维腺瘤。图 2a为轴位DWI图,示左乳腺后份肿块(白箭),呈明显高信号,与T2穿透效应有关;图 2b为轴位ADC图,示左乳腺肿块呈等或稍低信号(黑箭),ADC值为1.475×10-3 mm2/s 图 2 纤维腺瘤MRI图像 |
恶性组ADC值为(0.471~1.307)×10-3 mm2/s,平均(0.914±0.196)×10-3 mm2/s;良性组ADC值为(1.010~2.098)×10-3 mm2/s,平均(1.480±0.312)×10-3 mm2/s;2组ADC值差异有统计学意义(t=-8.28,P<0.05)。箱式图示乳腺良恶性病变的ADC值有差异,同时存在少量重叠(图 3)。
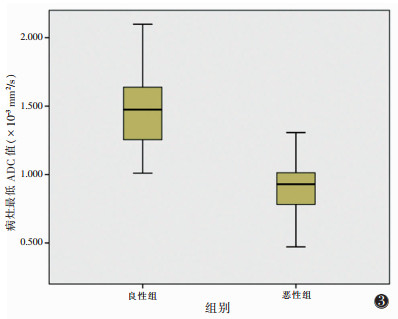 |
| 注:女性乳腺良恶性病变的ADC值有差异,同时存在少量重叠 图 3 女性乳腺良恶性病变ADC值箱式图 |
乳腺良恶性病变鉴别的最佳ADC阈值比较见表 1,AUC为0.954时鉴别乳腺良恶性病变具有较高诊断效能(图 4)。当ADC阈值为1.106×10-3 mm2/s时,约登指数为最大值(0.806),即敏感度与特异度之和最大,具有高特异度、高阳性似然比;当ADC阈值为1.253×10-3 mm2/s时,具有高敏感度、低阴性似然比。
| 表 1 乳腺良恶性病变鉴别的最佳ADC阈值比较 |
 |
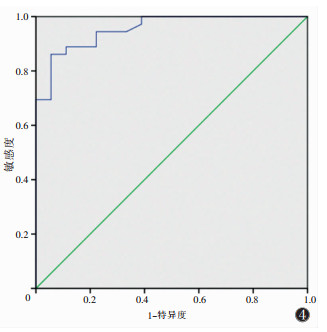 |
| 注:AUC为0.954时鉴别乳腺良恶性病变具有较高诊断效能 图 4 ADC值鉴别乳腺良恶性病变的ROC曲线 |
2组ADC值散点图见图 5,18例良性病变ADC值均 > 1.000×10-3 mm2/s;良恶性病变的ADC值在(1.010~1.307)×10-3 mm2/s之间存在重叠;以1.106×10-3 mm2/s为阈值,个别良性病变误诊为乳腺癌,少量乳腺癌漏诊;以1.253×10-3 mm2/s为阈值,个别乳腺癌漏诊,少量良性病变误诊为乳腺癌。
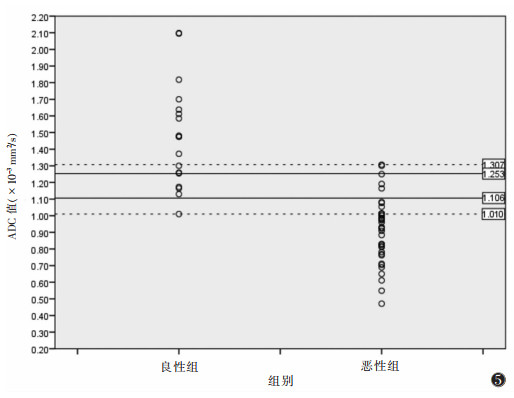 |
| 18例乳腺良性病变ADC值均大于1.000×10-3 mm2/s;乳腺良恶性病变的ADC值在(1.010~1.307)×10-3 mm2/s之间存在重叠(虚线所示);以1.106×10-3 mm2/s为阈值,个别良性病变误诊为乳腺癌,少量乳腺癌漏诊;以1.253×10-3 mm2/s为阈值,个别乳腺癌漏诊,少量良性病变误诊为乳腺癌 图 5 乳腺良恶性病变ADC值散点图 |
3 讨论 3.1 DWI及ADC值影响因素
DWI反映活体内水分子的扩散运动情况,常规DWI图像上可出现“T2穿透效应”或“黑化效应”,导致对水分子扩散情况误判。ADC图至少在2种b值基础上获得,能更真实地反映水分子扩散情况。通常情况下,b值越大,越能反映水分子真实扩散情况;同时,b值越大,噪声越大,图像分辨率下降,本研究最大b值800 s/mm2。
ADC值可能受MRI生产厂家[3]、DWI成像方式[4]、静磁场强度、b值选择、ADC值测量方法、增强与否、扫描层厚等因素影响,最公认的影响因素是静磁场强度和b值大小。不同应用条件产生的最佳ADC阈值也不同[5],相同条件下的结果具有更大参考价值。因此,本研究结果适用于联影3.0 T MRI、最大b值800 s/mm2、测量病灶实性部分最低ADC值等相似情况。
3.2 乳腺良恶性病变ADC值分析本研究中,恶性组平均ADC值为(0.914±0.196)×10-3 mm2/s,良性组为(1.480±0.312)×10-3 mm2/s,差异有统计学意义。Ohlmeyer等[4]应用Siemens 3.0 T MRI、最大b值800 s/mm2研究乳腺肿瘤,恶性肿瘤平均ADC值为0.90×10-3 mm2/s,良性病变平均ADC值为1.86×10-3 mm2/s。有学者采用Meta分析对13 847个乳腺病变进行研究得出,恶性病变平均ADC值为1.03×10-3 mm2/s,良性病变为1.50×10-3 mm2/s[6]。不同研究结果存在一定差异,可能与研究条件不同有关。值得关注的是,无论何种研究,乳腺良恶性病变的ADC值均存在一定程度的重叠[3-9]。
恶性肿瘤弥散受限明显,可能与恶性肿瘤细胞增殖快、肿瘤细胞密集、肿瘤细胞核大、细胞外间隙小、水分子扩散运动受限明显及ADC值呈低信号有关。良性肿瘤弥散受限较低,可能与细胞增殖慢、肿瘤细胞不密集、肿瘤细胞核浆比小、细胞外间质较多,水分子扩散运动受限不明显,以及ADC值呈稍低、等或稍高信号有关[8-10]。需注意的是,乳腺黏液腺癌中黏液成分越多,弥散受限越不明显,单纯性乳腺黏液腺癌的ADC值高达1.9×10-3 mm2/s[11]。
3.3 乳腺良恶性病变鉴别的最佳ADC阈值分析约登指数=敏感度+特异度-1,最大约登指数意味着敏感度+特异度的值最大,可在最大程度上鉴别乳腺良恶性病变,即最佳ADC阈值。本研究中,最大约登指数为0.806,对应的最佳ADC阈值1.106×10-3 mm2/s,敏感度86.1%,特异度94.4%。阳性似然比是真阳性率与假阳性率的比值,阳性似然比大,意味正确诊断乳腺癌的比例大;本研究中阳性似然比15.4(> 10),表明小于此阈值正确诊断乳腺癌具有显著性。阴性似然比是假阴性率与真阴性率的比值,阴性似然比小,意味排除乳腺癌可能性大;本研究中阴性似然比0.147(> 0.1),表明大于此阈值排除乳腺癌可能不具有显著性。Horvat等[9]应用GE 3.0 T MRI,约登指数为0.740(敏感度和特异度均为87%)。杨玲等[11]应用Philips 1.5 T MRI扫描仪,ADC值鉴别乳腺良恶病变的约登指数为0.646(敏感度77.08%、特异度87.50%)。刘世忠等[12]应用Siemens 1.5 T MRI扫描仪,ADC值鉴别乳腺良恶性病变的约登指数为0.591(敏感度84.62%、特异度74.47%)。以上研究中ADC值鉴别乳腺良恶性病变,3.0 T MRI的约登指数大于1.5 T MRI,可能与静磁场强度有关。
本研究约登指数为0.722时,所对应的ADC值为1.253×10-3 mm2/s,敏感度94.4%(高),特异度77.8%(不够高),阳性似然比4.25(<10),阴性似然比0.072(<0.1)。其优点是阴性似然比足够低(0.072),大于此阈值排除乳腺癌可能具有显著性,敏感度足够高(94.4%),乳腺癌漏诊可能性很小。其缺点是阳性似然比不够高(4.25),正确诊断乳腺癌比例不具有显著性,特异度77.8%提示将乳腺良性病变误诊为恶性病变比例较高,可能增加一定比例的穿刺活检或手术病例。
有学者推荐ADC值1.00×10-3 mm2/s作为鉴别乳腺病变良恶性的阈值,是一个绝对的ADC阈值[6],与本研究结果相符,可见,乳腺病灶ADC值<1.00×10-3 mm2/s,几乎100%为恶性肿瘤。
本研究中,乳腺良恶性病变的ADC值在(1.010~1.307)×10-3 mm2/s范围内存在一定重叠,ADC值<1.000×10-3 mm2/s基本上可诊断为恶性肿瘤;ADC值在(1.000~1.106)×10-3 mm2/s范围内恶性肿瘤可能很大,可能包括个别良性病变;ADC值在(1.000~1.253)×10-3 mm2/s范围内恶性肿瘤可能大,可能包括少量良性病变。以1.106×10-3 mm2/s为阈值,可最大程度区分乳腺良恶性病变,但有少量乳腺癌漏诊;以1.253×10-3 mm2/s为阈值,可减少乳腺癌漏诊,但有少量良性病变误诊为乳腺癌。在临床工作中,漏诊乳腺癌的危害性更大,因此推荐以1.253×10-3 mm2/s为阈值,即ADC值在(1.000~1.253)×10-3 mm2/s范围内的病变需慎重判断,应结合形态学观察(如T2WI信号、强化程度)、TIC曲线类型、其他影像学检查(如超声、钼靶X线摄影)、肿瘤标志物、临床症状及体征等综合判断[13-16]。
综上所述,以1.106×10-3 mm2/s为ADC阈值能最大程度区分乳腺良恶性病变,但有少量乳腺癌漏诊;以1.253×10-3 mm2/s为ADC阈值,诊断敏感度较高,但有少量良性病变误诊为乳腺癌,推荐在临床工作中应用。ADC值<1.000×10-3 mm2/s基本上可诊断为恶性肿瘤;对ADC值在(1.000~1.253)×10-3 mm2/s范围内的病变,应结合MRI常规序列、其他检查、临床资料等综合分析,除典型良性病变外,建议穿刺活检或短期(3、6个月)复查。
| [1] |
BRAY F, FERLAY J, SOERJOMATARAM I, et al. Global cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2020, 70(4): 313. |
| [2] |
张雪, 董晓平, 管雅喆, 等. 女性乳腺癌流行病学趋势及危险因素研究进展[J]. 肿瘤防治研究, 2021, 48(1): 87-92. DOI:10.3971/j.issn.1000-8578.2021.20.0498 |
| [3] |
GIANNELLI M, SGHEDONI R, IACCONI C, et al. MR scanner systems should be adequately characterized in diffusion-MRI of the breast[J]. PLoS One, 2014, 9(1): 86280. DOI:10.1371/journal.pone.0086280 |
| [4] |
OHLMEYER S, LAUN F B, PALM T, et al. Simultaneous multislice echo planar imaging for accelerated diffusion-weighted imaging of malignant and benign breast lesions[J]. Invest Radiol, 2019, 54(8): 524-530. DOI:10.1097/RLI.0000000000000560 |
| [5] |
WIELEMA M, DORRIUS M D, PIJNAPPEL R M, et al. Diagnostic performance of breast tumor tissue selection in diffusion weighted imaging: a systematic review and meta-analysis[J]. PLoS One, 2020, 15(5): 0232856. |
| [6] |
SUROV A, MEYER H J, WIENKE A. Can apparent diffusion coefficient (ADC) distinguish breast cancer from benign breast findings? A meta-analysis based on 13847 lesions[J]. BMC Cancer, 2019, 19(1): 955. DOI:10.1186/s12885-019-6201-4 |
| [7] |
吴杰, 敬宗林, 黄小华, 等. MRI动态增强扫描联合扩散峰度成像对乳腺良恶性病变的鉴别诊断价值[J]. 中国中西医结合影像学杂志, 2020, 18(4): 378-382. |
| [8] |
钟琦, 崔凤. 乳腺MRI对不同类型黏液腺癌的诊断价值[J]. 中国临床医学影像杂志, 2016, 27(2): 94-97. |
| [9] |
HORVAT J V, DURANDO M, MILANS S, et al. Apparent diffusion coefficient mapping using diffusion-weighted MRI: impact of background parenchymal enhancement, amount of fibroglandular tissue and menopausal status on breast cancer diagnosis[J]. Eur Radiol, 2018, 28(6): 2516-2524. DOI:10.1007/s00330-017-5202-4 |
| [10] |
杨静, 李新瑜, 黄咏文. 乳腺黏液癌的MRI表现[J]. 中国中西医结合影像学杂志, 2021, 19(6): 550-553. DOI:10.3969/j.issn.1672-0512.2021.06.011 |
| [11] |
杨玲, 胡少平, 陆成龙, 等. DWI-MRI联合钼靶对乳腺病变良恶性的鉴别价值[J]. 中国CT和MRI杂志, 2021, 19(2): 87-89, 111. |
| [12] |
刘世忠, 吴雄娟, 詹奕彦, 等. MRI动态增强曲线、DWI及ADC值用于乳腺疾病定性诊断的敏感性及特异性评估[J]. 中国CT和MRI杂志, 2017, 15(10): 67-70. |
| [13] |
陈艳, 崔利, 何江波, 等. MRI对乳腺黏液癌和纤维腺瘤的鉴别诊断价值[J]. 中国中西医结合影像学杂志, 2021, 19(4): 351353. |
| [14] |
陈艳虹, 王丽君, 汪登斌, 等. MRI对超声阴性、乳腺X线摄影中乳腺影像报告和数据系统4类单纯钙化病变的诊断价值[J]. 中华放射学杂志, 2021, 55(11): 1178-1183. |
| [15] |
崔春晓, 林青. 乳腺摄影新技术和人工智能在乳腺癌筛查诊断中的应用价值[J]. 中国中西医结合影像学杂志, 2021, 19(6): 513-515, 531. |
| [16] |
张力莹, 郝济森, 殷星, 等. 动态增强MRI联合集合序列对乳腺良恶性病变的诊断价值[J]. 临床放射学杂志, 2021, 40(8): 1495-1499. |
 2022, Vol. 20
2022, Vol. 20


