| CTA与经胸超声心动图在法洛四联症及其并发畸形诊断中的应用价值 |
法洛四联症(tetralogy of Fallot,TOF)是一种发绀性先天性心脏病,包括肺动脉狭窄、室间隔缺损、主动脉骑跨和右心室肥厚,发病率约1/3 500,占先天性心脏畸形的7%~10%[1-2]。TOF自然预后差,10岁内病死率高达70%,多数需经手术治疗,因此术前准确判断患儿心脏及并发其他畸形情况对明确手术指征、制订手术方案及评估围术期风险具有重要意义[3]。经胸超声心动图(transthoracic echocardiography,TTE)具有无创、无电离辐射及检查费用低等优点,常用于TOF的术前筛查,但声窗受限及操作医师主观性会影响其诊断,不容忽视[4]。MSCT扫描速度快、空间分辨力高,是TOF的重要检查方法。现回顾性分析35例TOF患儿的影像资料,探讨CTA及TTE在TOF及其并发畸形中的应用价值。
1 资料与方法 1.1 一般资料选取我院2015年1月至2019年1月收治的TOF患儿35例,其中男25例,女10例;年龄2个月~34个月,平均(18.3±5.2)个月。临床表现为不同程度发育迟缓,部分患儿伴发绀症状,听诊闻及心脏收缩期杂音。所有患儿均经心导管造影及手术确诊为TOF,临床资料完整且均行MSCTA及TTE检查。
1.2 仪器与方法① CTA:使用Philips 64层MSCT扫描仪,患儿检查前口服10%水合氯醛镇静,剂量0.5~0.6 mL/kg体质量。扫描参数:120 kV,80~150 mAs,层厚及层距均为5 mm。增强扫描对比剂使用碘海醇,剂量2.0 mL/kg体质量,采用心电门控扫描方式。原始图像由影像科1名技师行多MPR、CPR、MIP及VR,后处理图像由2名高年资医师采用盲法读片,意见不一致时协商取得一致结果。②TTE:使用Philips IE33超声诊断仪,频率5~10 MHz。按解剖位置扫查心脏结构及周围动脉,重点观察心内外畸形、主动脉及肺动脉发育情况。
1.3 统计学方法应用SPSS 22.0统计软件进行数据分析,计数资料以率表示,比较采用χ2检验,对肺动脉主干(main pulmonary artery,MPA)、右肺动脉(right pulmonary artery,RPA)及左肺动脉(left pulmonary artery,LPA)起始部直径采用重复方差分析,两两比较行LSD-t检验。以P<0.05为差异有统计学意义。
2 结果 2.1 CTA及TTE对TOF及其并发畸形的检出情况经心导管造影及手术证实,35例(图 1)共并发106处其他畸形。其中心内畸形54处,包括卵圆孔未闭25处、房间隔缺损9处、肺动脉瓣二叶化畸形10处,肺动脉瓣口狭窄10处(图 2)。心外畸形52处,包括动脉导管未闭18处(图 3)、体-肺侧支15处、冠状动脉异常8处、右位主动脉弓4处、永存左上腔静脉3处、迷走左头臂静脉2处、肺静脉异位引流2处。CTA与TTE对TOF的检出率均为100.0%。CTA及TTE对心内畸形的检出率分别为81.5%(44/54)、85.2%(46/54),差异无统计学意义(χ2=0.671,P>0.05),对心外畸形的检出率分别为98.1%(51/52)、61.5%(32/52),差异有统计学意义(χ2=18.639,P<0.05),总体检出率分别为89.6%(95/106)、73.6%(78/106),差异有统计学意义(χ2=7.485,P<0.05)。
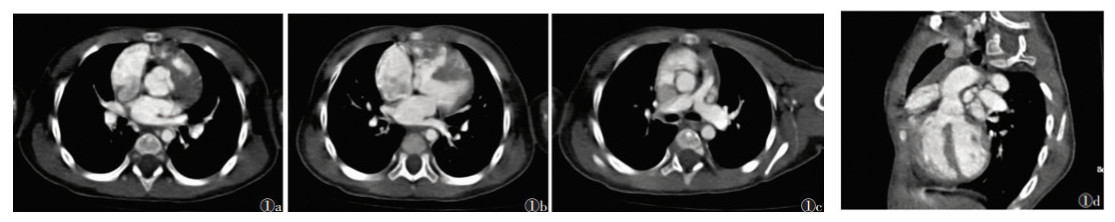 |
| 图 1 男,9个月,法洛四联症(TOF) 图 1a CTA 轴位示右心室仅少量对比剂进入,提示右心室肥厚 图 1b CTA 轴位示主动脉瓣下室间隔处可见对比剂相通 图 1c CTA 轴位示肺动 脉干狭窄 图 1d CTA CPR 示主动脉骑跨于左、右心室之上 |
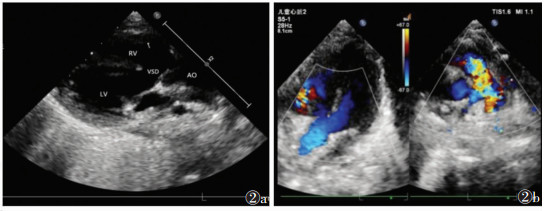 |
| 图 2 男,16个月,TOF 图 2a 经胸超声心动图示室间隔上部连续中断 ,升主动脉增宽骑跨于室间隔上 ,右室壁明显增厚 (RV,右室;LV,左室;VSD,室间隔缺损;AO,主动脉;箭头示增厚的右室壁) 图 2b CDFI 示 胸骨旁五腔心切面示主动脉前移骑跨在室间隔上,室间隔水平见双向分流,大动脉短轴切面示 肺动脉瓣狭窄,肺动脉内测及五彩花色血流束 |
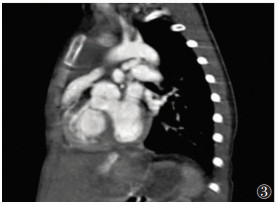 |
| 图 3 女,6个月TOF。CTA CPR示主动脉弓与肺动脉间可见迂曲的动脉导管 |
2.2 CTA及TTE对TOF相关解剖结构测量结果(表 1)
| 表 1 CTA及TTE对TOF相关动脉起始部直径测量结果比较(d/mm,x±s) |
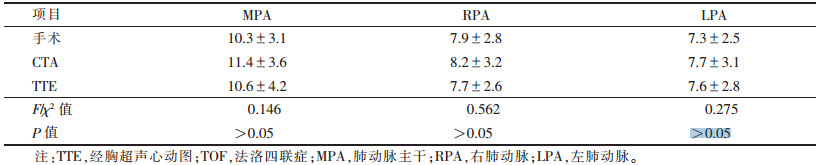 |
CTA及TTE测得的MPA、RPA及LPA起始部直径与手术结果比较差异均无统计学意义(均P>0.05)。CTA对RPA及LPA远端的显示率均为100.0%(35/35),TTE对RPA及LPA远端的显示率分别为45.7%(16/35)、51.4%(18/35)。CTA对RPA及LPA远端显示率明显高于TTE,差异均有统计学意义(χ2=44.891,38.136;均P<0.05)。
3 讨论TOF的病理解剖为肺动脉狭窄、室间隔缺损、主动脉骑跨和右心室肥厚,具有一定家族遗传性[4-5]。TOF的临床首发症状为缺氧性发绀,之后可出现杵状指,长期缺氧可致患儿末梢循环障碍,还可并发其他心内外畸形。从1944年Blalock与Taussig为TOF患儿行体肺分流术开始[6],经过多年的经验积累,TOF手术风险逐渐降低,术后效果良好,大部分患儿可存活至成年。TOF的手术方法是切开狭窄的肺动脉瓣、跨瓣补片以解除右室流出道梗阻;另外,外科医师也需对TOF并发的其他畸形进行手术干预,以确保患儿预后。因此,术前准确判断患儿心脏及并发畸形情况意义重大。
以往对TOF的术前诊断主要依靠心导管造影,但其对患儿创伤较大,医疗费用高昂,且肺动脉远端的显示较模糊,从而影响诊断准确率。TTE检查无创、无电离辐射、操作简便且费用较低,常作为TOF的首选筛查方法,但其易受肺组织气体影响,且对远场的病变检出率低,难以准确判断血管全貌[7-8]。MSCT扫描速度快、图像清晰,CTA可对目标血管与周围组织形成良好对比,其多角度成像可有效避免图像重叠,对TOF及其并发畸形的诊断起着重要作用。MSCT图像后处理包括MIP、MPR、CPR及VR等,其中MPR可通过调整层厚清晰观察心内结构,如瓣膜缺损等;CPR可通过旋转图像反映任意角度的解剖关系,如主动脉骑跨等;而MIP、VR多角度旋转观察技术,可有效弥补二维图像立体感的不足,同时能直观显示心外畸形[9]。本研究发现CTA及TTE检查对TOF的检出率均为100.0%,说明CTA及TTE可准确诊断TOF。CTA及TTE对TOF并发畸形的检出各具优劣。CTA对心内畸形的检出率为81.5%(44/54),略低于TTE的85.2%(46/54),但差异无统计学意义。CTA漏诊10例心内畸形,包括7例卵圆孔未闭、2例直径较小的房间隔缺损、1例肺动脉瓣口狭窄,原因可能是CTA时间分辨力相对较低,心腔内显示受限,对心内畸形及瓣膜活动不易辨别,也无法提供血流动力学相关指标,难以对患儿进行完整的心功能评估,而TTE的优势在于对瓣膜病变等心内畸形的诊断能力,联合TTE可有效弥补。CTA对心外畸形的检出率为98.1%(51/52),显著高于TTE的61.5%(32/52)。TTE漏误诊20处,包括体-肺侧支9处、冠状动脉异常6处、右位主动脉弓2处、动脉导管未闭2处、肺静脉异位引流并永存左上腔静脉1处;主要是由于TTE受声窗限制及肺内气体干扰,外部血管及侧支显示不佳所致。TTE可有效检查近端肺动脉狭窄部位及程度,但对远端肺动脉病变的诊断非常有限[10]。本研究CTA与TTE测得MPA、RPA及LPA起始部直径与手术结果比较差异均无统计学意义,但CTA对RPA及LPA远端显示率明显高于TTE,这是因为MSCT空间分辨力高,X线衰减在空气和软组织对比明显,因此远端血管显示较好,而TTE则因声窗限制对远端血管显示不佳。另外,CTA对心内外畸形总体检出率分别89.6%(95/106),显著高于TTE的73.6%(78/106),说明CTA对TOF并发畸形的检出总体优于TTE。
综上所述,CTA与TTE对TOF均具有很高的检出率。对于TOF并发畸形,TTE的优势在于对心内畸形如瓣膜异常的判断,而CTA的优势在于对心外畸形的判断,且其对心内外畸形的总体检出率也高于TTE。必要时两者联合应用,可做到优势互补,有效避免漏误诊。
| [1] |
石兢恒, 段庆红, 廖桂英, 等. 320排容积CT血管造影对法洛四联症的诊断价值[J]. 医学影像学杂志, 2018, 28(10): 1651-1654, 1658. |
| [2] |
李岩锋, 张兴雨. 256层螺旋CT血管造影在诊断重症婴幼儿法洛四联症中的临床价值分析[J]. 现代医用影像学, 2019, 28(3): 521-522. |
| [3] |
苏金花, 寇海燕, 梁莉. 实时三维超声心动图对法洛四联症患者右心室收缩功能变化的评估价值研究[J]. 海南医学院学报, 2016, 22(1): 96-98. |
| [4] |
畅芳叶, 刘洁琼, 米燕萍. 超声心动图分段分析诊断复杂先天性心脏病的应用价值[J]. 中西医结合心脑血管病杂志, 2019, 17(15): 2397-2398. DOI:10.12102/j.issn.1672-1349.2019.15.043 |
| [5] |
VILLAFANE J, FEINSTEIN J A, JENKINS K J, et al. Hot topics in tetralogy of Fallot[J]. J Am Coll Cardiol, 2013, 62(23): 2155-2166. DOI:10.1016/j.jacc.2013.07.100 |
| [6] |
USHA K, SHIVANI A, ARIN C, et al. The blalock and taussig shunt revisited[J]. Ann Card Anaesth, 2017, 20(3): 323-330. DOI:10.4103/aca.ACA_80_17 |
| [7] |
KASKINEN A K, HAPPONEN J M, MATTILA I P, et al. Longterm outcome after treatment of pulmonary atresia with ventricular septal defect:nationwide study of 109 patients born in 1970-2007[J]. Eur J Cardiothorac Surg, 2016, 49(5): 1411-1418. DOI:10.1093/ejcts/ezv404 |
| [8] |
YANG S H, LUO P H, TIAN X X, et al. Prenatal diagnosis of pulmonary atresia with ventricular septal defect[J]. J Med Ultrason (2001), 2018, 45(2): 341-344. DOI:10.1007/s10396-017-0809-2 |
| [9] |
陈晓琼, 廖锦堂. 经胸超声心动图与64排CT心血管造影评价法洛四联症肺动脉狭窄的价值比较[J]. 中国现代手术学杂志, 2013, 17(1): 55-58. |
| [10] |
白文伟, 刘小勇, 朱敏. 超声心动图联合256排CT心血管造影在法洛四联症诊断中的应用价值[J]. 实用临床医药杂志, 2018, 22(3): 96-98. |
 2021, Vol. 19
2021, Vol. 19


