| HIV感染合并骨梗死的MRI动态观察 |
骨梗死是由骨的滋养血管梗死所致,临床上较少见,但HIV感染患者骨梗死的发病率相对免疫功能正常者高。随着高效联合抗逆转录病毒疗法(highly active antiretroviral therapy,HAART)的广泛应用,骨梗死患病率明显增加。本研究对16例HIV感染合并骨梗死进行回顾性分析,探讨该病与HAART疗程的相关性。
1 资料与方法 1.1 一般资料选取我院2013年12月至2017年12月16例HIV感染合并骨梗死的患者进行回顾性分析;其中男12例,女4例;年龄24~42岁,平均(35.6±6.8)岁。首次疑诊6例,确诊3例,最终确诊16例。已排除可能的干扰项:酗酒史;大量使用糖皮质激素史;外伤史;下肢动脉、静脉栓塞及手术史。
1.2 仪器与方法采用Philips Achieva 1.5 T MRI扫描仪和膝关节线圈进行扫描。扫描序列:行横断面、冠状位和矢状位成像,FSE T1WI,TR 300~500 ms,TE 9 ms,FOV 20 cm×26 cm,矩阵(384~256)×(256~320);FSE T2WI,TR 3 500~4 000 ms,TE 90~120 ms,FOV 22 cm×24 cm,矩阵(192~256)×(256 ~320)。
1.3 追踪观察对已行9~32个月HAART治疗的患者进行追踪观察,对骨梗死膝关节进行3~5次追踪。观察项目:①统计双侧股骨下段及胫骨上段骨梗死椭圆形病灶数目。②测量骨梗死范围,每个病灶取最大层面进行面积测量,人工勾勒边界,将图像导入AutoCAD 2016软件进行计算,所有病灶面积相加得出骨梗死范围。
1.4 统计学分析采用SPSS 19.0统计软件进行数据分析。将每次测量的骨梗死面积(cm2)和HAART治疗时间(月)绘制散点图,并对两者行Pearson相关性分析及Logistic回归分析,以P < 0.05为差异有统计学意义。
2 结果 2.1 影像表现16例均双侧对称性发病,双侧髋关节、肩关节未见异常改变。16例均出现双侧股骨下段、胫骨上段多发的、类椭圆形、边界清楚的、地图板块样病变,病灶内部T1WI低信号、T2WI高信号,病灶边界呈线样T1WI低信号、T2WI低信号(图 1a)。6例(37.5%)在追踪观察中出现骨髓腔斑片样T1WI低信号、T2WI高信号(图 1b)。3例(18.8%)出现关节腔积液。9例(56.2%)出现双边征:病灶边界T1WI呈低信号,T2WI见内高外低双线平行迂曲走行信号(图 1c,1d)。
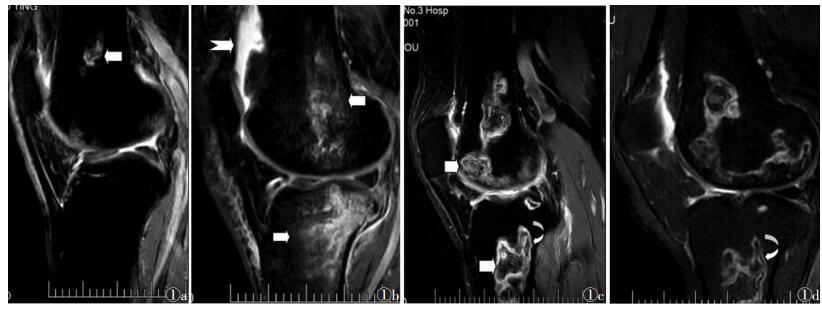 |
| 图 1 男,41岁,HIV感染3年,高效联合抗逆转录病毒疗法(HAART)治疗9个月,右膝关节矢状位FSE T2WI示股骨下段孤立类椭圆形T2WI高信号的骨梗死病灶(白箭),边界清楚,呈线样低信号 图 1b HAART治疗12个月,右膝关节矢状位T2WI STIR示股骨下段、胫骨上段骨髓腔出现斑片样水肿高信号(白箭),骨梗死病灶边界显示不清,见关节腔积液(燕尾箭) 图 1c HAART治疗18个月,右膝关节矢状位FSE T2WI示股骨下段、胫骨上段出现地图板块样骨梗死病灶,病灶范围扩大、数目增多(白箭),骨水肿减轻,见双边征(弧形箭) 图 1d HAART治疗24个月,右膝关节矢状位FSE T2WI,骨梗死病灶病灶境界清楚,内部信号减低,见双边征(弧形箭) |
2.2 追踪观察
16例随着HAART治疗时间的延长,骨梗死病灶数目进行性增多,病灶面积进行性扩大(图 1c,1d)。
2.3 骨梗死面积与HAART治疗时间的相关性16例骨梗死病变的面积和HAART治疗时间的散点图呈线性趋势(图 2)。Pearson相关性分析示骨梗死面积与HAART治疗时间具有相关性(r=0.964,P < 0.05),Logistic线性回归方程为:Y面积=5.389+0.400X治疗时间,回归系数95%置信区间为(0.356,0.444),决定系数R2=92.9%,说明骨梗死面积总变异的92.9%与HAART治疗时间有关。
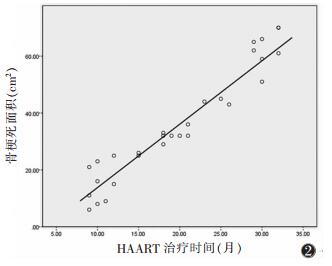 |
| 图 2 HIV感染合并骨梗死患者在HAART治疗不同时间段骨梗死面积的散点图 |
3 讨论
本研究针对HIV感染者HAART治疗后出现进展性骨梗死进行回顾性分析,探讨HAART治疗与骨梗死的发生及进展的相关性。
3.1 HAART介绍HAART是目前推荐的最有效治疗HIV的疗法,能够有效抑制HIV复制,重建免疫功能,提升CD4+T淋巴细胞计数[1]。HAART的治疗标准是HIV感染者CD4+T淋巴细胞计数小于350 μL-1[2]。HAART治疗方案应含3种抗病毒、2类核苷酸反转录酶抑制剂和1类非核苷酸反转录酶抑制剂[1-2];核苷酸反转录酶抑制剂:齐多夫定(AZT)、拉米夫定(3TC)、司他夫定(D4T)、替诺福韦(TDF);非核苷酸反转录酶抑制剂:奈韦拉平(NVP)、依非韦伦(EVF)。
3.2 骨梗死的病因和发病机制骨梗死是滋养骨髓、骨干的血管由于各种原因发生梗死导致的骨髓、骨脂肪梗死[3]。骨梗死最多发生于股骨下段、胫骨上段的骨骺及干骺端,常对称性发病[4]。骨梗死的病因很多,常与外伤、糖皮质激素治疗、酗酒、恶性肿瘤治疗、代谢病等多种致病因素有关。股骨下段、胫骨上段的骨髓脂肪组织较多、滋养血管分支细小、走行迂曲且相对稀少[5]。膝关节活动程度大,供血量多,但血管易受压,加上各种原因导致滋养血管堵塞,致使组织细胞持续缺血及缺氧,从而发生骨梗死[6]。本研究是在排除常见病因的情况下进行的研究,因此HAART治疗有可能也是引起骨梗死的病因。
3.3 骨梗死的MRI表现本研究发现16例HIV感染者骨梗死发生的部位仅限于双侧膝关节,且对称性发生、进展,而其他四肢骨、中轴骨未发现异常骨梗死改变。结合文献[5-6],总结骨梗死的MRI表现:①地图样改变,是骨梗死的典型MRI表现,病灶常呈类椭圆形,与骨干长轴走行一致,边界清楚、光滑锐利。②双边征,是指病灶的边界T2WI见内高外低双线平行迂曲走行的异常信号,是骨坏死、骨梗死特异的MRI征象[7]。③骨水肿,骨梗死发病的早期及进展期,在类椭圆形病灶周围出现的斑片样T2WI高信号影,边界不清,在骨梗死稳定病灶周围,骨水肿不多见[8]。
3.4 HAART治疗与骨梗死面积的相关性研究[9]发现,随着HAART疗程的延长,HIV感染者会出现不同程度的骨量减少,长时间的抗病毒治疗骨质疏松发病率明显增加。本研究16例随着HAART治疗时间的延长,骨梗死的范围扩大且数目增多。HIV感染者T淋巴细胞不仅表现为计数下降,且出现异常活化。HAART的治疗使患者免疫功能得到重建,异常活化的T淋巴细胞免疫功能活跃,细胞毒性T淋巴细胞分泌的细胞因子能够抑制成骨细胞及破骨细胞,导致骨代谢紊乱,且抗病毒药物能够引起肾小管的损伤,导致钙磷代谢紊乱,从而加剧骨代谢紊乱[10]。膝关节由于较为特殊的骨滋养血管、骨代谢紊乱及异常活化的T淋巴细胞损伤滋养血管易导致骨梗死[11]。
综上所述,HIV感染者骨梗死的进展与HAART治疗时间有相关性。但以往研究[11]发现,HIV感染者的骨梗死发生率较免疫功能正常者明显升高,是否骨梗死与HIV感染因素有关,本研究未做深入探讨。
| [1] |
柳忠泉, 宁铁林, 夏建晖, 等. 天津市2005-2009年抗艾滋病病毒治疗效果分析[J]. 中国预防医学杂志, 2011, 12(2): 158-160. |
| [2] |
谢桂芳, 黎小平, 潘玉勤. 高效抗反转录病毒疗法治疗艾滋病效果分析[J]. 右江民族医学院学报, 2013, 35(3): 292-293. DOI:10.3969/j.issn.1001-5817.2013.03.015 |
| [3] |
方庆明, 徐志伟, 雷杰华. 骨梗死X线与低场MRI表现分析对比[J]. 现代医用影像学, 2017, 26(5): 1288-1292. |
| [4] |
苏仲生, 蔡琳, 王明, 等. 骨梗死影像学表现与鉴别诊断[J]. 临床骨科杂志, 2017, 20(3): 325-328. DOI:10.3969/j.issn.1008-0287.2017.03.022 |
| [5] |
董进, 韩瑞, 张东友, 等. 3.0T磁共振成像技术对膝关节骨梗死的诊断价值[J]. 医学临床研究, 2016, 33(9): 1671-1673. |
| [6] |
Kanthawang T, Pattamapaspong N, Louthrenoo W. Acute bone in farction:a rare complication in thalassemia[J]. Skeletal Radiol, 2016, 45: 1013-1016. DOI:10.1007/s00256-016-2387-6 |
| [7] |
Zurlo JV. The double-line sign[J]. Radiology, 1999, 212: 541-542. DOI:10.1148/radiology.212.2.r99au13541 |
| [8] |
Robert W, Jordan, Prasad Aparajit, et al. The importance of early diagnosis in spontaneous osteonecrosis of the knee-A case series with six year follow-up[J]. Knee, 2016, 23: 702-707. DOI:10.1016/j.knee.2016.04.005 |
| [9] |
Yamagami R, Taketomi S, Inui H, et al. The role of medial meniscus posterior root tear and proximal tibial morphology in the development of spontaneous osteonecrosis and osteoarthritis of the knee[J]. Knee, 2017, 24: 390-395. DOI:10.1016/j.knee.2016.12.004 |
| [10] |
Mazzotta E, Agostinone A, Rosso R, et al. Osteonecrosis in hu man immunodeficiency virus (HIV) -infected patients:a multi centric case-control study[J]. J Bone Miner Metab, 2011, 29: 383-388. DOI:10.1007/s00774-010-0245-5 |
| [11] |
Patel N, Patel N, Espinoza LR. HIV infection and rheumatic di seases:The changing spectrum of clinical enigma[J]. Rheumatic Disease Clinics of North America, 2009, 35: 139-161. DOI:10.1016/j.rdc.2009.03.007 |
 2019, Vol. 17
2019, Vol. 17


