| CT身体成分参数预测急性缺血性脑卒中严重程度的价值 |
2. 武汉市第一医院综合医疗科, 湖北 武汉 430022;
3. 武汉市第一医院神经内科, 湖北 武汉 430022
2. Department of Geriatrics, Wuhan No.1 Hospital, Wuhan 430022, China;
3. Department of Neurology, Wuhan No.1 Hospital, Wuhan 430022, China
脑卒中因其高发病率、高复发率、高致残率和高经济负担,对全球公共卫生构成了重大威胁[1]。急性缺血性脑卒中(acute ischemic stroke,AIS)是最常见的卒中类型,占我国新发卒中的69.6%~72.8%[2-3]。早期准确评估病情严重程度不仅是临床决策的核心依据,更是优化治疗策略、改善患者功能预后的关键。近年来,身体成分在AIS发生和进展中的作用逐渐成为研究焦点。研究发现,内脏脂肪比例与静脉溶栓治疗AIS患者的预后相关[4]。骨骼肌质量下降与胰岛素抵抗、糖代谢异常相关,而这些代谢紊乱又会加重AIS患者的脑损伤程度,影响病情[5]。既往研究多集中于传统影像学对脑部病变的直接评估,而忽视了全身代谢状态对脑部病变的影响。CT成像可准确量化脂肪-肌肉参数区域分布,是评估身体成分的金标准[6]。然而,目前关于CT身体成分与AIS严重程度之间关系的研究较少。本研究旨在分析CT身体成分参数与AIS严重程度之间的关系,为临床提供更全面、精准的评估指标,指导制订个性化的治疗方案。
1 资料与方法 1.1 一般资料回顾性分析2022年1月至2024年12月我院诊断为AIS的患者84例,其中男53例,女31例;年龄39~93岁,平均(67.89±11.59)岁。
纳入标准:①年龄≥ 18岁;②72 h内发病并住院治疗的AIS患者;③DWI显示明确的AIS病灶;④住院期间行腹部CT检查。排除标准:①缺少相关的临床资料;②合并重度颅脑损伤或颅内肿瘤;③抑郁、焦虑、精神疾病患者;④严重心、肝、肾功能不全患者;⑤恶性肿瘤患者;⑥图像质量不佳。使用美国国立卫生研究院卒中量表(National Institutes of Health Stroke Scale,NIHSS)评估患者神经系统缺陷的严重程度,并依据评分分为轻度卒中组(NIHSS评分<5分)和中重度卒中组(NIHSS评分≥ 5分)。本研究经医院伦理委员会批准(批号:〔2024〕25号)。
1.2 仪器与方法采用Siemens SOMATOM Definition AS+ 64排CT机及Siemens SOMATOM Definition Flash双源CT机。患者取仰卧位,屏气扫描,头先进。扫描范围自膈顶至耻骨联合上缘。扫描参数:120 kV,自动管电流调制,螺距1.375,矩阵512×512,层厚5 mm,使用软组织算法重建2 mm层厚轴位图像。
1.3 图像分析选取L3中间层面腹部轴位CT图像[7],应用SliceOmaticV5.0(Tomovision,Canada)软件,根据骨骼肌组织CT阈值-29~150 HU,皮下脂肪组织CT阈值-190~-30 HU,内脏脂肪组织CT阈值-150~-50 HU[8-9],使用ABACS模块进行组织自动分割后分别测定骨骼肌面积(skeletal muscle area,SMA)、皮下脂肪面积(subcutaneous fat area,SFA)、内脏脂肪面积(visceral fat area,VFA)及骨骼肌密度(skeletal muscle density,SMD)(图 1,2)。计算VFA/SFA比值。
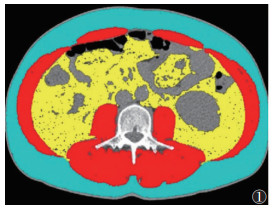 |
| 注:图1患者,男,39岁,轻度卒中。 图 1 L3层面轴位CT图像,使用SliceOmatic软件中自动分割模块计算身体成分,内脏脂肪组织、皮下脂肪组织、骨骼肌组织分别用黄色、蓝色、红色表示 |
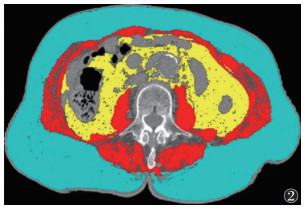 |
| 注:图2患者,女,93岁,中重度卒中 图 2 L3层面轴位CT图像,使用SliceOmatic软件中自动分割模块计算身体成分,内脏脂肪组织、皮下脂肪组织、骨骼肌组织分别用黄色、蓝色、红色表示 |
1.4 统计学分析
采用SPSS 26.0及MedCalc 20.0软件分析数据。正态分布的计量资料以x±s表示,组间比较行t检验;非正态分布的计量资料以M(QL,QU)表示,组间比较行Mann-Whitney U检验。计数资料以例(%)表示,组间比较行χ2检验。采用logistic回归分析评估AIS严重程度的独立预测因素。通过ROC曲线分析独立预测因素对AIS严重程度的预测价值。以P<0.05为差异有统计学意义。
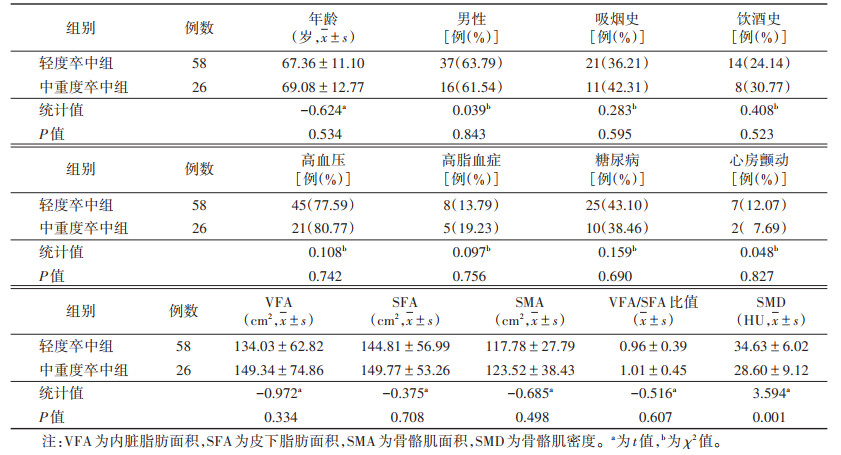
2 结果 2.1 2组一般资料及CT身体成分参数比较2组年龄、性别、吸烟史、饮酒史、高血压、高脂血症、糖尿病及心房颤动差异均无统计学意义(均P > 0.05)。2组VFA、SFA、SMA、VFA/SFA比值差异均无统计学意义(均P > 0.05)。2组SMD比较,差异有统计学意义(P=0.001)(表 1)。
| 表 1 2组一般资料及CT身体成分参数比较 |
 |
2.2 AIS严重程度的logistic回归分析
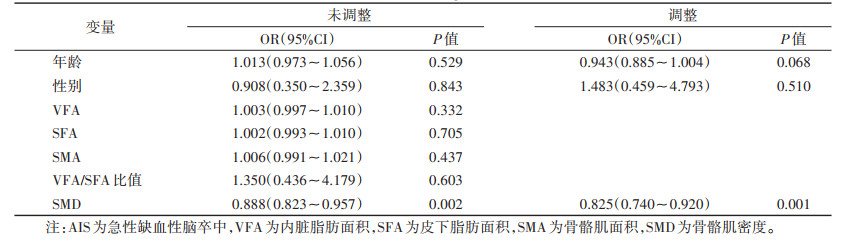
单因素logistic回归分析表明,SMD与AIS严重程度相关(OR=0.888,P=0.002)。调整年龄、性别后,SMD是AIS严重程度的独立保护因素(OR=0.825,P=0.001)(表 2)。
| 表 2 AIS严重程度的logistic回归分析 |
 |
2.3 SMD预测AIS严重程度的ROC曲线分析
ROC曲线显示,SMD预测AIS严重程度的AUC为0.761。当SMD的临界值为31.66 HU时,诊断敏感度为80.77%,特异度为81.03%(图 3)。
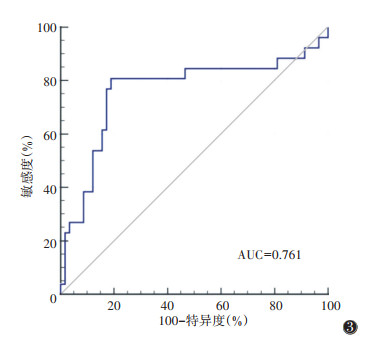 |
| 图 3 骨骼肌密度(SMD)预测急性缺血性脑卒中(AIS)严重程度的ROC曲线 |
3 讨论
近年来,随着人口老龄化的加剧,AIS的发病率呈持续上升趋势。身体成分(包括脂肪、肌肉及骨骼等)的异常与多种疾病的发生、发展及预后密切相关[10-11]。传统评估方法(如生物电阻抗、双能X线)存在空间分辨力低、无法区分脂肪类型等局限。CT成像是评估身体成分的金标准,其通过精确的密度分辨能力,可量化不同组织的体积和分布,为疾病机制研究和个体化治疗提供新视角。研究表明,身体成分可能通过代谢调控途径影响脑卒中病理进程[12]。然而,目前很少有研究使用CT成像来探讨身体成分对AIS严重程度的影响。因此,本研究旨在探讨CT身体成分参数与AIS严重程度的潜在关联。
有研究表明,基于内脏脂肪组织的代谢紊乱与心血管疾病风险相关[13]。近年来,内脏脂肪与脑血管疾病的关系成为研究热点,有研究表明内脏脂肪堆积与AIS的发生及预后密切相关[4, 14-17],而内脏脂肪组织与AIS严重程度的关系尚未明确。Kim等[4]基于CT评估内脏脂肪对127例接受静脉溶栓治疗的AIS患者临床结局的影响,结果显示低内脏脂肪组织比例和低VFA/SFA比值与AIS预后3个月良好结局相关。Yan等[16-17]研究证实,内脏脂肪及其遗传易感性与缺血性脑卒中存在因果关系,内脏脂肪积累与缺血性脑卒中发病风险显著相关,为脑卒中的一级预防提供了新靶点。内脏脂肪指数(visceral fat index,VFI)是一种基于性别、BMI、腰围、甘油三酯和高密度脂蛋白胆固醇水平计算的肥胖指标,其能够反映内脏脂肪的分布和代谢状况,可用于评估内脏脂肪组织的质量和功能情况。Chang等[15]研究发现,入住重症监护病房AIS患者的VFI与患者90 d死亡率呈正相关,可作为预测死亡的独立危险因素,说明VFI对AIS患者的短期预后具有一定的预测价值。但VFI计算模型是由欧洲人研究建立的,更适合欧美人群,国内学者也建立并验证了更适合中国人的VFI(Chinese visceral fat index,CVFI)计算模型。Xu等[14]对453例接受血管内取栓治疗的AIS患者的研究显示,CVFI与患者90 d不良预后呈正相关。Zhang等[18]研究显示CVFI与AIS风险呈正相关,与卒中风险相关,在预测AIS发生方面CVFI明显优于其他指标。本研究显示,VFA、SFA、VFA/SFA比值在不同AIS严重程度患者中差异均无统计学意义,表明以上参数与AIS严重程度无明显相关性。
骨骼肌是人体最重要的组织之一,其不仅是身体的支撑和运动的动力来源,还能够影响身体的新陈代谢、免疫系统和内分泌系统等多个方面。然而,随着年龄的增长、生活方式的改变及疾病的影响,肌肉质量和功能逐渐下降,甚至出现肌少症。研究表明,肌少症及肌肉质量减少与AIS初始卒中严重程度增加、预后不良及死亡风险升高紧密相关[19-20]。Ohyama等[21-22]通过生物电阻抗评估AIS患者的骨骼肌质量,发现骨骼肌质量指数与神经功能缺损严重程度、住院时间延长及不良功能预后独立相关。Lindström等[23]基于头颈部CTA数据测量咬肌的面积和密度,结果显示咬肌面积和密度是急性前循环闭塞患者机械取栓术后3个月生存率的独立预测因子,为个体化预后评估提供了新思路。Lee等[24]采用双能X线吸收法评估骨骼肌质量,表明身高校正的低骨骼肌质量是功能预后不良的独立预测因子。有研究者发现,颞肌厚度与甘油三酯葡萄糖指数是AIS患者死亡率和功能预后的独立预测因子,联合评估可提升风险分层能力,为急性脑卒中患者的预后评估提供了新的生物标志物组合[25]。然而,Nozoe等[26]认为颞肌厚度虽然对评估肌少症很重要,但与老年急性卒中患者的功能结局无关。研究表明,在L3层面上的骨骼肌和脂肪组织的横截面积能够反映出全身的骨骼肌及脂肪含量的状况[27-28]。本研究显示,SMA与AIS严重程度无明显相关,一方面可能由于基于腹部CT的骨骼肌参数不同于以往的检查方法;另一方面可能与样本量较小及年龄相关。SMD反映了骨骼肌脂肪浸润程度,骨骼肌内脂肪浸润越多,骨骼肌密度越低。Beşler等[19]研究显示,胸大肌及竖脊肌密度可用于预测AIS血管内治疗后随访中的死亡率,且胸大肌及竖脊肌密度是90 d死亡率的独立危险因素。目前尚未见SMD与AIS严重程度的研究报道。本研究显示,在调整年龄及性别后SMD是AIS严重程度的独立保护因素,随着SMD降低,AIS严重程度风险越高。ROC曲线分析显示,SMD预测AIS严重程度的AUC为0.761,表明SMD有助于减少医师评估AIS严重程度时的主观差异,为临床决策提供更可靠的依据。
本研究存在的局限性:①为单中心回顾性研究,样本量相对较小,可能导致结果出现一定偏倚;②由于样本原因未探讨CT身体成分参数在不同亚型脑卒中(如大动脉粥样硬化型、心源性栓塞型等)中的预测价值差异,后续将扩大样本量进一步研究。
综上所述,CT身体成分参数SMD能够有效预测AIS严重程度,可作为临床更全面、精准的评估指标,制订个体化的临床治疗策略。
| [1] |
GBD 2021 Causes of Death Collaborators. Global burden of 288 causes of death and life expectancy decomposition in 204 countries and territories and 811 subnational locations, 1990—2021: asystematicanalysis for the global burden of disease study 2021[J]. Lancet, 2024, 403(10440): 2100-2132. |
| [2] |
WANG W, JIANG B, SUN H, et al. Prevalence, incidence, and mortality of stroke in China: results from a nationwide population-based survey of 480687 adults[J]. Circulation, 2017, 135(8): 759-771. DOI:10.1161/CIRCULATIONAHA.116.025250 |
| [3] |
中华医学会神经病学分会, 中华医学会神经病学分会脑血管病学组. 中国急性缺血性卒中诊治指南2023[J]. 中华神经科杂志, 2024, 57(6): 523-559. |
| [4] |
KIM J H, CHOI K H, KANG K W, et al. Impact of visceral adipose tissue on clinical outcomes after acute ischemic stroke[J]. Stroke, 2019, 50(2): 448-454. DOI:10.1161/STROKEAHA.118.023421 |
| [5] |
ABE T, IWATA K, YOSHIMURA Y, et al. Low muscle mass is associated with walking function in patients with acute ischemic stroke[J]. J Stroke Cerebrovasc Dis, 2020, 29(11): 105259. DOI:10.1016/j.jstrokecerebrovasdis.2020.105259 |
| [6] |
MACDONALD A J, GREIG C A, BARACOS V. The advantages and limitations of cross-sectional body composition analysis[J]. Curr Opin Support Palliat Care, 2011, 5(4): 342-349. DOI:10.1097/SPC.0b013e32834c49eb |
| [7] |
NACHIT M, HORSMANS Y, SUMMERS R M, et al. AI-based CT body composition identifiesmyosteatosisas key mortality predictor in asymptomatic adults[J]. Radiology, 2023, 307(5): e222008. DOI:10.1148/radiol.222008 |
| [8] |
聂昕宇, 阳宁静, 吕家华, 等. L3椎体骨骼肌密度变化对食管鳞状细胞癌放化疗患者的预后预测价值[J/CD][J]. 肿瘤代谢与营养电子杂志, 2024, 11(3): 332-338. |
| [9] |
XIAO L S, LI R N, CUI H, et al. Use of computed tomography-derived body composition to determine the prognosis of patients with primary liver cancer treated with immune checkpoint inhibitors: a retrospective cohort study[J]. BMC Cancer, 2022, 22(1): 737. DOI:10.1186/s12885-022-09823-7 |
| [10] |
熊柏柱, 侯昌龙, 高飞, 等. 定量CT评估肌肉减少症和脂肪组织含量与肝癌TACE联合PD-1单抗治疗预后的相关性[J]. 放射学实践, 2024, 39(3): 399-404. |
| [11] |
张秀芹, 徐凯. 局部晚期宫颈癌患者同步放化疗后机体成分变化CT定量分析与预后的关系[J]. 中国医学计算机成像杂志, 2021, 27(6): 534-539. |
| [12] |
HALEY M J, WHITE C S, ROBERTS D, et al. Stroke induces prolonged changes in lipid metabolism, the liver and body composition in mice[J]. Transl Stroke Res, 2020, 11(4): 837-850. DOI:10.1007/s12975-019-00763-2 |
| [13] |
HUANG Y, LIU Y, MA Y, et al. Associations of visceral adipose tissue, circulating protein biomarkers, and risk of cardiovascular diseases: a mendelian randomization analysis[J]. Front Cell Dev Biol, 2022, 10: 840866. DOI:10.3389/fcell.2022.840866 |
| [14] |
XU L, CHEN S, XU J, et al. Association of Chinese visceral adiposity index with clinical outcome in patientsafter endovascular thrombectomy[J]. J Stroke Cerebrovasc Dis, 2024, 33(1): 107464. DOI:10.1016/j.jstrokecerebrovasdis.2023.107464 |
| [15] |
CHANG Y, ZHANG L, LI Y, et al. Derivation and validation of a new visceral adiposity index for predicting short-term mortality of patients with acute ischemic stroke in a Chinese population[J]. Brain Sci, 2023, 13(2): 297. DOI:10.3390/brainsci13020297 |
| [16] |
YAN B, YANG J, QIAN L, et al. Effect of genetic liability to visceral adiposity on stroke and its subtypes: a mendelian randomization study[J]. Int J Stroke, 2022, 17(2): 172-179. DOI:10.1177/17474930211006285 |
| [17] |
XU R, HU X, WANG T, et al. Visceral adiposity and risk of stroke: a mendelian randomization study[J]. Front Neurol, 2022, 13: 804851. DOI:10.3389/fneur.2022.804851 |
| [18] |
ZHANG D, HUO W, CHEN W, et al. Association of traditional and novel obesity indicators with stroke risk: findings from the rural Chinese cohort study[J]. Nutr Metab Cardiovasc Dis, 2024, 34(9): 2065-2074. DOI:10.1016/j.numecd.2024.05.001 |
| [19] |
BEŞLER M S, ÇAY N, SAYıN B. Effect of sarcopenia on mortality in acute stroke patients receiving endovascular treatment[J]. Interv Neuroradiol, 2024, 30(5): 728-737. DOI:10.1177/15910199241227465 |
| [20] |
RAVERA B, LOMBARDI C, BELLAVIA S, et al. Temporalis muscle thickness as a predictor of functional outcome afterreperfusion therapies for acute ischemic stroke: a retrospective, cohort study[J]. J Neurol, 2024, 271(9): 6015-6024. |
| [21] |
OHYAMA K, WATANABE M, NOSAKI Y, et al. Correlation between skeletal muscle mass deficit and poor functional outcome in patients with acute ischemic stroke[J]. J Stroke Cerebrovasc Dis, 2020, 29(4): 104623. DOI:10.1016/j.jstrokecerebrovasdis.2019.104623 |
| [22] |
HAN M, LIM I H, HONG S H, et al. Initial stroke severity and discharge outcome in patients with muscle mass deficit[J]. Sci Rep, 2024, 14(1): 1911. |
| [23] |
LINDSTRÖM I, PROTTO S, KHAN N, et al. Association of masseter area and radiodensity with three-month survival after proximalanterior circulation occlusion[J]. J Neurointerv Surg, 2021, 13(1): 25-29. DOI:10.1136/neurintsurg-2020-015837 |
| [24] |
LEE S H, CHOI H, KIM K Y, et al. Appendicular skeletal muscle mass associated with sarcopenia as a predictor of poor functional outcomes in ischemic stroke[J]. Clin Interv Aging, 2023, 18: 1009-1020. |
| [25] |
TUTAL GÜRSOY G, GÖRGÜLÜ Ü, TENGIRŞENK Z, et al. The relationship between temporal muscle thickness and triglyceride glucose index in sarcopenia with mortality and third-month functional outcomes in patientsafter acute stroke[J]. Medicine (Baltimore), 2023, 102(44): e35886. |
| [26] |
NOZOE M, KUBO H, KANAI M, et al. Reliability and validity of measuring temporal muscle thickness as the evaluation of sarcopenia risk and the relationship with functional outcome in older patients with acute stroke[J]. Clin Neurol Neurosurg, 2021, 201: 106444. |
| [27] |
VON GELDERN P, SALAS C, ALVAYAY P, et al. Nutritional assessment by subjective methods versus computed tomography topredict survival in oncology patients[J]. Nutrition, 2021, 84: 111006. |
| [28] |
LIU X, JI W, ZHENG K, et al. The correlation between skeletal muscle index of the L3 vertebral body and malnutritionin patients with advanced lung cancer[J]. BMC Cancer, 2021, 21(1): 1148. |
 2026, Vol. 24
2026, Vol. 24


