| 多模态超声预测乳腺癌腋窝淋巴结转移的临床价值 |
乳腺癌是女性最常见的癌症,也是全球女性因癌症死亡的第二大病因[1]。腋窝淋巴结转移(axillary lymph node metastasis,ALNM)是乳腺癌最常见的转移方式,其状态与治疗和预后密切相关。前哨淋巴结活检是临床评估腋窝淋巴结最常用的方法,但其为侵入性手术,术后可能会出现患肢疼痛、感觉异常和手臂肿胀等并发症。术前早期准确评估腋窝淋巴结状态对治疗方案的选择和预后评估至关重要。超声在乳腺癌筛查中应用广泛,超声造影可清晰显示肿瘤内部的微血流。本研究回顾性分析92例乳腺癌患者的多模态超声特征,探讨其与ALNM的关系,为术前无创预测ALNM提供参考。
1 资料与方法 1.1 一般资料回顾性收集2019年1月至2024年1月我院经病理证实的92例女性乳腺癌患者,均为单侧发病;年龄28~71岁,平均(53.0±10.2)岁;肿瘤最大径0.9~4.8 cm,平均(2.0±1.1)cm。根据术后病理结果分为ALNM组(30例)和无ALNM组(62例)。
纳入标准:①病理确诊为乳腺癌;②行乳腺癌切除术及腋窝淋巴结清扫术;③术前行灰阶超声、彩色多普勒超声及超声造影检查,且资料齐全。排除标准:①合并其他部位恶性肿瘤者;②灰阶超声、彩色多普勒超声或超声造影图像质量差;③术前行新辅助化疗者。本研究经医院伦理委员会批准(批号:WZ2025011),患者均签署知情同意书。
1.2 仪器与方法采用三星RS85超声诊断仪,L3-12A线阵探头,频率3~12 MHz。对比剂采用声诺维(SonoVue),加5 mL生理盐水充分震荡成混悬液备用。患者取仰卧位,双臂上举过头,充分暴露双侧乳腺及腋窝,采集病灶二维灰阶图像及彩色多普勒超声图像。选定病灶最大或血流最丰富切面进入造影模式,经肘静脉团注3 mL混悬液,后立即用5 mL生理盐水冲管,实时动态观察病灶区域显像情况,并储存动态图像,至少3 min。点击Vessel Max,行微血管造影成像,观察对比剂走行顺序,以及微血管形态。
1.3 图像分析参照美国放射学会乳腺超声影像报告与数据系统(breast imaging reporting and data system,BI-RADS)[2]对图像进行分析:①记录肿块位置(左侧、右侧)、象限(外上、外下、内上、内下)、最大径(≤2 cm、>2 cm)、形态(圆形、椭圆形、不规则形,将圆形和椭圆形合并为规则形)、生长方向(平行、不平行)、边缘(光整、不光整,不光整包括模糊、微小分叶、毛刺、成角)、后方回声衰减(无、有)、高回声晕(无、有)、微钙化(无、有)。②采用Adler半定量法[3]评估病灶血流分级。0级:肿块内无血流信号;Ⅰ级:少量血流,见1~2个点状或短棒状血流;Ⅱ级:中量血流,见3~4个点状血流或1条较长血管,其长度接近或超过病灶半径;Ⅲ级:多量血流,见≥ 5个点状血流,或≥ 2条较长血管。其中,0~Ⅰ级为血流不丰富,Ⅱ~Ⅲ级为血流丰富)。③分析超声造影资料,记录增强程度(低增强、等增强、高增强)、增强方向(向心性、非向心性)、增强范围(扩大、不扩大)、灌注缺损(无、有)、边缘呈放射状增强(无、有)、滋养血管(无、有)。由2位工作5年以上的超声医师对图像及视频资料进行分析,意见不一致时,与第3位工作10年以上的高级职称医师讨论分析,最终达成一致。
1.4 统计学方法采用SPSS 26.0软件进行数据分析。计数资料以例(%)表示,单因素分析组间比较行χ2检验或Fisher精确概率检验。多因素分析采用二元logistic回归分析,以有无ALNM为因变量,单因素分析中差异有统计学意义的指标为自变量,建立logistic回归模型,筛选乳腺癌ALNM的独立预测因素。绘制ROC曲线评估预测因素的诊断效能,采用MedCalc软件对AUC行两两比较。以P<0.05为差异有统计学意义。
2 结果 2.1 病理结果ALNM组30个病灶中,浸润性导管癌25个,浸润性导管癌伴导管原位癌3个,混合性癌2个(含浸润性导管癌+浸润性小叶癌1个,含80%黏液癌成分、20%浸润性导管癌成分1个);无ALNM组62个病灶中,浸润性导管癌39个,浸润性导管癌伴导管原位癌14个,导管原位癌6个,黏液癌2个,浸润性微乳头状癌1个。
2.2 ALNM的单因素分析ALNM组血流分级多为Ⅱ~Ⅲ级,增强方向为向心性、边缘呈放射状增强、内部有滋养血管的比例均高于无ALNM组(均P<0.05);2组其他超声特征比较,差异均无统计学意义(均P>0.05)(表 1;图 1,2)。
| 表 1 灰阶超声、彩色多普勒超声、超声造影特征与乳腺癌ALNM关系的单因素分析 |
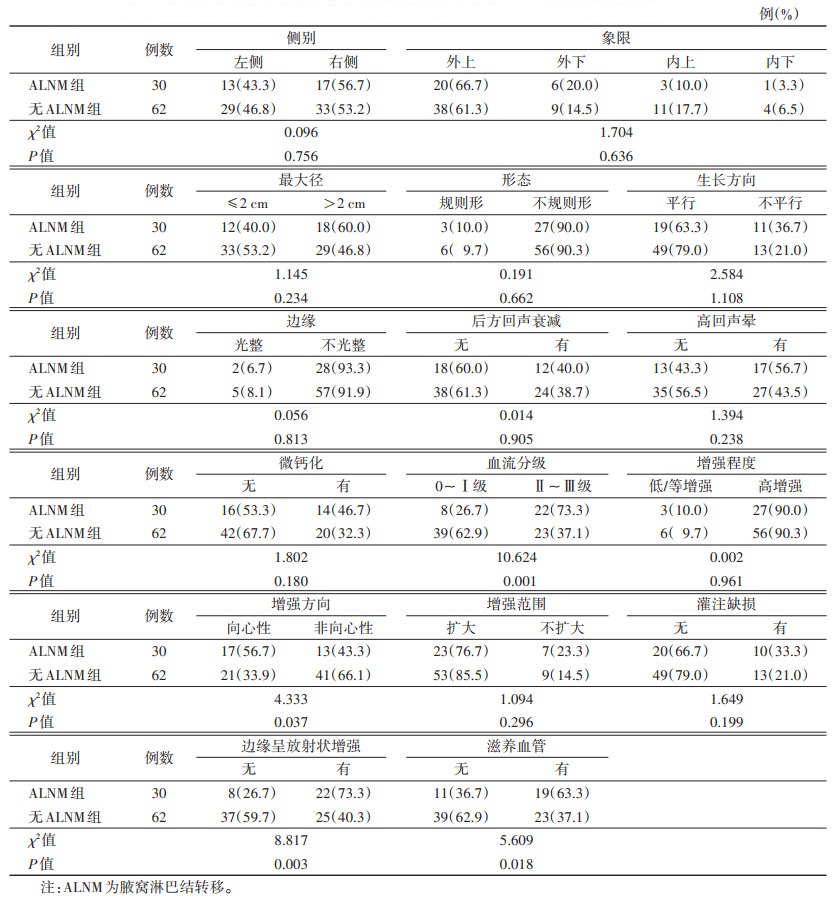 |
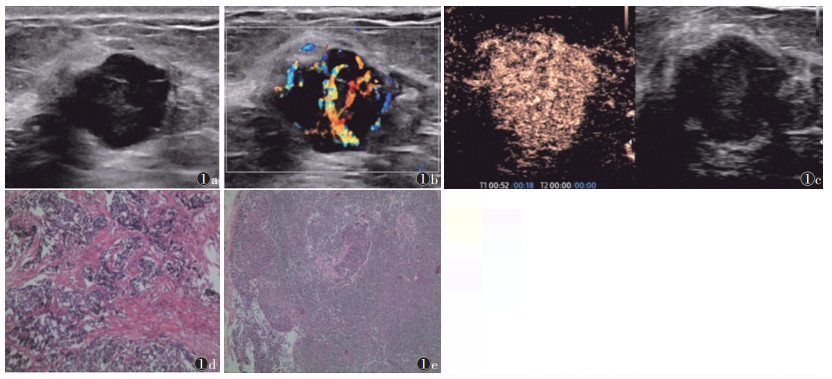 |
| 注:患者,女,53岁。图1a为灰阶超声,示病灶呈低回声,内部回声不均匀,形态不规则,边缘不光整,可见微分叶及毛刺;图1b为彩色多普勒超声,示病灶内见丰富血流信号,血流分级Ⅲ级;图1c为超声造影,示病灶呈不均匀高增强,内见滋养血管,边缘不光整,见放射状血管,增强范围较二维图像扩大;图1d为术后病理,示浸润性导管癌(HE染色,高倍放大);图1e为淋巴结术后病理,示腋窝淋巴结转移(HE染色,低倍放大) 图 1 乳腺癌伴腋窝淋巴结转移典型病例的灰阶超声、彩色多普勒超声、超声造影及病理图像 |
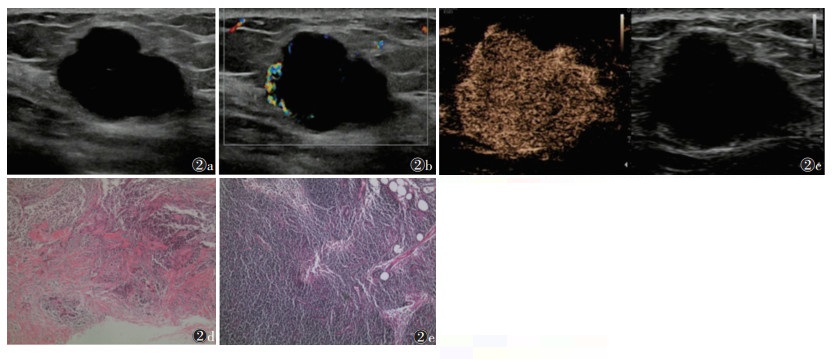 |
| 注:患者,女,56岁。图2a为灰阶超声,示病灶呈低回声,内部回声均匀,形态不规则,边缘模糊,可见微分叶;图2b为彩色多普勒超声,示病灶内见少量血流信号,血流分级Ⅰ级;图2c为超声造影,示病灶呈均匀高增强,形态不规则,增强范围较二维图像无明显扩大;图2d为术后病理,示浸润性导管癌(HE染色,低倍放大);图2e为淋巴结术后病理,示无腋窝淋巴结转移(HE染色,高倍放大) 图 2 乳腺癌无腋窝淋巴结转移典型病例的灰阶超声、彩色多普勒超声、超声造影及病理图像 |
2.3 ALNM的多因素分析
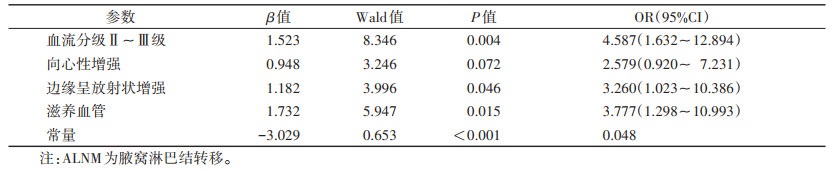
二元logistic回归分析显示,血流分级Ⅱ~Ⅲ级、边缘呈放射状增强、滋养血管均为乳腺癌ALNM的独立预测因素(均P<0.05)(表 2)。
| 表 2 ALNM的二元logistic回归分析 |
 |
2.4 各预测因素的诊断效能
ROC曲线显示,血流分级Ⅱ~Ⅲ级、边缘呈放射状增强、滋养血管预测乳腺癌ALNM的AUC分别为0.697(95%CI 0.592~0.788)、0.603(95%CI 0.496~0.704)、0.665(95%CI 0.559~0.760),三者联合诊断的AUC为0.837(95%CI 0.745~0.906)(图 3)。联合诊断效能高于单一指标诊断,差异均有统计学意义(联合诊断vs.血流分级Ⅱ~Ⅲ级,P=0.002 1;联合诊断vs.边缘呈放射状增强,P=0.000 1;联合诊断vs.滋养血管,P=0.001 3)。
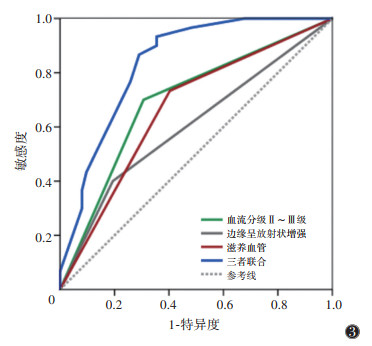 |
| 图 3 多模态超声特征单独及联合诊断腋窝淋巴结转移(ALNM)的ROC曲线 |
3 讨论
腋窝淋巴结状态是决定乳腺癌分期和预后的关键因素,有助于临床选择最佳的治疗方案,因此早期准确评估腋窝淋巴结至关重要。乳腺癌腋窝淋巴结浸润是一个动态病理过程,早期转移不会导致淋巴结大小及结构的实质性变化,此时很难区分转移性和非转移性淋巴结[4]。ALNM与乳腺实质和间质侵袭密切相关[5]。本研究评估乳腺癌原发病灶多模态超声特征与ALNM的相关性,筛选出差异有统计学意义的指标作为乳腺癌ALNM的独立预测因素并评估其诊断效能,以期术前早期预测ALNM。
肿瘤的新生血管形成是乳腺癌生长、侵袭、转移的关键[6]。本研究表明,血流分级Ⅱ~Ⅲ级的乳腺癌患者更易发生ALNM,风险是血流分级0~Ⅰ级的4.587倍。Santamaria等[7]研究显示,肿瘤动脉数量是浸润性乳腺癌ALNM的独立预测因素。肿瘤血供越丰富,Alder血流分级越高,侵袭性越强,更易导致引流区淋巴管浸润破坏,发生转移[8-9]。
超声造影广泛应用于乳腺良恶性病变的诊断,其经肘静脉注射微气泡,增强病灶与周围组织的对比度,清晰显示病灶边缘,帮助评估肿瘤内部微血管情况,对乳腺癌ALNM具有重要诊断价值[10]。本研究显示,病灶边缘呈放射状增强、内部含滋养血管是乳腺癌ALNM的独立预测因素,与Yu等[5, 11]研究结果一致。既往研究表明,超声造影呈放射状增强、可见滋养血管的乳腺癌病灶中微血管密度较高,血管内皮生长因子多呈高表达[12-13]。微血管密度增高易发生ALNM,血管内皮生长因子是重要的血管活性因子,可诱导病灶内大量新生血管形成[14],新生血管向周围组织延伸,造影时病灶边缘可出现放射状血流,新生血管变粗,走行扭曲,可形成粗大的滋养血管,肿瘤细胞快速增殖,恶性程度增高,侵袭性增加。
Guo等[15]研究认为,乳腺癌病灶呈向心性增强时易发生ALNM,原因可能是肿瘤生长分为无血管期和血管期,在无血管期,肿瘤依赖周围组织供血,直径多为1~2 mm,处于“休眠状态”;在血管期,肿瘤内新生血管形成,新生血管可促进肿瘤细胞生长,为其转移提供途径,此时血供方式转为向中心组织汇聚,超声造影呈向心性增强[16-17]。本研究单因素分析中对比剂呈向心性增强时发生ALNM的比例更高(56.7%),但多因素分析中差异无统计学意义。超声造影呈向心性增强与乳腺癌ALNM的关系尚需进一步研究证实。
本研究的局限性:①为单中心研究,可能存在选择偏倚,今后将行多中心研究。②样本量相对较小,且病灶病理类型不一致,可能对超声特征存在影响,今后将进一步扩大样本量,对不同病理类型的病灶进行更深入研究。③超声造影选取病灶最大或血流最丰富切面,可能不足以全面评估微循环特点。
综上所述,血流分级Ⅱ~Ⅲ级、边缘呈放射状增强、滋养血管是乳腺癌ALNM的独立预测因素,联合上述指标对乳腺癌ALNM具有较高的预测价值,可为临床治疗及预后评估提供参考。
| [1] |
TORRE L A, SIEGEL R L, WARD E M, et al. Global cancer incidence and mortality rates and trends -- an update[J]. Cancer Epidemiol Biomarkers Prev, 2016, 25(1): 16-27. DOI:10.1158/1055-9965.EPI-15-0578 |
| [2] |
MENDELSON E B, BÄHM-VÉLEZ M, BERG W A, et al. ACR BI-RADS ultrasound 2013[M]. Reston: American College of Radiology, 2013: 35.
|
| [3] |
ADLER D D, CARSON P L, RUBIN J M, et al. Doppler ultrasound color flow imaging in the study of breast cancer: preliminary findings[J]. Ultrasound Med Biol, 1990, 16(6): 553-559. DOI:10.1016/0301-5629(90)90020-D |
| [4] |
ZHANG H, SUI X, ZHOU S, et al. Correlation of conventional ultrasound characteristics of breast tumors with axillary lymph node metastasis and Ki-67 expression in patients with breast cancer[J]. J Ultrasound Med, 2019, 38(7): 1833-1840. DOI:10.1002/jum.14879 |
| [5] |
YU X, HAO X, WAN J, et al. Correlation between ultrasound appearance of small breast cancer and axillary lymph node metastasis[J]. Ultrasound Med Biol, 2018, 44(2): 342-349. DOI:10.1016/j.ultrasmedbio.2017.09.020 |
| [6] |
GAO X, LUO W, HE L, et al. Nomogram models for stratified prediction of axillary lymph node metastasis in breast cancer patients (cN0)[J]. Front Endocrinol (Lausanne), 2022, 13: 967062. DOI:10.3389/fendo.2022.967062 |
| [7] |
SANTAMARIA G, VELASCO M, FARRE X, et al. Power doppler sonography of invasive breast carcinoma: does tumor vascularization contribute to prediction of axillary status?[J]. Radiology, 2005, 234(2): 374-380. DOI:10.1148/radiol.2342031252 |
| [8] |
PARK A Y, KWON M, WOO O H, et al. A prospective study on the value of ultrasound microflow assessment to distinguish malignant from benign solid breast masses: association between ultrasound parameters and histologic microvessel densities[J]. Korean J Radiol, 2019, 20(5): 759-772. DOI:10.3348/kjr.2018.0515 |
| [9] |
WANG L, LI J, QIAO J, et al. Establishment of a model for predicting sentinel lymph node metastasis in early breast cancer based on contrast-enhanced ultrasound and clinicopathological features[J]. Gland Surg, 2021, 10(5): 1701-1712. DOI:10.21037/gs-21-245 |
| [10] |
LIU X, WANG M, WANG Q, et al. Diagnostic value of contrast-enhanced ultrasound for sentinel lymph node metastasis in breast cancer: an updated meta-analysis[J]. Breast Cancer Res Treat, 2023, 202(2): 221-231. DOI:10.1007/s10549-023-07063-2 |
| [11] |
VRAKA I, PANOURGIAS E, SIFAKIS E, et al. Correlation between contrast-enhanced ultrasound characteristics (qualitative and quantitative) and pathological prognostic factors in breast cancer[J]. In Vivo, 2018, 32(4): 945-954. DOI:10.21873/invivo.11333 |
| [12] |
DU J, LI F H, FANG H, et al. Correlation of real-time gray scale contrast-enhanced ultrasonography with microvessel density and vascular endothelial growth factor expression for assessment of angiogenesis in breast lesions[J]. J Ultrasound Med, 2008, 27(6): 821-831. DOI:10.7863/jum.2008.27.6.821 |
| [13] |
LI W, ZHOU Q, XIA S, et al. Application of contrast-enhanced ultrasound in the diagnosis of ductal carcinoma in situ: analysis of 127 cases[J]. J Ultrasound Med, 2020, 39(1): 39-50. DOI:10.1002/jum.15069 |
| [14] |
KONG D, ZHOU H, NEELAKANTAN D, et al. VEGF-C mediates tumor growth and metastasis through promoting EMT-epithelial breast cancer cell crosstalk[J]. Oncogene, 2021, 40(5): 964-979. DOI:10.1038/s41388-020-01539-x |
| [15] |
GUO Y, SONG Q, PAN Q. Correlation analysis between rim enhancement features of contrast-enhanced ultrasound and lymph node metastasis in breast cancer[J]. Am J Transl Res, 2021, 13(6): 7193-7199. |
| [16] |
杨雁雯, 周伟, 李伟伟, 等. 小乳腺癌的超声造影特征与腋窝淋巴结转移的相关性研究[J]. 中国超声医学杂志, 2023, 39(8): 867-870. |
| [17] |
NIU Z, XIAO M, MA L, et al. The value of contrast-enhanced ultrasound enhancement patterns for the diagnosis of sentinel lymph node status in breast cancer: systematic review and meta-analysis[J]. Quant Imaging Med Surg, 2022, 12(2): 936-948. DOI:10.21037/qims-21-416 |
 2025, Vol. 23
2025, Vol. 23


