| 临床-CT特征模型对耐多药肺结核的预测价值 |
耐多药肺结核(multidrug-resistant pulmonary tuberculosis,MDR-PTB)是指患者感染的结核分枝杆菌(mycobacterium tuberculosis,MTB)经体外药物敏感性试验(drug sensitive test,DST)证实至少对异烟肼和利福平耐药的结核病[1-2]。MDR-PTB是全球范围内的传染病,由于不能早期发现治疗,使其难以控制,对人类健康造成严重威胁。《2024年全球结核病报告》[3]显示,1年内新增MDR-PTB或利福平耐药结核病患者有40万例,我国约2.9万例。目前,DST仍是检测肺结核是否耐药的常用方法及金标准,但MTB培养耗时长(数周或数月),难以达到临床快速诊断的要求[4-5]。虽然越来越多的分子检测技术应用于临床,但当标本中MTB含量很少时会出现假阴性,且分子检测技术费用昂贵,具有一定局限性[6-7]。胸部CT检查在肺结核临床诊断及疗效判断中应用广泛,但文献报道的大多是耐药肺结核的影像学特征,对MDR-PTB的影像学特征研究较少。因此,本研究拟构建基于临床及胸部CT特征的MDR-PTB预测模型,旨在为临床提供一种无创、便捷、有效预测MDR-PTB的方法,为该病的早诊早治提供支持。
1 资料与方法 1.1 一般资料回顾性收集2019年1月至2023年12月我院收治的肺结核患者430例,其中MDR-PTB患者223例(MDR-PTB组),敏感性肺结核(DS-PTB)患者207例(DS-PTB组)。纳入标准:确诊为肺结核且有DST结果。排除标准:①临床资料或CT资料不完整;②CT图像质量差,影响病变观察及分析。收集患者的年龄、性别、治疗类型、咳嗽、咳痰、咯血、发热、胸痛、胸闷气促等资料。本研究经医院伦理委员会审批(批号:KLLY-2023-042),患者均知情同意。
1.2 仪器与方法采用Siemens Somatom Definition AS128 MSCT或Siemens Somatom Definition Flash双源CT。扫描参数:100~120 kV,120 mAs,准直器128×0.6 mm,螺距0.6,矩阵512×512,层厚5 mm,1 mm薄层重建,肺窗窗宽1 200 HU、窗位-600 HU,纵隔窗窗宽350 HU、窗位50 HU,标准算法重建。
1.3 图像分析由2位分别具有5、10年工作经验的胸部CT影像诊断医师在不知患者是否耐多药的情况下,分别判读CT图像,意见分歧时协商达成一致。分析以下胸部CT表现:①肺内病变(纤维化病变、钙化等);②气管性病变(支气管播散、肺不张等);③累及总肺叶数;④空洞(空洞并液平、厚壁空洞、多发空洞);⑤胸膜病变(胸膜增厚、包裹性积液等);⑥病情进展。
1.4 统计学分析采用SPSS 29.0软件进行统计分析。计数资料以例(%)表示。满足正态分布的连续变量组间比较行独立样本t检验,分类变量行χ2检验。2组临床及胸部CT特征行单因素分析,将肺结核是否耐多药状态作为因变量,2组间差异有统计学意义的特征作为自变量行多因素logistic回归分析。绘制ROC曲线评价该回归方程模型预测效能。采用Hosmer-Lemeshow检验验证模型校准度。以P<0.05为差异有统计学意义。
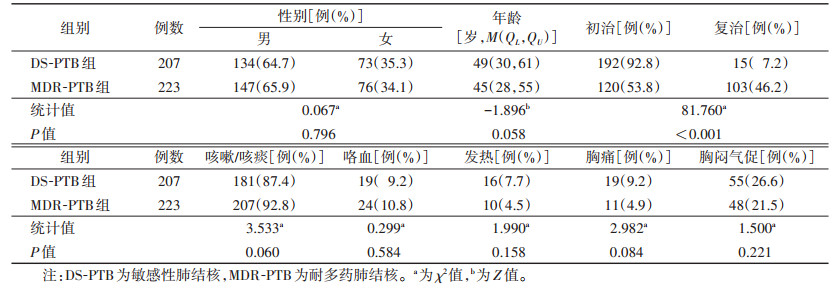
2 结果 2.1 2组临床资料比较MDR-PTB组复治率为46.2%(103/223),DS-PTB组为7.2%(15/207),差异有统计学意义(P<0.05);2组性别、年龄等差异均无统计学意义(均P>0.05)(表 1)。
| 表 1 2组临床资料比较 |
 |
2.2 2组胸部CT表现比较
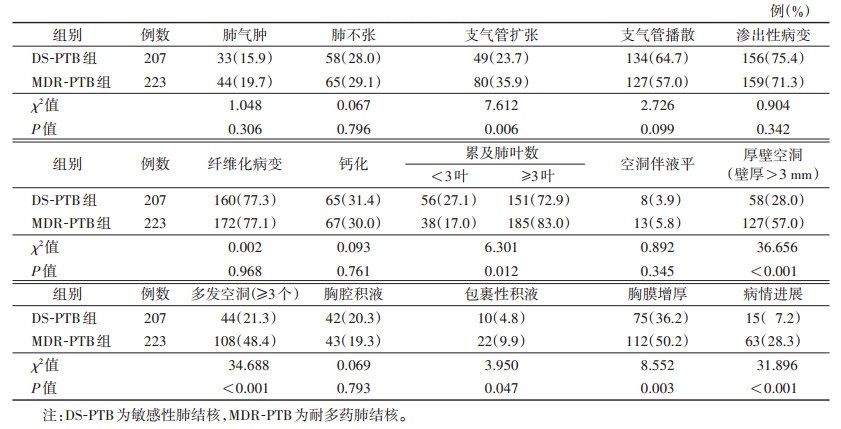
MDR-PTB组支气管扩张、病变累及肺叶≥3叶、厚壁空洞(壁厚>3 mm)、多发空洞(≥ 3个)、包裹性积液、胸膜增厚、病情进展情况均较DS-PTB组高,差异均有统计学意义(均P<0.05)(图 1a,1b);肺气肿、肺不张、支气管播散、渗出性病变、纤维化病变、钙化、空洞伴液平、胸腔积液情况差异均无统计学意义(均P>0.05)(表 2)。
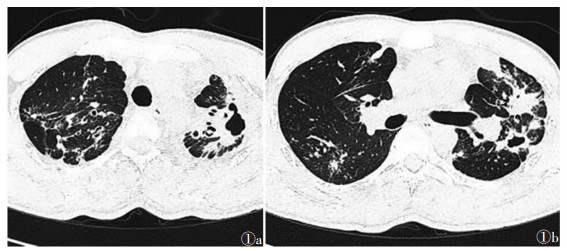 |
| 注:患者,男,32岁,复治MDR-PTB。图 1a,1b 为CT平扫示双肺多肺叶浸润性病变,伴多发性空洞形成(部分呈厚壁特征),以及广泛支气管扩张改变 图 1 耐多药肺结核(MDR-PTB)的CT图像 |
| 表 2 2组胸部CT表现 |
 |
2.3 MDR-PTB的多因素logistic回归分析
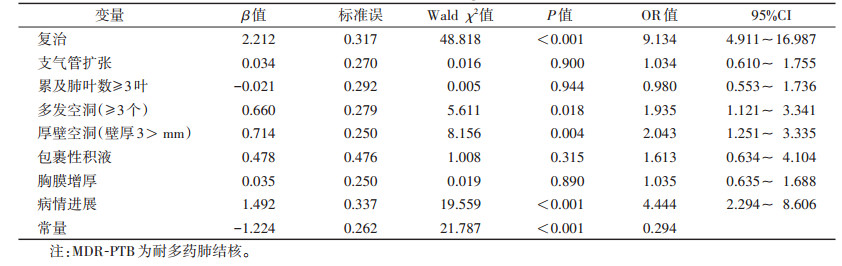
多因素logistic回归分析显示,复治、多发空洞、厚壁空洞、病情进展均为MDR-PTB的独立危险因素(表 3)。构建logistic回归方程:P=
| 表 3 MDR-PTB的多因素logistic回归分析 |
 |
2.4 ROC曲线分析
绘制logistic回归方程模型(临床-CT特征模型)的ROC曲线,其AUC为0.799,95%CI为0.756~0.841(图 2)。当约登指数为0.508时,临界值为0.570,模型特异度为89.9%,敏感度为61.0%,阳性预测值为76.8%,阴性预测值为72.6%。Hosmer-Lemeshow检验显示,χ2=6.209,P=0.624,表明该预测模型校准度及预测效能良好。
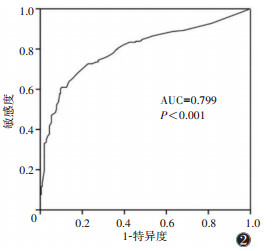 |
| 图 2 临床-CT特征模型预测MDR-PTB的ROC曲线 |
3 讨论
MDR-PTB具有治疗周期长、费用高、疗效差、病情反复等特点,是全球结核病控制的重点[8]。本研究发现,复治是发生MDR-PTB的关键因素,初治患者治疗不规律、方案不合理、依从性差等使免疫力下降,结核菌株大量繁殖导致复治时更易演变成MDR-PTB。支气管扩张与胶原蛋白沉积、纤维瘢痕形成有关,MDR-PTB抗结核治疗时间长,肺组织受损严重,肺纤维化牵拉易导致支气管扩张、扭曲[9]。本研究中MDR-PTB的支气管扩张检出率高于DS-PTB(P<0.05),与Du等[10-11]研究结果相似。本研究中MDR-PTB患者累及肺叶≥3叶更多,与文献[12]报道相符。MDR-PTB一般病程较长,治疗效果较DS-PTB差,且耐多药结核菌株生存能力更强,易在肺叶播散,肺部组织反复受到破坏。空洞在MDR-PTB中的检出率高于在DS-PTB中[13-14]。MDR-PTB空洞内MTB载量高,菌株毒力强,对肺组织破坏力大,易形成多发空洞。本研究中,MDR-PTB组更易出现≥3个空洞,与文献[15]结果一致。另外,本研究MDR-PTB组厚壁空洞的检出率明显高于DS-PTB组,与文献[16]报道一致;考虑是结核空洞壁具屏障作用,且空洞周围血供较差,尤其是厚壁空洞,可能会抑制抗结核药物渗透,难以达到有效抑菌及杀菌浓度,致使空洞病灶内反复持续排菌,逐步诱发形成MDR-PTB。本研究中,包裹性积液及胸膜增厚在MDR-PTB组的检出率更高,原因是MDR-PTB的MTB载量高,更多细菌进入胸膜腔,发生迟发型超敏反应而产生炎症,最终形成胸腔积液[17]。包裹性胸腔积液中纤维蛋白附着于胸膜上或肉芽组织增生,导致胸膜增厚。本研究中,MDR-PTB组病情进展占比高于DS-PTB组,考虑原因为MDR-PTB患者感染通常较严重,肺组织破坏较严重,不易好转。
本研究多因素logistic回归分析显示,复治、多发空洞、厚壁空洞、病情进展均为MDR-PTB的独立危险因素。基于此建立的回归方程模型显示,AUC为0.799,特异度为89.9%,敏感度为61.0%,对应回归模型预测最佳临界值为0.570,提示该模型对于预测肺结核患者产生耐多药具有一定的诊断价值。
本研究存在的不足:①为单中心回顾性分析,样本量偏小,可能产生选择偏倚。后续将通过多中心协作扩大样本量,并实施前瞻性研究方案以提高证据等级。②仅采用临床及胸部CT特征构建模型,后续将结合MDR-PTB的CT影像组学特征建立更全面的预测模型。
综上所述,MDR-PTB与DS-PTB的临床及胸部CT表现具有一定的差异性,当复治、多发空洞、厚壁空洞、病情进展等多种表现并存时高度提示为MDR-PTB;临床-CT特征模型可为MDR-PTB患者早期诊断提供影像学依据,有助于患者及时治疗。
| [1] |
ZHANG S X, QIU L, LI C, et al. Efficacy of integrating short-course chemotherapy with Chinese herbs to treat multi-drug resistant pulmonary tuberculosis in China: a study protocol[J]. Infect Dis Poverty, 2021, 10(1): 131. DOI:10.1186/s40249-021-00913-5 |
| [2] |
WULANDARI D A, HARTATI Y W, IBRAHIM A U, et al. Multidrug-resistant tuberculosis[J]. Clin Chim Acta, 2024, 559: 119701. DOI:10.1016/j.cca.2024.119701 |
| [3] |
World Health Organization. Global tuberculosis report 2024[R/OL]. (2024-10-29)[2025-04-15]. https://iris.who.int/bitstream/handle/10665/379339/9789240101531.
|
| [4] |
FARHA M, COX H, GHANE M, et al. Drug-resistant tuberculosis: a persistent global health concern[J]. Nat Rev Microbiol, 2024, 22(10): 617-635. DOI:10.1038/s41579-024-01025-1 |
| [5] |
DONG B, HE Z, LI Y, et al. Improved conventional and new approaches in the diagnosis of tuberculosis[J]. Front Microbiol, 2022, 13: 924410. DOI:10.3389/fmicb.2022.924410 |
| [6] |
NAIDO K, DOOKIE N. Can the GeneXpert MTB/XDR deliver on the promise of expanded, near-patient tuberculosis drug-susceptibility testing?[J]. Lancet Infect Dis, 2022, 22(4): e121-e127. DOI:10.1016/S1473-3099(21)00613-7 |
| [7] |
IEM V, BIMBA J S, SANTOS V S, et al. Pooling sputum testing to diagnose tuberculosis using xpert MTB/RIF and xpert ultra: a cost-effectiveness analysis[J]. BMC Infect Dis, 2023, 23(1): 341. DOI:10.1186/s12879-023-08330-9 |
| [8] |
PERRI F M, WOODWAR N, PHILLIPS P P, et al. Radiological cavitation, sputum mycobacterial load and treatment response in pulmonary tuberculosis[J]. Int J Tuberc Lung Dis, 2010, 14(12): 1596-1602. |
| [9] |
SONG Q, GUO X, ZHANG L, et al. New approaches in the classification and prognosis of sign clusters on pulmonary CT images in patients with multidrug-resistant tuberculosis[J]. Front Microbiol, 2021, 12: 714617. DOI:10.3389/fmicb.2021.714617 |
| [10] |
DU L, ZHANG Y, LV X, et al. Prevalence of multidrug-resistant tuberculosis in dalian, china: a retrospective study[J]. Infect Drug Resist, 2021, 14: 1037-1047. DOI:10.2147/IDR.S294611 |
| [11] |
龚磊, 何江涛, 王珊珊. 耐多药肺结核临床及影像特征分析[J]. 实用医技杂志, 2024, 31(8): 544-548. |
| [12] |
王剑, 付婷, 吕菊芬, 等. 耐多药/利福平耐药与利福平敏感肺结核患者胸部影像学特征分析[J]. 宁夏医学杂志, 2024, 46(12): 1089-1091. |
| [13] |
KIM W, LEE K S, KIM H S, et al. CT and microbiologic follow-up in primary multidrug-resistant pulmonary tuberculosis[J]. Acta Radiol, 2016, 57(2): 197-204. DOI:10.1177/0284185115575196 |
| [14] |
许金红, 杨松, 张立新, 等. 中国耐多药结核病发病危险因素的Meta分析[J]. 中国防痨杂志, 2019, 41(12): 1301-1309. |
| [15] |
LI C H, FAN X, LV S X, et al. Clinical and computed tomography features associated with multidrug-resistant pulmonary tuberculosis: a retrospective study in China[J]. Infect Drug Resist, 2023, 16: 651-659. DOI:10.2147/IDR.S394071 |
| [16] |
WANG Y X J, CHUNG M J, SKRAHIN A, et al. Radiological signs associated with pulmonary multi-drug resistant tuberculosis: an analysis of published evidences[J]. Quant Imaging Med Surg, 2018, 8(2): 161-173. DOI:10.21037/qims.2018.03.06 |
| [17] |
CHUCHOTTAWORN C, THANACHARTWE V, SANGSA- YUN P, et al. Risk factors for multidrug-resistant tuberculosis among patients with pulmonary tuberculosis at the central chest institute of thailand[J]. PLoS One, 2015, 10(10): e0139986. DOI:10.1371/journal.pone.0139986 |
 2025, Vol. 23
2025, Vol. 23


