| 双层探测器光谱CT定量参数鉴别纵隔淋巴结结核与非小细胞肺癌纵隔淋巴结转移瘤的价值 |
2. 山东大学齐鲁医学院公共卫生学院生物统计学系, 山东 济南 250012
2. Department of Biostatistics, School of Public Health of Cheeloo Collage of Medicine in Shandong University, Jinan 250012, China
《2024年全球结核病报告》[1]显示,我国仍是全球第三大结核病高负担国家。淋巴结结核是纵隔淋巴结肿大最常见的感染性原因,也是肺外结核中最常见的类型[2]。而淋巴结转移瘤是纵隔淋巴结肿大最常见的肿瘤性原因,其中以非小细胞肺癌最常见[3-4]。当纵隔淋巴结肿大、肺内无明显病灶或病灶不典型时,淋巴结的性质判断较困难。近年来,随着能谱CT技术的发展,能谱扫描及图像后处理可对病变进行多参数、定量分析,在客观评估病变的组织特性及功能状态方面具有较大的应用潜力,但在鉴别纵隔淋巴结结核和纵隔淋巴结转移瘤方面应用较少。本研究采用双层探测器光谱CT(spectral detector CT,SDCT)探讨纵隔淋巴结结核和非小细胞肺癌纵隔淋巴结转移瘤定量参数的差异。
1 资料与方法 1.1 一般资料回顾性纳入2020年1月至2022年12月在山东省胸科医院和山东省公共卫生临床中心行胸部SDCT检查并经临床确诊的患者89例共205个淋巴结,其中纵隔淋巴结结核41例共97个淋巴结(结核组),非小细胞肺癌纵隔淋巴结转移瘤48例共108个淋巴结(转移瘤组)。
纳入标准:①纵隔淋巴结经穿刺活检或手术病理证实为非小细胞肺癌淋巴结转移瘤,或抗肿瘤治疗后淋巴结缩小30%以上[5],且SDCT扫描前未行放化疗;②纵隔淋巴结经手术切除或穿刺后病理检查、实验室检查确诊为结核,或经临床和影像综合诊断并经抗结核药物治疗后SDCT显示缩小30%以上;③最短径>10 mm的纵隔淋巴结。排除标准:①淋巴结内有钙化;②肺结核合并肺癌;③临床资料证实可能存在合并混合感染;④CT图像质量差。本研究经山东省公共卫生临床中心伦理委员会批准(批号:GWLCZXEC-SOP-K-2024-162)。
1.2 仪器与方法采用Philips IQon光谱CT扫描仪,行胸部横断面平扫及增强扫描,扫描范围从肺尖至肺底。患者平卧,双手上举,深吸气后在屏气状态下扫描。扫描参数:120 kV,管电流采用自动调制技术(144~344 mAs),转速0.5 s,螺距0.8,层厚5 mm,重建层厚1 mm,层距1 mm。增强扫描经肘正中静脉注射对比剂碘克沙醇注射液(碘含量320 mg/mL),剂量1.5 mL/kg体质量,流率3~4 mL/s,后注射20 mL生理盐水。采用对比剂跟踪触发扫描,触发阈值150 HU,主动脉期增强扫描后,延迟90 s行静脉期扫描。
1.3 图像分析由2位具有10年以上淋巴结病变诊断经验的放射科医师共同对淋巴结形态学特征进行评估,并测量数值,意见不一致时,由1位具有15年以上淋巴结病变诊断经验的放射科医师评估。
在Philips星云V10后处理工作站(ISP,IntelliSpace Portal)对平扫、增强扫描光谱基图像进行后处理,获得碘密度(iodine density,ID)图、有效原子序数(effective atomic number,Zeff)图及40~200 keV虚拟单能级图像(virtual monoenergetic image,VMI)。利用compare功能观察并记录数据,保证3期扫描测量位置尽量在同一层面,ROI边缘与测量区边缘最短距离≥ 1 mm,面积≥ 10 mm3。
淋巴结最大层面数据测量:在动脉期40 keV能量图像上确定淋巴结最大层面,利用圆形工具尽量大地勾画病灶ROI,并复制至平扫及静脉期相同keV的图像上,记录同一层面40、70、100 keV的CT值。修改模式为ID图和Zeff图,记录相应的定量参数值。同时,利用圆形工具于同层面主动脉或颈动脉勾画ROI,得到相应的ID和Zeff,计算标准化碘密度(normalized iodine density,nID)、标准化有效原子序数(normalized effective atomic number,nZeff),以及40~70 keV、70~100 keV的能谱曲线斜率(λ40~70、λ70~100)。公式分别为:nID=最大层面淋巴结的ID/相同层面主动脉ID;nZeff=最大层面淋巴结的Zeff/相同层面主动脉Zeff;λ40~70=(CT值40 keV-CT值70 keV)/30;λ70~100=(CT值70 keV-CT值100 keV)/30。
淋巴结内高密度区数据测量:在动脉期40 keV能量图像上确定淋巴结高密度区的最大层面(高密度区域定义为动脉期及静脉期所选区域较淋巴结内其他区域密度明显增高),利用圆形工具尽量大地勾画病灶高密度区ROI,并将ROI复制至平扫及静脉期相同keV的图像上,然后用与最大层面数据测量相同的方法记录各期的40、70、100 keV的CT值,以及ID、Zeff,计算nID、nZeff、λ40~70和λ70~100。
淋巴结内低密度区数据测量:在动脉期40 keV能量图像上确定淋巴结低密度区的最大层面(动脉期及静脉期所选区域较淋巴结内其他区域均为低密度),后记录、计算各参数方法同最大层面数据测量。
1.4 统计学分析采用SPSS 22.0软件分析数据。计数资料以构成比(%)表示,组间比较行Pearson χ2检验或Fisher精确检验。计量资料先行Shapiro-Wilk正态性检验,满足正态分布时以x±s表示,组间比较行独立样本t检验;不满足正态分布时以M(P25,P75)表示,组间比较行Mann-Whitney U检验。定义肺癌纵隔淋巴结转移瘤为阳性、淋巴结结核为阴性,结核组与转移瘤组间动脉期、静脉期淋巴结SDCT参数中差异有统计学意义的参数分别行诊断试验。检验水准α为0.05。
2 结果 2.1 2组一般资料比较结核组41例中,男17例(41.46%),女24例(58.54%);年龄15~66岁,平均(33.50±13.19)岁,中位年龄33.50岁。转移瘤组48例中,男33例(68.75%),女15例(31.25%);年龄21~81岁,平均(61.15±9.98)岁,中位年龄63岁。2组性别、年龄比较差异均有统计学意义(
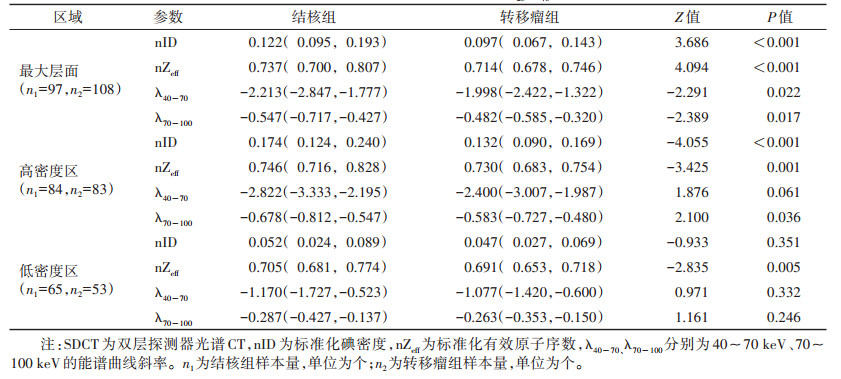
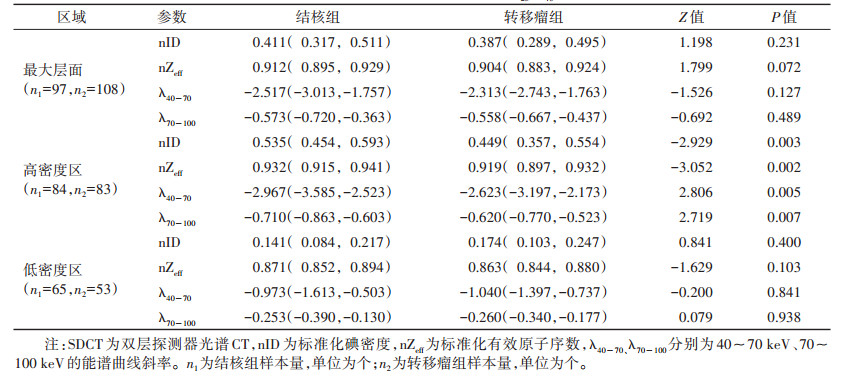
动脉期,2组淋巴结最大层面的nID、nZeff、λ40~70、λ70~100,淋巴结高密度区的nID、nZeff、λ70~100,以及淋巴结低密度区的nZeff差异均有统计学意义(均P<0.05)(表 1)。静脉期,2组淋巴结高密度区的nID、nZeff、λ40~70和λ70~100差异均有统计学意义(均P<0.05)。静脉期,2组淋巴结最大层面和低密度区各参数差异均无统计学意义(均P>0.05)(表 2)。平扫2组各参数差异均无统计学意义(均P>0.05)。
| 表 1 2组动脉期SDCT参数比较[M(P25,P75)] |
 |
| 表 2 2组静脉期SDCT参数比较[M(P25,P75)] |
 |
2.3 SDCT各参数的鉴别诊断效能
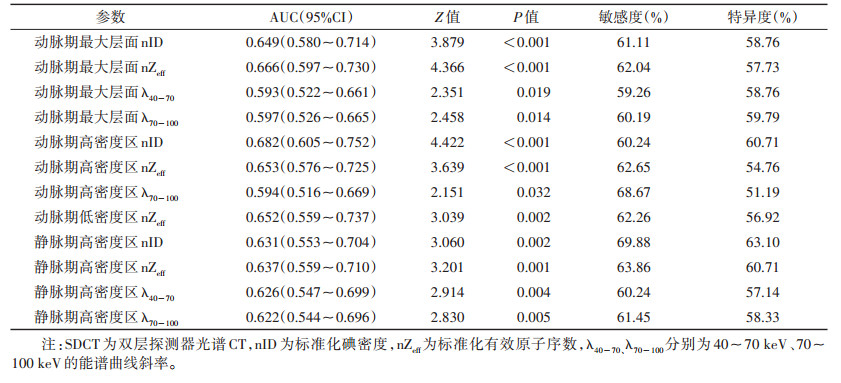
动脉期淋巴结内高密度区nID诊断非小细胞肺癌纵隔淋巴结转移瘤的AUC最高,为0.682,敏感度和特异度分别为60.24%和60.71%;而静脉期淋巴结内高密度区nID的AUC为0.631,敏感度和特异度分别为69.88%和63.10%(图 1,表 3)。
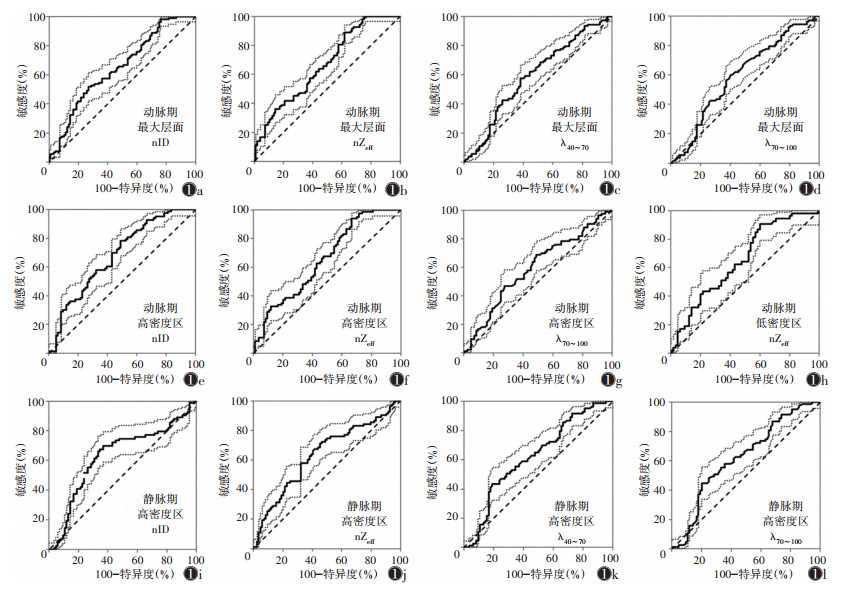 |
| 注:nID为标准化碘密度,nZeff为标准化有效原子序数,λ40~70、λ70~100分别为40~70 keV、70~100 keV的能谱曲线斜率 图 1 双层探测器光谱CT(SDCT)参数诊断非小细胞肺癌纵隔淋巴结转移瘤的ROC曲线(95%CI) |
| 表 3 SDCT参数诊断试验结果 |
 |
3 讨论
纵隔淋巴结结核常表现为多个病理时期的病变共存,导致其影像学特征复杂[6-7],且非典型结核性淋巴结的临床及影像学特征与淋巴转移瘤相似,因此仅靠常规CT检查很难区分[8]。淋巴结转移瘤肿瘤细胞大量迅速增殖导致血管受压、扭曲、血栓形成,使得淋巴结内出现缺血坏死区域,但淋巴结内的肿瘤细胞可诱导新血管生成,因此转移淋巴结中表现为高血供[8]。动脉期主要反映组织的血流灌注情况,静脉期主要反映组织的血流廓清能力,而这也是CT不同扫描时相表现不同的主要原因,因此本研究基于双时相影像特征进行分析。研究表明,淋巴结结核及淋巴结转移瘤的血供灌注模式均以向心性灌注为主,其中结核性淋巴结出现率为68.4%~80.4%[9-10],淋巴结转移瘤为80.3%~92.5%[9, 11]。Rizzo等[12]发现,不同区域转移性和非转移性淋巴结中的碘含量差异一致,与淋巴结的解剖部位无关。
穿刺活检或术后病理组织检查及细菌学检查是淋巴结结核的诊断金标准[6-7],然而,在某些情况下,两者无法进行,影响诊断。光谱CT作为第3代能谱CT成像,可对病变进行多参数定量分析,在客观评估病变组织特性及功能状态方面具有显著优势[13]。
碘是CT增强扫描对比剂的主要成分,通过对组织碘含量的定量分析,可有效反映组织器官的血供状况。能谱CT碘密度图能排除其他元素的影响,仅显示碘密度,能定量评价组织间血供的差异[13]。nID通过标准化处理能减少研究对象之间碘分布的生理波动,从而减少变异性。当单能级水平无限接近于碘K缘(33.2 keV)时,碘急剧衰减,碘等高原子序数物质的CT值相应明显增高[14],从而进一步增加病灶与背景组织的强化对比度。因此,本研究选择SDCT在40 keV的低能级图像上划分淋巴结内的高密度区及低密度区,结果发现,结核组与转移瘤组淋巴结高密度区的动脉期及静脉期nID差异均有统计学意义,而低密度区的动脉期及静脉期nID差异均无统计学意义。原因是低密度区主要包括无血供的液化坏死或干酪坏死区及部分血供较少的区域,动脉期则较好反映了淋巴结的动脉血供情况。另外,结核组淋巴结高密度区动脉期及静脉期的nID大于转移瘤组,可能是由于淋巴结结核的供血血管是结构完整的成熟血管,而淋巴结转移瘤的供血血管主要是由不成熟单层内皮细胞构成的肿瘤新生血管[12]。Chen等[15]研究发现,非转移性淋巴结的微血管密度远高于转移性淋巴结,是肿瘤原发病灶的1.4倍。
Zeff是光谱CT另一个重要功能参数,表示组成组织元素的原子序数组合。Zeff通过计算不同能量下的密度系数之比,消除了对材料密度的依赖,尤其是对CT值相近的物质,利用Zeff可对物质进行更准确分析[16]。本研究中结核组动脉期最大层面、高密度区及低密度区的nZeff均大于转移瘤组;2组静脉期仅高密度区的nZeff比较差异有统计学意义;2组平扫的nZeff差异无统计学意义。增强扫描后2组间的nZeff差异显示了不同性质淋巴结物质组成的不同。
能谱CT扫描还可进一步将组织间衰减系数的差异以特有的能谱衰减曲线形式表现出来,以更准确地分析组织的衰减特征[13]。平扫时λ主要反映组织成分的差异,增强扫描后则通过不同物质中对比剂的剂量对其进行区分。本研究中,2组淋巴结高密度区的动脉期λ70~100,以及高密度区的静脉期λ40~70与λ70~100差异均有统计学意义;而淋巴结低密度区动脉期及静脉期的λ40~70、λ70~100差异均无统计学意义;反映了淋巴结结核和淋巴结转移瘤不同的组织衰减特性,尤其是静脉期的差异更明显,可能是随时间延长,结核和肿瘤不同组织的血流廓清能力不同,加大了组织间衰减系数的差异,而低密度区病变由于是坏死或低血供部分,组织间衰减系数差异不明显。
本研究存在的不足:①样本量较小,可能对结果造成一定影响;②人工勾画病灶,存在主观性;③未行病理分析,对结果的解释不深入等,有待今后进一步分析。
综上所述,纵隔淋巴结结核和非小细胞肺癌纵隔淋巴结转移瘤的SDCT动脉期及静脉期的部分定量参数存在差异,这对两者的鉴别诊断具有一定价值。
| [1] |
World Health Organization. Global tuberculosis Report 2024[R/OL]. (2024-10-29)[2025-05-02]. https://iris.who.int/bitstream/handle/10665/379339/9789240101531.
|
| [2] |
SIVARATNAM L, NAWI A M, ABDUL MANAF M R. An evidence-based clinical pathway for the diagnosis of tuberculous lymphadenitis: a systematic review[J]. Int J Mycobacteriol, 2020, 9(2): 107-115. DOI:10.4103/ijmy.ijmy_207_19 |
| [3] |
CAMERON S E, ANDRADE R S, PAMBUCCIAN S E. Endobronchial ultrasound-guided transbronchial needle aspiration cytology: a state of the art review[J]. Cytopathology, 2010, 21(1): 6-26. DOI:10.1111/j.1365-2303.2009.00722.x |
| [4] |
CHEN W, ZHENG R, BAADE P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115-132. |
| [5] |
EISENHAUER E A, THERASSE P, BOGAERTS J, et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1)[J]. Eur J Cancer, 2009, 45(2): 228-247. DOI:10.1016/j.ejca.2008.10.026 |
| [6] |
FONTANILLA J M, BARNES A, VON REYN C F. Current diagnosis and management of peripheral tuberculous lymphadenitis[J]. Clin Infect Dis, 2011, 53(6): 555-562. DOI:10.1093/cid/cir454 |
| [7] |
DEVECI H S, KULE M, KULE Z A, et al. Diagnostic challenges in cervical tuberculous lymphadenitis: a review[J]. North Clin Istanb, 2016, 3(2): 150-155. |
| [8] |
CUI Q L, YIN S S, FAN Z H, et al. Diagnostic value of contrast-enhanced ultrasonography and time-intensity curve in differential diagnosis of cervical metastatic and tuberculous lymph nodes[J]. J Ultrasound Med, 2018, 37(1): 83-92. DOI:10.1002/jum.14311 |
| [9] |
YIN S S, CUI Q L, FAN Z H, et al. Diagnostic value of arrival time parametric imaging using contrast-enhanced ultrasonography in superficial enlarged lymph nodes[J]. J Ultrasound Med, 2019, 38(5): 1287-1298. DOI:10.1002/jum.14809 |
| [10] |
ZHANG J, HAO X, YANG Y, et al. Evaluation of supplementary diagnostic value of contrast-enhanced ultrasound for lymph node puncture biopsy[J]. J Thorac Dis, 2017, 9(11): 4791-4797. DOI:10.21037/jtd.2017.11.90 |
| [11] |
LING W, NIE J, ZHANG D, et al. Role of contrast-enhanced ultrasound (CEUS) in the diagnosis of cervical lymph node metastasis in nasopharyngeal carcinoma (NPC) patients[J]. Front Oncol, 2020, 10: 972. DOI:10.3389/fonc.2020.00972 |
| [12] |
RIZZO S, RADICE D, FEMIA M, et al. Metastatic and non-metastatic lymph nodes: quantification and different distribution of iodine uptake assessed by dual-energy CT[J]. Eur Radiol, 2018, 28(2): 760-769. DOI:10.1007/s00330-017-5015-5 |
| [13] |
RAJIAH P, PARAKH A, KAY F, et al. Update on multienergy CT: physics, principles, and applications[J]. Radiographics, 2020, 40(5): 1284-1308. DOI:10.1148/rg.2020200038 |
| [14] |
郑欢欢, 刘松, 朱妍, 等. 双层探测器光谱CT在评估食管癌分化程度及脉管神经侵犯中的应用价值[J]. 东南大学学报(医学版), 2022, 41(4): 510-516. |
| [15] |
CHEN W B, SHI Q Q, LI Z M, et al. Diagnostic value of spiral CT energy spectrum imaging in lymph node metastasis of colorectal cancer[J]. Int J Colorectal Dis, 2022, 37(9): 2021-2029. DOI:10.1007/s00384-022-04238-z |
| [16] |
RASSOULI N, ETESAMI M, DHANANTWARI A, et al. Detector-based spectral CT with a novel dual-layer technology: principles and applications[J]. Insights Imaging, 2017, 8(6): 589-598. DOI:10.1007/s13244-017-0571-4 |
 2025, Vol. 23
2025, Vol. 23


