| 基于TBSS对女性偏头痛脑白质变化的研究 |
2. 首都医科大学附属北京中医医院科研处, 北京 100010;
3. 北京中医药大学生命科学学院, 北京 100029;
4. 首都医科大学附属北京中医医院针灸科, 北京 100010
2. Office of Academic Research, Beijing Hospital of Traditional Chinese Medicine, Capital Medical University, Beijing 100010, China;
3. School of Life Sciences, Beijing University of Chinese Medicine, Beijing 100029, China;
4. Acupuncture and Moxibustion Department, Beijing Hospital of Traditional Chinese Medicine, Capital Medical University, Beijing 100010, China
偏头痛是一种常见的神经系统疾病,其患病率和致残率高、医疗负担重,严重影响了患者的生活质量。根据发作时是否伴视觉、感觉及运动等先兆症状,分为先兆和无先兆偏头痛,后者约占80%[1]。目前,偏头痛的发病机制尚未完全阐明。神经影像学已被广泛用于识别与偏头痛相关的大脑结构和功能异常的研究中。DTI是唯一一种能无创揭示大脑白质在体内的位置、方向和完整性的定量成像技术。各向异性分数(fractional anisotropy,FA)是其最重要的参数,可从0到1量化水分子的各向异性程度(0为完全不受限制,1为完全受限制)。FA与轴突数量、纤维密度、髓鞘形成程度和组织排列等有关。轴向扩散系数(axial diffusivity,AD)和径向扩散系数(radial diffusivity,RD)分别反映了轴突和髓鞘的完整性。平均扩散系数(mean diffusivity,MD)则测量了分子平均运动情况,受AD或RD影响[2]。有学者使用基于ROI的分析方法发现无先兆偏头痛患者额叶、内囊后肢和小脑半球的MD显著增加,FA显著降低。这些改变可能是由于细胞死亡导致细胞外间隙增加,细胞扩散不受限制引起的[3]。由于ROI分析存在一定局限性,许多研究应用基于纤维束示踪的空间统计(tract-based spatial statistics,TBSS)研究偏头痛相关的脑白质异常,发现胼胝体、额叶、内囊、脑干、丘脑等部位的白质微结构均发生改变[4-5]。此外,概率性纤维追踪法研究显示右侧额叶白质与疼痛相关网络有关联,包括眶额叶皮质、岛叶、丘脑和中脑。有学者认为这些观察结果可用适应不良的可塑性变化或白质的退行性过程来解释[4]。基于图论分析的研究还观察到无先兆偏头痛患者存在异常的全局网络特性和拓扑结构[6],虽有证据表明偏头痛存在大脑白质的异常,但在另一些研究中未发现显著变化[7-8]。
本研究应用TBSS方法比较女性无先兆偏头痛患者发作间期脑白质与健康志愿者间的差异,并进一步分析脑白质改变的DTI指标与临床参数之间的关系,为女性偏头痛患者的发病机制提供影像学依据。
1 资料与方法 1.1 一般资料招募2018年3月至2022年12月首都医科大学附属北京中医医院治疗的无先兆偏头痛患者,并招募健康志愿者。由一位具有20年以上临床经验的针灸科主任医师筛选并评估。无先兆偏头痛患者均独立完成问卷调查。通过患者过去1个月的回顾性评估计算偏头痛天数。采用视觉模拟评分法(visual analog scale,VAS)评估头痛强度(0~10分);采用头痛影响测试-6(headache impact test-6,HIT-6)问卷和偏头痛残疾程度评估问卷(migraine disability assessment questionnaire,MIDAS)评估与偏头痛相关的影响和残疾程度。使用贝克焦虑量表(Beck anxiety inventory,BAI)和贝克抑郁量表(Beck depression inventory,BDI)记录患者焦虑和抑郁状况。
无先兆偏头痛患者纳入标准:①符合国际头痛疾病分类Ⅲ的诊断标准[9];②18~65岁;③右利手;④偏头痛病程≥1年,每月发作>2次;⑤女性。健康志愿者纳入标准:①右利手、性别、年龄及教育水平与无先兆偏头痛患者相匹配;②健康状况良好,无偏头痛病史。
排除标准:其他类型的头痛;其他神经系统疾病和/或精神疾病;心血管疾病、急性传染病等;怀孕、哺乳及备孕期;近3个月内使用预防性治疗偏头痛的药物和针灸治疗;MRI检查禁忌证;大脑结构异常;酒精或药物滥用。
最终纳入偏头痛患者(偏头痛组)43例,年龄(38.19±10.62)岁,受教育年限(15.58±2.64)年,病程(17.02±9.58)年,过去1个月偏头痛天数(6.84± 6.15)d,VAS评分(7.57±1.42)分,HIT-6评分(67.84± 4.85)分,MIDAS(59.60±52.33)分,BAI(9.95± 8.12)分,BDI(8.93±6.16)分;健康志愿者(对照组)43例,年龄(36.81±11.65)岁,受教育年限(15.91± 3.09)年。
本研究经北京中医医院伦理委员会批准(伦理号:2021BL02-055-02)。研究符合《赫尔辛基宣言》(2013年修订)的原则。所有受试者在参与研究前均签署知情同意书。
1.2 仪器与方法2组均行MRI扫描,其中偏头痛组在头痛发作间期行MRI扫描(扫描前后≥72 h未出现偏头痛症状)。采用Siemens Skyra 3.0 T MRI扫描仪。受试者取仰卧位,保持静止、清醒和放松状态,闭眼避免思维活动,并以海绵垫固定头部。
扫描序列及参数:T1WI,TR 2 300 ms,TE 2.32 ms,层厚0.9 mm,间隔50%,层数192,翻转角8°,视野240 mm×240 mm,矩阵256×256;得到30个扩散方向的DTI数据,TR 5 600 ms,TE 95 ms,体素1.7 mm×1.7 mm×4.0 mm,无间隔,层数37,翻转角90°,视野220 mm×220 mm,矩阵128×128,b值取0、1 000 s/mm²。
1.3 DTI预处理和TBSS分析DTI数据处理在基于Matlab平台的PANDA工具箱(http://www. nitrc. org/projects/panda)和基于Linux系统的FSL软件上进行。将原始的DICOM文件转换为NIFTI格式后,对涡流效应、梯度方向和头部运动进行校正,提取脑蒙版,计算FA、MD、AD和RD,最后行TBSS分析。将所有个体FA图像利用线性和非线性配准至FMRIB58-FA模板的标准空间上,这些图像被转换至蒙特利尔神经学研究所(Montreal Neurological Institute,MNI)152标准空间(1 mm×1 mm×1 mm)。基于所有配准至标准空间的FA构建平均FA图及白质骨架。每个受试者对齐的FA图像以0.2的阈值投影至这个平均FA骨架中,MD、AD和RD图像也被投影至平均FA骨架上。
1.4 统计学分析采用SPSS 22.0软件进行数据分析。使用FSL软件对2组的DTI指标行随机非参数检验(置换5 000次)。使用无阈值集群增强对显著的聚类进行校正,之后应用家庭错误率(familywise error rate,FWE)行多重比较校正。校正后的P值设置为 < 0.05。选取2组差异有统计学意义的DTI指标,再与临床评分(包括疾病持续时间、过去1个月的偏头痛天数、VAS、HIT-6、MIDAS、BAI和BDI)行Pearson相关性分析。以P < 0.05为差异有统计学意义。
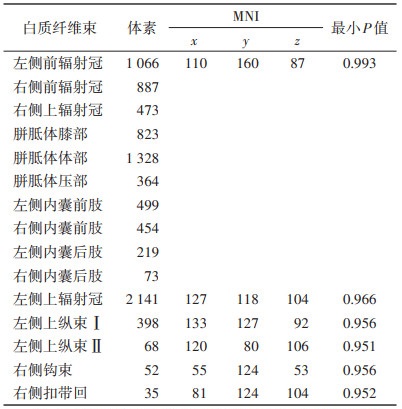
2 结果与对照组相比,偏头痛组在胼胝体膝、体及压部、双侧前辐射冠、双侧上辐射冠、双侧内囊前肢、双侧内囊后肢、左侧上纵束(superior longitudinal fasciculus,SLF)Ⅰ、Ⅱ、右侧钩束、右侧扣带回AD降低,全脑AD未见明显增加(表 1,图 1)。2组脑白质的FA、MD和RD差异均无统计学意义(均P>0.05)。
| 表 1 2组的脑白质AD差异 |
 |
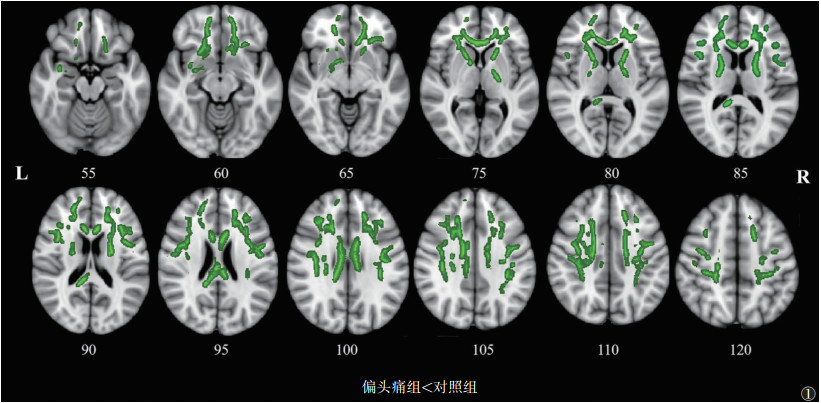 |
| 注:与对照组相比,女性偏头痛患者的脑白质AD显著降低(P<0.05,FWE校正)。绿色代表AD减低的白质纤维,AD为轴向扩散系数,FWE为家庭错误率 图 1 偏头痛组与对照组脑白质AD差异 |
偏头痛组与对照组相比,AD值变化的白质纤维束与偏头痛天数、VAS、HIT-6、MIDAS、BAI及BDI评分均未见明显相关性。
3 讨论既往DTI研究表明,偏头痛影响的大脑白质包括脑干、连合纤维(胼胝体)、投射纤维(辐射冠、内囊、丘脑辐射、额枕束和视神经辐射)和联络纤维(SLF、下纵束、钩束和扣带回)[10-11]。本研究TBSS分析显示,女性偏头痛患者的胼胝体、辐射冠、内囊、SLF、钩束和扣带回的AD显著降低,推测女性偏头痛患者存在与疼痛相关的脑白质内轴突损伤的表现,这些发现可帮助医师加深对偏头痛中枢机制的理解。
胼胝体是大脑半球间主要的连合纤维,在功能上整合左右大脑半球,传递知觉、学习、认知和意志信息。胼胝体的膝部包含投射到前额叶皮质、前扣带皮质、运动前皮质和补充运动区的纤维,体部包含投射到初级躯体感觉皮质的纤维,压部则包含投射到顶枕叶的视觉中心携带体感信息的纤维[12]。胼胝体切片试验证明偏头痛患者胼胝体参与了疼痛感知[13]。一项关于偏头痛的TBSS研究发现,偏头痛患者在胼胝体的膝、体、压部及右侧内囊前后肢的FA、MD和AD值均较低[5]。另一项研究比较了偏头痛患者和健康对照组的白质微观结构变化,发现偏头痛患者胼胝体膝的FA降低[14]。本研究仅胼胝体中的AD降低,而其他DTI指标均为阴性。
辐射冠由连接大脑皮质、脑干和丘脑的传入和传出纤维组成,这些纤维向下辐射并汇聚到内囊[15]。前辐射冠是边缘-丘脑皮质回路的一部分,包括从内囊到前额叶皮质的丘脑投射,与情绪调节相关[16]。前辐射冠的微结构改变与慢性腰痛[17]、原发性痛经[18]等与疼痛有关的疾病相关。一项全局概率性纤维追踪研究显示,偏头痛患者双侧丘脑前辐射MD及左侧丘脑前辐射RD均增加,且病程与右侧丘脑前辐射中的MD呈正相关[19]。在另一项应用TBSS分析无先兆偏头痛患者伴抑郁症状的研究中发现,丘脑前辐射中MD和RD的增加说明抑郁症状可能影响脑白质结构的完整性[20]。偏头痛患者左侧前辐射冠与灰质之间的功能连通性降低与偏头痛的病理生理学有关[21],偏头痛患者白质完整性遭到破坏,而白质完整性在疼痛处理的病理生理学中起着核心作用[19-21]。本研究显示,女性偏头痛患者双侧前、后辐射冠均受损,这与之前的结果相似,但本研究仅AD降低,FA、MD及RD未见异常。此外,投射纤维中的内囊也存在异常。内囊位于丘脑和基底节之间,由上行和下行轴突纤维组成,是连接大脑皮质与脑干和脊髓的主要途径[22]。内囊前肢包含丘脑辐射和皮质脊髓束的投射纤维;后肢包含感觉纤维、皮质脊髓束纤维和皮质延髓纤维[23]。先前的一项DTI研究提供了偏头痛患者白质微结构改变的客观证据,发现与对照组相比,无先兆偏头痛患者的额叶白质、内囊后肢和小脑半球的MD均显著增加,而FA显著降低[3]。另一项研究显示,与健康对照组相比,慢性偏头痛患者RD增加,与发作性偏头痛患者相比,MD增加出现在双侧上后辐射冠、胼胝体、内囊后肢及上纵束[24]。这些偏头痛患者出现的白质结构异常可能提示轴突异常、细胞密度降低和白质纤维束紊乱。本研究显示双侧内囊前肢和后肢的AD减少,提示内囊的轴突损伤可能参与了偏头痛的发生机制。
本研究发现偏头痛的联合纤维出现异常,包括SLF、钩束和扣带回。SLF连接额叶、顶叶和颞叶,分为Ⅰ~Ⅲ三段。SLFⅠ连接颞叶和下顶叶皮质,而SLFⅡ连接角回和额叶。SLF在许多高级皮质功能及空间处理,如语言、记忆、注意力和情感功能中起着重要作用[25]。这些均与疼痛处理的不同维度有关。与健康对照组相比,偏头痛患者左侧SLF的MD和AD降低[11]。本研究同样证实了SLFⅠ、Ⅱ的AD减低。研究发现,有抑郁症状的偏头痛患者,SLF的FA较低,MD和RD较高[20]。进一步行相关分析显示,SLF的FA和RD均值与抑郁量表显著相关;认为SLF通过背外侧前额叶皮质参与情绪调节环路,这可能是抑郁症严重程度的潜在生物标志物。本研究未发现SLF的DTI异常指标与焦虑及抑郁的严重程度之间有相关性,以及此区域与其他临床指标间的相关性。钩束和扣带回属于联络纤维,被视为边缘系统的一部分。钩束连接着额叶皮质和前颞叶,其结构异常与语言、记忆和情绪处理有关,特别是焦虑和疼痛[26]。而扣带回是一个重要的白质纤维束,连接额叶、顶叶和内侧颞叶,以及扣带回皮质下核团。研究认为,扣带回与认知控制、注意力、疼痛、运动和奖励有关[27]。有研究发现偏头痛患者的左侧钩束MD明显异常,双侧钩束RD异常,双侧扣带角束MD异常,右侧扣带角束RD异常,双侧扣带回MD和RD异常[26]。本研究中这2个白质纤维束也存在异常,说明其可能参与了偏头痛的多维度调节。
既往研究表明偏头痛对男女大脑结构和功能的影响不同[28-29]。有研究分析了22例偏头痛患者(11例男性,11例女性)和22例健康对照组的大脑功能和结构差异;发现偏头痛所致的脑岛叶和楔前叶的结构变化是女性患者特有的,而海马旁回的异常是男性患者特有的。与男性患者相比,女性患者的后岛叶和楔前叶的皮质更厚。对于偏头痛患者在热的反应表现中,女性比男性在参与情绪处理的大脑区域(杏仁核和海马旁回)激活更明显[29]。应用图论分析偏头痛患者大脑复杂网络的研究表明偏头痛更多影响女性患者,与男性患者相比,女性患者的脑功能网络表现出更差的弹性,更多的区域表现出降低的节点中心性,更多的功能连接显示异常[28]。
本研究存在的局限性:①偏头痛患者和对照组部分白质束中的AD减低,但其FA、MD和RD指标无明显变化,尚需进一步确认。②仅观察到女性无先兆偏头痛患者的白质异常,关于偏头痛与月经周期阶段之间的联系,以及关于性别差异的研究,需通过后续研究来解决。③虽然使用了先进的影像技术,但未考虑或比较其他相关的神经影像学技术,需进一步完善。④样本量相对较小,可能影响结果的普遍性和可推广性,在今后研究中需扩大样本量。
总之,女性无先兆偏头痛患者的连合纤维、投射纤维和联络纤维中涉及疼痛处理的轴突受损,这为无先兆偏头痛患者的白质微结构改变提供了客观证据,有助于阐明偏头痛的病理生理学机制。
| [1] |
GBD 2016 HEADACHE COLLABORATORS. Global, regional, and national burden of migraine and tensiontype headache, 1990-2016:a systematic analysis for the global burden of disease study 2016[J]. Lancet Neurol, 2018, 17(1): 954-976. |
| [2] |
WINSTON G P. The physical and biological basis of quantitative parameters derived from diffusion MRI[J]. Quant Imaging Med Surg, 2012, 2(4): 254-265. |
| [3] |
TAMAN S E, KAMR W H, BELAL T M, et al. Diffusion tensor magnetic resonance imaging: is it valuable in the detection of brain microstructural changes in patients having migraine without aura?[J]. Pol J Radiol, 2021, 86: e548-e556. DOI:10.5114/pjr.2021.110645 |
| [4] |
SZABÓ N, KINCSES Z T, PÁRDUTZ Á, et al. White matter microstructural alterations in migraine: a diffusionweighted MRI study[J]. Pain, 2012, 153(3): 651-656. DOI:10.1016/j.pain.2011.11.029 |
| [5] |
YU D, YUAN K, QIN W, et al. Axonal loss of white matter in migraine without aura: a tract-based spatial statistics study[J]. Cephalalgia, 2013, 33(1): 34-42. DOI:10.1177/0333102412466964 |
| [6] |
DAI L, ZHENG Q, CHEN X, et al. Altered brain structural topological properties and its correlations with clinical characteristics in episodic migraine without aura[J]. Neuroradiology, 2021, 63(12): 2099-2109. DOI:10.1007/s00234-021-02716-9 |
| [7] |
NEEB L, BASTIAN K, VILLRINGER K, et al. No microstructural white matter alterations in chronic and episodic migraineurs: a case-control diffusion tensor magnetic resonance imaging study[J]. Headache, 2015, 55(2): 241-251. DOI:10.1111/head.12496 |
| [8] |
MASSON R, DEMARQUAY G, MEUNIER D, et al. Is migraine associated to brain anatomical alterations? New data and coordinate-based meta-analysis[J]. Brain Topogr, 2021, 34(3): 384-401. DOI:10.1007/s10548-021-00824-6 |
| [9] |
HEADACHE CLASSIFICATION COMMITTEE OF THE INTERNATIONAL HEADACHE SOCIETY (IHS). The International Classification of Headache Disorders, 3rd edition[J]. Cephalalgia, 2018, 38: 1-211. |
| [10] |
CHOU B C, LERNER A, BARISANO G, et al. Functional MRI and Diffusion Tensor imaging in migraine: a review of migraine functional and white matter microstructural changes[J]. J Cent Nerv Syst Dis, 2023, 15: 11795735231205413. DOI:10.1177/11795735231205413 |
| [11] |
RAHIMI R, DOLATSHAHI M, ABBASI-FEIJANI F, et al. Microstructural white matter alterations associated with migraine headaches: a systematic review of diffusion tensor imaging studies[J]. Brain Imaging Behav, 2022, 16(5): 2375-2401. DOI:10.1007/s11682-022-00690-1 |
| [12] |
HOFER S, FRAHM J. Topography of the human corpus callosum revisited--comprehensive fiber tractography using diffusion tensor magnetic resonance imaging[J]. Neuroimage, 2006, 32(3): 989-994. DOI:10.1016/j.neuroimage.2006.05.044 |
| [13] |
STEIN B E, PRICE D D, GAZZANIGA M S. Pain perception in a man with total corpus callosum transection[J]. Pain, 1989, 38(1): 51-56. DOI:10.1016/0304-3959(89)90072-9 |
| [14] |
TANTIK PAK A, NACAR DOGAN S, SENGUL Y. Structural integrity of corpus callosum in patients with migraine: a diffusion tensor imaging study[J]. Acta Neurol Belg, 2023, 123(2): 385-390. DOI:10.1007/s13760-021-01863-3 |
| [15] |
YAKAR F, EROGLU U, PEKER E, et al. Structure of corona radiata and tapetum fibers in ventricular surgery[J]. J Clin Neurosci, 2018, 57: 143-148. DOI:10.1016/j.jocn.2018.08.041 |
| [16] |
KARABABA I F, BAYAZIT H, KILIÇASLAN N, et al. Microstructural changes of anterior corona radiata in bipolar depression[J]. Psychiatry Investig, 2015, 12(3): 367-371. DOI:10.4306/pi.2015.12.3.367 |
| [17] |
MA J, WANG X, QIU Q, et al. Changes in empathy in patients with chronic low back pain: a structural-functional magnetic resonance imaging study[J]. Front Hum Neurosci, 2020, 14: 326. |
| [18] |
LIU P, WANG G, LIU Y, et al. White matter microstructure alterations in primary dysmenorrhea assessed by diffusion tensor imaging[J]. Sci Rep, 2016, 6: 25836. DOI:10.1038/srep25836 |
| [19] |
CHONG C D, SCHWEDT T J. Migraine affects whitematter tract integrity: a diffusion-tensor imaging study[J]. Cephalalgia, 2015, 35(13): 1162-1171. DOI:10.1177/0333102415573513 |
| [20] |
YU D, YUAN K, ZHAO L, et al. White matter integrity affected by depressive symptoms in migraine without aura: a tract-based spatial statistics study[J]. NMR Biomed, 2013, 26(9): 1103-1112. DOI:10.1002/nbm.2924 |
| [21] |
QIN Z, LIANG H B, LI M, et al. Disrupted white matter functional connectivity with the cerebral cortex in migraine patients[J]. Front Neurosci, 2021, 15: 799854. |
| [22] |
AXER H, KEYSERLINGK D G. Mapping of fiber orientation in human internal capsule by means of polarized light and confocal scanning laser microscopy[J]. J Neurosci Methods, 2000, 94(2): 165-175. DOI:10.1016/S0165-0270(99)00132-6 |
| [23] |
WAKANA S, JIANG H, NAGAE-POETSCHER L M, et al. Fiber tract-based atlas of human white matter anatomy[J]. Radiology, 2004, 230(1): 77-87. DOI:10.1148/radiol.2301021640 |
| [24] |
COPPOLA G, DI RENZO A, TINELLI E, et al. Patients with chronic migraine without history of medication overuse are characterized by a peculiar white matter fiber bundle profile[J]. J Headache Pain, 2020, 21(1): 92. DOI:10.1186/s10194-020-01159-6 |
| [25] |
MAKRIS N, KENNEDY D N, MCINERNEY S, et al. Segmentation of subcomponents within the superior longitudinal fascicle in humans: a quantitative, in vivo, DTMRI study[J]. Cereb Cortex, 2005, 15(6): 854-869. DOI:10.1093/cercor/bhh186 |
| [26] |
CHONG C D, PEPLINSKI J, BERISHA V, et al. Differences in fibertract profiles between patients with migraine and those with persistent post-traumatic headache[J]. Cephalalgia, 2019, 39(9): 1121-1133. DOI:10.1177/0333102418815650 |
| [27] |
BUBB E J, METZLER-BADDELEY C, AGGLETON J P. The cingulum bundle: anatomy, function, and dysfunction[J]. Neurosci Biobehav Rev, 2018, 92: 104-127. DOI:10.1016/j.neubiorev.2018.05.008 |
| [28] |
LIU J, QIN W, NAN J, et al. Gender-related differences in the dysfunctional resting networks of migraine suffers[J]. PLoS One, 2011, 6(11): e27049. DOI:10.1371/journal.pone.0027049 |
| [29] |
MALEKI N, LINNMAN C, BRAWN J, et al. Her versus his migraine: multiple sex differences in brain function and structure[J]. Brain, 2012, 135(Pt8): 2546-2559. |
 2024, Vol. 22
2024, Vol. 22


