

2. 北京中医药大学北京中医药研究院,北京 102488
2. Beijing Research Institute of Chinese Medicine, Beijing University of Chinese Medicine, Beijing 102488, China
天然产物作为药物开发的宝库,在人类疾病治疗史上具有不可替代的地位,从17世纪的南美洲用金鸡纳树皮来治疗疟疾,到19世纪有机化学和分离技术的突破推动活性单体发现,天然产物独特的“化学空间”赋予其与生物大分子互补作用的特性,展现出复杂多样的生物学活性。然而,传统以结构发现为导向的研究模式已显疲态[1]。当前研究更聚焦于将活性天然产物作为分子探针,揭示生命活动调控机制,这为创新药物研发提供了新方式。尤其值得关注的是,天然活性分子作用靶点的解析,不仅能阐明药理机制,更是突破现有靶点资源匮乏的关键[2-4]。目前人类疾病约3万种,而已验证的药物靶点仅800余个,新靶点发现已成为新药研发的瓶颈问题。
尽管靶点鉴定技术快速发展,但天然产物由于其结构复杂性导致化学修饰困难,传统基于分子标记的亲和捕获技术适用性受限;其次,天然产物多通过多靶点协同作用或代谢产物发挥效应,单靶点筛选模式易造成关键作用机制遗漏。这些特性使得天然产物的靶点发现效率显著低于合成化合物,因此,开发适配天然产物特性的靶点鉴定策略,已成为突破当前药物研发困局的重要方向[5-6]。
2 天然药物靶点蛋白识别方法当前靶点鉴定技术主要分为基于药物-靶点亲和力的直接策略和依赖组学分析的间接策略。直接法通过生物素探针、化学交联等技术捕获物理相互作用,而间接法利用转录组学、人工智能等手段解析系统性差异[7]。本文将系统评述经典方法与新兴技术的优势局限,重点探讨其在天然产物研究中的适配性与创新应用。
2.1 直接靶点鉴定法在天然药物中的应用在直接靶点发现策略中,主要基于药物-靶点亲和力的共性科学原理来进行药物靶点的鉴定。自上世纪90年代哈佛大学的Schraiber博士以及Scripps研究所的Schultz博士提出化学生物学(chemical biology)这一概念以来,虽然对化学生物学的精准定义存在着不同意见,但当下普遍认可化学生物学是经过几十年的发展涌现出来的生物有机化学、生物化学、细胞生物学和药理学的复杂综合体。伴随化学生物学技术的不断进步,当下已然形成了一整套完备的化学生物学研究体系,其所运用的工具涵盖分子成像、代谢标记、活性探针以及生物正交反应等[8]。其中分子探针在天然药物活性分子作用机制研究领域发挥着至关重要的作用,成为近年来天然药物靶点鉴定方面的热门技术。
通常的药物分子探针构成包括:活性基团(reactive group)、报告基团(reporter group)及连接部位(linker)[9]。活性基团是探针的关键所在,其决定了探针的选择性和特异性,负责与靶点蛋白实现特异性结合;报告基团掌控着探针的灵敏度,使其能够快速探测、分离纯化靶蛋白;连接基团则起到桥梁作用,能够调节探针的大小、药代动力学、生物分布和带电情况等诸多属性。这些组成部分协同作用,使药物分子探针在药物靶点鉴定中发挥关键作用。
2.1.1 基于生物素探针的靶点鉴定技术生物素(biotin)在动植物中广泛分布,而生物素与亲和素(avidin)之间的相互作用是自然界中最强的非共价互作之一。因此,亲和素及其类似物已被广泛用作探针和亲和基质来使用,在生化检测、疾病诊断、抗体制备以及药物递送等诸多领域均具有广泛的应用[10]。生物素探针是鉴定天然产物作用靶点的常用方法。该技术通过将生物素标签键合到待研究的天然产物上,进而制备生物素标记的药物分子探针。随后将探针添加到细胞裂解液或活细胞中,通过药物与靶点蛋白的直接互作捕获靶点蛋白,然后利用生物素与亲和素的强结合特性,把靶点蛋白富集到固相载体上并通过质谱进行检测。目前该方法已经被广泛应用于多种天然产物的靶点鉴定当中。
Kwok等[11]通过构建生物素-小白菊内酯探针,鉴定出kappa B抑制因子激酶β(IKKβ)是小白菊内酯发挥抗炎作用的直接分子靶点。研究证实,小白菊内酯可与IKKβ的半胱氨酸179位点形成共价键,抑制IKKβ活性,阻断NF-κB信号通路激活从而达到抗炎效果。Liu等[12]制备了生物素-腺花素探针,从白血病细胞中鉴定出其直接作用靶点过氧化还原酶(Prx Ⅰ/Prx Ⅱ)。机制研究表明,腺花素通过靶向Prx Ⅰ和Prx Ⅱ的保守半胱氨酸,抑制了其过氧化物酶活性,进而发挥诱导急性早幼粒白血病细胞分化的功能。此外,Liu等[13]发现天然抗疟药物青蒿琥酯可以改善啮齿动物模型和人类患者的多囊卵巢综合征,并利用生物素标记的青蒿琥酯探针鉴定出长肽酶1(LONP1)是青蒿素抑制雄激素合成的关键靶点。分子对接模拟和相关功能实验显示,青蒿琥酯通过直接结合LONP1的蛋白水解结构域,诱导其构象变化并促进LONP1催化的CYP11A1降解,从而发挥阻止雄激素的过量生成作用。Liao等[14]利用生物素标记技术,构建了苏木酮A的生物素分子探针,从神经小胶质细胞中特异性捕获其作用靶点为肌苷-5′-单磷酸脱氢酶(IMPDH2),并发现苏木酮A可以与靶点蛋白IMPDH2的140位半胱氨酸发生共价结合,诱导靶点蛋白变构,从而抑制下游炎症相关信号通路并发挥抗神经炎症作用。此外,Zhang等[15]针对天然产物野马追内酯B构建了生物素标记的分子探针,运用该探针从人类蛋白质组芯片中筛选出去泛素化酶7(USP7)为野马追内酯B的直接作用靶点。即野马追内酯B通过诱导USP7的构象变化促进下游HO-1等相关蛋白表达发挥抗神经炎症作用。同时,诸如姜黄素、大头兔儿风药效物质Ainsliadimer A、蟾毒灵等天然产物的作用靶点发现也是通过构建生物素探针而实现的。由此可见,这些研究均是运用生物素标记的分子探针法揭示天然产物直接作用靶点的典型范例。
2.1.2 基于点击化学的靶点鉴定技术点击化学(click chemistry)这一概念由美国化学家Barry Sharpless在2000年左右提出,此命名生动地阐释了点击化学基于高特异性反应将两种分子相互连接起来的过程[16]。在点击化学的发展过程中,叠氮是最具影响力且应用最为广泛的点击化学试剂。目前主要衍生出了4类基于叠氮的点击化学反应:环加成反应、亲核开环反应、非醇醛的羰基化学以及碳碳多键的加成反应。目前常用的点击反应是2001年由Meldal教授报道的,该反应通过Cu(Ⅰ)催化,使炔基与叠氮基在室温下发生高效快速的环加成反应(copper-catalyzed azide-alkyne cycloaddition,CuAAC),以高于95%的产率得到单一区域选择性的1,4-二取代-1,2,3-三氮唑。
点击化学在药物靶点的鉴定中发挥了重要作用。例如人们将点击化学基团炔基与具有光交联特性的双吖丙啶基团(siazirine)进行组合使用,将其引入到药物分子构成双功能分子探针。当探针进入活细胞后与靶点蛋白结合,双吖丙啶被紫外光激活并与临近的靶点蛋白之间形成共价键,同时探针上的炔基会与偶联叠氮基团的生物素分子发生点击化学反应,使药物-靶点蛋白复合物标记上生物素标签并得到纯化与鉴定[17-18]。近年来,有学者将点击化学技术引入天然产物的靶点发现中。如Zhang等[19]针对具有抗菌活性的内源代谢分子衣康酸,通过在其末端引入炔基标签合成了点击化学探针C3A,并结合二甲基标记的定量化学蛋白质组学技术,在沙门氏菌中大规模鉴定了衣康酸修饰的蛋白。其中,包括参与沙门氏菌重要代谢过程的功能蛋白酶异柠檬酸裂解酶(ICL),即衣康酸通过共价修饰ICL的195位和318位半胱氨酸,影响ICL的热稳定性和活性,进而协助宿主防御沙门氏菌。Wang等[20]针对天然抗疟分子青蒿素,通过引入炔基构建了青蒿素点击化学探针,利用该探针在疟原虫体内系鉴定出124个青蒿素共价结合蛋白靶点,同时聚类分析还揭示了其中许多靶点参与了寄生虫的基本生物过程。Yang等[21]利用海洋天然产物VT01702偶联的荧光545-叠氮探针,基于CuACC反应在细胞裂解液中鉴定到了其直接作用靶点磷脂酰肌醇转移蛋白α/β(PITPα/β),进而通过质膜4-磷酸磷脂酰肌醇影响Hippo通路抑制肿瘤细胞分化。此外,像穿心莲内酯衍生物Andro、截短侧耳素P29、青蒿素类似物AP1等一系列天然产物的作用靶点阐明也是通过构建点击化学探针而实现的。由此可见,点击化学策略在推动天然产物作用靶点发现方面具有显著的优势。
此外,近年还发展起来一类基于活性蛋白质组学分析(activity-based protein profiling,ABPP)的靶点鉴定技术。例如,以巯基高度反应性分子探针作为化学工具,可以共价修饰蛋白质中的半胱氨酸,使其与待测活性分子竞争性与靶点蛋白结合并实现靶点鉴定。其中,碘代乙酰胺-炔基结构(IA-alkyne)是最常用的巯基反应性分子探针。这一方法首先将药物分子与蛋白质样品孵育,使其占据靶点蛋白的半胱氨酸活性结合位点,随后向样品中加入IA-alkyne探针封闭非特异性的半胱氨酸位点。这一方法排除了非特异性结合的蛋白位点,只有与药物分子发生特异性共价结合的靶点蛋白才能被检测到,因此利用该方法可以开展天然活性分子的靶点鉴定。如Li等[22]对分离自苦楝树的柠檬苦素类小分子nimbolide进行分析,发现其共价修饰了E3泛素连接酶RNF114的8位半胱氨酸,通过干扰RNF114对下游蛋白的识别进而抑制乳腺癌细胞的增殖。在最近的一项研究中,Spradlin等[23]利用ABPP技术,揭示了天然产物葫芦素B 2-O-β-d-葡萄糖苷共价靶向丝裂原活化蛋白激酶3(IMKK3),通过激活MAPK通路恢复耗竭T细胞的线粒体活力,从而增强抗肿瘤免疫。此外,绿原酸、海洋天然产物naamidine J以及阿苏卡霉素等天然产物的作用靶点阐明也是通过ABPP实现的。另外,还可以在IA-alkyne探针中引入稳定同位素,从而实现靶点蛋白的更加精确的定量分析。如Cravatt等开发的基于同位素标记串联正交酶水解的活性蛋白质分析技术(isotopic tandem orthogonal proteolysis-activity-based protein profiling,isoTOP-ABPP),实现了对活性半胱氨酸位点的精准定量鉴定。同时,Qin等[24]利用一种新型巯基反应性探针分子1-OH-Az,通过isoTOP-ABPP技术,确定了衣康酸修饰的靶点为果糖二磷酸醛缩酶A(ALDOA),即衣康酸通过共价修饰ALDOA抑制糖酵解通路,有效抑制了炎症刺激下巨噬细胞的炎症反应。由此可见,ABPP技术在天然产物靶点鉴定方面具有巨大的潜力。
2.1.3 基于光亲和探针的靶点鉴定技术光亲和标记(photoaffinity labeling,PLA)是近年来逐渐兴起的一种新型的靶点鉴定技术。该方法主要借助具有光反应性的光亲和基团,在受到特定波长光线激发后,产生高活性中间体,并迅速与距离最近的目标分子残基形成共价键,使分子探针与靶点蛋白之间形成稳定的复合物进而得到鉴定。常用的光亲和基团包括苯基叠氮类(azidomethyl benzene,AZs)、双吖丙啶类(diazirine,DAs)、二苯甲酮类(benzophenone,BPs)等[25-26]。
基于光亲和标记策略可以方便的实现天然产物的作用靶点鉴定。如Cheng等[27]通过构建四氮唑光亲和分子探针,通过竞争性蛋白质组分析和生物成像方法,从MCF7人乳腺癌细胞中鉴定到天然产物白桦脂酸的直接作用靶点为6-磷酸果糖-2-激酶(PFKFB1)及磷酸甘油酸激酶1(PGK1)等,从而解释了白桦脂酸抗乳腺癌的作用机制。Matarage等[28]开发了一种基于谷胱甘肽的光亲和探针DAZ-G,用于分析配体与钙感受受体(CaSR)的结合,发现咖啡因也能有效地与DAZ-G竞争,发挥CaSR变构激活剂的作用,从而为咖啡因摄入影响人体钙离子水平的机制做出了解释。在最近的一项研究中,Lyu等[29]利用插入了双吖丙啶基团的葛根素光亲和探针,发现葛根素的作用靶点蛋白为γ-氨基丁酸A型受体α1亚基(GABRA1)。结构生物学研究表明,葛根素通过结合在GABRA1的β3+/α1-界面,放大了GABA诱导的电流,对DMV-迷走神经轴发挥抑制作用,从而空肠对脂肪的吸收。此外,光亲和标记法还可以用于复杂成分的靶点群鉴定。天然提取物中复杂的化学成分,可以通过将天然提取物整体交联到预先键合有光敏基团(如二苯甲酮)的载体(如Fe3O4纳米粒)表面,进而制备天然产物成分芯片。这种天然产物芯片可以帮助人们开展复杂天然产物的多靶点鉴定。如Zhao等[30]将二苯甲酮结合于Fe3O4磁珠表面,在紫外光激发下使光敏基团活化为碳自由基,并将中药野菊花提取物键合到微球表面得到野菊花成分芯片,最终鉴定到野菊花提取物的直接作用靶点蛋白42个。由此可见,光亲和探针标记技术在天然产物的靶点鉴定方面具有广泛的应用价值。
2.1.4 基于化学交联的靶点鉴定技术化学交联的基本原理将天然产物通过化学键连接到生物相容的固相基质(如琼脂糖凝胶或磁性微球)上,进而去捕获细胞或组织裂解液中的药物靶点。其中,固相基质的活化为天然产物的交联提供了先决条件。例如,环氧氯丙烷活化的琼脂糖凝胶上的含氧三元环,可以与天然产物上的活泼羟基发生共价结合,从而将其固定在琼脂糖凝胶上,为药物靶标鉴定奠定基础[31-34]。
化学交联在天然产物的作用靶点发现方面具有广泛的应用空间。早在1983年,Abood等[35]就曾利用(R,S)-6-(2-羟乙基)尼古丁与环氧活化的琼脂糖偶联制备的亲和柱,从大鼠脑神经膜裂解物体系中分离出了烟碱胆碱能受体等相关靶点,其结合解离常数达到nmol·L-1级别。Liu等[36]从传统中药发现一个新型抗炎活性化合物1β-hydroxyalantolactone(IJ-5),利用IJ-5中的活性羟基,将其固定在环氧活化的琼脂糖载体表面,进而鉴定出其炎症治疗靶标为泛素连接酶UbcH5。机制研究显示,IJ-5通过靶向UbcH5的活性位点半胱氨酸,抑制了NF-κB炎症信号通路的激活从而发挥抗炎作用。此外,化学交联法的另一个优势是可以用于复杂成分的靶点群鉴定。如利用中药复杂组分中所含羟基与环氧活性基团的反应特性,可以高效键合肉苁蓉低分子糖并得到肉苁蓉低分子糖芯片,进而在RAW264.7细胞裂解液中成功鉴定了24个靶点蛋白,这些蛋白分别涉及Ecγ受体依赖的吞噬、TNF-α、NF-κB信号通路、糖酵解/糖原异生以及柠檬酸循环和呼吸电子运输过程等多条巨噬细胞激活信号通路,进而诠释了肉苁蓉低分子糖对巨噬细胞激活的作用机制[37]。由此可见,化学交联技术对天然产物单体及复杂成分的靶点鉴定都展现出极高的应用潜力。
2.1.5 基于蛋白质芯片的靶点鉴定技术蛋白质芯片(protein chip),也称为蛋白质微阵列(protein microarray),是一种基于DNA芯片原理发展而来的蛋白质组学技术。该技术通过高通量点样方法将大量重组蛋白有序地固定在固相载体上,这些重组蛋白通常带有His或GST标签,或通过共价键与载体结合。流动相中的待测药物分子与芯片上的蛋白质发生直接相互作用,这一过程可以通过引入荧光报告基团进行分析,从而实现靶点蛋白的鉴定[38-39]。尽管在确保蛋白质功能和结构完整性的前提下,成功表达和纯化大量蛋白质是一项耗时且费力的工作,蛋白质芯片仍具有细胞层面靶点鉴定方法无法替代的优势。在蛋白质芯片上,所有蛋白质以等量存在,为每种蛋白提供了平等结合药物分子的机会,从而避免了传统亲和层析倾向于结合细胞内高丰度靶点蛋白的局限性。因此,蛋白质芯片为药物靶点鉴定提供了一个高通量且强大的分析平台。
基于蛋白质芯片策略人们已经开展了多个天然产物的靶点鉴定。如Zhang等[40]利用包含16 368个重组蛋白的蛋白质组芯片,对三氧化二砷(As2O3,砒霜主要成分)的抗白血病靶点进行鉴定,累计鉴定出360种蛋白质,并最终确定己糖激酶Ⅱ(hexokinase 2,HK2)是As2O3作用的关键作用靶点。机制研究表明,As2O3通过共价结合HK2的256和704位半胱氨酸抑制其酶活,从而发挥抗早幼粒细胞白血病的作用。Huang等[39]利用酵母蛋白质芯片对生物素修饰的雷帕霉素进行靶点鉴定,发现了肿瘤抑制因子TEPP和TOR信号通路组分NIR1P为其潜在靶点蛋白,首次揭示了雷帕霉素调节TOR相关疾病(如糖尿病和癌症)的分子机制。此外,如雷公藤红素、野黄芩苷、芍药苷等一系列天然产物的作用靶点的阐明也是借助蛋白质芯片筛选实现的。由此可见,蛋白质芯片技术在促进天然产物作用靶点的发现上展现出了明显的优越性。
2.1.6 基于非标记策略的靶点鉴定技术在传统的亲和色谱靶点鉴定方法中,通常需要先合成标签修饰的分子探针。然而,对于那些本身缺乏可修饰基团的分子来说,这种方法显然难以实施。此外,对分子进行修饰还可能面临活性改变的风险。鉴于此,近年来发展出了一系列基于非标记策略的靶点鉴定方法。这些方法用于靶点鉴定的基本科学原理是,通过药物分子与靶点蛋白结合后,所形成的药物-靶点蛋白复合物可以一定程度上稳定蛋白质的构象,进而提高靶点蛋白耐受高热、蛋白酶解以及其他极端苛刻物理条件的能力,最终通过化学蛋白质组学方法进行鉴定[41]。下面对目前应用较为广泛的几种主流非标记策略进行介绍。
基于蛋白质热稳定性差异的靶点鉴定方法(cellular thermal shift assay,CETSA):高温刺激能够使蛋白质的空间结构发生不可逆的变化,原本处于结构内部的疏水性基团暴露于分子表面,导致蛋白分子之间相互碰撞而发生聚沉。当蛋白质与药物分子结合时,形成的复合物增强了蛋白稳定性,因此需要更高的温度才能诱导蛋白变性,因此可以根据蛋白质的变性溶解温度来预测潜在的药物靶点[42-43]。例如Miettinen等[44]利用CETSA发现了醌还原酶2(NQO2)可能是导致对乙酰氨基酚肝毒副作用的靶点蛋白。由于早期的CETSA主要依赖免疫印迹作为检测手段,大大限制了可检测的蛋白范围。为了能够在全蛋白质组学水平开展药物作用靶点的分析,后期发展出了热蛋白质组分析(thermal proteome profiling,TPP)技术。这一方法通过将CETSA技术与定量质谱相结合,进而实现了在全蛋白质组学水平无偏的直接作用靶点鉴定。例如,Kirsch等[45]利用TPP方法,将来源黏性细菌的天然活性分子VioA进行细胞原位孵育,随后进行一系列温度梯度刺激,裂解细胞后对蛋白质组进行定量标记并发现VioA能够靶向核糖体合成的关键蛋白——核仁蛋白14(NOP14),进而发挥对急性淋巴白血病的抑制作用。此外,有研究团队基于TPP策略鉴定了藤黄酸诱导前列腺癌细胞发生焦亡的作用靶点为冠层3同源蛋白(CNPY3),即藤黄酸通过促进CNPY3与SIRT1结合,激活溶酶体依赖的细胞焦亡信号通路[46]。在最近的一项研究中,Khan等[47]通过TPP(结合转录组学分析,首次揭示了右美沙芬(一种吗啡类中枢镇咳药)通过作用于胶原蛋白靶点群发挥抗纤维化作用的机制。此外,该方法已被应用于诸如原苏木素A、香叶草基柚皮素以及醉茄内酯等天然活性成分的靶点鉴定中,显示出其在天然产物作用靶点发现方面的显著优势。
基于蛋白水解敏感性差异的靶点鉴定方法:蛋白质的构象受多种因素影响,如翻译后修饰及配体结合等,因此这些因素均可能改变蛋白质对蛋白水解酶的敏感度[48]。药物亲和靶点稳定性(drug affinity responsive target stability,DARTS)分析[49]以及有限蛋白水解质谱技术(limited proteolysis mass spectrometry,LiP-MS)[50]均是基于蛋白质与药物分子结合后,由于其稳定性增高导致其抵抗蛋白酶解能力增强,进而其丰度增高而得到鉴定的。例如,Wang等[51]采用DARTS法鉴定沙利霉素(salinomycin)在神经母细胞瘤中的结合蛋白,并通过质谱检测分析证实了核仁素NCL为沙利霉素的结合靶标。Chen等[52]借助LiP-MS技术,通过将贯叶金丝桃素(Hyperforin,HPF)与脂肪细胞裂解液孵育,进而使用蛋白酶K、胰蛋白酶进行有限的蛋白水解,通过和液相色谱-串联质谱最终确认了二氢硫辛酰胺S-乙酰转移酶(Dlat)是贯叶金丝桃素发挥介导的脂肪细胞产热作用的直接靶点。Hu等[53]通过LiP-MS揭示了齐墩果酸减轻结肠炎的靶点是有Src同源性2的蛋白酪氨酸磷酸酶2(SHP2)。即齐墩果酸通过与SHP2的PTP结构域活性中心的3个关键氨基酸位点结合,保持SHP2的活性“开放”状态,进而选择性地抑制T细胞中的STAT3信号从而缓解结肠炎症状。这些实例表明,基于蛋白水解敏感性差异的鉴定策略在天然产物结合靶点分析中具有广泛的适用性。
基于化学变性剂诱导蛋白质稳定性差异的靶点鉴定方法(stability of proteins from rates of oxidation,SPROX):蛋白质在化学变性剂(如胍盐、尿素)作用下发生变性后更易受到氧化修饰。当药物分子与蛋白质结合时,能够增强蛋白质抵抗变性剂的能力,进而影响其氧化修饰的程度。因此,通过对比药物干预前后蛋白质氧化修饰水平的变化,可以有效鉴定出潜在的药物作用靶点蛋白。SPROX技术正是利用这一原理,依据蛋白质与药物分子结合后甲硫氨酸氧化速率降低的特性来鉴定靶点[54]。Lu等[55]将抗组胺剂克立马丁(Clemastine)与疟原虫裂解液体系共同孵育,随后利用尿素诱导样本变性,并以过氧化氢进行氧化处理,随后采用TMT进行定量标记及LC-MS/MS分析并确定克立马丁抗疟靶标为TCP-1环复合物(TRiC/CCT)。Kaur等[56]利用SPROX结合同位素标记定量技术成功鉴定到环孢素A(cyclosporin A)的抗肿瘤靶点亲环素A。此外,该团队还利用SPROX技术,鉴定了天然抗癌化合物Manasantin A在人乳腺癌细胞中的靶点蛋白为延长因子1α(EF1α)。该技术在未来天然药物作用靶点的发现与确证研究中,有望发挥重要作用。值得注意的是,该方法所使用的无标记分子,可能会与非目标蛋白质发生非特异结合,从而导致假阳性的情况。
基于有机溶剂诱导蛋白质溶解度差异的靶点鉴定方法(differential precipitation of proteins,DiffPOP):丙酮、乙醇、甲醇和乙腈等有机溶剂通常可用于沉淀蛋白质和去除污染物。药物分子-蛋白质复合物具有较低的能量状态,所以未折叠的蛋白质比游离蛋白质需要更多的能量。因此,药物分子结合后的靶点蛋白对有机溶剂诱导的变性和沉淀的抗性更强[57]。基于此原理提出了DiffPOP的新方法,可有效用于鉴定药物的靶点蛋白。该方法通过逐步添加90%甲醇和1%乙酸,将蛋白质差异性沉淀为多个组分,随后用冷丙酮清洗这些组分中的蛋白质沉淀,将其溶解并胰酶消化与鉴定。Xu等[58]利用此法成功鉴定到丝氨酸羟甲基转移酶2(SHMT2)为组蛋白去甲基化酶抑制剂JIB-04的直接作用靶点。JIB-04可能干扰了宿主中靶点蛋白保护Tat蛋白的能力,从而使得HIV病毒保持在静息状态。由此可见,DiffPOP在识别药物与蛋白质之间的相互作用方面,提供了一种新颖且高效的技术手段。
靶标响应可及性变化谱(target-responsive accessibility profiling,TRAP)技术:TRAP是新近发展起来的一项靶点鉴定新技术,其主要原理是药物分子与靶蛋白结合后,由于空间位阻或变构效应,导致靶蛋白对应区域的活性赖氨酸残基无法被工具探针共价标记。在此基础上使用氘代甲醛和硼烷-吡啶络合物进行二甲基化标记,使赖氨酸残基发生+32.06 Da的质量偏移,进而通过质谱检测确定靶标蛋白。为了实现对多个代谢物靶点的高通量鉴定,Tian等[59]运用TRAP技术在细胞中成功鉴定了10种糖酵解代谢物的靶点群,总共发现了913个可及性发生变化的候选靶点。进一步机制研究表明,糖酵解代谢物对靶点群有着丰富的调控模式,其中包括对碳代谢酶活性的干扰、对转录蛋白功能的影响以及对靶点翻译后修饰水平的调控等。除此之外,利用TRAP技术还实现了对天然产物水飞蓟宾silibinin以及沙地蟾蜍素的靶点识别。
pH依赖蛋白沉淀法(pH-dependent protein precipitation,pHDPP):叶明亮团队基于药物结合蛋白相较于未结合蛋白具有更高稳定性的原理,即药物结合蛋白对酸性试剂引起的蛋白变性沉淀更具耐受性,开发出一种非修饰药物靶点蛋白质组学鉴定新方法——pHDPP。首先通过筛选4种pH值变性剂,包括抗坏血酸(Vc)、柠檬酸(CA)、盐酸(HCl)和甲酸(FA),发现Vc和CA在研究配体诱导稳定性方面表现出良好的性能。随后利用定量蛋白质组学技术对一系列已知靶点的模型药物进行验证,并成功鉴定到抗肿瘤药物甲氨蝶呤(MXT)的作用靶点二氢叶酸还原酶(DHFR)以及亚胺二磷酸腺苷(AMP-PNP)的靶点蛋白细胞周期依赖性激酶9(CDK9)等,证实了该方法的可行性和稳定性。此外,该团队还利用pH值变性剂CA,从Hela细胞中筛选出45个双氢青蒿素的潜在靶标蛋白[60]。由此可见,pHDPP具备高特异性、高通量、低成本、操作简便等优点,有效解决了传统基于药物修饰的化学蛋白质组学方法中配体修饰的难题。
此外,近年来还陆续发展起来了基于多重巯基反应谱(multiplex thiol reactivity profiling,MTRP)以及基于降解的蛋白质分析(degradation-based protein profiling,DBPP)的药物靶点鉴定方法,其在揭示天然活性分子的作用靶点方面均具有良好的发展前景。
2.1.7 基于高通量技术平台的靶点筛选策略噬菌体展示技术:该技术是一项独特的基因重组表达技术,亦是一种简便有效的筛选工具。通过将大量不同的多肽或蛋白质展示在噬菌体表面,并与潜在的靶分子进行相互作用筛选,可以找出与靶分子具有高亲和力的肽或蛋白质。这些肽或蛋白质可以作为进一步研究药物靶点的候选物,有助于深入了解靶分子的生物学功能。因此,噬菌体展示技术可以用于快速筛选和识别与特定疾病相关的潜在药物靶点。1985年,Scott等[61]首次实现丝状噬菌体表达外源基因,开启了噬菌体展示技术研究。噬菌体展示是最广泛使用的体外抗体筛选技术,已助力多种人源抗体获批临床治疗。阿霉素是一种广泛使用的抗癌药物,但其作用机制尚未完全明确。通过固定化阿霉素筛选T7噬菌体文库,研究人员发现阿霉素能够结合核仁磷蛋白hNopp140的C末端。进一步的结合验证实验显示,阿霉素与hNopp140的结合解离常数达到nM级别。阿霉素通过与hNopp140结合,干扰其在rDNA转录和核仁生物合成中的调控功能,进而发挥抗肿瘤细胞增殖作用[62]。这一研究结果证实了噬菌体展示技术在鉴定活性天然产物靶点方面的有效性,为探索天然产物的作用机制提供了一种新颖的工具。
基于酵母突变株的药物靶点发现技术:酿酒酵母(Saccharomyces cerevisiae)等模式生物已被证实是探究药物分子作用机制的有力工具,这主要归功于众多与人类疾病关联的基因在酵母中存在高度保守的同源基因。1999年,Giaever等[63]研究指出,通过平行分析携带药物靶基因杂合缺失的酵母菌株,能够在体内有效监测药物分子的活性靶点。Lum等[25]描述了使用一个全基因组范围的标记杂合子池来评估78种化合物在酿酒酵母中的靶点。具体而言,研究团队在固醇生物合成途径中鉴定出羊毛甾醇合成酶是抗心绞痛药物莫西多明的作用靶点,这一发现或许能够阐释莫西多明降低胆固醇的机制。除此之外,研究还揭示了rRNA加工外切体可能是细胞生长抑制剂5-氟尿嘧啶的潜在靶点。这一研究结果有力地证明了利用酵母突变株系统进行高通量药物靶点发现的可行性,基于酵母突变株的药物靶点发现技术有望加速新药的靶点识别过程,提高药物开发的效率和成功率。
2.2 间接靶点鉴定法在天然药物中的应用 2.2.1 基于细胞生物学机制的靶标预测方法许多天然产物的作用机制研究是基于其药用植物的传统应用而展开的,因此,可以从目前已知的针对该类疾病的分子信号通路出发,逐步探寻这些活性成分可能的作用靶标蛋白。例如,雷公藤的传统功效涵盖祛风除湿、通络止痛、消肿止痛等,临床上常用于治疗类风湿关节炎等病症。雷公藤内酯作为一种结构独特的二萜类天然活性分子,展现出抗炎、免疫抑制、抗肿瘤等多种活性;然而,其具体的作用靶标至今尚未明确。鉴于抗炎生物活性通常与炎症转录因子的活性调控紧密相关,约翰·霍普金斯大学的研究人员[64]系统地探究了雷公藤内酯对细胞转录不同阶段以及参与各阶段的不同功能性蛋白的调控作用。最终,他们发现雷公藤内酯的抗炎作用分子靶标是转录因子TFIIH的XPB/ERCC3亚基,为阐明雷公藤内酯的抗炎分子机制提供了关键的实验依据。兰赫尔辛基大学的Yadav等[65]将药物-细胞表型数据与药物-靶标相互作用信息相结合,计算出每个靶标的成瘾打分(target addiction score,TAS)。随后,他们依据TAS以及细胞系的CRISPR Cas9基因敲除数据,筛选出关键的选择性靶标。该研究团队将这一分析流程应用于20种三阴性乳腺癌细胞系以及310种肿瘤药物的高通量筛选数据中,发现组蛋白去乙酰酶HDACs可能是具有潜在合成致死性的关键靶标群。由此可见,基于细胞生物学机制的靶标预测,对许多机制尚不明确的药物的靶点发现可能具有一定的提示作用。
2.2.2 基于转录组学的靶标预测方法近年来,随着药物调控细胞转录数据的迅速积累,药物靶点预测迎来了新的机遇[66]。在该领域,主要使用的数据库包括CMap(connectivity map)数据库和LINCS(the library of integrated network-based cellular signatures)数据库。在最近的一项研究中,Liu等[67]根据CMAP数据库的综合分析,研究了肝脏细胞和下丘脑细胞的6个不同基因表达数据后发现,雷公藤红素能有效缓解内质网应激和瘦素抵抗。这一发现为雷公藤红素作为潜在的抗肥胖治疗药物提供了重要实验依据。Wu等[68]通过单细胞转录组学分析发现,吸烟相关COPD患者及烟熏小鼠肺泡上皮祖细胞的昼夜节律和细胞周期通路存在显著差异。差异基因富集于衰老、凋亡及细胞外基质调控通路。经药物基因互作数据库筛选获得41个潜在药靶,结合肺细胞图谱筛选出15个肺组织特异性靶点。类器官验证揭示PGE2/PGI2通过激活NR1D1(Rev-erbα)受体,可修复吸烟诱导的肺上皮损伤。该研究建立了从组学分析到靶点验证的系统药靶发现策略。上述方法在基于药物调控细胞组转录数据的药物靶点预测领域取得了一定的进展,但是由于数据信息利用少和假设简单,这一方法的准确性还有待进一步提高。
2.2.3 基于预测工具的靶标预测方法药物-靶点相互作用预测依赖于丰富的化学分子和蛋白靶点数据,利用已知的三维结构数据库展开检索,寻找符合模型要求的化合物,最终将其与中药成分结构进行对比,评价中药各成分的生物活性和成药性。Liu等[69]开发了药效团匹配与潜在识别靶标平台PharmTargetDB。该平台包含7 000多个重要靶标结构的信息和药效团模型,涵盖了349种生物功能和110种临床适应症。用户可以通过将查询化合物的药效团与内部数据库中的药效团模型进行匹配来开展预测。该团队在2017年对抗菌剂卡那霉素(kanamycin)的作用靶点进行了预测,并通过对排名前1%的候选药效团结合实验评估进行筛选,最终确定了氨基糖苷磷酸转移酶以及核苷酸转移酶为其作用靶点[70]。刘广欣等[71]基于此方法研究了甘草中的抗痴呆活性物质,前期实验提示其可能作用于乙酰胆碱酯酶(AChE)。随后,研究人员建立了基于AChE配体的HipHop药效团模型,用于将甘草中的成分与药效团进行匹配。最终确定了甘草中6种潜在的抗AChE成分,并深入分析了这6种化合物与AChE的相互作用,以阐明其药效物质基础。随着药物-靶点预测模型准确性的提升,众多数据库提供了药物、靶点及其相互作用的详细信息,获得更有效的预测结果。
2.2.4 基于深度学习策略的靶点鉴定传统生物物理学手段探究药物-靶点相互作用受限于高昂的设备、试剂和人力成本。而人工智能(artificial intelligence,AI)在药物设计领域取得显著成就,为生物活性预测、分子靶点发现和新药设计带来便利。计算机科学家于1956年提出构建具备完全人类智能的计算机理念,催生了人工智能概念[72]。作为模拟、延展和扩充人类智能的新技术科学,AI的发展受数据、算法和算力三大支柱推动。机器学习(machine learning,ML)使计算机自主学习、识别模式并构建模型进行预测,深度学习(deep learning,DL)则是ML的进阶形式。近年来,随着算力的提升,深度学习在图像识别、自然语言处理等应用中取得了巨大成就,药物靶标相互作用的预测逐渐由传统机器学习转向深度学习[73]。计算机技术在药物-靶点相互作用预测领域持续演进,多种模型和技术的创新不断为药物研发拓展出更为广袤的潜在可能性。其常见的算法模型包括卷积神经网络(convolutional neural network,CNN)、循环神经网络(recurrent neural network,RNN)和图神经网络(graph neural network,GNN)等[74-75]。
Yang等[76]提出了一种深度学习和多视图集成学习网络MINDG,发现MINDG能够提高整体模型的性能,能够对已知的药物靶点进行较好的复现。并且根据清华大学Duan等[77]解析的SARS-CoV-2 3CL蛋白酶序列输入模型,预测包括法维拉韦、阿比朵尔等10种潜在的靶向药物。传统的药物研究方法主要聚焦于单个药物分子同特定靶点之间的相互作用。然而随着生物信息学、基因组学和化学信息学的发展,研究人员逐渐认识到,药物的作用范围绝非仅局限于独立的药物靶点关系。系统生物学通过对化学信息与基因组学信息的综合考量,揭示药物与生物大分子之间更为繁杂的相互作用网络。系统生物学的核心理念涵盖了包括药物分子的化学结构,其与多个潜在靶点的结合模式,以及与基因表达、通路调控之间错综复杂的关系,这种综合性的研究方法能够深度揭示药物对整个生物系统的影响。AI融合算法分析与生物实验,开辟了药物-靶点相互作用预测的新途径。我国科学家利用AI从“药用植物来源化合物成分数据库”筛选出30种可能对2019-nCoV有治疗作用的药物、活性天然产物和中药,表明虎杖、山豆根等中药材中可能含有抗2019-nCoV的有效成分,为其临床应用提供科学依据[78]。这显示AI助力的药物研发有利于天然产物的有效开发。
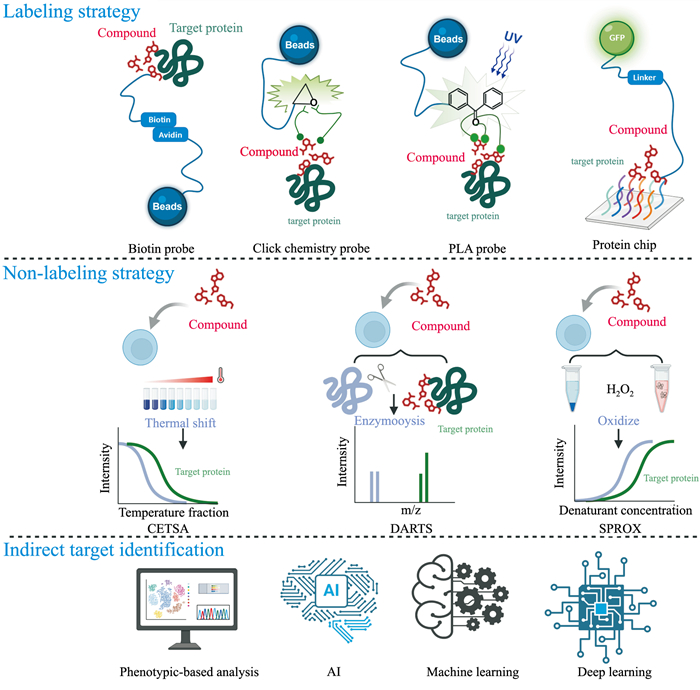
3 展望靶点预测对是深度揭示天然药物作用机制的关键环节。当前,天然产物靶点鉴定正处于方法学革新的关键转折点。一方面,化学生物学的快速发展极大地推动了天然活性分子的靶点发现进程。另一方面,随着AI与深度学习算法的迭代升级,其与传统化学生物学技术的深度融合将催生突破性进展(Fig 1)。
|
| Fig 1 Overview of identification methods for targets of natural bioactive molecules |
近来,AlphaFold 3凭借其高精度结构预测能力,为天然产物-蛋白质复合物研究提供了新思路。其在预测蛋白质与天然产物小分子结合模式时,精度和效率显著提升。最新研究显示,对于TIM3蛋白与配体复合物的结构预测,AlphaFold 3的结果与实验晶体结构高度一致[79]。未来,结合其开源性和高性能计算,有望加速天然产物靶点鉴定及药物研发。
此外,基于分子结构的计算预测模型成为突破瓶颈的关键——分子对接、生物活性指纹及机器学习等策略已成功解析多种天然产物的作用靶点[80]。Cockroft等[81]通过将20个公开的天然产物数据库与生物活性数据库ChEMBL进行交叉比对,生成了一个包含天然产物结构及其相关蛋白质靶点的数据集。该数据集包含1 943种独特化合物和1 023种独特靶点的5 589个化合物-靶点对。用于训练k-最近邻、随机森林和多层感知器模型等算法,对1 907个靶点的预测准确率达89.2%,在抗阿尔茨海默病天然产物筛选中发现8个多靶点先导物。随着算法迭代与多源数据整合能力的提升,定制化机器学习模型将更精准地揭示天然产物多靶点协同机制,为加速天然药物研发提供智能化解决方案。
| [1] |
Carter G T. Natural products and pharma 2011: strategic changes spur new opportunities[J]. Nat Prod Rep, 2011, 28(11): 1783-9. doi:10.1039/c1np00033k |
| [2] |
Koehn F E. High impact technologies for natural products screening[J]. Prog Drug Res, 2008, 65(65): 176-210. |
| [3] |
Lachance H, Wetzel S, Kumar K, et al. Charting, navigating, and populating natural product chemical space for drug discovery[J]. J Med Chem, 2012, 55(13): 5989-6001. doi:10.1021/jm300288g |
| [4] |
郭颖, 郭宗儒. 个性化操作: 天然产物的结构改造[J]. 中国新药杂志, 2014, 23(7): 753-8, 780. Guo Y, Guo Z R. Individual operation: structure modification of natural products[J]. Chin J New Drugs, 2014, 23(7): 753-8, 780. |
| [5] |
曾克武, 屠鹏飞. 中药作用靶点方法学研究进展[J]. 中国科学: 化学, 2018, 48(11): 1420-8. Zeng K W, Tu P F. Recent progress on the methodology for target study of traditional Chinese medicine[J]. Sci China Chem, 2018, 48(11): 1420-8. |
| [6] |
Zhu Y, Xiao T, Lei S, et al. Application of chemical biology in target identification and drug discovery[J]. Arch Pharm Res, 2015, 38(9): 1642-50. doi:10.1007/s12272-015-0643-2 |
| [7] |
赵晶, 申凯, 寇俊萍, 等. 天然活性成分作用靶点识别及确证方法的研究进展[J]. 现代生物医学进展, 2014, 14(17): 3369-72, 3361. Zhao J, Shen K, Kou J P, et al. Advance in methods of identifying and verifying targets of natural products[J]. Prog Mod Biomed, 2014, 14(17): 3369-72, 3361. |
| [8] |
Borman S. Chemistry, biology cross-fertilization[J]. Chem Eng News Archive, 2007, 85(40): 31-2. doi:10.1021/cen-v085n040.p031 |
| [9] |
Prescher J A, Bertozzi C R. Chemistry in living systems[J]. Nat Chem Biol, 2005, 1(1): 13-21. doi:10.1038/nchembio0605-13 |
| [10] |
刘石锋, 陈倩, 洪广成, 等. 生物素-亲和素系统的应用研究进展[J]. 生物技术, 2018, 28(5): 503-7. Liu S F, Chen Q, Hong G C, et al. Research advances on the application of biotin-avidin system[J]. Biotechnology, 2018, 28(5): 503-7. |
| [11] |
Kwok B H, Koh B, Ndubuisi M I, et al. The anti-inflammatory natural product parthenolide from the medicinal herb Feverfew directly binds to and inhibits IkappaB kinase[J]. Chem Biol, 2001, 8(8): 759-66. doi:10.1016/S1074-5521(01)00049-7 |
| [12] |
Liu C X, Yin Q Q, Zhou H C, et al. Adenanthin targets peroxiredoxin Ⅰ and Ⅱ to induce differentiation of leukemic cells[J]. Nat Chem Biol, 2012, 8(5): 486-93. doi:10.1038/nchembio.935 |
| [13] |
Liu Y, Jiang J J, Du S Y, et al. Artemisinins ameliorate polycystic ovarian syndrome by mediating LONP1-CYP11A1 interaction[J]. Science, 2024, 384(6701): eadk5382. doi:10.1126/science.adk5382 |
| [14] |
Liao L X, Song X M, Wang L C, et al. Highly selective inhibition of IMPDH2 provides the basis of antineuroinflammation therapy[J]. Proc Natl Acad Sci USA, 2017, 114(29): E5986-94. |
| [15] |
Zhang X W, Feng N, Liu Y C, et al. Neuroinflammation inhibition by small-molecule targeting USP7 noncatalytic domain for neurodegenerative disease therapy[J]. Sci Adv, 2022, 8(32): eabo0789. doi:10.1126/sciadv.abo0789 |
| [16] |
Kolb H C, Finn M G, Sharpless K B. Click chemistry: diverse chemical function from a few good reactions[J]. Angew Chem Int Ed, 2001, 40(11): 2004-21. doi:10.1002/1521-3773(20010601)40:11<2004::AID-ANIE2004>3.0.CO;2-5 |
| [17] |
Chang P V, Prescher J A, Sletten E M, et al. Copper-free click chemistry in living animals[J]. Proc Natl Acad Sci USA, 2010, 107(5): 1821-6. doi:10.1073/pnas.0911116107 |
| [18] |
Saxon E, Bertozzi C R. Cell surface engineering by a modified Staudinger reaction[J]. Science, 2000, 287(5460): 2007-10. doi:10.1126/science.287.5460.2007 |
| [19] |
Zhang Y, Qin W, Liu D, et al. Chemoproteomic profiling of itaconations in Salmonella[J]. Chem Sci, 2021, 12(17): 6059-63. doi:10.1039/D1SC00660F |
| [20] |
Wang J, Zhang C J, Chia W N, et al. Haem-activated promiscuous targeting of artemisinin in Plasmodium falciparum[J]. Nat Commun, 2015, 6: 10111. doi:10.1038/ncomms10111 |
| [21] |
Yang H, Zhang X, Wang C, et al. Microcolin H, a novel autophagy inducer, exerts potent antitumour activity by targeting PITPα/β[J]. Signal Transduct Target Ther, 2023, 8(1): 428. doi:10.1038/s41392-023-01667-2 |
| [22] |
Li F L, Fu V, Liu G, et al. Hippo pathway regulation by phosphatidylinositol transfer protein and phosphoinositides[J]. Nat Chem Biol, 2022, 18(10): 1076-86. doi:10.1038/s41589-022-01061-z |
| [23] |
Spradlin J N, Hu X, Ward C C, et al. Harnessing the anti-cancer natural product nimbolide for targeted protein degradation[J]. Nat Chem Biol, 2019, 15(7): 747-55. doi:10.1038/s41589-019-0304-8 |
| [24] |
Qin W, Qin K, Zhang Y, et al. S-glycosylation-based cysteine profiling reveals regulation of glycolysis by itaconate[J]. Nat Chem Biol, 2019, 15(10): 983-91. doi:10.1038/s41589-019-0323-5 |
| [25] |
Lum P Y, Armour C D, Stepaniants S B, et al. Discovering modes of action for therapeutic compounds using a genome-wide screen of yeast heterozygotes[J]. Cell, 2004, 116(1): 121-37. doi:10.1016/S0092-8674(03)01035-3 |
| [26] |
Seo S Y, Corson T W. Small molecule target identification using photo-affinity chromatography[J]. Methods Enzymol, 2019, 622: 347-74. |
| [27] |
Cheng K, Lee J S, Hao P, et al. Tetrazole-based probes for integrated phenotypic screening, affinity-based proteome profiling, and sensitive detection of a cancer biomarker[J]. Angew Chem Int Ed, 2017, 56(47): 15044-8. doi:10.1002/anie.201709584 |
| [28] |
Matarage Don N N J, Padmavathi R, Khasro T D, et al. Glutathione-based photoaffinity probe identifies caffeine as a positive allosteric modulator of the calcium-sensing receptor[J]. ACS Chem Biol, 2024, 19(7): 1661-70. doi:10.1021/acschembio.4c00335 |
| [29] |
Lyu Q, Xue W, Liu R, et al. A brain-to-gut signal controls intestinal fat absorption[J]. Nature, 2024, 634(8035): 936-43. doi:10.1038/s41586-024-07929-5 |
| [30] |
Zhao M, Yao L, Zhang X, et al. Global identification of the cellular targets for a multi-molecule system by a photochemically-induced coupling reaction[J]. Chem Commun (Camb), 2021, 57(28): 3449-52. doi:10.1039/D1CC00392E |
| [31] |
Cuatrecasas P, Wilchek M, Anfinsen C B. Selective enzyme purification by affinity chromatography[J]. Proc Natl Acad Sci USA, 1968, 61(2): 636-43. doi:10.1073/pnas.61.2.636 |
| [32] |
Taunton J, Hassig C A, Schreiber S L. A mammalian histone deacetylase related to the yeast transcriptional regulator Rpd3p[J]. Science, 1996, 272(5260): 408-11. doi:10.1126/science.272.5260.408 |
| [33] |
Hirota T, Lee J W, St John P C, et al. Identification of small molecule activators of cryptochrome[J]. Science, 2012, 337(6098): 1094-7. doi:10.1126/science.1223710 |
| [34] |
Hackler L, Dormán G, Kele Z, et al. Development of chemically modified glass surfaces for nucleic acid, protein and small molecule microarrays[J]. Mol Divers, 2003, 7(1): 25-36. doi:10.1023/B:MODI.0000006534.36417.06 |
| [35] |
Abood L G, Latham W, Grassi S. Isolation of a nicotine binding site from rat brain by affinity chromatography[J]. Proc Natl Acad Sci USA, 1983, 80(11): 3536-9. doi:10.1073/pnas.80.11.3536 |
| [36] |
Liu L, Hua Y, Wang D, et al. A sesquiterpene lactone from a medicinal herb inhibits proinflammatory activity of TNF-α by inhibiting ubiquitin-conjugating enzyme UbcH5[J]. Chem Biol, 2014, 21(10): 1341-50. doi:10.1016/j.chembiol.2014.07.021 |
| [37] |
王丽超, 刘丹, 姜勇, 等. 基于分子亲和色谱技术的肉苁蓉低分子糖巨噬细胞激活作用靶点群鉴定与机制分析[J]. 中国中药杂志, 2017, 42(19): 3666-71. Wang L C, Liu D, Jiang Y, et al. Targets identification and mechanism analysis for macrophage activation of low molecular weight saccharides from Cistanche deserticola based on molecular affinity chromatography[J]. China J Chin Mater Med, 2017, 42(19): 3666-71. |
| [38] |
Hueber W, Kidd B A, Tomooka B H, et al. Antigen microarray profiling of autoantibodies in rheumatoid arthritis[J]. Arthritis Rheum, 2005, 52(9): 2645-55. doi:10.1002/art.21269 |
| [39] |
Huang J, Zhu H, Haggarty S J, et al. Finding new components of the target of rapamycin (TOR) signaling network through chemical genetics and proteome chips[J]. Proc Natl Acad Sci USA, 2004, 101(47): 16594-9. doi:10.1073/pnas.0407117101 |
| [40] |
Zhang H N, Yang L, Ling J Y, et al. Systematic identification of arsenic-binding proteins reveals that hexokinase-2 is inhibited by arsenic[J]. Proc Natl Acad Sci USA, 2015, 112(49): 15084-9. doi:10.1073/pnas.1521316112 |
| [41] |
Cui Z, Li C, Chen P, et al. An update of label-free protein target identification methods for natural active products[J]. Theranostics, 2022, 12(4): 1829-54. doi:10.7150/thno.68804 |
| [42] |
Mateus A, Määttä T A, Savitski M M. Thermal proteome profiling: unbiased assessment of protein state through heat-induced stability changes[J]. Proteome Sci, 2017, 15: 13. |
| [43] |
Molina D M, Jafari R, Ignatushchenko M, et al. Monitoring drug target engagement in cells and tissues using the cellular thermal shift assay[J]. Science, 2013, 341(6141): 84-7. doi:10.1126/science.1233606 |
| [44] |
Miettinen T P, Björklund M. NQO2 is a reactive oxygen species generating off-target for acetaminophen[J]. Mol Pharm, 2014, 11(12): 4395-404. doi:10.1021/mp5004866 |
| [45] |
Kirsch V C, Orgler C, Braig S, et al. The cytotoxic natural product vioprolide a targets nucleolar protein 14, which is essential for ribosome biogenesis[J]. Angew Chem Int Ed, 2020, 59(4): 1595-600. doi:10.1002/anie.201911158 |
| [46] |
Zhang X W, Li L, Liao M, et al. Thermal proteome profiling strategy identifies CNPY3 as a cellular target of gambogic acid for inducing prostate cancer pyroptosis[J]. J Med Chem, 2024, 67(12): 10005-11. doi:10.1021/acs.jmedchem.4c00140 |
| [47] |
Khan M M, Galea G, Jung J, et al. Dextromethorphan inhibits collagen and collagen-like cargo secretion to ameliorate lung fibrosis[J]. Sci Transl Med, 2024, 16(778): eadj3087. doi:10.1126/scitranslmed.adj3087 |
| [48] |
Lomenick B, Hao R, Jonai N, et al. Target identification using drug affinity responsive target stability (DARTS)[J]. Proc Natl Acad Sci USA, 2009, 106(51): 21984-9. doi:10.1073/pnas.0910040106 |
| [49] |
Amemiya T, Koike R, Fuchigami S, et al. Classification and annotation of the relationship between protein structural change and ligand binding[J]. J Mol Biol, 2011, 408(3): 568-84. doi:10.1016/j.jmb.2011.02.058 |
| [50] |
Schopper S, Kahraman A, Leuenberger P, et al. Measuring protein structural changes on a proteome-wide scale using limited proteolysis-coupled mass spectrometry[J]. Nat Protoc, 2017, 12(11): 2391-410. doi:10.1038/nprot.2017.100 |
| [51] |
Wang F, Zhou S, Qi D, et al. Nucleolin is a functional binding protein for salinomycin in neuroblastoma stem cells[J]. J Am Chem Soc, 2019, 141(8): 3613-22. doi:10.1021/jacs.8b12872 |
| [52] |
Chen S, Liu X, Peng C, et al. The phytochemical hyperforin triggers thermogenesis in adipose tissue via a Dlat-AMPK signaling axis to curb obesity[J]. Cell Metab, 2021, 33(3): 565-80. doi:10.1016/j.cmet.2021.02.007 |
| [53] |
Hu J, Liu W, Zou Y, et al. Allosterically activating SHP2 by oleanolic acid inhibits STAT3-Th17 axis for ameliorating colitis[J]. Acta Pharm Sin B, 2024, 14(6): 2598-612. doi:10.1016/j.apsb.2024.03.017 |
| [54] |
West G M, Tang L, Fitzgerald M C. Thermodynamic analysis of protein stability and ligand binding using a chemical modification- and mass spectrometry-based strategy[J]. Anal Chem, 2008, 80(11): 4175-85. doi:10.1021/ac702610a |
| [55] |
Lu K Y, Quan B, Sylvester K, et al. Plasmodium chaperonin TRiC/CCT identified as a target of the antihistamine clemastine using parallel chemoproteomic strategy[J]. Proc Natl Acad Sci USA, 2020, 117(11): 5810-7. doi:10.1073/pnas.1913525117 |
| [56] |
Kaur U, Meng H, Lui F, et al. Proteome-wide structural biology: an emerging field for the structural analysis of proteins on the proteomic scale[J]. J Proteome Res, 2018, 17(11): 3614-27. doi:10.1021/acs.jproteome.8b00341 |
| [57] |
Cowan D A. Thermophilic proteins: stability and function in aqueous and organic solvents[J]. Comp Biochem Physiol A Physiol, 1997, 118(3): 429-38. doi:10.1016/S0300-9629(97)00004-2 |
| [58] |
Xu M, Moresco J J, Chang M, et al. SHMT2 and the BRCC36/BRISC deubiquitinase regulate HIV-1 Tat K63-ubiquitylation and destruction by autophagy[J]. PLoS Pathog, 2018, 14(5): e1007071. doi:10.1371/journal.ppat.1007071 |
| [59] |
Tian Y, Wan N, Zhang H, et al. Chemoproteomic mapping of the glycolytic targetome in cancer cells[J]. Nat Chem Biol, 2023, 19(12): 1480-91. doi:10.1038/s41589-023-01355-w |
| [60] |
Zhang X, Wang K, Wu S, et al. Highly effective identification of drug targets at the proteome level by pH-dependent protein precipitation[J]. Chem Sci, 2022, 13(42): 12403-18. doi:10.1039/D2SC03326G |
| [61] |
Scott J K, Smith G P. Searching for peptide ligands with an epitope library[J]. Science, 1990, 249(4967): 386-90. doi:10.1126/science.1696028 |
| [62] |
Jin Y, Yu J, Yu Y G. Identification of hNopp140 as a binding partner for doxorubicin with a phage display cloning method[J]. Chem Biol, 2002, 9(2): 157-62. doi:10.1016/S1074-5521(02)00096-0 |
| [63] |
Giaever G, Shoemaker D D, Jones T W, et al. Genomic profiling of drug sensitivities via induced haploinsufficiency[J]. Nat Genet, 1999, 21(3): 278-83. doi:10.1038/6791 |
| [64] |
Titov D V, Gilman B, He Q L, et al. XPB, a subunit of TFⅡH, is a target of the natural product triptolide[J]. Nat Chem Biol, 2011, 7(3): 182-8. doi:10.1038/nchembio.522 |
| [65] |
Yadav B, Gopalacharyulu P, Pemovska T, et al. From drug response profiling to target addiction scoring in cancer cell models[J]. Dis Model Mech, 2015, 8(10): 1255-64. doi:10.1242/dmm.021105 |
| [66] |
Zhu Y, Ouyang Z, Du H, et al. New opportunities and challenges of natural products research: When target identification meets single-cell multiomics[J]. Acta Pharm Sin B, 2022, 12(11): 4011-39. doi:10.1016/j.apsb.2022.08.022 |
| [67] |
Liu J, Lee J, Salazar Hernandez M A, et al. Treatment of obesity with celastrol[J]. Cell, 2015, 161(5): 999-1011. doi:10.1016/j.cell.2015.05.011 |
| [68] |
Wu X, Bos I S T, Conlon T M, et al. A transcriptomics-guided drug target discovery strategy identifies receptor ligands for lung regeneration[J]. Sci Adv, 2022, 8(12): eabj9949. doi:10.1126/sciadv.abj9949 |
| [69] |
Liu X, Ouyang S, Yu B, et al. PharmMapper server: a web server for potential drug target identification using pharmacophore mapping approach[J]. Nucleic Acids Res, 2010, 38(Web Server issue): W609-14. |
| [70] |
Wang X, Shen Y, Wang S, et al. PharmMapper 2017 update: a web server for potential drug target identification with a comprehensive target pharmacophore database[J]. Nucleic Acids Res, 2017, 45(W1): W356-60. doi:10.1093/nar/gkx374 |
| [71] |
刘广欣, 赵泽丰, 解景, 等. 基于药效团和分子对接技术对甘草中AChE抑制成分的虚拟筛选[J]. 中国中药杂志, 2020, 45(10): 2431-8. Liu G X, Zhao Z X, Xie J, et al. Virtual screen of effective AChE inhibitory constituents from Glycyrrhizae Radix et Rhizoma based on pharmacophore and molecular docking[J]. China J Chin Mater Med, 2020, 45(10): 2431-8. |
| [72] |
Yang X, Wang Y, Byrne R, et al. Concepts of artificial intelligence for computer-assisted drug discovery[J]. Chem Rev, 2019, 119(18): 10520-94. doi:10.1021/acs.chemrev.8b00728 |
| [73] |
唐跃威, 刘治平. 基于深度学习与多层次信息融合的药物靶标亲和力预测[J]. 中国生物工程杂志, 2021, 41(11): 40-7. Tang Y W, Liu Z P. Drug-target affinity prediction based on deep learning and multi-layered information fusion[J]. China Biotechnol, 2021, 41(11): 40-7. |
| [74] |
Wang T, Wu M B, Zhang R H, et al. Advances in computational structure-based drug design and application in drug discovery[J]. Curr Top Med Chem, 2016, 16(9): 901-16. |
| [75] |
Acharya C, Coop A, Polli J E, et al. Recent advances in ligand-based drug design: relevance and utility of the conformationally sampled pharmacophore approach[J]. Curr Comput Aided Drug Des, 2011, 7(1): 10-22. doi:10.2174/157340911793743547 |
| [76] |
Yang H, Chen Y, Zuo Y, et al. MINDG: a drug-target interaction prediction method based on an integrated learning algorithm[J]. Bioinformatics, 2024, 40(4): btae147. doi:10.1093/bioinformatics/btae147 |
| [77] |
Duan Y, Zhou H, Liu X, et al. Molecular mechanisms of SARS-CoV-2 resistance to nirmatrelvir[J]. Nature, 2023, 622(7982): 376-82. doi:10.1038/s41586-023-06609-0 |
| [78] |
吴昊, 林铭, 孙懿, 等. 新一代人工智能技术驱动下的新药研发[J]. 中国药理学通报, 2019, 35(7): 889-93. Wu H, Lin M, Sun Y, et al. Research and development of new drugs driven by novel generation AI technology[J]. Chin Pharmacol Bull, 2019, 35(7): 889-93. doi:10.3969/j.issn.1001-1978.2019.07.001 |
| [79] |
Abramson J, Adler J, Dunger J, et al. Accurate structure prediction of biomolecular interactions with AlphaFold 3[J]. Nature, 2024, 630(8016): 493-500. doi:10.1038/s41586-024-07487-w |
| [80] |
许奇, 张洪榕, 阮诺冰, 等. 基于人工智能辅助药物质量评价结合药效学研究木犀草素对db/db小鼠糖脂代谢及肝脏氧化应激损伤的作用及机制[J]. 中国药理学通报, 2025, 41(2): 323-33. Xu Q, Zhang H R, Ruan R B, et al. Effects of luteolin on glucose and lipid metabolism and liver oxidative stress injury in db/db mice based on artificial intelligence assisted drug quality evaluation and pharmacodynamics and its mechanisms[J]. Chin Pharmacol Bull, 2025, 41(2): 323-33. doi:10.12360/CPB202407045 |
| [81] |
Cockroft N T, Cheng X L, Fuchs J R. STarFish: a stacked ensemble target fishing approach and its application to natural products[J]. J Chem Inf Model, 2019, 59(11): 4906-20. doi:10.1021/acs.jcim.9b00489 |

