

2. 郑州大学药学院药理学系,河南 郑州 450066
2. Dept of Pharmacology, School of Pharmacy, Zhengzhou University, Zhengzhou Henan 450066, China
脑缺血/再灌注损伤(cerebral ischaemia reperfusion injury,CIRI)是神经内科中常见的一种多发病,病情危重,高致残率及高死亡率的急性脑血管病,严重危害人类生命健康[1]。研究显示,CIRI发生后出现的氧化应激、炎症反应、细胞凋亡等是导致神经元损伤的重要病因[2]。但是目前有关CIRI神经元损伤的具体分子机制尚不清楚。细胞焦亡是一种新的炎症表现,可调节性细胞坏死,广泛参与多种疾病的发生发展。研究显示大鼠CIRI后神经元焦亡指数明显升高,焦亡相关蛋白cleaved caspase-1/pro-caspase-1、GSDMD-N/GSDMD、IL-1β和IL-18表达均明显升高,抑制caspase-1介导的细胞焦亡能够明显减轻CIRI大鼠神经损伤[3],提示caspase-1介导的细胞可能是CIRI神经损伤的重要机制。因此,以caspase-1介导的细胞焦亡为切入点探究CIRI神经损伤的药物治疗尤为重要。
银杏叶提取物(ginkgo biloba extract,GBE)是从银杏叶中获取的醇提取物,主要有效成分包括黄酮类、萜内酯类,具有抗炎、抗氧化和氧自由基以及神经保护作用[4]。以往研究显示GBE能够通过抑制炎症因子释放,降低脑组织氧化应激及炎症水平,改善CIRI大鼠神经损伤[5]。但是目前有关GBE对CIRI大鼠神经元焦亡的作用及机制尚不清楚。磷脂酰激醇3-激酶(phosphatidylin-ositol-3-kinase,PI3K)/蛋白激酶B(protein kinase B,Akt)信号通路与CIR后神经炎症反应密切相关。神经节苷脂能够通过调控PI3K/Akt通路抑制炎症反应,降低炎症因子释放,从而达到神经元保护作用,提示激活PI3K/Akt通路可能是治疗CIRI的关键[6]。既往文献报道,GBE能够通过调控PI3K/Akt通路,降低氧自由基,改善创伤性大鼠CIRI[7]。但是有关GBE能否通过调控PI3K/Akt通路介导的细胞焦亡参与CIRI神经元损尚不清楚。为此,本研究拟通过线栓法构建大鼠CIR模型,探究GBE对CIRI大鼠神经元损伤及焦亡的影响,阐明PI3K/Akt信号通路在GBE介入治疗CIRI中的作用,以期为GBE介入治疗CIRI提供更多的实验依据。
1 材料与方法 1.1 材料 1.1.1 动物♂,SPF级,SD大鼠124只,体质量(180~200) g,购买于郑州大学医学院实验动物学部,生产许可证号:SCXK(豫)2018-0007,使用许可证号:SYXK(豫)2019-0013。动物房设置条件:温度:(25±2)℃,湿度:50%~65%,12 h/12 h昼夜交替光照,模拟昼夜,自由饮食、饮水,适应性喂养1周。动物实验符合3R原则,且本实验通过我院动物医学伦理委员会审查(批件号:2021LL017)。
1.1.2 药物与主要试剂GBE(北京中检院);TNF-α、IL-1β、IL-18、IL-6检测试剂盒(上海拜力生物科技有限公司,批号分别:20160645TNF1M、20165200IL1M、20160648IL18M、20180052IL6M);苏木精-伊红(hematoxylin-eosin,HE)检测试剂盒、anti-β-actin、HRP标记的山羊抗鼠IgG、HRP标记的山羊抗兔IgG(碧云天生物技术公司,批号:C0105S、AF0003、A0412、A0408);2, 3, 5-三苯基氯化四氮唑(TTC)试剂(武汉华翔科洁生物技术有限公司,批号:298-96-4);anti-NLRP3、anti-ASC、anti-caspase-1、anti-GSDMD、anti-IL-1β、anti-IL-18、anti-p-PI3K、anti-PI3K、anti-p-Akt、anti-Akt(美国Cell Signaling Technology,批号分别:9158、5759、13158、83383、39754、12703、67775、4249、4060、4685)。
1.1.3 实验仪器酶标仪(长春乐镤科技有限公司,型号:LP-5117);荧光倒置显微镜(日本/奥林巴斯Olympus,型号:CKX53);高速冷冻离心机(湖南可成仪器设备有限公司,型号:H3-18KR);凝胶成像系统(美国Bio-Rad伯乐公司,型号:Gel Doc XR+);-80 ℃冷冻冰箱(日本SANYO公司,型号:MDF-C8V(N))。
1.2 方法 1.2.1 CIRI大鼠模型构建、分组及给药[8-9]将124只雄性SD大鼠按照随机数字表法分为假手术组(Sham)24只和造模组100只。造模组大鼠均采用线栓法构建大鼠CIR模型。具体步骤如下:利用线栓法构建大鼠中脑动脉栓塞/再灌注模型,即缺血性脑卒中大鼠模型。3%戊巴比妥钠(30 mg·kg-1)腹腔注射麻醉,大鼠颈部正中切口,分离颈总动脉、颈外动脉和颈内动脉,结扎颈总动脉远端和颈外动脉近心端,之后在颈总动脉分叉处剪开小口,插入手术线栓(4-0),线栓从颈总动脉延伸至颈内动脉并向上到达大脑中动脉,从而造成大脑中动脉起始端及其侧枝缺血,90 min后拔出线栓,缝合皮肤。假手术组大鼠仅行相同手术操作,不结扎。100只造模大鼠共有96只SD大鼠造模成功,随后将96只造模成功大鼠随机分为CIR组、GBE低剂量组(GBE-L)、GBE高剂量组(GBE-H)及PI3K抑制剂组(LY294002),每组各24只。GBE-L、GBE-H组分别对应腹腔注射GBE 25 mg·kg-1·d-1和100 mg·kg-1·d-1,共给药7 d,LY294002组大鼠腹腔注射100 mg·kg-1·d-1 GBE的同时行头皮切开术,经侧脑室一次性注射PI3K抑制剂LY294002(10 μL,10 mmol ·L-1),Sham组和CIR组大鼠腹腔注射等量的生理盐水。各组大鼠给药结束后腹腔注射1%戊巴比妥钠麻醉大鼠,取血、断头,取脑组织,保存备用。
1.2.2 神经功能评分、脑组织含水量计算每组随机选取6只SD大鼠采用Zea-Longa[9]法进行神经功能评分,0分:无神经学损伤症状;1分:左前肢无法完全伸展;2分:左侧肢出现瘫痪,并伴有追尾现象以及行走向左侧转圈;3分:出现行走时向一侧偏倒,站立不行,打滚;4分:出现明显的意识障碍,且无自发活动,其中1~3分为造模成功。大鼠脑组织含水量测定,各组大鼠给药结束后处死,取出大脑,称量大脑湿种重量,之后将大脑组织放置于恒温烘箱中进行烘烤24 h,称量大脑干质量,计算得出各组大鼠脑组织含水量。脑组织含水量=(脑湿重-脑干重)/脑湿重×100%。
1.2.3 HE染色观察脑组织病理学形态变化每组随机选取6只SD大鼠,经10%多聚甲醛固定脑组织标本、脱水、透明石蜡包埋,制备组织切片,切片厚度约3~5 μm,之后行HE染色、封片后于400倍显微镜下观察组织病理学变化。
1.2.4 脑梗死体积测定实验结束后,每组随机选取6只SD大鼠,迅速取出大鼠脑组织并放置于-20 ℃冰箱冰冻至硬,行冠状切片,切片厚度约2 mm,于37 ℃,避光条件下,将切片放置于2% TTC染色液中,着色30 min,最后使用4%的多聚甲醛固定,拍照分析。正常脑组织染色呈红色,梗死脑组织染色呈白色,实验结果采用ImageJ进行图像分析,计算各组大鼠脑梗死体积。
1.2.5 血清TNF-α、IL-6、IL-1β、IL-18含量检测给药结束后,每组随机选取6只SD大鼠尾静脉采血,4 ℃,3 000 r·min-1离心10 min,吸取上清液,按照ELISA试剂盒进行TNF-α、IL-6、IL-1β及IL-18含量检测。
1.2.6 TUNEL染色检测神经元焦亡切片制备同HE,行TUNEL染色及神经元染色,之后按照检测试剂盒说明书进行操作,显微镜下,每张切片随机选取5个视野,计算各组大鼠脑组织神经元焦亡率。神经元焦亡率=TUNEL阳性细胞数/神经元细胞总数×100%。
1.2.7 Western blot检测焦亡相关蛋白及PI3K/Akt通路蛋白表达每组随机选取6只SD大鼠,收集大鼠脑组织,剪碎后混合加入蛋白酶抑制剂的RIPA细胞裂解液,于4 ℃条件下,裂解30 min。将离心管放置于离心机内,并设置:4 ℃,13 400×g离心10 min,吸取上清液。BCA法测定蛋白质浓度,蛋白质变性,蛋白上样,于SDS-PAGE凝胶电泳,分离蛋白。凝胶湿转转膜法转至PVDF膜上。室温条件下PVDF采用6%BSA封闭1 h,TBST洗膜后孵育anti-NLRP3、anti-ASC、anti-caspase-1、anti-GSDMD、anti-IL-1β、anti-IL-18、anti-p-PI3K、anti-PI3K、anti-p-Akt、anti-Akt、anti-β-actin,稀释比例均为1 ∶ 1 000,4 ℃下孵育16 h。次日取出PVDF膜,TBST洗涤后加入相应HRP标记的山羊抗鼠IgG、山羊抗兔IgG孵育2 h。TBST洗涤3次,滴加显影液,采用ImageJ软件进行NLRP3、ASC、caspase-1、GSDMD、IL-1β、IL-18、p-PI3K、p-Akt蛋白表达定量。
1.2.8 统计学方法实验数据采用SPSS 22.0软件分析。数据以x±s表示,多组间比较采用单因素方差分析,组间两两比较采用LSD-t检验。检验水准α=0.05。
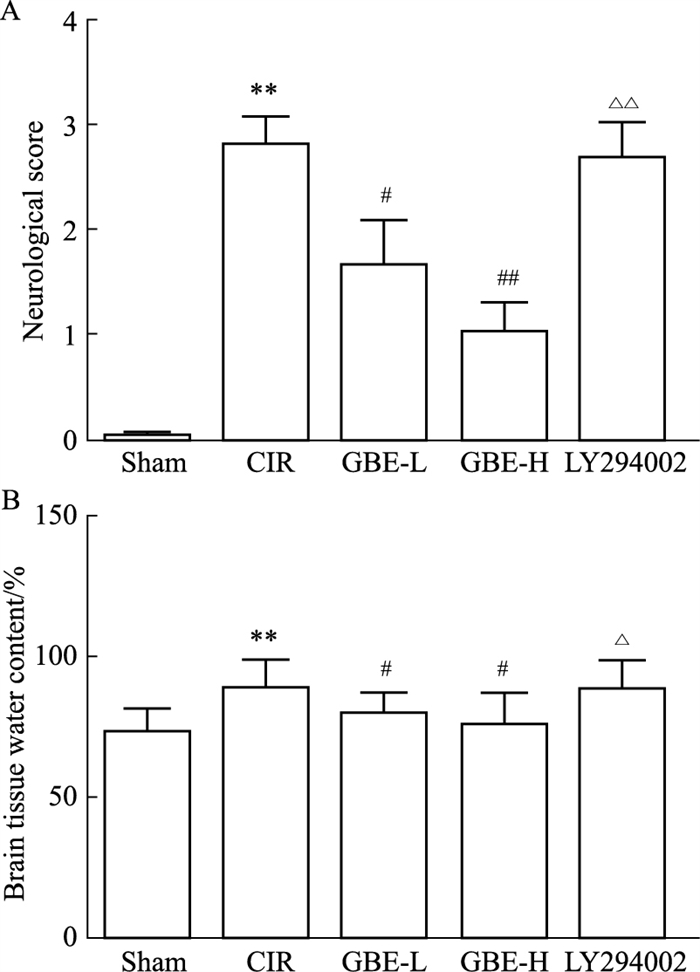
2 结果 2.1 各组大鼠神经功能损伤评分、脑组织含水量比较如Fig 1所示,与Sham组相比,CIR组大鼠神经功能损伤评分、脑组织含水量均明显升高(P < 0.01)。与CIR组相比,GBE-L、GBE-H组大鼠神经功能损伤评分、脑组织含水量均明显降低(P < 0.05或P < 0.01)。与GBE-H组相比,LY294002组大鼠神经功能损伤评分、脑组织含水量均明显升高(P < 0.05或P < 0.01)。
|
| Fig 1 Comparison of neurological function injury scores, brain tissue water content of rats in each group (x±s, n=6) A: Neurological score; B: Brain tissue water content. **P < 0.01 vs Sham group; #P < 0.05, ##P < 0.01 vs CIR group; △P < 0.05, △△P < 0.01 vs GBE-H group. |
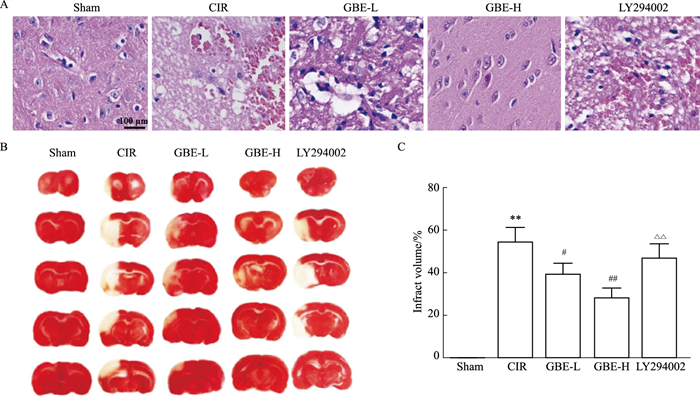
如Fig 2所示,HE染色显示,Sham组大鼠脑组织细胞排列整齐,结构清晰完整,细胞核着色均匀。CIR组大鼠脑组织细胞肿胀变形,排列紊乱,细胞间间隙变宽,有坏死灶的形成。与CIR组相比,GBE-L、GBE-H组大鼠脑组织细胞形态相对整齐,结构完整,细胞间间隙减小,病理损伤明显减轻。与GBE-H组相比,LY294002组大鼠脑组织细胞肿胀,细胞排列紊乱,病理损伤明显加重。TTC染色显示,Sham组大鼠物脑梗死病灶。与Sham组相比,CIR组大鼠大鼠脑梗死体积明显增加(P < 0.01)。与CIR组相比,GBE-L和GBE-H组大鼠脑梗死体积明显降低(P < 0.05或P < 0.01)。与GBE-H组相比,LY294002组大鼠脑梗死体积明显增加(P < 0.01)。
|
| Fig 2 Changes in pathological structure of brain tissue of rats in each group (x±s, n=6) A: Morphological changes in brain histopathology observed by HE staining (×200); B: TTC staining for cerebral infarct volume; C: Quantification of B.**P < 0.01 vs Sham group; #P < 0.05, ##P < 0.01 vs CIR group; △△P < 0.01 vs GBE-H group. |
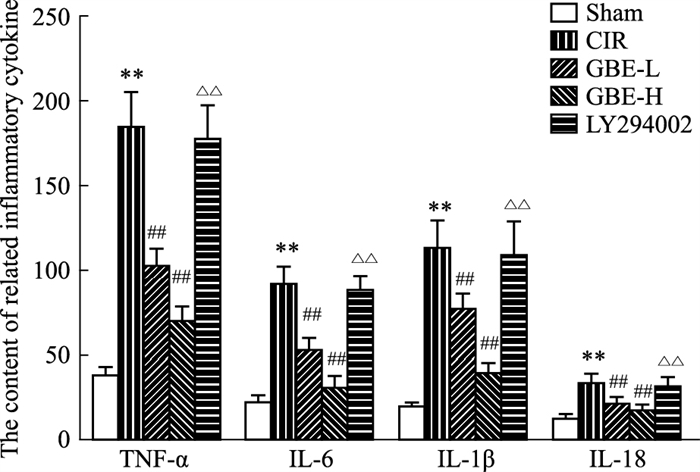
如Fig 3所示,与Sham组相比,CIR组大鼠血清TNF-α、IL-6、IL-1β、IL-18含量均明显升高(P < 0.01)。与CIR组相比,GBE-L、GBE-H组大鼠血清TNF-α、IL-6、IL-1β、IL-18含量均明显降低(P < 0.05或P < 0.01)。与GB-H组相比,LY294002组大鼠血清TNF-α、IL-6、IL-1β、IL-18含量均明显升高(P < 0.01)。
|
| Fig 3 Comparison of serum levels of TNF-α, IL-6, IL-1β and IL-18 in each group of rats (x±s, n=6) **P < 0.01 vs Sham group; ##P < 0.01 vs CIR group; △△P < 0.01 vs GBE-H group. |
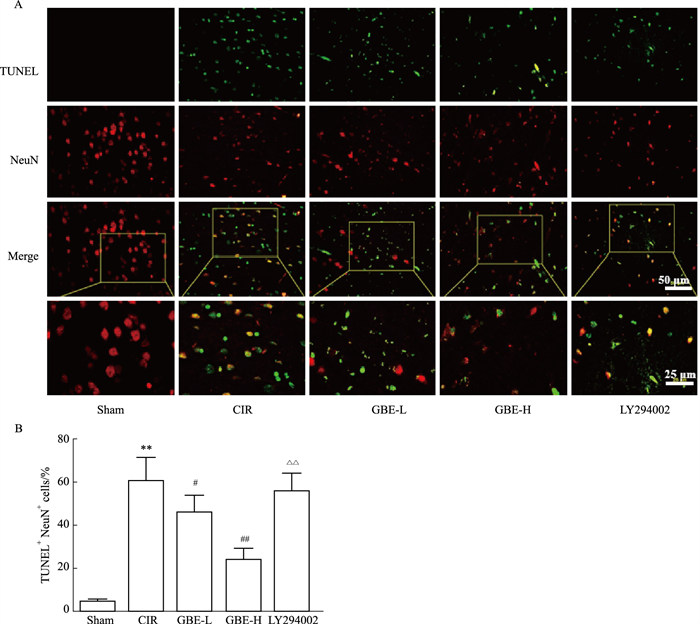
如Fig 4所示,与Sham组相比,CIR组大鼠神经元焦亡指数升高(P < 0.01)。与CIR组相比,GBE-L、GBE-H组大鼠神经元焦亡指数降低(P < 0.01)。与GBE-H组相比,LY294002组大鼠神经元焦亡指数升高(P < 0.01)。
|
| Fig 4 Comparison of neuron pyroptosis index in each group of rats (x±s, n=6) A: Neuronal pyroptosis detected by TUNEL staining; B: The ratio of TUNEL+ NeuN+ cells. **P < 0.01 vs Sham group; #P < 0.05, ##P < 0.01 vs CIR group; △△P < 0.01 vs GBE-H group. |
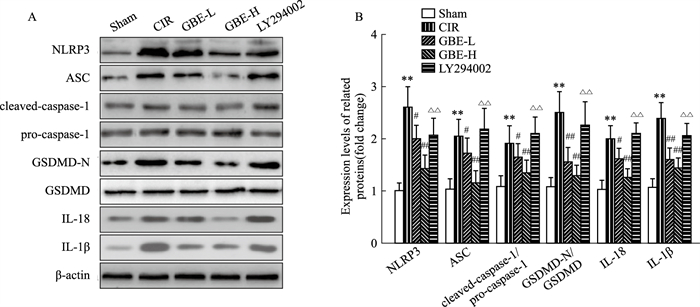
为进一步明确GBE对CIR神经元焦亡的影响,本研究通过Western blot检测焦亡相关蛋白表达。如Fig 5所示,与Sham组相比,CIR组大鼠脑组织NLRP3、ASC、cleaved caspase-1/pro-caspase-1、GSDMD-N/ GSDMD、IL-1β、IL-18蛋白表达均明显升高(P < 0.01)。与CIR组相比,GBE-L, GBE-H组大鼠NLRP3、ASC、cleaved caspase-1/pro-caspase-1、GSDMD-N/GSDMD、IL-1β、IL-18蛋白表达均明显降低(P < 0.05或P < 0.01)。与GBE-H组相比,LY294002组大鼠NLRP3、ASC、cleaved caspase-1/pro-caspase-1、GSDMD-N/GSDMD、IL-1β、IL-18蛋白表达均明显升高(P < 0.01)。
|
| Fig 5 Expression of pyroptosis-related proteins in brain tissue of rats in each group (x±s, n=6) A: The bands of pyroptosis-related proteins; B: Quantification of A. **P < 0.01 vs Sham group; #P < 0.05, ##P < 0.01 vs CIR group; △△P < 0.01 vs GBE-H group. |
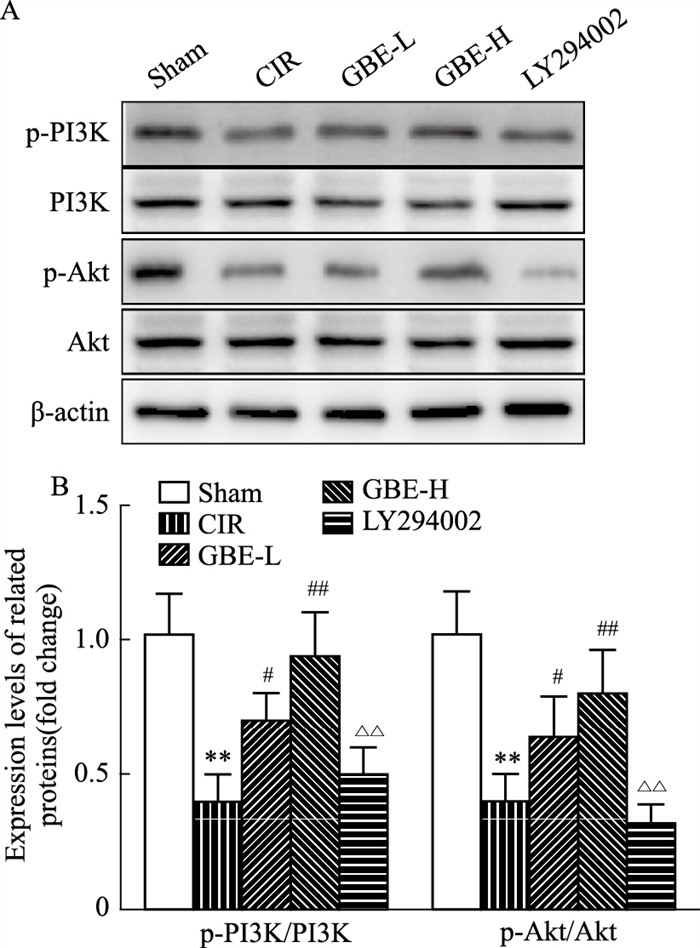
为进一步阐明GBE对CIR神经元焦亡的作用机制,本研究通过Western blot检测PI3K/Akt通路蛋白表达。如Fig 6所示,与Sham组相比,CIR组大鼠脑组织p-PI3K/PI3K、p-Akt/Akt均明显降低(P < 0.01)。与CIR组相比,GBE-L, GBE-H组大鼠脑组织p-PI3K/PI3K、p-Akt/Akt均明显升高(P < 0.01)。与GBE-H组相比,LY294002组大鼠脑组织p-PI3K/PI3K、p-Akt/Akt均明显降低(P < 0.01)。
|
| Fig 6 Expression of PI3K/Akt pathway protein in rats of each group (x±s, n=6) A: The bands of pyroptosis-related proteins; B: Quantification of A. **P < 0.01 vs Sham group; #P < 0.05, ##P < 0.01 vs CIR group; △△P < 0.01 vs GBE-H group. |
线栓法是动物CIRI模型构建的经典方法,具有操作简单,符合临床脑梗死的病症等特点。本研究显示线栓法结扎大脑中动脉后大鼠神经功能评分及脑梗死体积均显著增加,表明CIR模型构建成功。GBE广泛应用于治疗阿尔茨海默病及帕金森病等中枢神经系统退行性疾病,具有良好的临床疗效。本研究显示,CIRI大鼠给予GBE干预后能够明显降低大鼠神经功能评分,脑组织含水量及脑梗死体积,表明GBE能够缓解CIRI大鼠继发的脑水肿,改善神经功能损伤。
炎症反应、细胞凋亡等是CIRI发生后产生的常见性继发神经性损伤,其中以CIRI炎症反应为最常见的病理学反应机制,也是导致神经功能障碍的主要原因[10]。研究发现,IL-1β、TNF-α和IL-6等释放增加会导致血脑屏障破坏及大量神经细胞死亡,而经干扰素治疗后能够抑制炎症细胞因子水平,减轻CIRI神经损伤,提示抑制炎性反应是防治CIRI神经功能损伤的重要方式[11-12]。本研究结果显示,经GBE干预后TNF-α、IL-6、IL-1β、IL-18均明显降低,表明GBE能够通过抑制炎症反应,改善CIR神经损伤。焦亡是以NOD样受体蛋白3(NOD-like receptor protein 3,NLRP3)炎症小体活化介导的炎症性细胞死亡方式,参与CIRI发生发展[13]。既往研究发现在CIRI大鼠脑组织中焦亡相关蛋白表达明显升高,而抑制caspase-1表达能够明显改善CIR神经损伤[3]。另外,在CIRI大鼠NLRP3炎性小体亦被明显激活,而采用NLRP3抑制MCC950处理后能够明显改善CIRI继发的神经功能损伤[14]。本研究结果显示,GBE能够抑制焦亡相关蛋白表达及神经元焦亡,减轻神经功能损伤。PI3K/Akt信号通路参与CIRI神经炎症反应,激活信号通路能够降低炎症细胞因子释放,抑制炎症反应,从而发挥脑神经元保护作用[15]。研究证实在蛛网膜下腔出血大鼠模型中丙泊酚能够通过激活PI3K/Akt信号通路,抑制炎症因子表达,发挥神经功能保护作用,且此保护作用可明显被PI3K抑制剂LY294002阻断[16]。另外,瓜蒌桂枝颗粒能够通过激活PI3K/Akt信号通路,抑制细胞焦亡,发挥脑缺血/再灌注损伤神经保护作用,而给予PI3K抑制剂LY294002处理后能够阻断瓜蒌桂枝颗粒对神经元焦亡的作用,加重脑缺血/再灌注后神经损伤[17]。本研究结果显示经GBE干预后PI3K/Akt信号通路蛋白表达均明显升高。此外,通过对大鼠侧脑室注射PI3K抑制LY294002,此时GBE对CIR的保护作用被明显逆转,炎症因子及脑组织焦亡相关蛋白、神经元焦亡指数均明显增加。
综上所述,GBE能够改善大鼠CIR神经元损伤,促进PI3K/Akt通路活化,抑制神经元焦亡相关。以上研究结果初步揭示了GBE治疗脑梗死的新机制,为其作为脑梗死临床治疗提供了可靠的实验依据。
| [1] |
罗佳, 吴宇, 刘京东, 等. 香叶醇通过调控Nrf2/HO-1途径调节氧化应激减轻大鼠脑缺血/再灌注损伤[J]. 中国药理学通报, 2024, 40(3): 431-9. Luo J, Wu Y, Liu J D, et al. Geraniol attenuates cerebral ischemia-reperfusion injury in rats by regulating oxidative stress via Nrf2/HO-1 pathway[J]. Chin Pharmacol Bull, 2024, 40(3): 431-9. doi:10.12360/CPB202310025 |
| [2] |
Zhang M, Liu Q, Meng H, et al. Ischemia-reperfusion injury: molecular mechanisms and therapeutic targets[J]. Signal Transduct Target Ther, 2024, 9(1): 12. doi:10.1038/s41392-023-01688-x |
| [3] |
Shi M, Chen J, Liu T, et al. Protective effects of remimazolam on cerebral ischemia/reperfusion injury in rats by inhibiting of NLRP3 inflammasome-dependent pyroptosis[J]. Drug Des Devel Ther, 2022, 16: 413-23. doi:10.2147/DDDT.S344240 |
| [4] |
胡哲, 赵军, 宋嵬, 等. 银杏叶提取物对脑缺血/再灌注损伤模型大鼠的脑保护作用[J]. 中国比较医学杂志, 2022, 32(9): 55-61. Hu Z, Zhao J, Song W, et al. Protective effect of ginkgo biloba extract on the brain in a cerebral ischemia-reperfusion injury rat model[J]. Chin J Comp Med, 2022, 32(9): 55-61. doi:10.3969/j.issn.1671-7856.2022.09.008 |
| [5] |
Song W, Zhao J, Yan X S, et al. Mechanisms associated with protective effects of ginkgo biloba leaf extracton in rat cerebral ischemia reperfusion injury[J]. J Toxicol Environ Health A, 2019, 82(19): 1045-51. doi:10.1080/15287394.2019.1686215 |
| [6] |
Gong G, Yin L, Yuan L, et al. Ganglioside GM1 protects against high altitude cerebral edema in rats by suppressing the oxidative stress and inflammatory response via the PI3K/AKT-Nrf2 pathway[J]. Mol Immunol, 2018, 95: 91-8. doi:10.1016/j.molimm.2018.02.001 |
| [7] |
Guo Y, Mao M, Li Q, et al. Extracts of Ginkgo flavonoids and ginkgolides improve cerebral ischaemia-reperfusion injury through the PI3K/Akt/Nrf2 signalling pathway and multicomponent in vivo processes[J]. Phytomedicine, 2022, 99: 154028. doi:10.1016/j.phymed.2022.154028 |
| [8] |
Chen Y, Wu J, Zhu J, et al. Artesunate provides neuroprotection against cerebral ischemia-reperfusion injury via the TLR-4/NF-κB pathway in rats[J]. Biol Pharm Bull, 2021, 44(3): 350-6. doi:10.1248/bpb.b20-00604 |
| [9] |
Liu Y, Zhu X, Tong X, et al. Syringin protects against cerebral ischemia/reperfusion injury via inhibiting neuroinflammation and TLR4 signaling[J]. Perfusion, 2022, 37(6): 562-9. doi:10.1177/02676591211007025 |
| [10] |
Zhang H, Feng Y, Si Y, et al. Shank3 ameliorates neuronal injury after cerebral ischemia/reperfusion via inhibiting oxidative stress and inflammation[J]. Redox Biol, 2024, 69: 102983. doi:10.1016/j.redox.2023.102983 |
| [11] |
Xiang M, Wang L, Guo S, et al. Interferon regulatory factor 8 protects against cerebral ischaemic-reperfusion injury[J]. J Neurochem, 2014, 129(6): 988-1001. doi:10.1111/jnc.12682 |
| [12] |
Cai Q, Zhao C, Xu Y, et al. Qingda granule alleviates cerebral ischemia/reperfusion injury by inhibiting TLR4/NF-kappaB/NLRP3 signaling in microglia[J]. J Ethnopharmacol, 2024, 324: 117712. doi:10.1016/j.jep.2024.117712 |
| [13] |
Huang Y, Xu W, Zhou R. NLRP3 inflammasome activation and cell death[J]. Cell Mol Immunol, 2021, 18(9): 2114-27. doi:10.1038/s41423-021-00740-6 |
| [14] |
Franke M, Bieber M, Kraft P, et al. The NLRP3 inflammasome drives inflammation in ischemia/reperfusion injury after transient middle cerebral artery occlusion in mice[J]. Brain Behav Immun, 2021, 92: 223-33. |
| [15] |
Li J, Dong S, Quan S, et al. Nuciferine reduces inflammation induced by cerebral ischemia-reperfusion injury through the PI3K/Akt/NF-kappaB pathway[J]. Phytomedicine, 2024, 125: 155312. doi:10.1016/j.phymed.2023.155312 |
| [16] |
Zhang H B, Tu X K, Chen Q, et al. Propofol reduces inflammatory brain injury after subarachnoid hemorrhage: Involvement of PI3K/Akt pathway[J]. J Stroke Cerebrovasc Dis, 2019, 28(12): 104375. doi:10.1016/j.jstrokecerebrovasdis.2019.104375 |
| [17] |
Zhang Y, Wang H, Li H, et al. Gualou Guizhi Granule protects against OGD/R-induced injury by inhibiting cell pyroptosis via the PI3K/Akt signaling pathway[J]. Evid Based Complement Alternat Med, 2021, 2021: 6613572. |

