

2. 浙江大学药学院,浙江 杭州 310058;
3. 宁波大学附属康宁医院,浙江 宁波 315201
2. College of Pharmaceutical Sciences, Zhejiang University, Hangzhou 310058, China;
3. the Affiliated Kangning Hospital of Ningbo University, Ningbo Zhejiang 315201, China
阿尔茨海默病(Alzheimer’s disease, AD),又叫老年性痴呆,是一种以获得性记忆减退、认知功能障碍等为主要特征的中枢神经系统退行性疾病[1]。目前我国AD患病人数已超过1 000万,占全球病例总数的25%,而且随着人口老龄化加剧,AD病人数会更多,这将给我国的社会经济和卫生系统带来沉重的负担和巨大的挑战[2]。目前多数学者认为,与淀粉样前体蛋白(amyloid precursor protein,APP)代谢通路相关的β-淀粉样蛋白(β-amyloid protein,Aβ)沉积和神经炎症在AD病理进程中起着至关重要的作用[3]。因此,目前新药研发的热点之一是寻找Aβ相关靶点及其作用效果与作用机制研究[4],并取得突出的成果,如2018年我国创制了首个靶向Aβ寡糖分子的AD新药(GV-971)[5]。
中药因具有多靶点、多系统、多途径作用,疗效稳定,毒副作用小的特点,在治疗AD上具有优良的临床应用价值,并可弥补化学药作用机制单一的缺点[6]。研究表明[7],多种中药可通过调控Aβ水平,降低神经炎性,从而有效改善AD症状以及缓解AD进程。其中,黄酮类成分如黄芩苷和银杏叶提取物,能够抑制Aβ沉积以及减轻神经炎症从而发挥对AD的治疗作用[8-9]。蒙花苷是一种黄酮苷类活性成分,广泛存在于野菊花等植物中。据文献[10-11]报道,蒙花苷具有抑制乙酰胆碱酯酶活性的作用,也可通过NF-κB、MAPKs、TNF及PI3K/Akt信号通路起到抗炎与神经保护作用,可作为AD治疗的候选药物。本课题组长期致力于抗老年痴呆组分的中药研究,积累了中药治疗AD候选药物研发的基础[12-13]。课题组已构建AD斑马鱼模型,研究发现蒙花苷具有抑制乙酰胆碱酯酶活性、消除Aβ沉积与有效缓解神经炎症的综合作用,并提出了蒙花苷对AD多种病理特征改善与症状相互关联的机制探索新思路[14]。本研究则从Aβ沉积和神经炎症两个重要病理特征评价蒙花苷对APP/PS1小鼠在行为学方面的治疗效果,深入探究蒙花苷防治老年痴呆症效果,展示中药治疗AD的独到之处。
1 材料 1.1 动物SPF级15周龄雄性APP/PS1转基因小鼠40只,同周龄C57BL/6J小鼠8只,体质量均为(30±5) g,均由杭州子源实验动物科技有限公司提供,动物许可证号:SCXK(浙)2019-0004。屏障级动物实验室喂养适应1周后进行实验,小鼠自由饮水和摄食,室温控制在(23~25)℃,湿度控制在50%~70%,自然光线,每12 h昼夜交替。动物实验开展于杭州市医学院动物实验中心,各项动物实验操作均符合伦理委员会标准,伦理审查批号(MR-33-23-013971)。
1.2 药物与主要试剂盐酸多奈哌齐片(Donepezil, DPZ,批号:02230250,植恩生物技术股份有限公司);蒙花苷(纯度≥90%,宝鸡市方晟生物开发有限公司);Aβ42 ELISA Kit(CSB-E10787m)购自华美;胶质纤维酸性蛋白(glial fibrillary acidic protein, GFAP) antibody(16825-1-AP)、Presenilin-1-Specific antibody(16163-1-AP)、β-分泌酶(BACE1) antibody(12807-1-AP)均购自Proteintech;BCA蛋白定量检测试剂盒(G2026)、SDS-PAGE凝胶制备试剂盒(G2037)均购自Servicebio;ECL(HK0005)购自HaokeBio。
1.3 仪器Morris水迷宫(中国医学科学院药物研究所);数字化全切片病理扫描仪(江丰生物,型号KF-FL-020);正置白光拍照显微镜(Nikon,型号Eclipse Ci-L);3D Histech(丹吉尔,Pannoramic SCAN);全波长酶标仪(Molecular Devices,Spectramax M2);匀浆仪(Servicebio,KZ-Ⅱ);冷冻离心机(Haier Biomedica,LX-165T2R)。
2 方法 2.1 动物分组与给药适应性饲养1周后,将40只APP/PS1小鼠随机分为模型组、蒙花苷高剂量组(Lianrin-H, 120 mg·kg-1)、蒙花苷中剂量组(Lianrin-M, 60 mg·kg-1)、蒙花苷低剂量组(Lianrin-L, 30 mg·kg-1)、阳性对照组多奈哌齐(DPZ, 0.92 mg·kg-1),8只野生型C57BL/6J小鼠为正常组。6组小鼠每天灌胃1次,药物干预组按上述剂量灌胃,其余2组以等体积生理盐水灌胃。
2.2 行为学检测(Morris水迷宫法)给药4周后以Morris水迷宫系统检测APP/PS1小鼠学习获得能力以及空间记忆能力。实验时将水池以4个等距离点均分为4个象限区,平台置于第1象限中间。实验前,在水池中加适量可食白色素并混匀,达到小鼠视觉无法辨别池内有无平台的目的。利用跟踪系统,实验分为两部分,一、定位航行试验:将小鼠面朝池壁于4个象限各放入1次,开始计时。若小鼠找到平台,则计时停止,将小鼠入水后到爬上平台的时间记为逃避潜伏期(PLA);若小鼠未能找到平台,则在60 s时停止计时,并将其引导至平台并停留10 s以强化记忆,这时PLA记为60 s。实验历时4 d,每组小鼠每天训练1次,整个过程记录PLA。二、空间探索试验:获得性训练结束后,d 5撤掉平台,将小鼠在第1象限入水点面向池壁放入水池,记录小鼠在60 s内穿越平台所在位置的次数(NCP)、该象限行程以及停留时间百分比,作为空间探索能力的指标。
2.3 小鼠组织取材行为学实验结束后,小鼠吸入异氟烷麻醉,心脏灌注生理盐水后,于冰上快速取出全脑,分成2份,左脑置于4%多聚甲醛中固定,制备石蜡包埋切片用于TUNEL染色和IHC染色;右脑于-80 ℃冻存以备Western blot检测。
2.4 TUNEL染色采用TUNEL染色法检测小鼠CA1区组织神经元凋亡情况,取各组小鼠左脑CA1区组织石蜡切片脱蜡,根据TUNEL试剂盒说明进行修剪、脱水、包埋、切片、染色、封片,最后镜检合格的样片。使用Visiopharm软件选取组织全部区域,使用荧光共表达模块,计算细胞凋亡率。凋亡率=TUNEL阳性细胞数/细胞总数×100%。
2.5 免疫组织化学(IHC)染色各组小鼠左脑石蜡切片脱蜡;EDTA缓冲液修复抗原;用3%H2O2液37 ℃孵育25 min,PBS缓冲液洗涤3次后吸干,适当滴入3%BSA均匀覆盖组织,封闭30 min;4 ℃孵育一抗过夜,室温孵育二抗50 min,DAB显色,自来水冲洗终止反应;苏木精复染,脱水,透明,封片。使用Visiopharm软件,选取组织全部区域,神经元中棕黄色颗粒即为阳性表达。采用Image-Pro Plus 6.0图像分析软件分析样本Aβ42、GFAP阳性累积光密度值(IOD)、面积(Area)以及阳性细胞率,用IOD/Area求得平均光密度值(MOD)。数值越大表示其含量越多,指标阳性表达越强,数值越小表示阳性表达减弱。
2.6 蛋白免疫印迹(Western blot)检测BCA法定量检测脑组织匀浆蛋白浓度,10%SDS-PAGE分离目的蛋白,湿法转膜,5%脱脂牛奶封闭1 h。稀释一抗,4 ℃孵育过夜,用TBST在室温下脱色摇床上洗3次,每次5 min。于室温下孵育二抗30 min后,用TBST在室温下脱色摇床上洗3次,每次5 min。ECL试剂盒显色检测蛋白条带。以β-actin灰度值作为内参照,采用Alpha软件进行图像灰度值分析。
2.7 统计学方法用SPSS 21.0软件对实验数据进行统计分析。计量资料以x±s表示。Morris水迷宫实验中PLA采用重复测量方差分析进行统计,其他数据均采用单因素方差分析(One-way ANOVA)进行统计。经方差齐性检验,若方差齐性,组间多重比较采用最小差值法(LSD);若方差不齐,将采用Dunnett T3法进行多重比较。检验水准α=0.05。
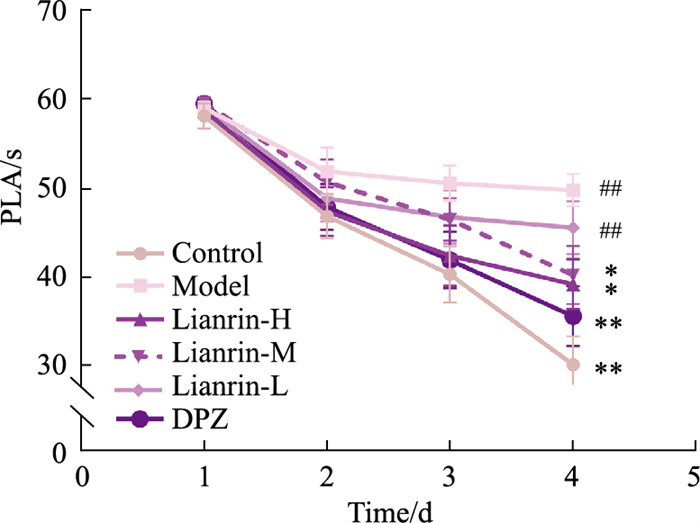
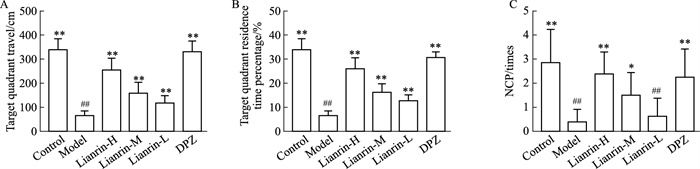
3 结果 3.1 蒙花苷对APP/PS1小鼠学习记忆能力的影响Morris水迷宫实验结果见Fig 1和Fig 2。前4天的定位航行实验显示,d 1各组小鼠PLA无明显差异,但随着训练次数的增加,各组小鼠PLA总体呈下降趋势。与正常组相比,模型组小鼠PLA明显较长(P < 0.01);与模型组相比,蒙花苷高、中剂量组小鼠PLA明显减少(P < 0.05),行动轨迹清晰,能较快找到目标平台。d 5空间探索实验显示,与正常组相比,模型组小鼠NCP明显减少(P < 0.01),且在目标象限的行程较短(P < 0.01),目标象限停留时间百分比也明显较低(P < 0.01);与模型组相比,蒙花苷高、中剂量组小鼠NCP明显增加(P < 0.05),且在目标象限的行程较长(P < 0.01),目标象限的停留时间百分比也明显增加(P < 0.01)。
|
| Fig 1 Effect of linarin on PLA of mice in Morris water maze test (x±s, n=8) ##P < 0.01 vs Control group; *P < 0.05, **P < 0.01 vs Model group. |
|
| Fig 2 Comparison of target quadrant travel, target quadrant residence time percentage and NCP in Morris water maze test (x±s, n=8) ##P < 0.01 vs Control group; *P < 0.05, **P < 0.01 vs Model group. |
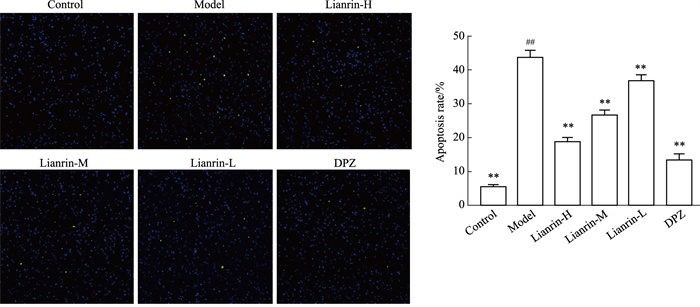
当细胞发生凋亡时会引起细胞核固缩、DNA断裂等,TUNEL可对细胞核内断裂的DNA进行染色,在荧光激发下会产生绿色荧光信号。如Fig 3所示,与正常组相比,模型组小鼠海马CA1区组织细胞凋亡率明显较高(P < 0.01);与模型组相比,阳性对照组以及蒙花苷各剂量组CA1区组织细胞凋亡率均明显较低(P < 0.01)。这表明,蒙花苷能改善小鼠海马组织细胞凋亡,对海马神经元具有明显的保护作用。
|
| Fig 3 Apoptosis in CA1 region of hippocampus in mice of each group (x±s, n=3) ##P < 0.01 vs Control group; **P < 0.01 vs Model group. |
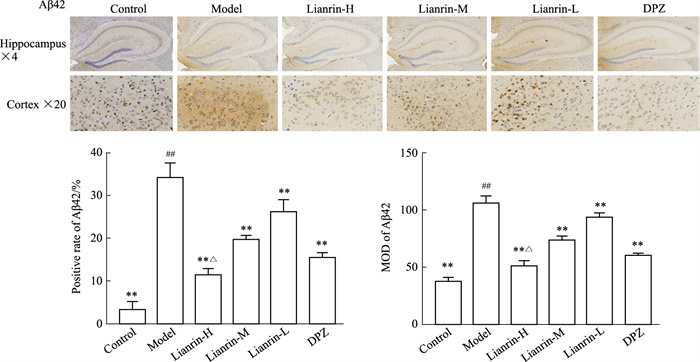
各组小鼠脑组织Aβ42蛋白定性分析和定量表达分别如Fig 4所示。显微镜下,Aβ42阳性表达为棕黄色,强阳性为棕褐色。与正常组相比,模型组小鼠脑组织中Aβ42阳性表达棕黄色、棕褐色明显增多;与模型组相比,阳性对照组以及蒙花苷各剂量组Aβ42阳性表达明显减少。从定量上看,与正常组相比,模型组小鼠脑组织中Aβ42平均光密度值以及细胞阳性率明显高于正常组(P < 0.01);与模型组相比,阳性对照组以及蒙花苷各剂量组均可明显降低Aβ42平均光密度值以及细胞阳性率(P < 0.01),蒙花苷各组Aβ42平均光密度值以及细胞阳性率随着药物浓度的增加呈剂量依赖性降低。
|
| Fig 4 Comparison of protein expression of Aβ42 in brain tissue of mice (x±s, n=3) ##P < 0.01 vs Control group; **P < 0.01 vs Model group; △P < 0.05 vs DPZ group. |
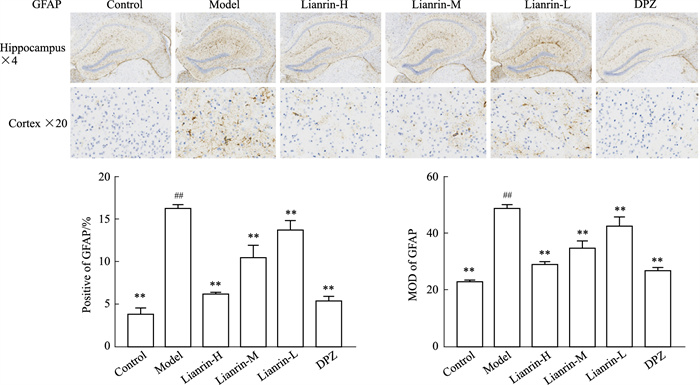
GFAP蛋白是星形胶质细胞内的中间丝蛋白,也是该细胞的标志蛋白,其阳性以及强阳性表达为棕黄色、棕褐色。GFAP表达上调的程度代表星形胶质细胞活跃程度,在脑损伤的炎症中会出现以GFAP为特征的纤维化[15]。各组小鼠脑组织GFAP蛋白定性分析和定量表达分别如Fig 5所示。与正常组相比,模型组小鼠脑组织中GFAP阳性表达棕黄色、棕褐色明显增多;与模型组相比,阳性对照组以及蒙花苷各剂量组GFAP阳性表达明显减少。从定量上看,与正常组相比,模型组小鼠脑组织中GFAP平均光密度值以及细胞阳性率明显高于正常组(P < 0.01);与模型组相比,阳性对照组以及蒙花苷各剂量组GFAP平均光密度值以及细胞阳性率均明显降低(P < 0.01),蒙花苷各剂量组随着药物浓度的增加,GFAP平均光密度值以及细胞阳性率均呈剂量依赖性降低。结果表明蒙花苷可能通过抑制星形胶质细胞的激活来改善AD小鼠神经炎性反应。
|
| Fig 5 Comparison of protein expression of GFAP in brain tissue of mice (x±s, n=3) ##P < 0.01 vs Control group; **P < 0.01 vs Model group. |
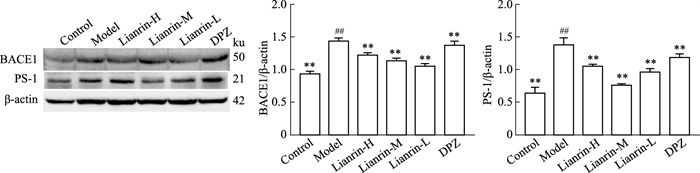
各组小鼠脑组织BACE1和PS-1蛋白表达结果见Fig 6。与正常组相比,模型组小鼠脑组织中BACE1和PS-1蛋白表达水平升高;与模型组相比,各药物干预组小鼠脑组织中BACE1和PS-1蛋白表达水平均明显降低,提示不同浓度的蒙花苷均能有效抑制BACE1和PS-1蛋白的表达,其中抑制BACE1蛋白表达以蒙花苷低剂量组效果最优,而抑制PS-1蛋白表达以蒙花苷中剂量组效果最优。
|
| Fig 6 Expression level of BACE1 and PS-1 in brain tissue of mice (x±s, n=3) ##P < 0.01 vs Control group; **P < 0.01 vs Model group. |
主流Aβ级联学说认为,脑内Aβ的形成和清除代谢失衡,大量的Aβ聚积成不溶性的淀粉样蛋白,沉积于脑内形成淀粉样斑块,胶质细胞被过度激活并加速神经炎症的反应,产生神经毒性作用[16]。Aβ沉积形成老年斑是AD病理发展的核心机制,其中,Aβ42最容易聚集纤维化,有更强的神经细胞毒性,是主要的致病蛋白。因此,抑制Aβ42的聚集可以有效防治AD的进程[17]。参与Aβ形成的2个关键酶是BACE1和PS-1蛋白。BACE1是一种跨膜天冬氨酸蛋白酶,负责在β-分泌酶位点切割APP,产生β淀粉样蛋白片段。因此,抑制BACE1活性可以减少β淀粉样蛋白的产生[18]。PS-1是γ-分泌酶复合物的催化活性中心,PS-1发生突变也会导致APP异常剪切而导致Aβ42生成增加最终沉积形成老年斑[19]。本研究结果显示,与正常组相比,APP/PS1小鼠Aβ42表达明显增加,而蒙花苷各剂量组可明显降低Aβ42、BACE1以及PS-1。这表明,蒙花苷能有效抑制APP经β-分泌酶和γ-分泌酶水解,从而减少Aβ42在脑内的沉积。另一方面,阳性对照组的效果明显不如蒙花苷。由此可知,对照药物多奈哌齐的疗效主要体现在增强神经细胞活力、减少神经元死亡而改善AD患者认知功能,蒙花苷则能抑制Aβ形成的2个关键酶,后者在减少APP裂解及Aβ42的生成方面的效果更佳。
神经炎症是Aβ沉积引起的继发性反应,胶质细胞过度活化所表现的交互作用可能会导致神经炎症,引发级联反应[20]。Taipa等[21]研究表明,GFAP表达水平增高是星形胶质细胞激活的主要表现,也侧面反映中枢神经功能损伤程度。由Fig 5可知,蒙花苷能抑制GFAP蛋白表达,具有缓解星形胶质细胞异常活化的作用;而TUNEL染色结果进一步证实蒙花苷能提高神经元抗凋亡能力。这也从不同的角度验证了Landfield等[22]的研究结论——GFAP与学习记忆能力减退之间关系密切。
AD患者脑内伴有明显的胶质细胞反应,老年斑块周围出现大量星形胶质细胞,激活星形胶质细胞在老年斑的形成中起到重要作用[23]。研究发现[24],Aβ可促进星形胶质细胞释放细胞因子,如TNF-α、IL-1β等,这些物质对神经元有毒性作用,而星形胶质细胞的激活又能诱导Aβ神经毒性的产生,使神经元凋亡并坏死,Aβ沉积以及神经炎症作为在AD病理进程中重要的核心环节,两者相互促进,会形成恶性循环。星形胶质细胞的增强激活会增加炎症介质的释放,使得Aβ42产物增加,而Aβ42产物增多则进一步激活星形胶质细胞释放炎症因子而增加Aβ42产物的生成,从而发生级联放大作用。Aβ42与GFAP表达联系密切,蔡志友等[25]所做实验的直线相关分析表明Aβ42与GFAP表达成显著正相关。
本研究通过Morris水迷宫实验表明,经过不同剂量的蒙花苷干预后,APP/PS1小鼠在目标象限行程、停留时间百分比和穿越平台的次数均明显增加,逃避潜伏期逐渐缩短,说明蒙花苷明显改善小鼠的学习记忆能力并提升认知功能。这表明,动物行为学的结果与TUNEL染色以及IHC染色和Western blot检测等方面的研究结果是一致的。多方面的研究结果交证表明,蒙花苷具有减少APP裂解和Aβ42生成,抑制星形胶质细胞活化,缓解神经炎症,改善AD小鼠学习记忆损伤的作用。
| [1] |
Knopman D S, Amieva H, Petersen R C, et al. Alzheimer disease[J]. Nat Rev Dis Primers, 2021, 7(1): 1-21. doi:10.1038/s41572-020-00234-1 |
| [2] |
Jia L F, Quan M N, Fu Y, et al. Dementia in China: epidemiology, clinical management, and research advances[J]. Lancet Neurol, 2020, 19(1): 81-92. doi:10.1016/S1474-4422(19)30290-X |
| [3] |
王彬斌, 冯晓晓, 恩特扎尔·别尔克红, 等. 开心散对APP/PS1小鼠神经炎症和Aβ沉积的作用研究[J]. 中草药, 2021, 52(24): 7511-9. Wang B B, Feng X X, Entzal B, et al. Pharmacological effects of Kaixin San on neuroinflammation and Aβ deposition in APP/PS1 mice[J]. Chin Tradit Herb Drug, 2021, 52(24): 7511-9. |
| [4] |
Alexander G C, Emerson S, Kesselheim A S. Evaluation of aducanumab for Alzheimer disease: scientific evidence and regulatory review involving efficacy, safety, and futility[J]. JAMA, 2021, 325(17): 1717-8. doi:10.1001/jama.2021.3854 |
| [5] |
Wang X Y, Sun G Q, Feng T, et al. Sodium oligomannate therapeutically remodels gut microbiota and suppresses gut bacterial amino acids-shaped neuroinflammation to inhibit Alzheimer's disease progression[J]. Cell Res, 2019, 29(10): 787-803. doi:10.1038/s41422-019-0216-x |
| [6] |
祝雨辰, 邝柏宇, 梁金萍, 等. 人参、石菖蒲及其药对防治阿尔茨海默症的药理作用研究进展[J]. 中国药理学通报, 2024, 40(5): 817-22. Zhu Y C, Kuang B Y, Liang J P, et al. Advance in pharmacological effects of ginseng, acorus calamus and its couplet medicine on Alzheimer's disease[J]. Chin Pharmacol Bull, 2024, 40(5): 817-22. doi:10.12360/CPB202304011 |
| [7] |
张梦玉, 郑艳杰, 叶红霞, 等. 基于TLR4/NF-κB信号通路探究红花黄色素对不同月龄APP/PS1小鼠学习记忆能力的影响[J]. 中国药理学通报, 2024, 40(1): 76-82. Zhang M Y, Zheng Y J, Ye H X, et al. Effect of safflower yellow on learning and memory ability of APP/PS1 mice at different months based on TLR4/NF-κB signaling pathway[J]. Chin Pharmacol Bull, 2024, 40(1): 76-82. doi:10.12360/CPB202306068 |
| [8] |
于文静, 杨苗, 贺春香, 等. 黄芩苷通过TLR4/MyD88/NF-κB通路抑制链脲佐菌素诱导的阿尔茨海默病大鼠模型神经炎症反应[J]. 中国药理学通报, 2023, 39(1): 83-9. Yu W J, Yang M, He C X, et al. Baicalin inhibits streptozotocin-induced neuroinflammation in Alzheimer's disease rat model by TLR4/MyD88/NF-κB pathway[J]. Chin Pharmacol Bull, 2023, 39(1): 83-9. doi:10.12360/CPB202204021 |
| [9] |
Singh M, Jindal D, Kumar R, et al. Molecular docking and network pharmacology interaction analysis of Gingko Biloba (EGB761) extract with dual target inhibitory mechanism in Alzheimer's disease[J]. J Alzheimers, 2023, 93(2): 705-26. doi:10.3233/JAD-221222 |
| [10] |
肖林雨, 段婷, 夏勇生, 等. 蒙花苷通过抑制TLR4/NF-κB通路抑制小鼠脊髓损伤后小胶质细胞活化介导的神经炎症和神经元凋亡[J]. 南方医科大学学报, 2024, 44(8): 1589-98. Xiao L Y, Duan T, Xia Y S, et al. Linarin inhibits microglia activation-mediated neuroinflammation and neuronal apoptosis in mouse spinal cord injury by inhibiting the TLR4/NF-κB pathway[J]. J South Med Univ, 2024, 44(8): 1589-98. |
| [11] |
Mottaghipisheh J, Taghrir H, Boveiri Dehsheikh A, et al. Linarin, a glycosylated flavonoid, with potential therapeutic attributes: acomprehensive review[J]. Pharmaceuticals, 2021, 14(11): 1104. doi:10.3390/ph14111104 |
| [12] |
Wu E C, Lian Y T, Zhao S L, et al. Involvement of the Sch9/Rim15/Msn2 signaling pathway in the anti-aging activity of dendrobine from Dendrobium nobile Lindl. via modification of oxidative stress and autophagy[J]. Chin Med, 2023, 18 (1): 111.
|
| [13] |
Wang J Y, Fasina O B, Manzoor M, et al. A new gentiopicroside derivative improves cognitive deficits of AD mice via activation of Wnt signaling pathway and regulation of gut microbiota homeostasis[J]. Phytomedicine, 2023, 113: 154730. doi:10.1016/j.phymed.2023.154730 |
| [14] |
Pan H Y, Zhang J H, Wang Y Y, et al. Linarin improves the dyskinesia recovery in Alzheimer's disease zebrafish by inhibiting the acetylcholinesterase activity[J]. Life Sci, 2019, 222: 112-6. doi:10.1016/j.lfs.2019.02.046 |
| [15] |
Pereira J B, Janelidze S. Smith R, et al. Plasma GFAP is an early marker of amyloid-β but not tau pathology in Alzheimer's disease[J]. Brain, 2021, 144 (11): 3505-16.
|
| [16] |
徐佳雯, 沈佳红, 温雨欣, 等. 组胺H1受体激动剂通过Akt/NF-κB通路抑制脂多糖诱导的星形胶质细胞炎症反应[J]. 中国药理学通报, 2024, 40(2): 317-23. Xu J W, Shen J H, Wen Y X, et al. Histamine 1 receptor agonist inhibits LPS-induced immune responses in astrocytes via Akt/NF-κB signaling pathway[J]. Chin Pharmacol Bull, 2024, 40(2): 317-23. doi:10.12360/CPB202310038 |
| [17] |
龙燕, 柯璇, 洪浩, 等. CysLT1R对APP-HEK293细胞Aβ生成的调控作用及其机制[J]. 中国药理学通报, 2021, 37(12): 1666-74. Long Y, Ke X, Hong H, et al. Effect of CysLT1R on Aβ production and the underlying mechanism in APP-HEK293 cells[J]. Chin Pharmacol Bull, 2021, 37(12): 1666-74. doi:10.3969/j.issn.1001-1978.2021.12.008 |
| [18] |
Das B, Yan R. A close look at BACE1 inhibitors for Alzheimer's disease treatment[J]. CNS Drugs, 2019, 33(3): 251-63. doi:10.1007/s40263-019-00613-7 |
| [19] |
孙宁宁, 贺小平, 刘珊, 等. 还脑益聪靶向HAMP调节铁代谢改善AD模型小鼠认知障碍的机制研究[J]. 中国药理学通报, 2024, 40(7): 1240-8. Sun N N, He X P, Liu S, et al. Study on the machanism of Huannao Yicong Deoction targeting HAMP to regulate iron metabolism and improve cognitive impairment in AD model mice[J]. Chin Pharmacol Bull, 2024, 40(7): 1240-8. doi:10.12360/CPB202312027 |
| [20] |
Mila-Aloma M, Slvado G, Gispert J D, et al. Amyloid beta, tau, synaptic, neurodegeneration, and glial biomarkers in the preclinical stage of the Alzheimer's continuum[J]. Alzheimers Dement, 2020, 16(10): 1358-71. doi:10.1002/alz.12131 |
| [21] |
Taipa R, Ferreira V, Brochado P, et al. Inflammatory pathology markers (activated microglia and reactive astrocytes) in early and late onset Alzheimer disease: a post mortem study[J]. Neuropathol Appl Neurobiol, 2018, 44(3): 298-313. doi:10.1111/nan.12445 |
| [22] |
Landfield P W, Rose G, Sandles L, et al. Patterns of astroglial hypertrophy and neuronal degeneration in the hippocampus of aged memory deficient rats[J]. J Geroncol, 1997, 32(1): 3-12. |
| [23] |
陶一鸣, 杜艳军, 王静芝, 等. TLR4/NF-κB信号通路在阿尔茨海默病炎性反应中的表达及电针干预影响[J]. 中华中医药学刊, 2021, 39(1): 168-72. Tao Y M, Du Y J, Wang J Z, et al. Role of TLR4/NF-κB signaling pathway and effect of electroacupuncture on Alzheimer's disease inflammatory response[J]. Chin J Mod Appl Pharm, 2021, 39(1): 168-72. |
| [24] |
Tsai C L, Erickson K I, Sun H S, et al. A cross-sectional examination of a family history of Alzheimer's disease and ApoE epsilon 4 on physical fitness, molecular biomarkers, and neurocognitive performance[J]. Physiol Behav, 2021, 230: 113268. doi:10.1016/j.physbeh.2020.113268 |
| [25] |
蔡志友, 晏勇, 张骏, 等. 糖尿病大鼠认知功能及海马组织GFAP、IL-1β、TNF-α和Aβ表达[J]. 上海交通大学学报(医学版), 2009, 29(2): 130-4. Cai Z Y, Yan Y, Zhang J, et al. Cognitive function and expression of GFAP, IL-1β, TNF-α and Aβ in hippocampal tissues of diabetic rats[J]. J Shanghai Jiao Tong Univ(Med Sci), 2009, 29(2): 130-4. |

