


2. 徐州医科大学附属医院麻醉科,江苏 徐州 221002
张红星(1982-),男,博士,教授,博士生导师,研究方向:抑郁情绪的调节机制,通信作者,E-mail:hongxing.zhang@xzhmu.edu.cn
 ,
ZHOU Dong-yu1,
HAN Yi1,
JI Ran1,
AI Lin1,
XIE An1,
ZHAI Xiao-jing1,
CAO Jun-li1,2
,
ZHOU Dong-yu1,
HAN Yi1,
JI Ran1,
AI Lin1,
XIE An1,
ZHAI Xiao-jing1,
CAO Jun-li1,2
 ,
ZHANG Hong-xing1
,
ZHANG Hong-xing1

2. Dept of Anesthesiology, Affiliated Hospital of Xuzhou Medical University, Xuzhou Jiangsu 221002, China
突触是神经元与神经元之间或神经元与其他类型细胞之间的功能联系部位。根据所使用的信息传递媒质不同,突触可分为电突触和化学性突触。其中,化学性突触以神经递质为信息传递媒质,是最常见的类型。神经递质在突触信息传递中发挥重要作用,常见的神经递质主要有谷氨酸(glutamic acid,Glu)、去甲肾上腺素(norepinephrine,NE)、多巴胺(dopamine,DA)、γ-氨基丁酸(γaminobutyric acid,GABA)、5-羟色胺(5-hydroxytryptamine,5-HT)等。这些神经递质并非独立参与病理生理过程,而是存在复杂的时空与功能联系,共同完成信息整合与传递。梳理不同神经递质系统之间的对话机制,有利于理解相关疾病的发展和转归过程,有利于拓展相关药物的药理机制,更好地指导基础研究与临床实践。本文回顾了高级中枢神经系统中N-甲基-D-天冬氨酸受体(N-methyl-D-aspartate receptor,NMDA-R)和α2肾上腺素受体(alpha 2 adrenergic receptor,α2-AR)及其下游分子靶点在神经精神疾病中的功能作用,综述了二者之间对话的可能分子机制,并对相关领域内未来的基础与临床研究方向进行了展望。
1 谷氨酸能系统与去甲肾上腺素能系统Glu是一种广泛分布于中枢神经系统的兴奋性神经递质,分为离子型和代谢型。离子型谷氨酸受体属于配体门控离子通道,包括NMDA-R、α-氨基-3-羟基-5-甲基-4-异噁唑受体(α-amino-3-hydroxy-5-methyl-4-isoxazole-propionate receptor,AMPA-R)和海人藻酸受体(kainic acid receptor,KA-R),均属于非选择性的阳离子通道,可介导Glu快速兴奋性突触传递。代谢型Glu受体属于G蛋白偶联受体,通过下游的第二信使发挥信号转导作用,其作用产生的时效较长。Glu受体亚型及其拮抗剂与激动剂见Tab 1。
| Glutamate receptor | Subtype | Antagonist | Agonist |
| Ionic | NMDA-R | Ketamine, MK-801, Memantine | Quinolinic acid, NMDA |
| AMPA-R | NBQX, Topiramate, Capric acid | CX546, Ampalex | |
| KA-R | KY382884, Evans blue | Kainic acid | |
| Metabotropic | mGLUR1-8 | ADX-47273, MPEP, VU29 | LY404039, VU0361737 |
NE广泛分布于中枢和周围神经系统。中枢NE及其受体主要参与心血管活动、情绪、体温、摄食及觉醒的调节;在外周,相较于β受体,NE激动α受体的作用更强。蓝斑核(locuscoeruleus,LC)是中枢NE合成的主要来源,其去甲肾上腺素能投射几乎到达大脑的所有区域。肾上腺素能受体分为α型肾上腺素受体(α1、α2)和β型肾上腺素受体(β1、β2、β3),均为G蛋白偶联受体。其中α2-AR主要分布于突触前膜,属于突触前受体。肾上腺素能受体亚型相关的拮抗剂与激动剂见Tab 2。
| Adrenergic receptor | Antagonist | Agonist |
| α1 | Tamsulosin | Phenylephrine, Methoxamine |
| α2 | Idazoxan, Yohimbine | Dexmedetomidine, Clonidine |
| β1 | Atenolol, Acebutolol | Dobutamine, Salmeterol |
| β2 | Betaxolol, PF-4348235 | Salbutamol, Terbutaline |
| β3 | Bopindolol | Mirabegron, L755507, Solabegron |
现有的临床研究与基础研究表明,NMDA-R和α2-AR之间存在密切联系。例如:α2-AR激动剂能缓解苯环利定诱导的工作记忆损害和视觉注意力缺陷[1],逆转慢性缩窄损伤(chronic constriction injury,CCI)诱发的脊髓背角中NMDA-R磷酸化以治疗疼痛[2],干扰氯胺酮在体内的代谢过程[3];NMDA-R拮抗剂能中和单独使用右美托咪定时造成的高血压和心动过缓[4],预防甚至逆转α2-AR激动剂使用后延迟出现的热和触觉超敏反应[5],镇痛药物花姜酮通过上调NMDA NR2B受体水平,下调大脑区域内α2-AR的蛋白表达,缓解神经病理性疼痛[6]。所以,NMDA-R和α2-AR之间可能存在功能对话。
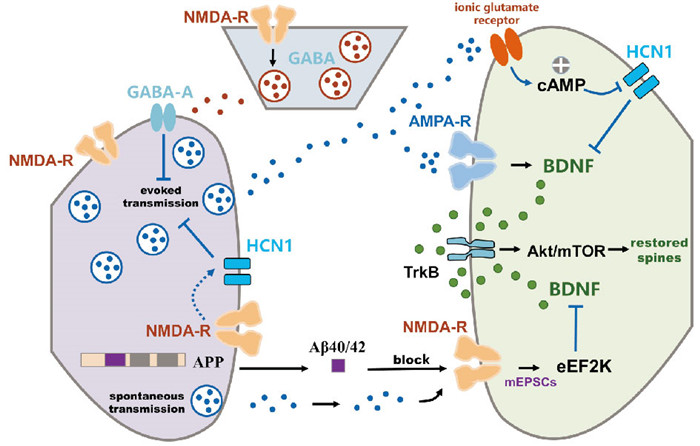
2 NMDA-R的下游机制NMDA-R是一种接受电压与受体配体双重门控的离子型谷氨酸受体,其组成亚基有GluN1、GluN2A、GluN2B、GluN2C、GluN2D、GluN3A和GluN3B,对Na+、K+、Ca2+都具有通透性,参与学习记忆、树突和轴突发育、触发多种形式的突触可塑性等。NMDA-R还具有以下特点:①需要甘氨酸作为共激动剂;②在静息电位水平通道被Mg2+阻塞,只有当膜电位去极化达一定水平时,Mg2+从通道内移出,阻塞方可解除;③通道上有与多种物质结合的调制位点,可与内源性物质或药物(如苯环利定、氯胺酮)结合,使通道变构,改变通道对Na+、K+、Ca2+的通透性。本文重点关注NMDA-R在抑郁症、阿尔茨海默病(Alzheimer′s disease,AD)、疼痛等疾病中的下游分子机制(Fig 1)。
|
| Fig 1 Downstream molecular mechanisms of NMDA-R |
重性抑郁障碍(major depressive disorder,MDD),又称临床抑郁症,主要临床表现是持久而显著的情绪低落、快感缺失、行为绝望和社交回避,严重者可能同时伴有失眠、食欲减退、思考能力下降、疼痛等症状,甚至出现自杀倾向[7]。相比于传统抗抑郁药物的起效缓慢、治愈率低、不良反应多,氯胺酮是起效迅速、作用持久、具有全新作用机制的新型抗抑郁药物,可以通过拮抗NMDA-R发挥其抗抑郁效果。
2.1.1 NMDA-R-eEF2K-BDNF-TrkB大脑内有两种形式的神经传递:诱发传递和自发传递。不同于依赖动作电位刺激产生的诱发传递,自发传递是指含有谷氨酸递质的突触囊泡与突触前膜偶然融合,激活突触后膜上的NMDA-R,继而引起树突内Ca2+内流,并产生微小兴奋性突触后电流(miniature excitatory post-synaptic current,mEPSCs){Espinosa, 2009 #2},mEPSCs激活真核延伸因子2激酶(eukaryotic elongation factor 2 kinase,eEF2K),使eEF2磷酸化,进而调节各类蛋白质翻译过程[8],比如阻碍脑源性神经营养性因子(brain-derived neurotrophic factor,BDNF)的合成。BDNF是成人脑内含量最丰富的营养因子,在神经元发育、分化和维持中起重要作用,是抑郁情绪形成和抗抑郁药物发挥效果的关键效应物。氯胺酮正是通过阻断自发性NMDA-R-mEPSCs传递,削弱eEF2K的活性,引起BDNF翻译过程去抑制,BDNF与酪氨酸激酶受体B(tyrosine kinase receptor B,TrkB)结合后,启动细胞内级联反应,发挥快速、持久的抗抑郁作用[8]。
2.1.2 NMDA-R-AMPA-R-BDNF-TrkB氯胺酮通过拮抗皮质-边缘系统GABA能中间神经元上的NMDA-R,降低其兴奋性,解除GABA能中间神经元介导的去抑制,增加Glu的释放,激活突触后膜上的AMPA-R,使得突触后膜部分去极化,促进BDNF合成增加。BDNF与TrkB结合后,启动细胞内级联反应,最终使得突触数量和功能增加。该过程迅速重建了情绪调节回路中因应激和抑郁情绪所损耗的神经元树突棘,发挥快速持续的抗抑郁作用[9]。
2.1.3 NMDA-R-HCN1-Glu-BDNF氯胺酮不仅是NMDA-R拮抗剂,也是超极化激活环核苷酸门控(hyperpolarization-activated cyclic nucleotide-gated,HCN1)阳离子通道拮抗剂,氯胺酮在HCN1通道敲除小鼠中不再具备抗抑郁作用,表明HCN1通道与氯胺酮快速持久的抗抑郁作用关系密切。研究者推测,氯胺酮降低突触前HCN1通道活性,可能是由突触前NMDA-R抑制介导的。这也与其他研究结果一致,例如:NMDA-R的缺失导致HCN通道功能的降低,NMDA-R激活导致HCN1通道表面蛋白表达增加,NMDA-R激活引起的Ca2+内流是HCN通道活性增加所必需的等。虽然尚不明确突触前NMDA-R是如何调控HCN1通道功能的,但上述证据证实NMDA-R可以调节HCN1通道的功能[10]。所以,氯胺酮不仅能直接抑制HCN1通道,还可能通过阻断NMDA-R间接调节其活性。
氯胺酮引起的细胞外Glu水平升高和Glu循环增加是其发挥快速抗抑郁作用的关键,已知突触前HCN1通道可以增强内嗅皮层Ⅲ层神经元中mEPSCs,模拟氯胺酮诱导的CA1区域兴奋性突触后电位增强,表明抑制突触前HCN1通道能促进Glu释放[11]。经历单个长时间应激的小鼠在接受氯胺酮注射后,前额叶皮质(prefrontal cortex,PFC)中HCN1蛋白表达迅速降低,BDNF表达增加,焦虑和抑郁症状迅速缓解[12]。Kim等[13]证实,海马背侧CA1区HCN1通道敲除的小鼠表现出的抗焦虑和抗抑郁样行为与成熟BDNF蛋白表达增加和mTOR磷酸化有关,提示抑制HCN1通道能促进BDNF增加。综上所述,氯胺酮可以直接阻断或通过阻断NMDA-R间接阻断HCN通道,调节Glu、BDNF水平升高,发挥快速、持续的抗抑郁作用。
2.1.4 NMDA-R-LHb神经元爆发放电外侧缰核(lateral habenula,LHb)是多种抑郁动物模型中一致高度活跃的脑区,密切参与抑郁症的病理生理过程。LHb神经元爆发放电活动会诱导抑郁样行为,反之,LHb神经元低活性能逆转抑郁样表型。抑郁小鼠LHb神经元胞体周围的星型胶质细胞表面Kir4.1表达增加,使得神经元与神经胶质细胞紧密连接处K+减少,神经元内外K+梯度增大,导致神经元膜电位超极化、低电压敏感的T型钙通道失活,引起LHb神经元NMDA-R依赖性爆发放电,最终加重抑郁状态。氯胺酮能阻断NMDA-R,从而抑制LHb爆发放电活动,达到缓解抑郁情绪的效果[14]。
2.2 ADAD是发生于老年和老年前期,以进行性认知功能障碍和行为损害为特征的中枢神经系统退行性疾病,损害智力发展,并扰乱神经认知功能。中重度AD患者虽可使用NMDA-R拮抗剂美金刚来缓解症状,但目前没有药物可以治愈或阻断AD的发病进程。AD发病的核心是淀粉样前体蛋白(amyloid precursor protein,APP)差异化加工。正常状态下,APP分别在α-分泌酶作用下裂解,产生sAPPα和C83羧基端片段,或在β-分泌酶、γ-分泌酶作用下,依次裂解产生大小不同的胞外单体,其中最显著的是Aβ40/42[15]。疾病状态下,APP加工途径之间的失衡导致神经毒性单体聚集增加,进而产生Aβ寡聚化和斑块形成。致病性Aβ聚集后,阻塞离子通道(包括NMDA-R、AMPA-R、ACh-R)、扰动钙稳态,导致线粒体氧化应激、能量代谢受损、糖调节异常和突触功能改变,并最终引起神经元细胞死亡。
Ca2+调节障碍导致的神经元功能失调和认知功能下降也是AD的公认发病机制,而过度激活的NMDA-R正是调节Ca2+内流的主要靶点。有研究表明,Aβ诱导神经元细胞释放Glu,激活突触外NMDA-R,触发凋亡信号,导致神经元功能障碍。同时,过度激活状态的NMDA-R本身也可引起兴奋性神经毒性,破坏脑内神经元。在该疾病状态下,NMDA-R自身也发生了变化,比如脑内纹状体中GluN2B与Glu的亲和力明显增加,但患者脑内维持钙稳态至关重要的NMDA-R抑制性亚单位GluN3A表达水平明显降低,GluN3A缺乏会进一步加重钙稳态失调,加速AD发生[16]。因此,NMDA-R是介导AD的关键受体,或将成为治愈或阻断AD的发病进程的潜在靶点。
2.3 疼痛疼痛是一种与实际或潜在的组织损伤相关的、不愉快的感觉和情感体验,或与此相似的经历。NMDA-R促进疼痛感觉的传递,并促进长期的突触可塑性变化。疼痛状态下的情感维持是由前扣带皮质中依赖于NMDA-R长期突触可塑性增强触发的[17],脊髓背角神经元的突触前和突触后NMDA-R活性增强,会导致疼痛超敏反应[18];反之,阻断NMDA-R可缓解疼痛。围手术期低剂量氯胺酮可减少阿片类药物的消耗和特定外科手术后的慢性术后疼痛[19],加巴喷丁类化合物通过抑制α2δ-1-NMDAR复合物的突触间运输,减轻神经性疼痛[18]。因而,NMDA-R参与疼痛的发生和缓解过程,其或可与其他镇痛药物联合使用,以达到更好的镇痛效果。
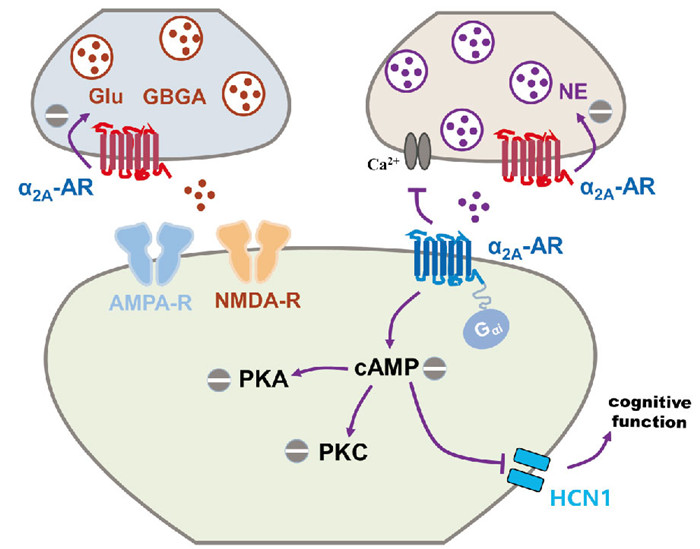
3 α2-AR的下游机制α2-AR属于7次跨膜的G蛋白偶联受体,是参与去甲肾上腺素能传递调节的最重要受体家族。α2-AR共有3种亚型:α2A、α2B和α2C,其中α2A-AR是调节中枢系统NE水平的主要亚型。本文重点关注α2-AR在抑郁症、认知功能障碍、注意力缺陷多动障碍(attention deficit and hyperactivity disorder,ADHD)、癫痫等疾病中的作用机制(Fig 2)。
|
| Fig 2 Downstream molecular mechanisms of α2-AR |
抑郁症患者的LC、PFC、海马、血小板中高亲和力构象状态α2-AR(α2A-AR为主)密度增加,α2-AR关键调节因子(如GRK2/3、抑制蛋白2、亲棘蛋白)水平下降,提示G蛋白与α2-AR偶联增强[20]。成年海马神经发生和营养因子表达增加是抵抗抑郁情绪的关键一步,但海马神经元前体细胞上α2-AR的激活会抑制海马祖细胞增殖,阻碍成年海马的神经形成,所以α2-AR拮抗剂能促进海马新生神经元的形态成熟,以及BDNF、血管内皮生长因子的表达[21]。临床基因学研究表明,抑郁状态下会出现α2A-AR功能获得性突变体和α2C-AR功能丧失突变体,但这种异常的功能状态在经过系统的药物治疗后可恢复正常。因此,抑郁障碍可能与α2-AR敏感性和反应性增强有关。
去甲肾上腺素神经元突触前膜上的α2-AR(自受体)是调节NE释放的关键受体。研究证实,α2-AR拮抗剂可以加强去甲肾上腺素再摄取抑制剂(noradrenaline reuptake inhibitors,NRIs)的抗抑郁效果,NRIs能抑制突触前膜的NE再摄取作用,提高突触胞体及末端区域外的NE浓度[22],但该过程会激活突触前膜上α2-AR通过负反馈机制抑制NE释放,阻止细胞外NE进一步增加。若同时联用α2-AR拮抗剂,阻止内源性激动剂水平升高引起的自受体激活,能明显增强NRIs诱导的细胞外NE增加[22],长期单独使用NRIs造成的α2-AR脱敏引起的NE进一步增加也与该研究结果相符。综上所述,拮抗α2-AR可能是治疗抑郁症的一条潜在途径。
3.2 认知功能障碍 3.2.1 工作记忆错乱工作记忆(working memory,WM)是一种能将信息进行短暂储存并加工,以指导下一步行为的短期记忆,是思维操纵和有意识行为的基础。WM错乱常见于精神分裂症、注意力分散等疾病。PFC的认知功能受儿茶酚胺类神经递质(NE、DA)的控制,PFC中NE的消耗会影响WM、分散注意力。研究表明,WM主要是由PFC神经元延迟期依赖性放电来维持的,但这种短暂激活的微电路会被高水平的环磷酸腺苷(cyclic adenosine monophosphate,cAMP)破坏。突触后膜上的α2A-AR激活后,降低了cAMP水平,关闭HCN通道,减少突触性分流以增加PFC神经元网络的功能连接,最终改善WM[23]。因此,突触后膜上的α2A-AR在WM的调节中扮演重要角色,是治疗精神分裂症的潜在靶点。
3.2.2 精神紧张α2-AR激动剂在术后阶段或重症监护中常被用作镇静剂。研究表明,在多巴胺β羟化酶敲除的小鼠体内注射美托咪定后,翻正反射消失,镇静作用存在;而在α2A-AR敲除小鼠中,右美托咪定(dexmedetomidine,Dex)的镇静作用完全丧失[24]。这说明镇静作用是由非去甲肾上腺素神经元上的α2A-AR介导的。
3.2.3 调节神经元兴奋性突触后膜上的α2-AR能通过调节离子通道的方式,影响神经元兴奋性[20],包括直接调节内向整流K+通道使神经元活性减弱、间接调节HCN1通道、抑制突触前Ca2+通道减少神经递质的释放等。
3.3 注意力缺陷多动障碍(attention deficit and hyperactivity disorder,ADHD)ADHD是一种认知行为发育障碍,包括过度活跃、冲动和持续注意力不足。ADHD导致的行为障碍与PFC去甲肾上腺素能系统和多巴胺能系统之间的失衡、PFC谷氨酸信号障碍、LC神经元α2-AR亚敏感性密切相关[25]。α2-AR激动剂胍法辛和可乐定已被证明对儿童和青少年ADHD的治疗有效。药物可能通过以下几种方式起效:激活PFC中NE神经元突触前膜上的自受体,修复系统间失衡;激活PFC突触后膜α2-AR,产生记忆增强效应;激活PFC突触前膜上异受体,减少Glu释放[25]。因此,α2-AR是治疗ADHD的关键靶点。
3.4 癫痫癫痫即俗称的“羊角风”或“羊癫风”,是大脑神经元突发性异常放电,导致大脑功能短暂障碍的一种慢性疾病。可乐定有促癫痫作用,而选择性α2A-AR激动剂Dex、胍法辛是抗癫痫药物,可以明显降低癫痫的发作时间。在α2A-AR敲除小鼠中,两种类型的药物作用均消失,说明α2A-AR是发挥促惊厥和抗惊厥作用的主要亚型[26]。研究者又在多巴胺β-羟化酶敲除小鼠中验证两种药物的作用,抗惊厥效果存在,而促惊厥效果消失。提示Dex和胍法辛是作用于突触后膜上的α2-AR,发挥抗惊厥作用,而可乐定是通过激活去甲肾上腺素能神经元上突触前膜α2-AR(自受体),减少NE释放,引起癫痫阈值的降低[26],进而诱导癫痫的发生。因此,不同神经元突触部位的α2-AR对癫痫发作的影响是不一致的。
3.5 α2-AR对高级中枢系统中其他神经递质的影响 3.5.1 抑制突触前膜释放Glu在慢性眼高压模型中,α2-AR激动剂能抑制谷氨酸转运体,并下调NMDA-R水平,起到保护视网膜神经节细胞的作用[27]。UK-14, 304(α2-AR激动剂)在明显降低终纹床核中mEPSCs的同时,增加配对双脉冲比率[28],这提示α2-AR主要通过降低突触前膜的Glu释放频率来抑制其兴奋性突触传递。
3.5.2 减少突触前膜释放GABA脑干的去甲肾上腺素能输入参与调节脑室旁核神经元的兴奋性,α2-AR激活后,能减弱室旁核至脊髓的GABA能信号输出[29]。脑干去甲肾上腺素能神经元的输入能减少结节乳头核中组胺能神经元GABA能抑制性突触后电位的幅度和频率,使组胺能神经元去抑制,该过程是由突触前膜上的α2-AR调节的[30]。
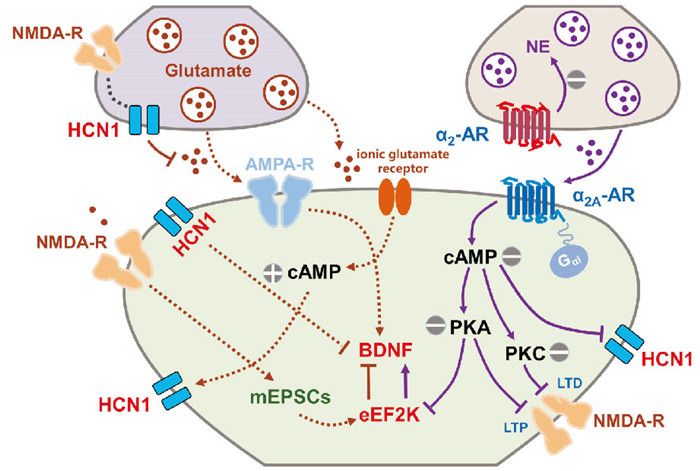
4 NMDA-R与α2-AR可能的共同作用靶点及相互调控作用如前所述,NMDA-R和α2-AR之间存在着共同的分子靶点(Fig 3),提示NMDA-R和α2-AR之间存在相互作用的对话基础。
|
| Fig 3 Possible co-action targets between NMDA-R and α2-AR |
属非典型α激酶家族的Ca2+/CaM蛋白依赖性丝氨酸/苏氨酸激酶,通过磷酸化eEF2,阻止真核生物蛋白质翻译的过程。BDNF是生命早期神经元发育、存活和功能所必需的,包括参与调节突触形成、突触可塑性、神经发育等过程。因此,BDNF在抑郁症发展和缓解过程中担任重要角色。
静息状态下,突触前膜自发释放的Glu激活突触后膜上的NMDA-R,继而引起树突内Ca2+内流,并产生mEPSCs,激活eEF2K,使eEF2磷酸化,进而抑制BDNF的翻译过程。同时,α2-AR可与Gαi偶联,胞内cAMP水平下降,蛋白激酶A(protein kinase A,PKA)活性下调,抑制eEF2K活动性,促进BDNF和其他突触相关蛋白翻译。因此,eEF2K和BDNF是NMDA-R与α2-AR共同的分子靶点。
4.1.2 HCN通道HCN通道在前脑广泛表达,如PFC和海马,参与调节神经元的兴奋性和节律性、神经元活动、突触传递和突触可塑性,从而介导各种病理生理功能。如前所述,氯胺酮能直接阻断HCN通道,或通过拮抗NMDA-R间接降低HCN通道的活性,启动HCN1-BDNF-TrkB-mTOR信号通路,降低HCN1表达,上调BDNF及PSD95水平,改善PFC空间认知功能,最终缓解抑郁、焦虑症状。同样,PFC突触后膜上的α2A-AR激活后,可降低cAMP,也能抑制HCN通道,减少突触性分流以增加PFC神经元的功能连接,改善WM。因此,HCN通道可能是NMDA-R与α2-AR共同的离子通道靶点。
4.2 NMDA-R和α2-AR及其相关药物的相互调控作用 4.2.1 功能关联MK-801和可乐定都能减少楔形核中星型胶质细胞活化,缓解神经性疼痛感觉[31];(S)-氯胺酮和Dex在脑缺血状态下,均能上调抗凋亡基因蛋白表达,保护大脑神经元[32]。静脉输注米伐佐罗(一种选择性α2-AR激动剂)明显减弱了鞘内注射NMDA引起的心动过速反应,提示脊髓α2-AR和NMDA-R在调节心率方面,存在功能拮抗的可能性[33];Dex作为镇静药物单独使用后,常出现高血压和心动过缓,这些不良反应在与氯胺酮联合使用后大大降低,并能发挥更好的镇静效应[4]。所以,NMDA-R和α2-AR相关药物在功能上存在相互协同或相互拮抗的作用。
4.2.2 物质代谢氯胺酮的正常代谢对其发挥抗抑郁作用是必不可少的,但α2-AR激动剂能干扰氯胺酮代谢生成去甲氯胺酮,以及进一步代谢为6-羟基去甲氯胺酮(6-hydroxynorketamine,6HNK)或5, 6脱氢去甲氯胺酮(5, 6-dehydronorketamine,DHNK)的过程。已知去甲氯胺酮、6HNK和DHNK分别在NMDA-R、AMPA-R和α7-烟碱乙酰胆碱受体处有活性,这些特性与氯胺酮发挥抗抑郁作用密不可分[3]。综上所述,α2-AR激动剂或可能通过阻碍氯胺酮代谢的方式,拮抗其药理学作用。
4.3 其他除了上述共同分子信号靶点外,α2-AR可通过下游分子调节NMDA-R的活性。例如:NE激活α1-AR、α2-AR,诱导PFC中Ⅰ/Ⅱ层至Ⅴ层锥体神经元NMDA-R依赖性长时程突触抑制,以改善认知功能[34]。Dex可以保护海马CA1区神经元免受温和短暂性脑缺血引起的功能损伤,激活突触前α2-AR能抑制NE和Glu释放,同时激活突触后α2-AR下调PKA活性,减少Ca2+内流,最终共同阻碍NMDA-R介导的长期突触增强,达到保护神经元的目的[35]。
5 总结与展望NMDA-R和α2-AR分享诸多的下游分子靶点(eEF2K、BDNF、HCN1通道等),其中一些分子已经被证实是调控神经精神疾病和药物研发的重要靶点。进一步研究NMDA-R和α2-AR发挥病理生理功能的共享分子机制,或有利于研发基于共同分子靶点的全新药物,为相关神经精神疾病药物研发提供新策略和新方向。
NMDA-R拮抗剂可以缓解抑郁情绪、预防中风和中枢神经系统创伤中的神经元变性、抑制神经性疼痛、预防阿片类镇痛药耐受性的发展等,但也存在不可忽视的副作用,如氯胺酮能引起成年大鼠大脑皮质细胞的急性神经退行性变化和成年人的类精神病反应。α2-AR激动剂在临床上常用于镇痛、镇静催眠、记忆巩固、降血压,但使用后也不免出现迟发性感觉超敏反应、口干、头晕、意识模糊等副作用。这些不良反应限制了药物的临床应用。研究表明,MK-801能预防甚至逆转α2-AR激动剂使用后延迟出现的热觉和触觉超敏反应,α2-AR激动剂可以改善NMDA-R拮抗剂造成的空间工作记忆缺陷和视觉注意力损害。这些证据提示,NMDA-R拮抗剂与α2-AR激动剂联合用药可能是预防不良反应,实现安全用药的有效策略。(S)-氯胺酮和Dex均可在脊柱水平上与内吗啡肽-1产生协同的抗伤害效果,且三者以有效剂量联用时,表现出更有效的抗伤害效果。这些证据提示,合理使用NMDA-R和α2-AR的相关药物,可能减轻其他药物的不良反应,达到更好的治疗效果。然而,目前尚没有关于两种药物治疗临床疾病的指南,药物联合使用的临床适用症和可能出现的一些新的不良反应也有待进一步研究。综上所述,两种受体相关药物联合使用具有无限优势和广阔前景,但仍需进一步深入探索NMDA-R和α2-AR之间的对话机制,证实联合用药的安全性和有效性,以期能为指导临床复合用药、创新联合用药方案奠定理论基础。
| [1] |
Marrs W, Kuperman J, Avedian T, et al. Alpha-2 adrenoceptor activation inhibits phencyclidine-induced deficits of spatial working memory in rats[J]. Neuropsychopharmacology, 2005, 30(8): 1500-10. doi:10.1038/sj.npp.1300700 |
| [2] |
Roh D H, Kim H W, Yoon S Y, et al. Intrathecal clonidine suppresses phosphorylation of the N-methyl-D-aspartate receptor NR1 subunit in spinal dorsal horn neurons of rats with neuropathic pain[J]. Anesth Analg, 2008, 107(2): 693-700. doi:10.1213/ane.0b013e31817e7319 |
| [3] |
Sandbaumhüter F A, Theurillat R, Bettschart-Wolfensberger R, et al. Effect of the α2-receptor agonists medetomidine, detomidine, xylazine, and romifidine on the ketamine metabolism in equines assessed with enantioselective capillary electrophoresis[J]. Electrophoresis, 2017, 38(15): 1895-904. doi:10.1002/elps.201700017 |
| [4] |
Li H P, Liu K P, Yao L. Dexmedetomidine in combination with ketamine for pediatric procedural sedation or premedication: a meta-analysis[J]. Am J Emerg Med, 2021, 50: 442-8. doi:10.1016/j.ajem.2021.08.073 |
| [5] |
Quartilho A, Mata H P, Ibrahim M M, et al. Production of paradoxical sensory hypersensitivity by alpha 2-adrenoreceptor agonists[J]. Anesthesiology, 2004, 100(6): 1538-44. doi:10.1097/00000542-200406000-00029 |
| [6] |
Chia J S M, Izham N A M, Farouk A A O, et al. Zerumbone modulates α2A-adrenergic, TRPV1, and NMDA NR2B receptors plasticity in CCI-induced neuropathic pain in vivo and LPS-induced SH-SY5Y neuroblastoma in vitro models[J]. Front Pharmacol, 2020, 11: 92. doi:10.3389/fphar.2020.00092 |
| [7] |
姚娇, 杨岩涛, 艾启迪, 等. 神经递质功能与抑郁症发病的研究进展[J]. 中国药理学通报, 2023, 39(7): 1217-21. Yao J, Yang Y T, Ai Q D, et al. Review of research progress on neurotransmitter function and depression[J]. Chin Pharmacol Bull, 2023, 39(7): 1217-21. |
| [8] |
Monteggia L M, Gideons E, Kavalali E T. The role of eukaryotic elongation factor 2 kinase in rapid antidepressant action of ketamine[J]. Biol Psychiatry, 2013, 73(12): 1199-203. doi:10.1016/j.biopsych.2012.09.006 |
| [9] |
Krystal J H, Charney D S, Duman R S. A new rapid-acting antidepressant[J]. Cell, 2020, 181(1): 7. doi:10.1016/j.cell.2020.02.033 |
| [10] |
Luo P, He G, Liu D. HCN channels: new targets for the design of an antidepressant with rapid effects[J]. J Affect Disord, 2019, 245: 764-70. doi:10.1016/j.jad.2018.11.081 |
| [11] |
Huang Z, Li G, Aguado C, et al. HCN1 channels reduce the rate of exocytosis from a subset of cortical synaptic terminals[J]. Sci Rep, 2017, 7: 40257. doi:10.1038/srep40257 |
| [12] |
Compans B, Camus C, Kallergi E, et al. NMDAR-dependent long-term depression is associated with increased short term plasticity through autophagy mediated loss of PSD-95[J]. Nat Commun, 2021, 12(1): 2849. doi:10.1038/s41467-021-23133-9 |
| [13] |
Kim C S, Chang P Y, Johnston D. Enhancement of dorsal hippocampal activity by knockdown of HCN1 channels leads to anxiolytic- and antidepressant-like behaviors[J]. Neuron, 2012, 75(3): 503-16. doi:10.1016/j.neuron.2012.05.027 |
| [14] |
Ma S, Chen M, Jiang Y, et al. Sustained antidepressant effect of ketamine through NMDAR trapping in the LHb[J]. Nature, 2023, 622(7984): 802-9. doi:10.1038/s41586-023-06624-1 |
| [15] |
Thinakaran G, Koo E H. Amyloid precursor protein trafficking, processing, and function[J]. J Biol Chem, 2008, 283(44): 29615-9. doi:10.1074/jbc.R800019200 |
| [16] |
Zhong W, Wu A, Berglund K, et al. Pathogenesis of sporadic Alzheimer's disease by deficiency of NMDA receptor subunit GluN3A[J]. Alzheimers Dement, 2022, 18(2): 222-39. doi:10.1002/alz.12398 |
| [17] |
Bliss T V, Collingridge G L, Kaang B K, et al. Synaptic plasticity in the anterior cingulate cortex in acute and chronic pain[J]. Nat Rev Neurosci, 2016, 17(8): 485-96. doi:10.1038/nrn.2016.68 |
| [18] |
Chen J, Li L, Chen S R, et al. The α2δ-1-NMDA receptor complex is critically involved in neuropathic pain development and gabapentin therapeutic actions[J]. Cell Rep, 2018, 22(9): 2307-21. doi:10.1016/j.celrep.2018.02.021 |
| [19] |
Peltoniemi M A, Hagelberg N M, Olkkola K T, et al. Ketamine: a review of clinical pharmacokinetics and pharmacodynamics in anesthesia and pain therapy[J]. Clin Pharmacokinet, 2016, 55(9): 1059-77. doi:10.1007/s40262-016-0383-6 |
| [20] |
Cottingham C, Wang Q. α2 adrenergic receptor dysregulation in depressive disorders: implications for the neurobiology of depression and antidepressant therapy[J]. Neurosci Biobehav Rev, 2012, 36(10): 2214-25. doi:10.1016/j.neubiorev.2012.07.011 |
| [21] |
Yanpallewar S U, Fernandes K, Marathe S V, et al. Alpha2-adrenoceptor blockade accelerates the neurogenic, neurotrophic, and behavioral effects of chronic antidepressant treatment[J]. J Neurosci, 2010, 30(3): 1096-109. doi:10.1523/JNEUROSCI.2309-09.2010 |
| [22] |
Prokosch V, Panagis L, Volk G F, et al. Alpha2-adrenergic receptors and their core involvement in the process of axonal growth in retinal explants[J]. Invest Ophthalmol Vis Sci, 2010, 51(12): 6688-99. doi:10.1167/iovs.09-4835 |
| [23] |
Wang M, Ramos B P, Paspalas C D, et al. Alpha2A-adrenoceptors strengthen working memory networks by inhibiting cAMP-HCN channel signaling in prefrontal cortex[J]. Cell, 2007, 129(2): 397-410. doi:10.1016/j.cell.2007.03.015 |
| [24] |
Gilsbach R, Röser C, Beetz N, et al. Genetic dissection of alpha2-adrenoceptor functions in adrenergic versus nonadrenergic cells[J]. Mol Pharmacol, 2009, 75(5): 1160-70. doi:10.1124/mol.109.054544 |
| [25] |
Langer S Z. α2-Adrenoceptors in the treatment of major neuropsychiatric disorders[J]. Trends Pharmacol Sci, 2015, 36(4): 196-202. doi:10.1016/j.tips.2015.02.006 |
| [26] |
Szot P, Lester M, Laughlin M L, et al. The anticonvulsant and proconvulsant effects of alpha2-adrenoreceptor agonists are mediated by distinct populations of alpha2A-adrenoreceptors[J]. Neuroscience, 2004, 126(3): 795-803. doi:10.1016/j.neuroscience.2004.04.030 |
| [27] |
Jung K I, Kim J H, Park C K. α2-Adrenergic modulation of the glutamate receptor and transporter function in a chronic ocular hypertension model[J]. Eur J Pharmacol, 2015, 765: 274-83. doi:10.1016/j.ejphar.2015.08.035 |
| [28] |
Egli R E, Kash T L, Choo K, et al. Norepinephrine modulates glutamatergic transmission in the bed nucleus of the stria terminalis[J]. Neuropsychopharmacology, 2005, 30(4): 657-68. doi:10.1038/sj.npp.1300639 |
| [29] |
Li D P, Atnip L M, Chen S R, et al. Regulation of synaptic inputs to paraventricular-spinal output neurons by alpha2 adrenergic receptors[J]. J Neurophysiol, 2005, 93(1): 393-402. doi:10.1152/jn.00564.2004 |
| [30] |
Stevens D R, Kuramasu A, Eriksson K S, et al. Alpha 2-adrenergic receptor-mediated presynaptic inhibition of GABAergic IPSPs in rat histaminergic neurons[J]. Neuropharmacology, 2004, 46(7): 1018-22. doi:10.1016/j.neuropharm.2004.01.004 |
| [31] |
Chen J J, Lue J H, Lin L H, et al. Effects of pre-emptive drug treatment on astrocyte activation in the cuneate nucleus following rat median nerve injury[J]. Pain, 2010, 148(1): 158-66. doi:10.1016/j.pain.2009.11.004 |
| [32] |
Engelhard K, Werner C, Eberspächer E, et al. The effect of the alpha 2-agonist dexmedetomidine and the N-methyl-D-aspartate antagonist S(+)-ketamine on the expression of apoptosis-regulating proteins after incomplete cerebral ischemia and reperfusion in rats[J]. Anesth Analg, 2003, 96(2): 524-31. |
| [33] |
Kim S Y, Raikoff K, Wülfert E, et al. Mivazerol, a selective alpha 2-adrenoceptor agonist, attenuates tachycardia by intrathecal injection of N-methyl-D-aspartate in the rat[J]. Eur J Pharmacol, 1996, 316(2-3): 249-52. doi:10.1016/S0014-2999(96)00801-1 |
| [34] |
Marzo A, Bai J, Caboche J, et al. Cellular mechanisms of long-term depression induced by noradrenaline in rat prefrontal neurons[J]. Neuroscience, 2010, 169(1): 74-86. doi:10.1016/j.neuroscience.2010.04.046 |
| [35] |
Zhou L, Qin S J, Gao X, et al. Dexmedetomidine prevents post-ischemic LTP via presynaptic and postsynaptic mechanisms[J]. Brain Res, 2015, 1622: 308-20. doi:10.1016/j.brainres.2015.06.040 |