


2. 上海中医药大学药学院,上海 201203;
3. 广西中医药大学第一附属医院脑病一科,广西 南宁 530001
 ,
HU Zhi-han2,
SUN Chun-ying1,
ZHU Xiao-dong1,
LI Fang-cun1,
JIANG Ming-he1,
QIN Hong-ling3,
CHEN Wei3,
HU Yue-qiang3
,
HU Zhi-han2,
SUN Chun-ying1,
ZHU Xiao-dong1,
LI Fang-cun1,
JIANG Ming-he1,
QIN Hong-ling3,
CHEN Wei3,
HU Yue-qiang3

2. School of Pharmacy, Shanghai University of Traditional Chinese Medicine, Shanghai 201203, China;
3. Dept of Brain Diseases, the First Affiliated Hospital of Guangxi University of Traditional Chinese Medicine, Nanning 530001, China
血管性痴呆(vascular dementia, VaD)是由于脑血管病变引起的脑组织供血障碍,进而导致脑机能衰竭而产生智能损害的综合征,临床表现为认知和记忆等功能障碍[1]。在世界范围内,VaD占全部痴呆患者总数的25%~50%,成为导致痴呆的第二大原因[2]。随着社会人口结构不断老龄化和脑血管疾病的增加,其发病率呈指数式上升,严重危害人类的身心健康。因此,对于本病的防治已成为当前仍需解决的医学和社会问题[3]。
随着人们对VaD发病机制研究的深入,线粒体稳态平衡在本病发生中所起到的作用受到越来越多的关注。线粒体稳态是一种由线粒体分裂和融合、线粒体生物合成和线粒体自噬等动态调节的过程[4]。最新一项研究证明[5],线粒体质量异常与衰老等疾病的发生密切相关。因此,研究线粒体稳态调控,特别是针对线粒体的动力学平衡及自噬机制进行探索,对延缓VaD的进展,具有重要的理论和现实意义。本团队前期研究证实[6],温肺降浊方(Wenfei Jiangzhuo formula, WFJZF)可以通过降低VaD大鼠线粒体相关蛋白细胞色素(cytochrome, Cytc)、凋亡蛋白(bcl2-associated X, Bax)的表达,减少神经元凋亡。最新研究表明[7],Bax的高表达促进线粒体动力相关蛋白(dynamics-related proteins1, Drp1)定位于线粒体外膜,加强线粒体分裂活性。磷酸甘油酸变位酶5(phosphoglycerate mutase 5, PGAM5)能够介导Drp1易位到受损的线粒体,从而构成PGAM5-Drp1轴调控线粒体动力学系统。有鉴于此,本研究拟从PGAM5-Drp1轴与线粒体稳态的关系着手,探讨温肺降浊方防治VaD的作用机制,为VaD的中医治疗提供新思路。
1 材料 1.1 实验动物健康成年雄性SD大鼠,由湖南斯莱克景达实验动物有限公司提供,动物许可证号:SCXK(湘)2019-0004。所有大鼠饲养于广西中医药大学科学实验中心动物房,室温保持在(23±3) ℃, 湿度保持在(45±10)%,自由摄食摄水,间隔3 d测量大鼠体质量并记录。本研究经广西中医药大学科学实验中心动物伦理委员会审查,No DW20230425-105。
1.2 温肺降浊方制备由制附子20 g(先煎)、党参15 g、干姜10 g、田七10 g、酒大黄10 g、炙甘草6 g组成。所有药物购买于广西中医药大学第一附属医院门诊中药房,本方分2次煎煮,取汁200 mL, 加热浓缩至含有原药材1.5 kg·L-1。盐酸多奈哌齐(思博海)5 mg,批号:国药准字H20010723。
1.3 主要试剂和仪器苏木精、伊红Y(水溶)、环氧树脂(货号:H8070、E8090、B9080),北京索莱宝科技有限公司;丙酮酸钠(货号:ST1661),上海碧云天生物技术有限公司;PGAM5抗体、Drp1抗体、OPA1抗体、Mfn2抗体(货号:ab308447、ab184247、ab42364、ab124773),英国Abcam公司;三色预染蛋白Marker 10~250 ku(货号:WJ103),上海雅酶生物医药科技有限公司。
Multiskan SkyHigh全波长酶标仪,美国Thermo公司;BX53生物显微镜,奥林巴斯株式会社;120 kV HT7800RuliTEM透射电镜,株式会社日立制作所;DMi8相差显微镜,恩斯特·徕茨有限公司;PowerPac 3000电泳仪,美国Bio-Rad公司。
2 方法 2.1 模型制备和分组适应性喂养大鼠2周,体质量(250±30) g,随机分为6组:Sham group、Model group、Donepezil group、WFJZF-L group、WFJZF-M group、WFJZF-H group(n=6)。大鼠通过永久性双侧颈总动脉闭塞(2 VO)建立VaD大鼠模型。具体方法[8]:用1% 40 mg·kg-1戊巴比妥钠腹腔内麻醉大鼠,经颈部正中切口暴露双侧颈总动脉,轻轻分离双侧颈总动脉和迷走神经,用6-0号丝线结扎双侧血管。Sham group只暴露动脉不进行结扎。整个手术过程操作轻柔,减少触碰迷走神经,术后用加热毯维持大鼠体温。
2.2 给药本次实验共给药3周,各组大鼠于造模1周后开始药物干预。Sham group和Model group灌胃等体积蒸馏水;Donepezil group灌胃20 mg·kg-1多奈哌齐,1次/日;WFJZF-L group、WFJZF-M group、WFJZF-H group分别按2.95、5.9、11.8 g·kg-1[6],灌胃3 mL,早、晚各1次。
2.3 取材在末次给药后,各组大鼠提前禁食禁水24 h,1% 戊巴比妥钠3 mL腹腔过量麻醉。立刻断头取脑,每组取3只进行心脏灌注,将其用4%多聚甲醛固定10 d,进行石蜡包埋。其余3只剥离海马组织,放入冻存管,-80 ℃冰箱保存。
2.4 水迷宫测试于造模后1周和4周分别进行水迷宫检测,以判定模型制备是否成功和药物治疗效果。定位航行实验:本实验连续开展5 d,令大鼠在水池中自由游行60 s,以适应水中环境。于水池4个象限边缘中间位置标记,平台低于水面2 cm。将大鼠面朝池壁从4个标记点放入水中,间隔5 min。于60 s内成功停留站台,即完成实验;若60 s未成功找到站台,人工引导10 s。第1~2天为训练实验,后3天记录逃避潜伏期数据,以均数来评估大鼠空间记忆能力。空间探索实验:第6天移除池中平台,将大鼠沿非平台所在的象限位置入水,记录其60 s内穿过原平台区域的次数。
2.5 HE染色取出包埋好的组织蜡块,冰冻切片机切片厚4 μm,水浴锅展片,脱水,进行HE染色,中性树胶封片,光镜下观察。
2.6 高尔基染色于海马组织上取5~10 mm厚的组织块(冠状切面),经蒸馏水快速洗涤去除血液,置于高尔基固定液中。根据试剂盒要求将溶液A、B混匀,将组织置于A和B混合液中,室温避光2周。将组织转移至溶液C中,避光7 d,振动切片机切成100~200 μm的切片,室温下干燥3天,蒸馏水洗涤2次,每次4 min,根据溶液D和溶液E以及水的配比,配置1 ∶2的配制液,将玻片置于混合液中,梯度酒精和无水乙醇分别脱水,二甲苯通透,封片后用3D扫描仪进行图片采集,选择二级树突进行定量分析。
2.7 透射电镜于海马组织上取2 mm厚的组织块(冠状切面),置于电镜固定液中,4 ℃固定1.5~2.0 h,梯度酒精脱水,环氧树脂Epon 812于丙酮(1 ∶1)渗透1 h,甲苯胺蓝染色1 min,置于铜网上。于铜网滴加20 μL醋酸铀,染色40 min,用HT7800RuliTEM透射电镜进行观察拍照。
2.8 免疫组化取出海马组织的包埋蜡块,组织切片,抗原修复,PBS冲洗,过氧化氢消除内源性过氧化物酶,血清封闭,滴加PGAM5(1 ∶200)、Drp1(1 ∶200)、OPA1(1 ∶200)一抗孵育,4 ℃过夜;再次加入二抗37 ℃孵育40 min,DAB显色,苏木精复染,梯度酒精分化,自来水返蓝,中性树胶封片,光学显微镜下随机观察每张切片不同视野,以棕黄色为阳性表达,采用Image-Pro测定每个视野中的平均光密度值。
2.9 蛋白免疫印迹(Western blot)从-80 ℃冰箱取出脑组织,剪出一部分组织放入装有钢珠的1.5 mL EP管中,自动制冷匀浆机匀浆,加RIPA裂解液,加入PMSF蛋白酶抑制剂,BCA蛋白检测试剂盒进行定量分析。根据分子量制备相应分离胶,通过电泳、转膜、5% BSA封闭,TBST洗膜,一抗稀释比例:PGAM5(1 ∶2 000)、Drp1(1 ∶2 000)、OPA1(1 ∶2 000)、Mfn1(1 ∶2 000)、Mfn2(1 ∶2 000)孵育,4 ℃过夜;TBST洗膜3次,每次10 min,稀释二抗比例为(1 ∶5 000),将PVDF膜放置于二抗中,37 ℃摇床孵育1.5 h,TBST洗膜,超敏ECL显色后曝光,采用ImageJ 8.0软件进行分析,以线粒体蛋白COX4为内参,计算目的蛋白相对表达量。
2.10 统计学方法采用SPSS 26.0进行统计分析。计量资料以x±s表示;若组内样本符合正态分布,则采用单因素方差分析(one-way ANOVA),多样本均数与单组均数间的比较用LSD-t检验,检验水准α=0.05。若组内样本不符合正态分布,则采用两独立样本非参数检验,多样本均数与单组均数间比较用Mann-Whitney U检验;等级资料采用c2检验;所有输出结果均以P<0.05。
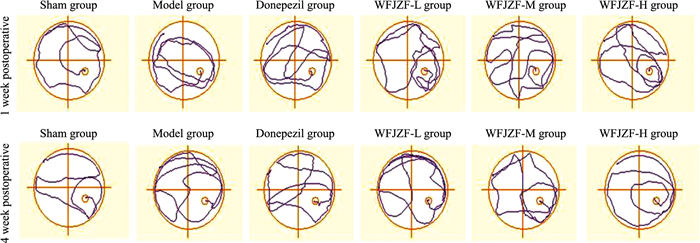
3 结果 3.1 温肺降浊方对VaD模型大鼠认知水平的影响术后1周水迷宫测试提示,与Sham group比较,Model group及各干预组大鼠逃避潜伏期延长,穿越平台次数减少,提示模型制备成功。术后4周水迷宫测试提示,与Sham group比较,Model group大鼠逃避潜伏期延长(P<0.05),穿越平台次数减少(P<0.05);与Model group比较,Donepezil group和WFJZF-H group大鼠逃避潜伏期缩短(P<0.05),穿越平台次数增加(P<0.05),见Tab 1和Fig 1。
| Group | 1 week postoperative | 4 weeks postoperative | |||
| Escape latency/s | Number of platform crossings/time | Escape latency/s | Number of platform crossings/time | ||
| Sham | 20.01±2.44 | 4.02±0.73 | 23.18±3.69 | 5.33±0.31 | |
| Model | 44.11±5.24# | 2.51±0.41# | 40.07±4.59# | 3.01±0.18# | |
| Donepezil | 42.26±5.02# | 2.59±0.49# | 37.82±3.71* | 3.68±0.27* | |
| WFJZF-L | 42.17±5.09# | 2.55±0.40# | 39.59±4.38 | 3.17±0.14 | |
| WFJZF-M | 42.41±5.21# | 2.56±0.43# | 38.89±4.90 | 3.24±0.20 | |
| WFJZF-H | 42.43±4.55# | 2.58±0.43# | 36.77±3.16* | 4.12±0.23* | |
| #P<0.05 vs Sham; *P<0.05 vs Model. | |||||
|
| Fig 1 Morris water maze trajectory in postoperative groups of rats |
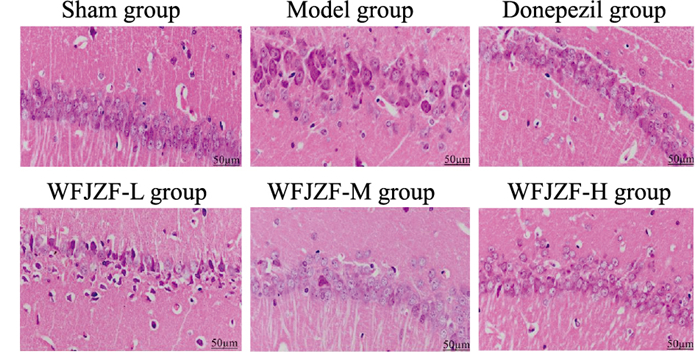
如Fig 2所示,Sham group大鼠海马神经元排列紧密,数量较多,形态饱满。Model group海马神经元形态稀疏,胞质破裂、水肿,细胞核缩小;Donepezil group和WFJZF-H group海马神经元数量增多,排列较Model group紧密,形态逐渐规整。
|
| Fig 2 Histopathological changes in hippocampus of rats in each group (HE staining, ×200) |
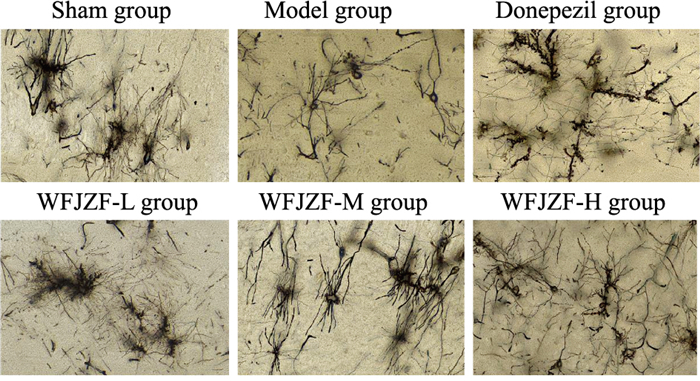
如Fig 3和Tab 2所示,假手术组大鼠海马组织树突棘形态规整,排列紧密,二级树突密布;与Sham group比较,Model group大鼠海马组织树突棘明显减少,二级树突结构基本消失,排列稀散(P<0.05);与Model group相比,Donepezil group和WFJZF-H group二级树突结构明显增多(P<0.05)。
|
| Fig 3 Distribution of neural ultrasynaptic structures in rat hippocampal tissue (Golgi staining, ×400) |
| Group | Secondary dendrites(number) |
| Sham | 41.33±9.02 |
| Model | 12.67±2.08# |
| Donepezil | 25.33±5.03* |
| WFJZF-L | 15.00±1.73 |
| WFJZF-M | 17.67±1.53 |
| WFJZF-H | 32.01±7.21* |
| #P<0.05 vs Sham; *P<0.05 vs Model. | |
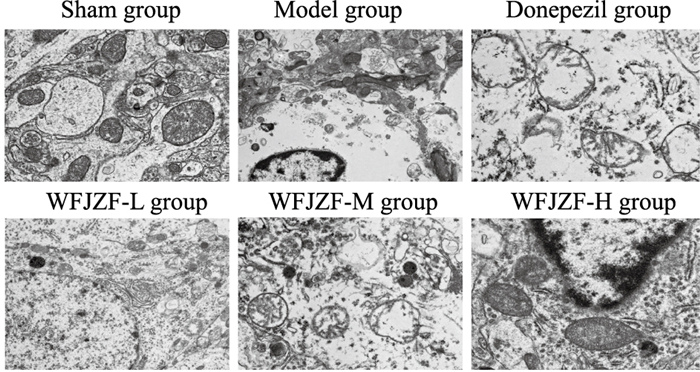
如Fig 4所示,Sham group大鼠海马神经元线粒体排列密布,结构性完整;Model group大鼠海马神经元线粒体数量减少,体积缩小,细胞外膜破裂,膜厚度增加,线粒体嵴减少,结构空洞;与Model group相比较,Donepezil group和WFJZF-H group大鼠海马神经元线粒体损伤程度减少,结构较为完整。
|
| Fig 4 Mitochondrial changes in hippocampal tissue of rats in each group (transmission electron microscopy, ×12 000) |
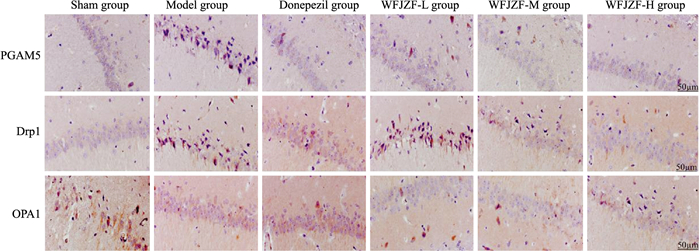
如Fig 5和Tab 3所示,与Sham group相比,Model group海马神经元中PGAM5、Drp1阳性蛋白表达升高(P<0.05),OPA1阳性蛋白表达下降(P<0.05);与Model group相比,Donepezil group和WFJZF-H group中PGAM5、Drp1阳性蛋白表达下降(P<0.05),OPA1阳性蛋白表达升高(P<0.05)。
|
| Fig 5 Positive protein expression of PGAM5, Drp1, and OPA1 in CA1 region of hippocampus in various groups of rats (immunohistochemistry, ×400) |
| Group | PGAM5 | Drp1 | OPA1 |
| Sham | 0.22±0.08 | 0.41±0.13 | 1.15±0.13 |
| Model | 1.47±0.65# | 1.35±0.45# | 0.26±0.19# |
| Donepezil | 0.47±0.09* | 0.53±0.26* | 0.99±0.10* |
| WFJZF-L | 1.04±0.34 | 1.17±0.21 | 0.27±0.21 |
| WFJZF-M | 0.98±0.40 | 0.89±0.23 | 0.32±0.17 |
| WFJZF-H | 0.38±0.07* | 0.51±0.20* | 1.02±0.09* |
| #P<0.05 vs Sham; *P<0.05 vs Model. | |||
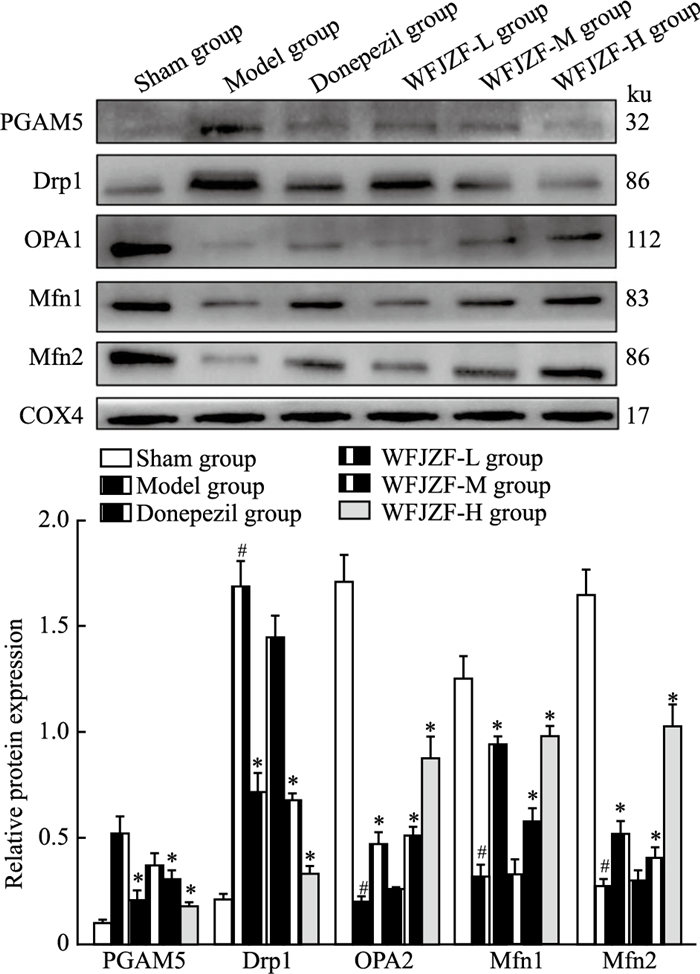
如Fig 6显示,与假手术比较,Model group大鼠海马组织PGAM5和Drp1蛋白表达升高(P<0.05),OPA1、Mfn1/2蛋白表达下降(P<0.05);与Model group比较,Donepezil group和WFJZF-M group、WFJZF-H group PGAM5和Drp1蛋白表达下降(P<0.05),OPA1、Mfn1/2蛋白表达升高(P<0.05)。
|
| Fig 6 PGAM5-Drp1 signaling pathway related protein expression in rat hippocampal tissue #P<0.05 vs Sham; *P<0.05 vs Model |
中药及单体多次报道[9-10]对血管性痴呆和阿尔茨海默病有效。前期研究显示[11],温肺降浊方能够抑制海马神经元线粒体相关凋亡蛋白的表达,对大鼠海马神经元具有一定的保护作用。
然而,痴呆所引起的神经损伤多与线粒体稳态密切相关。线粒体稳态指线粒体处于不断分裂与融合的动态过程,线粒体融合增加了神经元中线粒体膜电位的强度和ATP的水平,使神经细胞应对脑缺血缺氧的能力提升,并且机体能够快速识别和去除功能障碍的线粒体,以保持细胞内稳态平衡。相反,神经元中线粒体分裂增加会导致线粒体去极化,细胞ATP水平下降,引起神经元凋亡,最终导致细胞内稳态失衡[12]。研究认为[13-14],哺乳动物线粒体的融合主要分布在线粒体外膜上的线粒体融合蛋白1/2(mitochondrial fusion protein 1/2, Mfn1/2),以及线粒体内膜上的神经萎缩相关蛋白1(opticatrophyprotein-1, OPA1)共同调控,而分裂主要由Drp1调控,融合和分裂蛋白的活性和动态平衡共同决定线粒体的整体表现。一般线粒体的分裂发生在融合之后,表现较为突出的分裂因子诱导细胞质中Drp1聚集在线粒体膜上,导致双层膜断裂完成分裂。最新证据指出[15],老年性痴呆大鼠组织内OPA1表达量减少,引起Drp1表达水平上调,而抑制Drp1表达,OPA1及Mfn1/2蛋白表达量明显增加,线粒体融合作用增强。反之,Drp1表达的上升往往可以直接抑制线粒体融合性。PGAM5是磷酸甘油酸变位酶超家族成员之一,是一种定位于线粒体外膜的蛋白[16]。最新研究显示[17],PGAM5与线粒体损伤有关,它可通过Ser 637位点的Drp1去磷酸化促进线粒体裂变、细胞凋亡和线粒体自噬性死亡信号放大,最终引起细胞死亡。已经证实敲低或者抑制PGAM5可通过抑制Drp1减少心肌缺血/再灌注(I/R)损伤中的细胞凋亡和坏死性凋亡[18]。同时,本次实验的研究结果与上述科学结论基本一致。因此,调控PGAM5-Drp1轴对减轻线粒体分裂,增强线粒体融合至关重要。
本实验中,术后1周模型组大鼠逃避潜伏期明显延长,穿越平台次数减少,提示着模型大鼠空间学习和记忆能力存在障碍。而术后4周温肺降浊方干预后,模型大鼠的逃避潜伏期缩短,穿越平台次数增多,说明温肺将浊方对VaD模型大鼠的认知障碍具有改善作用。此外,海马体在人类记忆、认知和学习能力方面发挥着重要的作用,是目前神经痴呆领域研究的重点。HE染色、高尔基染色提示模型组大鼠的细胞结构稀松,出现水肿,细胞核缩小现象,海马组织树突棘减少,二级树突结构基本消失。经过温肺降浊方干预后,细胞水肿减少,排列逐渐密集,海马组织二级树突结构明显增加,提示海马神经元损伤是VaD进展的可能机制,而温肺降浊方对VaD大鼠的神经元损伤具有保护效应。
为进一步证明海马神经元损伤与线粒体稳态的相关性,透射电镜提示,VaD模型大鼠海马组织中线粒体数量减少,外膜破裂、膜厚度增加,线粒体嵴减少,结构空洞,提示了VaD发生发展过程中神经元及神经细胞中线粒体均损伤,线粒体动态平衡被打破。经过温肺降浊方干预后,海马组织中线粒体损伤明显减少,结构较为完整,说明温肺降浊方能够减轻海马组织损伤,调控线粒体稳态平衡。此外,模型组中海马组织内OPA1、Mfn1、Mfn2蛋白表达下降,PGAM5、Drp1蛋白表达升高。经过温肺降浊方干预后,海马组织内OPA1、Mfn1、Mfn2蛋白表达升高,PGAM5、Drp1蛋白表达下降。综上所述,温肺降浊方可以调控PGAM5-Drp1信号轴以改善线粒体稳态平衡,从而提升大脑认知水平,发挥脑保护效应。
| [1] |
Wang X, Zhang B, Xia R, et al. Inflammation, apoptosis and autophagy as critical players in vascular dementia[J]. Eur Rev Med Pharmacol Sci, 2020, 24(18): 9601-14. |
| [2] |
Eshraghi M, Adlimoghaddam A, Mahmoodzadeh A, et al. Alzheimer's disease pathogenesis: role of autophagy and mitophagy focusing in microglia[J]. Int J Mol Sci, 2021, 22(7): 30-3. |
| [3] |
Tian Z, Ji X, Liu J, et al. Neuroinflammation in vascular cognitive impairment and dementia: current evidence, advances, and prospects[J]. Int J Mol Sci, 2022, 23(11): 6224-8. doi:10.3390/ijms23116224 |
| [4] |
Wang W, Qiao O, Ji H, et al. Autophagy in vascular dementia and natural products with autophagy regulating activity[J]. Pharmacol Res, 2021, 17(11): 756-61. |
| [5] |
Edogten M, Ergul A. Vascular contributions to cognitive impairment/dementia in diabetes: role of endothelial cells and pericytes[J]. Am J Physiol Cell Physiol, 2022, 23(4): C1177-89. |
| [6] |
Yueqiang, H, No ng, T, L in, W, et al. Efficacy and mechanism of Wenfei Jiangzhuo decoction combined with donepezil hydrochloride tablets in the treatment of vascular dementia[J]. Am J Chin Med, 2019, 28(13): 1378-81. |
| [7] |
Feng L, He H, Xiong X, et al. Plasma-derived phosphoglycerate mutase 5 as a biomarker for Parkinson's disease[J]. Front Aging Neurosci, 2022, 7(14): 102-16. |
| [8] |
Farkas E, Luiten P, Bari F. Permanent bilateral common carotid artery occlusion in the rat: a model for chronic cerebral hypoperfusion-related neurodegenerative diseases[J]. Brain Res Rev, 2007, 54(1): 162-80. doi:10.1016/j.brainresrev.2007.01.003 |
| [9] |
杨岩涛, 赵佳柱, 肖佳妹, 等. 人参皂苷治疗阿尔茨海默病的药理作用研究进展[J]. 中国药理学通报, 2021, 37(12): 1638-43. Yang Y T, Zhao J Z, Xiao J M, et al. Progress of pharmacologic effects of ginsenosides in the treatment of Alzheimer's disease[J]. Chin Pharmacol Bull, 2021, 37(12): 1638-43. doi:10.3969/j.issn.1001-1978.2021.12.003 |
| [10] |
马婧怡, 张万鑫, 陈虹, 等. 松果菊苷对血管性痴呆大鼠氧化应激损伤的保护作用[J]. 中国药理学通报, 2014, 30(5): 638-42. Ma J Y, Zhang W X, Chen H, et al. Protective effect of pinealoside against oxidative stress injury in rats with vascular dementia[J]. Chin Pharmacol Bull, 2014, 30(5): 638-42. doi:10.3969/j.issn.1001-1978.2014.05.011 |
| [11] |
Hu Y, Chen W, Wu L, et al. Clinical observation of the efficacy and mechanism of the Wenfei Jiangzhuo formula in lung and kidney deficiency-type vascular dementia[J]. All Life, 2020, 13(1): 144-50. doi:10.1080/26895293.2020.1729869 |
| [12] |
Peng D, Wang Y, Huang T, et al. Ligustilide improves cognitive impairment via regulating the SIRT1/IRE1α/XBP1s/CHOP pathway in vascular dementia rats[J]. Oxid Med Cell Longev, 2022, 16(12): 63-77. |
| [13] |
Yao R, Ren C, Xia Z, et al. Organelle-specific autophagy in inflammatory diseases: a potential therapeutic target underlying the quality control of multiple organelles[J]. Autophagy, 2021, 7(2): 385-401. |
| [14] |
Schäfer J, Bozkurt S, Michaelis J, et al. Global mitochondrial protein import proteomics reveal distinct regulation by translation and translocation machinery[J]. Mol Cell, 2022, 82(2): 435-46. doi:10.1016/j.molcel.2021.11.004 |
| [15] |
Zhong G, James M, Smeltz M, et al. Age-related changes in expression and activity of human hepatic mitochondrial glutathione transferase zeta1[J]. Drug Metab Dispos, 2018, 46(8): 1118-28. doi:10.1124/dmd.118.081810 |
| [16] |
Chen C, Yang C, Wang J, et al. Melatonin ameliorates cognitive deficits through improving mitophagy in a mouse model of Alzheimer's disease[J]. J Pineal Res, 2021, 71(4): 127-34. |
| [17] |
Adebayo M, Singh S, Singh A, et al. Mitochondrial fusion and fission: the fine-tune balance for cellular homeostasis[J]. FASEB J, 2021, 35(6): 216-20. |
| [18] |
Chan D. Mitochondrial dynamics and its involvement in disease[J]. Annu Rev Pathol, 2020, 24(15): 235-59. |