


邢露(1987-),女,博士,讲师,研究方向:分子药理学与药代动力学,共同第一作者,E-mail:xinglu_jzs@xiyi.edu.cn。
 ,
XING Lu
,
XING Lu ,
LI Peng-quan,
ZHAO Dong,
CHU Hai-qing,
HE Chun-xia,
QIN Wei,
LI Hui-jin,
FU Jia,
ZHANG Ye,
XIAO Li,
CAO Hui-ling
,
LI Peng-quan,
ZHAO Dong,
CHU Hai-qing,
HE Chun-xia,
QIN Wei,
LI Hui-jin,
FU Jia,
ZHANG Ye,
XIAO Li,
CAO Hui-ling

血管钙化是指类似于骨样结构的钙化斑块出现在血管部位,引起血管内血流改变,血压增加等一系列病理现象的心血管疾病并发症,可导致心血管疾病患者的高发病率和死亡率。血管钙化的发生包含一系列复杂的病理过程,涉及不同的机制,目前并没有有效的手段可在血管钙化发生后对其病理过程进行逆转。骨形态发生蛋白7(bone morphogenetic protein 7,BMP-7)是一种分泌型的细胞外基质蛋白,在人体正常的骨形成与异常的血管钙化中均可发挥一定的调节作用,BMP-7目前被认为是内源性血管钙化抑制因子。该文对BMP-7在血管钙化中的作用及机制研究进展以及目前的临床应用现状进行综述,为BMP-7影响血管钙化的机制深入研究提供新思路,为基于BMP-7的血管钙化早期诊断试剂盒与药物研发提供参考。
1 血管钙化与骨形成密切相关 1.1 血管钙化是一个主动的、可调控的异位骨化病理过程血管钙化是一个主动的、可调控的心血管系统异位钙化过程,归属心血管并发症,常伴随多种疾病病理条件,比如糖尿病、慢性肾病、动脉粥样硬化等而发生,并且可作为上述疾病的预警信号,具有重要的临床意义。内膜钙化和中膜钙化为血管钙化的主要及常见类型。血管中膜和内膜中的内皮细胞和血管平滑肌细胞(vascular smooth muscle cells,VSMCs)之间可通过外泌体进行细胞通讯。初始的血管钙化是一个模拟骨生成的生物钙化过程,体内血钙和血磷浓度的异常增加诱导核心结合因子α1(core binding factor α1,Cbfα1)表达增加,进一步调控骨形态发生蛋白-2(bone morphogenetic protein-2,BMP-2)、骨钙素(osteocalcin,OCN)和Ⅰ型胶原蛋白等的表达增加,同时在体内病理微环境高糖、高钾及炎症等影响下氧化应激、自噬等调控异常,内稳态失衡,骨桥蛋白(osteopontin,OPN)、焦磷酸盐和胎球蛋白-A等表达降低,VSMCs发生表型转换,分泌基质囊泡和凋亡小体,同细胞外基质共同作用形成钙磷沉积位点,发生血管钙化[1-2]。血管钙化与多种机制密切相关,涉及公认的钙磷代谢紊乱机制、细胞凋亡机制、细胞控制学说、miRNA调节机制、H2S和短链脂肪酸等的调节机制以及细胞外基质重塑机制。多种机制背景下的多个原因交叠造成血管钙化这一病理结果。关于体内血管钙化的调控并非是单一的,而是不同的病理微环境会响应不同的调控反应。但是最终呈现的结果形式一致,即血管钙化发生、血管壁硬度增加、顺应性降低、心血管疾病的发病率和死亡率风险增加[3]。
血管钙化是一个涉及多种因素的复杂过程,发病机制尚不明晰。一旦发生,尚无可逆转钙化的有效干预措施,目前主要以预防为主。探寻具体病理微环境下导致血管钙化的靶标分子及一系列的联动机制,从起因到过程到病变结果的清晰阐释对于临床针对性治疗意义重要。血管钙化发病机制的研究,有助于我们更深刻地认识其疾病发生发展的过程,开发有效的治疗手段,对降低心血管疾病患者的死亡率具有重要意义。
1.2 骨形成中的类骨质钙化与血管钙化密切相关骨形成的方式包含膜内化骨和软骨内化骨,两者都是首先形成类骨质,然后再钙化为骨质。骨形成涉及的关键转录因子包括性别决定区Y框蛋白9、Cbfα1、转录激活因子4和转录激活蛋白-1。成骨细胞由特殊的间充质细胞经成熟过程转化而来,是未终末分化的特化细胞,它一方面负责骨基质的沉积,另一方面可调节破骨细胞。成骨细胞包含发挥囊泡运输和分泌作用的质膜区域,可分泌OPN、OCN、Ⅰ型胶原蛋白和ALP,其中Ⅰ型胶原蛋白在成骨细胞分化开始时就表达,可在细胞外基质重塑过程中为骨骼提供结构支撑,使钙质以羟基磷灰石形式沉积[4]。
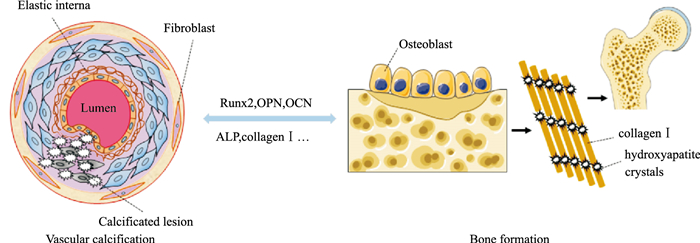
血管钙化是血管中发生的一种异位骨化病理改变,钙磷以羟基磷灰石形式异常沉积在血管壁,是血管内皮层和平滑肌层应对病理微环境作用的结果。异位骨化的发生会刺激机体自身固有免疫应答,比如巨噬细胞会刺激促成骨基因等,从而驱动组织内的细胞分化为软骨细胞。骨形成中类骨质钙化为骨质的过程与血管钙化过程都涉及羟基磷灰石的沉积钙化,两者也受到共同调控因子的调节,包括Cbfα1、ALP、OPN、OCN和Ⅰ型胶原蛋白等[3](Fig 1)。骨形成机制的揭示将为血管钙化中细胞发生转换的机制的阐明,提供可参考的信息。
|
| Fig 1 Interactive regulation between vascular calcification and bone formation |
BMPs蛋白家族最初因其诱发异位骨生成而命名,该家族成员结构类似,是一类高度保守的功能蛋白。除BMP-1外,其余均属于转化生长因子-β(transforming growth factor beta,TGF-β)家族。BMPs家族共有20个成员,包括BMP-1至BMP-15等。BMPs家族蛋白与骨骼发育、眼睛发育、胚胎发育、造血组织和神经组织的发育等多项生命活动有关,涉及细胞增殖分化、细胞凋亡和细胞间通讯等。BMP信号通路通过调节Smads转录因子磷酸化和核易位,刺激基因转录。BMP、糖蛋白Wnt家族和性类固醇激素是已知重要的骨合成代谢因素和骨矿物质含量的决定因素[5]。
BMP-2是BMPs家族中目前研究比较清楚的强成骨活性诱导因子。在人和动物的不同器官中均有不同程度的表达,参与骨形成、生长发育、脂肪沉积和癌症发生等。在骨形成中,BMP-2可促使间充质细胞分化为成骨/成软骨细胞。BMP-2异常的过度表达与进行性骨化性肌炎有关[6]。BMP-2激活的信号通路可调节血管生成,促进血管病变,增加钙化机率,是血管钙化中强有力的促进因素[7]。BMP-4和BMP-2属于同一亚组,两者在血管钙化的区域均有表达。VSMCs和内皮细胞均可表达BMP及其受体。研究显示,冠状动脉钙化合并慢性肾功能不全(chronic kidney disease,CKD)患者,其血清中的BMP-4水平与冠状动脉钙化指数呈正相关。BMP-7在体内也发挥多种重要作用,包括诱导骨生成,调节胚胎期肾脏发育,维持成熟机体内肾脏功能,促进细胞增殖以及参与细胞外基质调控等。近年来,BMP-7在血管钙化中的保护作用也受到关注,其发挥保护作用的机制还有待阐明。
BMPs家族成员之间结构相似,高度保守,在多种组织和细胞当中都发挥重要的调节作用,那么其具体的成员蛋白在不同的细胞当中如何配合实现差异性的功能调控还需要进一步的研究。另外BMPs家族中不同的蛋白之间针对同样的病变,或是协同发挥相同的作用,或是发挥相反的作用,像BMP-2和BMP-4均促进血管钙化,而BMP-7则抑制血管钙化,那这种同家族成员之间作用的差异就提示我们这些蛋白虽然具有相似的结构,但是它们的不同的结构域和基序或许起着更加关键精细的调控作用。
2.2 BMP-7可发挥多种调节作用BMP-7也叫作骨调素1(osteogenic protein-1,OP-1),在人类中由BMP-7基因编码,位于人类的第20号染色体上。BMP-7是TGF-β超家族中的一类分泌蛋白,可在细胞与细胞之间进行信号传导,以保证生物体从一个单细胞经过分裂、分化过程,成为成熟的有机体[8]。
人的BMP-7基因大小为1293bp,首先编码产生由431个氨基酸组成的大小约49.3 ku的BMP-7前体蛋白。前体蛋白包含信号肽、前导肽和成熟肽。其中在前导肽上含有1个N-糖基化位点,成熟肽上含有3个N-糖基化位点,以使BMP-7能够正确折叠和分泌。它的羧基端是由7个半胱氨酸组成的保守区,形成链内和链间的二硫键,为TGF-β家族共有。BMP-7前体蛋白没有活性,分泌后C末端被酶解释放,再经二硫键结合成为有活性的成熟蛋白质。成熟的BMP-7是分子量大小约为35 ku的可溶性的同源二聚体糖蛋白[8]。Groppe等[9]利用X线晶体衍射技术发现,BMP-7二聚体包含1个α螺旋和8个β折叠链,形似“蝴蝶状”,由核心向两侧伸出两个“翅膀”状结构,以使二聚体稳定。
BMP-7在骨组织、肾脏、肝脏、眼睛和血管等中广泛表达,可诱导软骨和骨形成、拮抗促纤维化,在体内的稳态维持和组织再生方面发挥内源性调节作用[10]。BMP-7通过与其细胞膜上受体结合,使下游Smads因子磷酸化,进而将信号传递到细胞核以调控靶基因的转录。BMP-7受体包括Ⅰ型受体和Ⅱ型受体,属于丝氨酸/苏氨酸激酶受体。Ⅰ型受体有激活素受体样激酶2(activin receptor-like kinase 2,ALK2)、ALK3和ALK6。BMP-7与ALK2和ALK6的亲和力较强。Ⅱ型受体包括ActRⅡ、ActRⅡB和BMPRⅡ。BMP-7与Ⅱ型受体结合后磷酸化Ⅰ型受体,随后磷酸化Smads因子并与之结合,共同发挥细胞内第二信使的作用[8]。
BMP-7前体蛋白经弗林蛋白酶Furin加工后成为有活性的形式,激活后的BMP-7首先与其所在细胞膜上的Ⅱ型受体结合,紧接着磷酸化Ⅰ型受体,我们推测不同种类的Ⅱ型受体和Ⅰ型受体可能是BMP-7在不同组织和细胞中发挥不同调控作用的原因之一,对应响应的下游Smads蛋白类型或有不同,进而可对细胞核中的不同靶基因进行调控。Smads是BMP-7等TGF-β超家族受体的主要信号转导器,包含受体调节型Smads(R-Smads)、协同型Smads(Co-Smads)和抑制型Smads(I-Smads)。R-Smads由Smad1、Smad2、Smad3、Smad5和Smad8/9组成。Smad4是唯一已知的人类Co-Smads,可与R-Smad合作招募共同调节剂。I-Smads包含Smad6和Smad7,可抑制R-Smads活性。在正常生理条件和病理条件下,不同的组织和细胞当中参与调控的Smads类型及方式不同[11]。不同类型的Smads的分工和组合也使BMP-7调控的多样性成为可能。
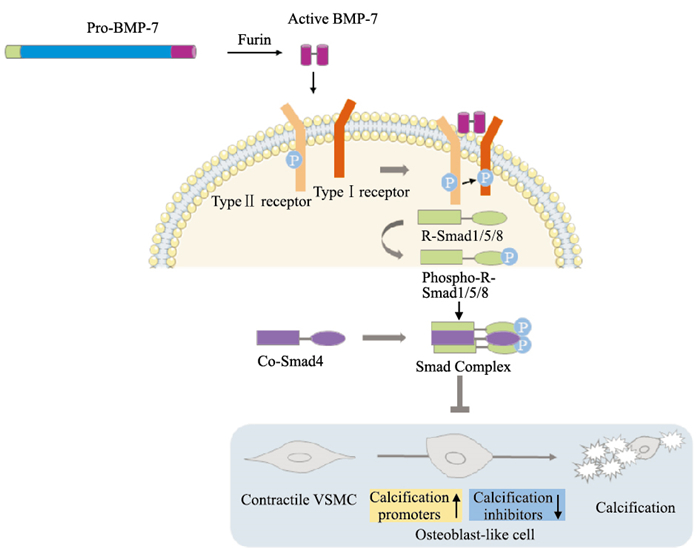
在血管钙化中,随着Ⅰ型受体的磷酸化,下游Smad1/5/8发生磷酸化,信号继续呈递给Co-Smad4引起Smad复合物的磷酸化并募集共同调节因子,通过影响与血管钙化相关的目标基因,打破正常生理条件下的钙化促进因子和抑制因子的表达,从而抑制VSMCs从收缩表型转化为成骨样表型导致钙化的过程(Fig 2)。BMP-7调控过程中涉及到的具体的目标基因及对应调控方式还有待研究,目前尚不明晰。除了Smads途径,BMP-7也可通过MAPKs、PI3K/AKT、RAS/ERK和JNK等发挥调控作用[8]。
|
| Fig 2 BMP-7 inhibits vascular calcification through Smads pathway |
BMP-7在不同的组织中发挥不同的调节作用,那么BMP-7在血管等不同组织中与哪些信号分子相关,存在哪些相同和不同之处,发挥关键作用的调控机制是什么需要结合组织细胞的特异性进行深入研究。
2.3 BMP-7为体内血管钙化抑制因子多项研究表明,BMP-7可预防或减轻血管钙化[12-15]。VSMCs逐渐转化为成骨/成软骨化细胞表型,是血管钙化发生的重要环节。BMP-7可抑制血清、血小板衍生生长因子亚基BB或TGF-β1刺激下的原发性人主动脉VSMCs增殖,维持其收缩表型。BMP-7在脉管系统中发挥抗炎作用,有助于维持血管完整性[12]。BMP-7在健康成人肾脏中表达,在肾纤维化模型中发挥关键保护作用。与BMP-2相反,BMP-7可能有助于防止慢性肾脏疾病患者的钙化。在慢性肾病中,肾纤维化引起循环BMP-7减少,导致VSMCs表型重塑、增殖和中膜增厚,加之升高的磷酸盐水平的协同作用,最终造成血管钙化[13]。在尿毒症合并动脉粥样硬化低密度脂蛋白受体(low-density lipoprotein receptor,LDLR)基因敲除的小鼠模型中发现,BMP-7可减轻血管钙化,下调骨钙素过表达。同时检测到血管钙化病变与BMP拮抗剂Gremlin表达也有关[14]。另一项尿毒症合并LDLR基因敲除小鼠的研究证实,BMP-7不仅可减轻血管钙化,还可纠正与尿毒症相关的高磷血症,刺激原位骨骼磷酸盐沉积,通过直接作用于VSMCs,防止血管钙化[15]。
采用高磷诱导VSMCs钙化模型研究发现,BMP-7可降低高磷诱导的钙盐沉积和细胞钙离子浓度,下调垂体特异转录因子-1和Cbfα1在mRNA水平和蛋白水平的表达,抑制VSMCs向成骨细胞表型转化,从而抑制钙化发生[16]。Kang等[17]采用高水平的维生素D诱导的C57BL/6小鼠体内血管钙化模型证明,经重组人BMP-7预处理和治疗过的小鼠,血管钙化程度减轻,OPN和OCN表达下调,可能与抑制骨的重吸收有关。外源性BMP-7给药,可减轻腺嘌呤诱导的慢性尿毒症大鼠的血管钙化,改善骨疾病[18]。然而最近Gravesen等[19]的研究发现,在一步法5/6肾切除术加高磷酸盐饮食和阿法骨化醇联合诱导的尿毒症大鼠模型中,BMP-7治疗可降低纤维化和上皮间质转化的基因表达,但没有降低主动脉组织中的钙含量和钙化相关基因的表达,这可能与该大鼠体内更加复杂的病理环境有关。
在与衰老相关的血管钙化的研究中,对比提取自老年大鼠(oVSMC)和幼年大鼠VSMCs中(yVSMC)的miRNAs,发现oVSMC组miR-542-3p的表达比yVSMC组低四倍。miR-542-3p表达下调,可促进VSMCs成骨转化。yVSMCs中高表达的miR-542-3p下调BMP-7,抑制成骨分化。而过表达BMP-7,可逆转上述抑制作用。miR-542-3p通过靶向BMP-7,调节VMSCs的成骨分化[20]。BMP-7在衰老相关的血管钙化病理进程中,似乎存在更加精细复杂的调控机制。
目前,关于BMP-7在血管钙化中发挥保护作用的机制研究还不是很深入。在不同病理条件下,如糖尿病、肾脏相关疾病、动脉粥样硬化以及衰老情况下BMP-7如何调控血管钙化的发生发展,与体内哪些分子有关以及具体的上下游调控关系还需要针对性地利用细胞模型和动物模型进行探究。同时BMP-7与BMPs家族中其他成员之间的相互配合也是研究中不容忽视的重要方面。
3 BMP-7在血管钙化及其他疾病中的临床应用 3.1 BMP-7或可作为临床上血管钙化的检测指标之一多项临床研究表明,BMP-7为抑制血管钙化的分泌蛋白,可预防或减轻血管钙化[21-23]。洪慧等[21]发现维持性血液透析患者(maintenance hemodialysis,MHD)血清中的磷、钙磷乘积和全段甲状旁腺激素(intact parathyroid hormone,iPTH)以及腹主动脉的钙化率高于健康志愿者,而Irisin水平和BMP-7水平低于健康志愿者。进一步对比MHD患者中的钙化组和非钙化组,钙化组血清中磷、钙磷乘积和iPTH水平较高,而Irisin和BMP-7的水平较低。张琢等[22]也同样统计了临床上30例MHD患者的血清中BMP-7与腹主动脉钙化的相关性,也得到了相同的结论。洪慧等[21]研究也表明,MHD患者血清中OPN的升高,Klotho蛋白和BMP-7的降低促进血管钙化发生。王冬梅等[23]研究发现CKD5期患者颈动脉钙化发生率较健康对照组高,血清BMP-2高于健康对照组,BMP-7低于健康对照组,这提示BMP-7与颈动脉钙化呈负相关。
欧美流行病学调查数据显示,糖尿病人群中BMP-7表达水平与血管钙化趋势相反。BMP-7是体内除了胎球蛋白A、MGP等之外的血管钙化抑制因子。BMP-7缺失可导致循环磷酸盐浓度升高,最终促进血管钙化[24]。
3.2 BMP-7在多种疾病中具有潜在的临床应用价值临床上,BMP-7可用于帮助椎体融合,防止神经损伤。在骨移植失败的情况下,BMP-7也可用于治疗胫骨不愈合[5]。在成熟机体内,BMP-7能够使成骨潜能的细胞分化增殖促进类似自体骨的新骨生长,在骨缺损和脊柱融合术等治疗中发挥重要作用。2004年,FDA批准BMP-7作为脊柱融合手术中的基因工程产品。该产品适用于骨质疏松、糖尿病、吸烟等导致的不能提供自体骨髓移植的病人。
BMP-7作为内源性诱导纤维化的TGF-β信号级联的抑制剂,具有治疗慢性肾病的潜力。在各种肾脏疾病相关的动物模型中,包括急性肾缺血、阻塞性肾损伤、糖尿病肾病、新月体肾炎和CKD等都证明,BMP-7具有抗纤维化作用和肾脏保护作用[13]。BMP-7在促炎单核细胞或M1型巨噬细胞分化为抗炎M2型巨噬细胞中发挥关键作用。BMP-7在动脉粥样硬化中发挥抗炎作用。BMP-7可抑制心肌梗塞后的不良重塑,在心脏疾病中具有潜在治疗意义[8]。采用小鼠模型进行研究发现,注射BMP-7后对小鼠健康有益的棕色脂肪细胞增加,而正常的白色脂肪细胞水平不变,BMP-7也可影响食物摄入,提示BMP-7或许可用于肥胖的治疗[25]。
BMP-7在骨折修复、骨不连等相关骨病、血管钙化、肾脏疾病、心脏疾病及肥胖等中均展现出潜在的临床应用价值。
4 结论与展望BMP-7作为BMPs蛋白家族中与血管钙化呈负相关的分泌蛋白,有望成为防治血管钙化的潜在靶标。血管钙化和骨代谢关系密切,BMP-7在骨发育和血管钙化中都发挥重要作用。BMP-7刺激人骨髓成骨细胞和骨源性成骨细胞的分化过程,增加骨形成减少骨吸收。血管钙化受到VMSCs转分化形成的成骨样细胞的调控,其中VMSCs与成骨细胞均来自共同的祖细胞谱系,具有多向转分化的能力。BMP-7可抑制VMSCs增殖,在体外刺激VMSCs收缩表型标志物的表达[12]。BMP-7对于正常的骨矿化的促进作用,有助于降低异位钙化的压力。多项临床统计分析均表明BMP-7是血管钙化抑制因子。目前FDA已经批准BMP-7作为脊柱融合手术中的基因工程产品,可促进患者骨生长。这提示BMP-7有望成为潜在的靶标,用于研发预防与治疗血管钙化的药物。
但是,目前已发表的有关BMP-7与血管钙化的研究,临床血清学统计分析居多,尚缺少深入的机制研究。虽然多项研究表明,BMP-7对慢性肾脏病患者的血管钙化具有一定的预防作用,有望成为这类患者预防和治疗血管钙化的潜在新靶标,但是BMP-7影响血管钙化的分子机制尚不明晰。基于肾脏疾病的血管钙化的深入研究明晰BMP-7作用于血管钙化的分子机制,将极大促进靶向BMP-7的诊断试剂盒与新药研发,提升血管钙化的早期预防与治疗水平,改善患者预后。
| [1] |
周鑫, 邢露, 贺春霞, 等. 骨膜蛋白—一种有潜力的疾病早期诊断分子标志物[J]. 中国药理学通报, 2022, 38(5): 650-4. Zhou X, Xin L, He C X, et al. Periostin—a potential molecular marker for early diagnosis of disease[J]. Chin Pharmacol Bull, 2022, 38(5): 650-4. doi:10.12360/CPB202108095 |
| [2] |
Zhou X, Xu S N, Yuan S T, et al. Multiple functions of autophagy in vascular calcification[J]. Cell Biosci, 2021, 11(1): 159. doi:10.1186/s13578-021-00639-9 |
| [3] |
Lee S J, Lee I K, Jeon J H. Vascular calcification-new insights into its mechanism[J]. Int J Mol Sci, 2020, 21(8): 2685. doi:10.3390/ijms21082685 |
| [4] |
Salhotra A, Shah H N, Levi B, et al. Mechanisms of bone development and repair[J]. Nat Rev Mol Cell Biol, 2020, 21(11): 696-711. doi:10.1038/s41580-020-00279-w |
| [5] |
Bordukalo-Nikšić T, Kufner V, Vukičević S. The role of BMPs in the regulation of osteoclasts resorption and bone remodeling: from experimental models to clinical applications[J]. Front Immunol, 2022, 13: 869422. doi:10.3389/fimmu.2022.869422 |
| [6] |
Halloran D, Durbano H W, Nohe A. Bone morphogenetic protein-2 in development and bone homeostasis[J]. J Dev Biol, 2020, 8(3): 19. doi:10.3390/jdb8030019 |
| [7] |
Yang P, Troncone L, Augur Z M, et al. The role of bone morphogenetic protein signaling in vascular calcification[J]. Bone, 2020, 141: 115542. doi:10.1016/j.bone.2020.115542 |
| [8] |
Aluganti Narasimhulu C, Singla D K. The role of bone morphogenetic protein 7 (BMP-7) in inflammation in heart diseases[J]. Cells, 2020, 9(2): 280. doi:10.3390/cells9020280 |
| [9] |
Groppe J, Greenwald J, Wiater E, et al. Structural basis of BMP signalling inhibition by the cystine knot protein noggin[J]. Nature, 2002, 420(6916): 636-42. doi:10.1038/nature01245 |
| [10] |
Strippoli R, Moreno-Vicente R, Battistelli C, et al. Molecular mechanisms underlying peritoneal EMT and fibrosis[J]. Stem Cells Int, 2016, 2016: 3543678. |
| [11] |
Xu X, Zhou R, Duan Q, et al. Circulating macrophages as the mechanistic link between mosaic loss of Y-chromosome and cardiac disease[J]. Cell Biosci, 2023, 13(1): 135. doi:10.1186/s13578-023-01075-7 |
| [12] |
Dorai H, Vukicevic S, Sampath T K. Bone morphogenetic protein-7 (osteogenic protein-1) inhibits smooth muscle cell proliferation and stimulates the expression of markers that are characteristic of SMC phenotype in vitro[J]. J Cell Physiol, 2000, 184(1): 37-45. doi:10.1002/(SICI)1097-4652(200007)184:1<37::AID-JCP4>3.0.CO;2-M |
| [13] |
Li R X, Yiu W H, Tang S C. Role of bone morphogenetic protein-7 in renal fibrosis[J]. Front Physiol, 2015, 6: 114. |
| [14] |
Jara A, Chacón C, Burgos M E, et al. Expression of gremlin, a bone morphogenetic protein antagonist, is associated with vascular calcification in uraemia[J]. Nephrol Dial Transplant, 2009, 24(4): 1121-9. |
| [15] |
Davies M R, Lund R J, Mathew S, et al. Low turnover osteodystrophy and vascular calcification are amenable to skeletal anabolism in an animal model of chronic kidney disease and the metabolic syndrome[J]. J Am Soc Nephrol, 2005, 16(4): 917-28. doi:10.1681/ASN.2004100835 |
| [16] |
Kang Y H, Jin J S, Son S M. Long Term effect of high glucose and phosphate levels on the OPG/RANK/RANKL/TRAIL system in the progression of vascular calcification in rat aortic smooth muscle cells[J]. Korean J Physiol Pharmacol, 2015, 19(2): 111-8. doi:10.4196/kjpp.2015.19.2.111 |
| [17] |
Kang Y H, Jin J S, Yi D W, et al. Bone morphogenetic protein-7 inhibits vascular calcification induced by high vitamin D in mice[J]. Tohoku J Exp Med, 2010, 221(4): 299-307. doi:10.1620/tjem.221.299 |
| [18] |
Lee C T, Kuo W H, Tain Y L, et al. Exogenous BMP-7 administration attenuated vascular calcification and improved bone disorders in chronic uremic rats[J]. Biochem Biophys Res Commun, 2022, 621: 8-13. doi:10.1016/j.bbrc.2022.06.101 |
| [19] |
Gravesen E, Lerche Mace M, Nordholm A, et al. Exogenous BMP-7 in aortae of rats with chronic uremia ameliorates expression of profibrotic genes, but does not reverse established vascular calcification[J]. PLoS One, 2018, 13(1): e0190820. doi:10.1371/journal.pone.0190820 |
| [20] |
Liu H, Wang H, Yang S, et al. Downregulation of miR-542-3p promotes osteogenic transition of vascular smooth muscle cells in the aging rat by targeting BMP-7[J]. Hum Genomics, 2019, 13(1): 67. doi:10.1186/s40246-019-0245-z |
| [21] |
洪慧, 李军, 帅欢, 等. 血清Sclerostin、OPN、Klotho蛋白、BMP-7水平与维持性血液透析患者血管钙化的关系研究[J]. 现代生物医学进展, 2021, 21(5): 972-6. Hong H, Li J, Shuai H, et al. The relationship between serum levels of sclerostin, osteopontin, klotho and bone morphogenetic protein 7 and vascular calcification in maintenance hemodialysis patients[J]. Progress Modern Biomed, 2021, 21(5): 972-6. |
| [22] |
张琢, 吴雪莹, 徐天华, 等. 维持性血液透析30例血清骨形成蛋白7与腹主动脉钙化相关性研究[J]. 中国实用内科杂志, 2018, 38(12): 1165-8. Zhang Z, Wu X Y, Xu T H, et al. Correlation analysis of serum bone morphogenetic protein-7 with abdominali aorta calcification in maintenance hemodialysis[J]. Chin J Pract Intern Med, 2018, 38(12): 1165-8. |
| [23] |
王冬梅, 王科, 方媛, 等. 慢性肾脏病5期患者血清BMP-2及BMP-7与颈动脉钙化的相关性研究[J]. 安徽医科大学学报, 2016, 51(5): 762-4. Wang D M, Wang K, Fang Y, et al. Correlation between serum concentrations of BMP-2 and BMP-7 and calcification of carotid artery in patients with CKD5[J]. Acta Univer Med Anhui, 2016, 51(5): 762-4. |
| [24] |
Freedman B I, Bowden D W, Ziegler J T, et al. Bone morphogenetic protein 7 (BMP-7) gene polymorphisms are associated with inverse relationships between vascular calcification and BMD: the diabetes heart study[J]. J Bone Miner Res, 2009, 24(10): 1719-27. doi:10.1359/jbmr.090501 |
| [25] |
Saini S, Duraisamy A J, Bayen S, et al. Role of BMP7 in appetite regulation, adipogenesis, and energy expenditure[J]. Endocrine, 2015, 48(2): 405-9. doi:10.1007/s12020-014-0406-8 |