


2. 安徽医科大学实验动物中心,安徽 合肥 230032
 ,
WANG Xu-lei1,
CHU Zhu-ping1,
GUO Ting-ting1,
XU Nuo1,
WANG Kang1,
LI Ying1,
WEI Wei1,
YAN Shang-xue1,2
,
WANG Xu-lei1,
CHU Zhu-ping1,
GUO Ting-ting1,
XU Nuo1,
WANG Kang1,
LI Ying1,
WEI Wei1,
YAN Shang-xue1,2

2. Experimental Animal Center, Anhui Medical University, Hefei 230032, China
骨关节炎(osteoarthritis,OA)是一种慢性退行性疾病,随着年龄的增加,OA的患病率及严重程度逐渐升高,OA的特征表现为软骨和关节组织退化、剧烈疼痛和行动不便[1]等,是导致老年人疼痛和残疾的主要原因[2]。OA几乎可以累及任何关节,但通常影响最多的是手、膝盖、臀部和脚[3]。目前临床的主要治疗药物是抗炎药,只能缓解症状,但对关节软骨几乎无保护或修复作用,而且随着时间的推移,病情往往会恶化[4]。临床上缺少有效缓解软骨破坏的OA治疗药物。
OA是一种涉及所有关节腔室(软骨、软骨下骨和滑膜)的病理变化的疾病。虽然滑膜炎症和软骨下骨硬化是重要的贡献者,但病理性软骨细胞分化被认为是软骨退变的主要驱动因素。软骨损伤是OA病理过程的中心环节。随着OA的加重,大量软骨细胞丢失,细胞外基质(extracellular matrix,ECM)降解,Ⅱ型胶原(type Ⅱ collagen,ColⅡ)水平降低,基质金属蛋白酶(matrix metalloprotein,MMP)13等大量产生,进一步加剧了膝关节软骨退行性变。有研究表明,在OA软骨细胞中G蛋白偶联受体激酶2(G protein-coupled receptor kinase,GRK2)的水平和活性增强,抑制GRK2膜募集可恢复G蛋白偶联受体(G protein-coupled receptor,GPCR)信号传导平衡防止病理性软骨细胞肥大[5-6]。应用GRK2抑制剂帕罗西汀(Paroxetine,PX)可以防止小鼠OA软骨细胞肥大,减轻OA进展,并促进软骨再生[7-8]。芍药苷-6-氧-苯磺酸酯(CP-25)是一种GRK2抑制剂,可以调节GRK2活性恢复EP4信号转导发挥作用[9]。课题组前期研究表明,CP-25通过选择性抑制GRK2活性来抑制类风湿性关节炎滑膜细胞和巨噬细胞等功能,改善类风湿关节炎关节损伤,具有抗炎以及保护关节损伤的作用[9]。CP-25具有环己烷并二氧杂环结构,其与GRK2结合能力高于PX[10]。在OA发病过程中,滑膜炎和软骨损伤是常见的病理过程,因此,CP-25是否可以通过靶向抑制软骨细胞GRK2活性从而发挥对OA的治疗作用值得深入探索。
1 材料 1.1 实验动物10周龄C57BL/6J小鼠(雄性,25~30 g),购自于斯贝福(北京)生物科技有限公司,合格证号:SCXK(京)2021-0100。小鼠饲养于安徽医科大学临床药理研究所SPF级动物房,室温(21~23) ℃,12 h/12 h光暗交替,自由获取水和食物。SPF级C57BL/6J小鼠,(雄性,7~10 d),安徽省实验动物中心提供,合格证号:SCXK(皖)2021-001,用于提取原代膝关节软骨细胞。本实验已通过安徽医科大学临床药理研究所动物实验伦理审查委员会批准(编号:PZ-2022-036)。
1.2 药物与试剂CP-25由安徽医科大学临床药理研究所合成;盐酸帕罗西汀(货号:HYP-78246)购自美国MCE公司;Anti-Collagen Ⅱ抗体(货号:ab34712)、Anti-GRK2抗体(货号:ab228705),购自美国Abcam公司;Anti-Aggrecan软骨蛋白聚糖抗体(货号:13880-1-AP)购自武汉三鹰公司;Anti -MMP-13抗体(OTI2D8)(货号:NBP2-45887)购自美国Novus公司;β-actin抗体(货号:T0022)购自美国Affinity公司;Ⅱ型胶原酶(来源于溶组织梭菌)(货号:C6885)购自美国Sigma公司;细胞膜蛋白与包浆蛋白抽提试剂盒(产品编号: P0033)、RIPA裂解液(强)(产品编号: P0013B)、PMSF蛋白酶抑制剂(产品编号: ST2573-100g)购自上海碧云天生物技术有限公司;HyClone DMEM/F12 1 ∶ 1 ∶液体培养基(货号: SH30023.FS)购自美国思拓凡生物科技公司;Opti-MEM减血清培养基(货号:31985070)、lipofectamine 3000转染试剂(货号: L3000015)购自赛默飞世尔科技公司。
1.3 主要仪器激光共聚焦成像显微镜(型号:Leica TCS SP8;德国Leica公司);组织原位细胞扫描分析系统(型号:Pannoramic MIDI;匈牙利3DHISTECH公司);小动物Micro-CT成像系统(型号:IMAGING 100;合肥锐视医疗科技有限公司);Tanon超灵敏化学发光成像仪(型号:Tanon 4600;上海天能生命科学有限公司)。
2 方法 2.1 小鼠DMM手术模型建立取36只C57BL/6J小鼠用舒泰50(50 mg·kg-1)麻醉后,取仰卧位,以膝关节为中心备皮及局部消毒。沿髌骨内侧作纵向切口。用微型燕尾剪打开关节囊。然后对髁间区域的脂肪垫进行钝性剥离,暴露出内侧半月板胫副韧带(medial meniscus collateral tibial ligament,MMTL),离断MMTL后使内侧半月板(medial meniscus,MM)不稳定。缝合关节内侧肌肉和皮肤。另取12只C57BL/6J小鼠作为假手术组,手术中仅暴露关节腔后即缝合,缝合处局部以碘伏消毒防止感染。
2.2 分组及给药造模后,将模型小鼠随机分为模型组、CP-25(70 mg·kg-1)给药组和PX(15 mg·kg-1)给药组,假手术组和模型组给予等量药物溶媒。手术后开始灌胃给药,持续12周后处死动物。
2.3 小鼠膝关节Micro-CT成像手术12周后,使用安乐死装置处死小鼠,取手术侧膝关节,剔除周围肌肉组织,拍摄膝关节CT影像并使用CT vox软件3D重建膝关节图片。采用国际骨关节炎研究学会(the International Society for Osteoarthritis Research, OARSI)评分系统[11]评估膝关节软骨的破坏及CP-25用药后对膝关节的影响。
2.4 病理学检查软骨组织经4%多聚甲醛室温固定48 h,脱钙2周后,石蜡纵向包埋、切片后分别进行番红O-固绿染色和Masson染色,镜下观察组织病理学变化。
2.5 免疫组织化学检测Aggrecan、ADAMTS5在膝关节组织中的表达水平切片经烘烤、二甲苯、梯度乙醇脱蜡至水后,用Triton X-100通透、EDTA修复液冷修复抗原、3%过氧化氢内源性阻断和5%山羊血清封闭后,一抗4 ℃孵育过夜,次日,将切片复温30 min后加二抗室温孵育30 min,DAB染色和苏木精复染后梯度乙醇脱水,中性树胶封片,玻片扫描仪扫描观察结果。
2.6 免疫荧光检查膝关节组织中GRK2、Aggrecan、Col Ⅱ的表达水平切片脱蜡水化后,分别Triton X-100通透、EDTA修复液冷修复抗原、3%过氧化氢内源性阻断、5%山羊血清封闭,一抗4 ℃过夜孵育。次日复温30 min后滴加荧光二抗室温避光孵育2 h,DAPI孵育10 min,PBS清洗后组织上滴加抗荧光淬灭剂盖上盖玻片,指甲油固定,激光共聚焦成像显微镜下观察软骨组织中GRK2、Aggrecan、Col Ⅱ的表达。
2.7 C57BL/6J原代小鼠膝关节软骨细胞的分离培养取6只7~10天C57/BL6J小鼠,CO2安乐死箱处死动物,在超净台中用微型燕尾剪收集后肢膝关节软骨置于1%双抗的PBS培养皿中,剪成1 mm3大小的碎片,用含双抗的PBS洗3次,移至50 mL离心管中,离心(1 200 r·min-1;5 min)用巴氏吸管吸取上清,加1 mL质量浓度为2 g·L-1的Ⅱ型胶原蛋白酶,消化6 h,用40 μm无菌过滤器滤除未消化的组织后离心滤液离心1 200 r·min-1,5 min,弃去上清,加F12/DMEM完全培基重悬细胞并分瓶放入培养箱37 ℃、5% CO2培养。24 h后首次换液。为保持软骨细胞的正常形态(卵圆形或多边形)实验仅使用原代或第一代软骨细胞。提取的小鼠原代细胞经甲苯胺蓝染色和Col Ⅱ免疫荧光染色鉴定证实为软骨细胞。
2.8 细胞免疫荧光检测软骨细胞中GRK2、Col Ⅱ、MMP13的表达水平细胞接种于12孔板的细胞爬片,待细胞贴壁后,对细胞加入刺激剂和药物处理,加入PGE2(8 μmol·L-1)刺激4 h后,给药组分别加入CP-25(终浓度10 μmol·L-1)和PX(终浓度10 μmol·L-1),培养24 h后取出12孔板,4%多聚甲醛固定30 min,Triton X-100通透,5%山羊血清封闭30 min,滴加一抗4 ℃孵, 育过夜。次日复温30 min后滴加荧光二抗室温避光孵育2 h,DAPI孵育10 min,PBS清洗后倒置于滴加抗荧光淬灭剂的载玻片上,指甲油固定盖玻片四周,激光共聚焦成像显微镜下观察软骨细胞中GRK2、Col Ⅱ、MMP13的表达。
2.9 Western blot检测CP-25对软骨细胞中GRK2膜蛋白及总蛋白的作用将软骨细胞接种于6孔板,分为对照组、PGE2刺激组、CP-25给药组、PX给药组、siGRK2组和Negative control(NC)组。将PGE2(8 μmol·L-1)刺激软骨细胞24 h,刺激的同时分别加入CP-25(终浓度10 μmol·L-1)和PX(终浓度10 μmol·L-1),siGRK2组转染24 h后再加入PGE2(8 μmol·L-1)刺激24 h。收集软骨细胞总蛋白和膜蛋白(提取步骤参考碧云天膜蛋白抽提试剂盒说明书),将提取的蛋白BCA定量,将上述总蛋白或膜蛋白样品加入电泳槽,电泳将蛋白分离开,随后用200 mA的电流将蛋白转移到PVDF膜上,将转好的膜放入无蛋白快速封闭液封闭15 min,接着用TBST将膜摇床上摇洗3次,用TBS洗1次,将膜敷上一抗,4 ℃孵育16 h左右后洗膜,随后将其放进HRP标记的二抗中孵育2 h,用化学发光成像仪显影,使用ImageJ分析蛋白条带。
2.10 统计学处理计量资料以x±s表示,使用GraphPad Prism 8.0.2软件进行统计分析,两组间比较采用独立样本t检验,多组间均数比较采用ANOVA单因素方差分析。
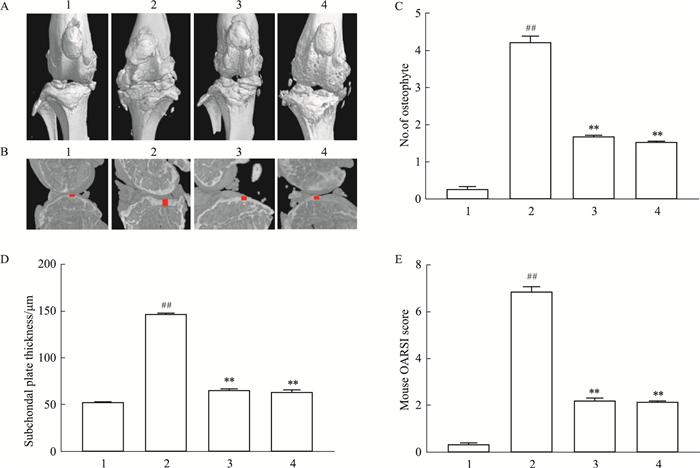
3 结果 3.1 CP-25给药对OA小鼠膝关节组织结构的影响显微计算机断层扫描(Micro-CT)系统扫描膝关节的3D重建图像。结果显示,OA组小鼠软骨退变严重,骨赘形成明显,关节腔间隙变窄,软骨下板厚度增加,OARSI评分升高。CP-25和PX用药可显著减少小鼠膝骨关节骨赘数量,改善软骨表面侵蚀,恢复膝关节间隙,降低软骨下板厚度,结果有统计学差异,见Fig 1(A,B)。
|
| Fig 1 Effect of CP-25 on knee tissue structure in OA mice (x±s, n=5) 1:Sham; 2:DMM+Solvent; 3:DMM+CP-25; 4:DMM+PX. A: 3D reconstructed images of knee joints highlighting changes to the femoral and tibial surfaces as well as the medial and lateral menisci. Quantified changes in; B: Sagittal view of the medial joint compartment visualizing subchondral bone changes; a red line marks subchondral plate thickness. Quantified changes in; C: Number of knee osteophytes; D: subchondral bone plate thickness; E: Knee OARSI score; ##P < 0.01 vs Sham group; **P < 0.01 vs Model group. |
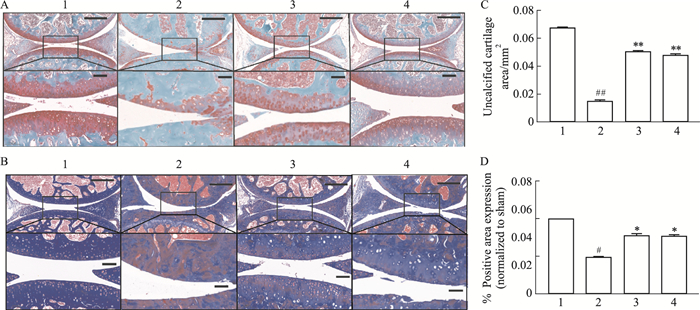
对小鼠膝关节组织切片进行病理学检查,观察各组小鼠膝关节组织的病理改变。番红固绿染色结果显示,模型组小鼠几乎无番红O阳性染色,软骨组织退变严重,CP-25给药组和PX给药组番红O呈强阳性染色,软骨组织厚度较模型组增加。表明CP-25给药组和PX给药组小鼠膝关节组织中含有更多的蛋白多糖沉积(Fig 2A),和假手术组相比,模型小鼠膝关节未钙化软骨细胞面积明显降低。和模型组相比,CP-25给药和PX给药小鼠膝关节未钙化软骨细胞面积明显升高(Fig 2C)。Masson染色结果显示,模型组小鼠膝关节组织中Masson蓝色阳染面积占比明显低于假手术组,与模型小鼠相比CP-25给药和PX给药小鼠膝关节组织中蓝染更明显,胶原纤维含量更丰富,结果具有统计学差异(Fig 2B、2D)。
|
| Fig 2 Effect of CP-25 on histopathology of knee joints in OA mice (n=4) 1:Sham+Solvent; 2:DMM+Solvent; 3:DMM+CP-25; 4:DMM+PX. A: Safranin-O/Fast Green staining; scale bar, 50 μm; B: Masson staining; scale bar, 50 μm; C: Uncalcified cartilage area statistics; D: Positive area expression rate statistics; #P < 0.05, ##P < 0.01 vs Sham group; *P < 0.05, **P < 0.01 vs Model group. |
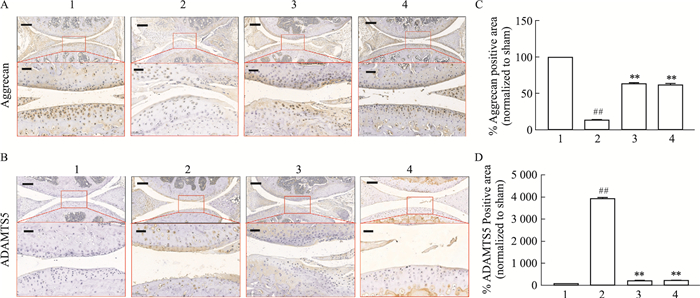
与假手术组相比,模型组膝关节组织中Aggrecan蛋白表达水平降低,ADAMTS5蛋白表达水平升高,CP-25治疗组小鼠膝关节组织中Aggrecan蛋白表达水平升高,ADAMTS5蛋白表达水平降低,且Aggrecan和ADAMTS5阳性面积占比差异具有统计学意义(Fig 3A-D)。
|
| Fig 3 Effect of CP-25 on expression of Aggrecan and ADAMTS 5 in knee joints of OA mice (x±s, n=3) 1:Sham; 2:DMM+Solvent; 3:DMM+CP-25; 4:DMM+PX. A: Aggrecan expression in knee joints; scale bar, 100 μm; inside red frame scale bar, 50 μm; B: ADAMTS5 expression in knee joints; scale bar, 100 μm; inside red frame scale bar, 50 μm; C: Statistical chart of Aggrecan positive area percentage; D: Statistical chart of ADAMTS5 positive area percentage; ##P < 0.01 vs Sham group; **P < 0.01 vs Model group. |
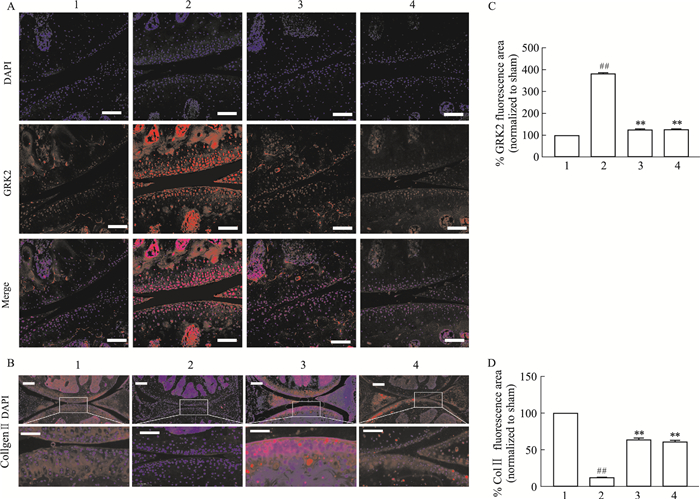
检测膝关节组织GRK2和Col Ⅱ表达水平,Fig 4A-B结果显示,模型小鼠膝关节组织中GRK2蛋白表达水平明显升高,Col Ⅱ蛋白表达水平明显降低,CP-25和PX给药可降低小鼠膝关节组织中GRK2蛋白表达,升高Col Ⅱ蛋白表达水平,差异具有统计学意义。
|
| Fig 4 Effect of CP-25 on expression of GRK2 and Col II in knee joints of OA mice (x±s, n=4) 1:Sham; 2:DMM+Solvent; 3:DMM+CP-25; 4:DMM+PX. A: GRK2 immunofluorescence staining; scale bar, 100 μm; B: Col Ⅱ immunofluorescence staining; scale bar, 100 μm, inside white frame scale bar, 50 μm; C: GRK2 fluorescence area (%) statistics; D: Col Ⅱ fluorescence area (%) statistics; ##P < 0.01 vs Sham group; **P < 0.01 vs Model group. |
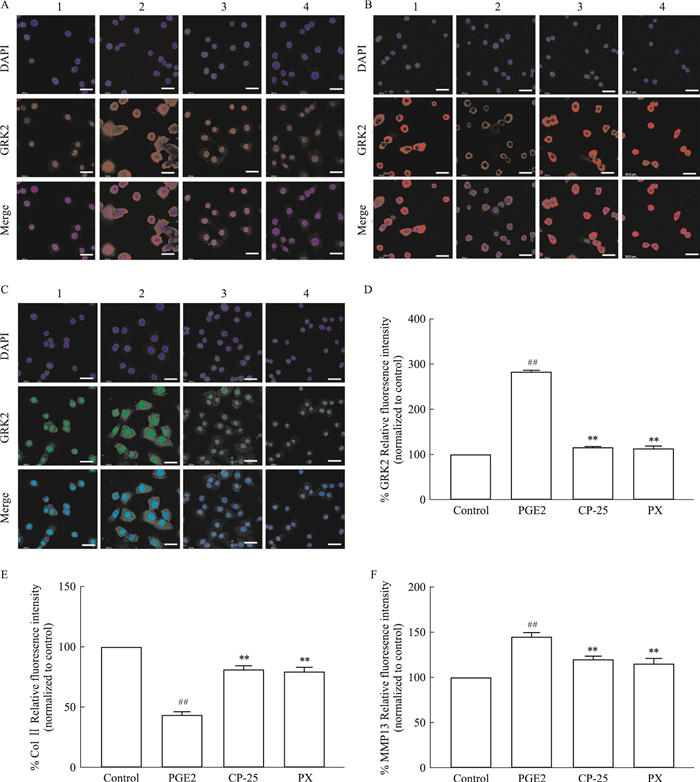
Ⅱ、MMP13表达的影响对小鼠软骨细胞给予PGE2(8 μmol·L-1)刺激,分别加入CP-25(10 μmol·L-1)和PX(10 μmol·L-1)治疗24 h,PGE2与对照组相比,PGE2刺激组可诱导软骨细胞GRK2和MMP13表达显著升高,Col Ⅱ相对荧光强度显著降低,CP-25与PX给药可显著降低软骨细胞中GRK2、MMP13相对荧光强度,增强Col Ⅱ相对荧光强度。
|
| Fig 5 The protein expression detected by cell immunofluorescence (x±s, n=5) 1:Control; 2:PGE2(8 μmol·L-1); 3:CP-25(10 μmol·L-1); 4:PX(10 μmol·L-1). A: Chondrocyte GRK2 fluorescence staining; B: Chondrocyte Col II fluorescence staining; C: Chondrocyte MMP13 fluorescence staining; scale bar, 30 μm; D: GRK2 relative fluorescence intensity (%) statistics; E: Statistical diagram of Collagen II relative fluorescence intensity (%); F: Statistical diagram of MMP13 relative fluorescence intensity (%); ##P < 0.01 vs Control group; **P < 0.01 vs PGE2 group. |
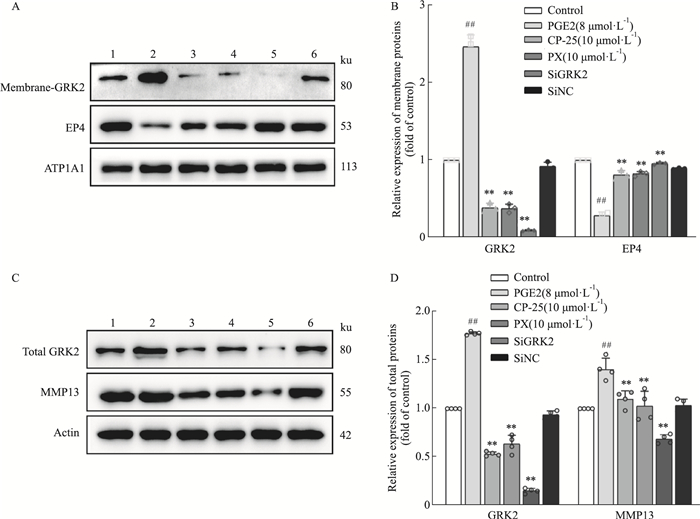
检测PGE2刺激对软骨细胞中GRK2和EP4蛋白水平,结果表明,PGE2可诱导软骨细胞GRK2的总蛋白和膜蛋白水平显著升高,EP4的表达水平显著降低,MMP13水平升高;CP-25可降低软骨细胞的GRK2总蛋白和细胞膜蛋白表达水平,升高EP4的膜表达水平,降低MMP13的表达水平,与干扰GRK2作用相似(Fig 6)。
|
| Fig 6 Effect of CP-25 administration on chondrocyte protein expression (n=3 or 4) 1:Control; 2:PGE2(8 μmol·L-1); 3:CP-25(10 μmol·L-1); 4:PX(10 μmol·L-1); 5:SiGRK2; 6:SiNC. A: Chondrocyte membrane protein expression level; B: Chondrocyte membrane protein expression level statistics; C: Chondrocyte total protein expression level; D: Chondrocyte total protein expression level statistics; ##P < 0.01 vs Control group; **P < 0.01 vs PGE2 group. |
OA是一种难治性疾病,临床缺乏治疗药物,迫切需要发现新的药物。CP-25作为一种新的GRK2抑制剂,在治疗类风湿关节炎动物模型中显示了良好的软骨损伤修复作用[12]。同时文献研究显示,PX作为GRK2抑制剂对OA小鼠也呈现了良好的治疗作用。本研究显示,CP-25给药能显著降低OARSI评分,明显减少OA模型小鼠膝关节骨赘形成数量,降低骨板厚度,增加关节软骨细胞层厚度和软骨基质中Ⅱ型胶原含量,对小鼠OA具有明显的治疗作用。PX治疗效果与CP-25相似。由于PX是5-羟色胺再摄取抑制剂,是临床常用的抗抑郁药,具有神经精神系统方面的副作用,患者在使用PX期间可能会出现头晕、头痛、乏力以及兴奋的神经精神系统改变[13]。OA是慢性疾病,治疗时间长,CP-25是由天然药物成分Pae乙酰化修饰制备而成,副作用少,具有较强的临床应用前景。
本研究表明,在DMM手术后GRK2表达的进行性增加,这表明GRK2的表达增加导致EP4受体脱敏,进而阻碍软骨基质再生。GRK2诱导EP4受体脱敏作为OA中软骨细胞肥大和软骨变性的病理驱动因素。番红固绿染色显示CP-25治疗的软骨(红色)厚度明显增加,Masson染色中胶原纤维(蓝色)染色更深,而模型组有大量肌纤维染色(红色)。当OA发生时,关节软骨从健康状态转变为分解代谢状态,软骨细胞大量丢失,正常的软骨细胞表型发生转变,分泌大量的MMPs、具有血小板反应蛋白基序的去整合素和金属蛋白酶(a disintegrin and metalloproteinase with thrombospondin motifs,ADAMTs)以及炎性因子等,软骨细胞内分解代谢大于合成代谢,软骨细胞失去了维持软骨完整性的能力。免疫组化和免疫荧光结果表明,CP-25治疗可以显著降低GRK2、ADAMTS5以及MMP13的表达,显著升高软骨细胞外基质蛋白(ColⅡ、Aggrecan)的表达。细胞免疫荧光结果进一步表明,CP-25可以降低GRK2、软骨分解蛋白(MMP13)的产生,升高ColⅡ的表达水平。本研究表明GRK2是OA进展的主要驱动因素,并且GRK2抑制是OA的治疗方法。我们还证明了CP-25可以防止OA小鼠软骨退化,促进基质再生。
关节软骨是抵抗OA发生的第一道防线[14]。软骨破坏一直被认为是诱发骨关节炎的重要因素。关节软骨由软骨细胞及细胞外基质组成。有大量证据表明,软骨基质的合成代谢和分解代谢的不平衡,特别是细胞外基质的分解代谢增强是导致OA软骨基质丢失的重要原因。关节机械损伤会引起基质金属蛋白酶(尤其是MMP 13)的激活[15],肥大的软骨细胞通过分泌大量蛋白水解酶(如MMP 13),导致关节软骨损伤和钙化,在OA的发生和进展中发挥核心作用[16]。本研究发现,OA小鼠软骨组织和PGE2诱导的软骨细胞中MMP13、ADAMT5水平明显升高,细胞外基质蛋白ColⅡ和Aggrecan水平明显降低,提示OA过程中软骨细胞基质分解代谢增强,软骨基质大量丢失。CP-25给药可降低MMP13、ADAMT5水平,升高ColⅡ和Aggrecan水平,对软骨基质发挥保护作用。
有研究表明,前列腺素PGE2是介导OA炎症和疼痛的重要介质。PGE2通过前列腺素受体EP4激活GPCR信号通路在OA软骨细胞损伤中发挥了重要作用。PGE2刺激后,GRK2与GPCR上的Gβγ亚基结合,介导GRK2向膜募集,招募β-arrestins,导致GPCR磷酸化和脱敏,蛋白激酶A(PKA)活性降低。PKA是抑制软骨细胞肥大的转录因子合成代谢信号,并抑制软骨细胞中MMP13和ADMATS5的表达[16]。本研究中,PGE2体外可刺激软骨细胞GRK2总蛋白和膜表达水平升高,降低EP4表达,诱导EP4受体脱敏,导致软骨细胞中MMP13和ADMATS5表达升高,ColⅡ和Aggrecan水平降低,促进了软骨细胞基质降解。而CP-25作为GRK2抑制剂,可降低GRK2的总表达和膜表达水平,促进EP4受体复敏,恢复GPCR信号通路,降低PGE2诱导的MMP13和ADMATS5水平,升高ColⅡ和Aggrecan水平,发挥了软骨基质保护作用。本研究验证了CP-25对OA的治疗效果。
综上,CP-25通过抑制GRK2的表达与活性,可以促进软骨基质再生,减少软骨基质降解,对OA小鼠膝关节软骨具有显著的保护作用。CP-25有望成为治疗骨关节炎的潜在药物。
| [1] |
D'Amico D, Olmer M, Fouassier A M, et al. Urolithin A improves mitochondrial health, reduces cartilage degeneration, and alleviates pain in osteoarthritis[J]. Aging Cell, 2022, 21(8): 13662. doi:10.1111/acel.13662 |
| [2] |
O'Neill T W, McCabe P S, McBeth J. Update on the epidemiology, risk factors and disease outcomes of osteoarthritis[J]. Best Pract Res Clin Rheumatol, 2018, 32(2): 312-26. doi:10.1016/j.berh.2018.10.007 |
| [3] |
Katz J N, Arant K R, Loeser R F. Diagnosis and treatment of hip and knee osteoarthritis: a review[J]. JAMA, 2021, 325(6): 568-78. doi:10.1001/jama.2020.22171 |
| [4] |
Bao J P, Chen Z G, Xu L H. Rapamycin protects chondrocytes against IL-18-induced apoptosis and ameliorates rat osteoarthritis[J]. Aging (Albany NY), 2020, 12(6): 5152-67. |
| [5] |
Kamal F A, Mickelsen D M, Wegman K M, et al. Simultaneous adrenal and cardiac g-protein-coupled receptor-Gβγ inhibition halts heart failure progression[J]. J Am Coll Cardiol, 2014, 63(23): 2549-57. doi:10.1016/j.jacc.2014.02.587 |
| [6] |
Kamal F A, Travers J G, Schafer A E, et al. G protein-coupled receptor-G-protein βγ-subunit signaling mediates renal dysfunction and fibrosis in heart failure[J]. J Am Soc Nephrol, 2017, 28(1): 197-208. doi:10.1681/ASN.2015080852 |
| [7] |
Bouley R A, Weinberg Z Y, Waldschmidt H V, et al. A new paroxetine-based GRK2 inhibitor reduces internalization of the μ-opioid receptor[J]. Mol Pharmacol, 2020, 97(6): 392-401. doi:10.1124/mol.119.118661 |
| [8] |
Carlson E L, Karuppagounder V, Pinamont W J, et al. Paroxetine-mediated GRK2 inhibition is a disease-modifying treatment for osteoarthritis[J]. Sci Transl Med, 2021, 13(580): eaau8491. doi:10.1126/scitranslmed.aau8491 |
| [9] |
Yang X Z, Wei W. CP-25, a compound derived from paeoniflorin: Research advance on its pharmacological actions and mechanisms in the treatment of inflammation and immune diseases[J]. Acta Pharmacol Sin, 2020, 41(11): 1387-94. doi:10.1038/s41401-020-00510-6 |
| [10] |
Han C C, Li Y, Zhang Y, et al. Targeted inhibition of GRK2 kinase domain by CP-25 to reverse fibroblast-like synoviocytes dysfunction and improve collagen-induced arthritis in rats[J]. Acta Pharm Sin B, 2021, 11(7): 1835-52. doi:10.1016/j.apsb.2021.01.015 |
| [11] |
Pritzker K P H, Gay S, Jimenez S A, Ostergaard K, et al. Osteoarthritis cartilage histopathology: grading and staging[J]. Osteoarthritis Cartilage, 2006, 14(1): 13-29. doi:10.1016/j.joca.2005.07.014 |
| [12] |
Tu J J, Guo Y, Hong W, et al. The regulatory effects of paeoniflorin and its derivative paeoniflorin-6'-O- Benzene Sulfonate CP-25 on inflammation and immune diseases[J]. Front Pharmacol, 2019, 5(10): 57. |
| [13] |
Wei D, Chen Y, Wu C, et al. Effect and safety of paroxetine for vasomotor symptoms: Systematic review and meta-analysis[J]. BJOG, 2016, 123(11): 1735-43. doi:10.1111/1471-0528.13951 |
| [14] |
Wei Y, Luo L, Gui T, et al. Targeting cartilage EGFR pathway for osteoarthritis treatment[J]. Sci Transl Med, 2021, 13(576): eabb3946. doi:10.1126/scitranslmed.abb3946 |
| [15] |
滕辉, 陈斯佳, 王婷玉. MicroRNA-204/-211敲除加重DMM小鼠骨关节炎滑膜增生和滑膜炎症[J]. 中国药理学通报, 2023, 39(5): 926-31. Teng H, Chen S J, Wang T Y. MicroRNA-204/-211 knockdown aggravated synovial hyperplasia and synovial inflammation in osteoarthritis of DMM mice[J]. Chin Pharmacol Bull, 2023, 39(5): 926-31. doi:10.12360/CPB202212025 |
| [16] |
van der Kraan P M, van den Berg W B. Chondrocyte hypertrophy and osteoarthritis: role in initiation and progression of cartilage degeneration[J]. Osteoarthritis Cartilage, 2012, 20(3): 223-32. doi:10.1016/j.joca.2011.12.003 |