

2. 甘肃中医药大学药学院, 甘肃 兰州 730000
2. College of Pharmacy, Gansu University of Chinese Medicine, Lanzhou 730000, China
本文以视交叉上核(suprachiasmatic nucleus,SCN)及催眠原为核心,阐述其自身的调节机制以及其与各种睡眠觉醒调节机制的解剖联系,归纳其潜在的调节机制。借睡眠环境、睡眠习惯对SCN及催眠原的影响,理解失眠的认知行为在睡眠觉醒调节中的重要意义。
1 睡眠昼夜节律系统 1.1 SCN—睡眠昼夜节律系统的调控核心SCN位于下丘脑,是睡眠昼夜节律系统的调控核心,将昼夜生理和行为节律(包括睡眠和清醒、温度、进食、神经内分泌和自主神经效应)与每天24 h周期性同步,以匹配环境光暗循环,从而协调优化内部时间节律[1]。
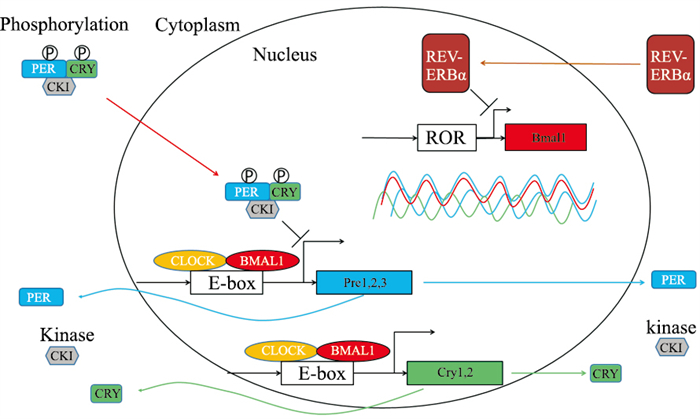
SCN节律的分子遗传机制是Fig 1所示的转录-翻译负反馈回路,其中最关键的转录因子和基因包括脑和肌肉芳基烃受体核转运体样1 (brain and muscle aryl hydrocarbon receptor nuclear translocator-like 1,BMAL1)、昼夜运动输出周期Kaput(circadian locomotor output cycle Kaput,CLOCK)、周期1-3(period1-3,Per1-3)和隐花色素1-2(cryptochrome 1-2,Cry1-2)。CLOCK和BMAL1通过与启动子区域中的E-box元件结合,异二聚化并促进Per1-3和Cry1-2的转录,在细胞质被翻译为蛋白质产物并蓄积,而累积的蛋白质产物可以进入细胞核负反馈抑制Pre1-3、Cry1-2的转录,以维持自身的生物节律[2]。
|
| Fig 1 Molecular mechanism of circadian clock system |
白天光信号经光暗通路传入,Per和Cry被激活,转录产物在细胞质中积累,磷酸化并与酪蛋白激酶I(casein kinase I,CKI)形成三聚体复合物,其可转移到细胞核中,通过与CLOCK和BMAL1结合来介导反馈抑制。夜间蛋白复合物直接抑制这些基因的激活,从而在整个夜晚关闭转录,直到早晨到来时蛋白质降解[3]。此外,有报道REV-ERBα和维甲酸相关孤儿受体(retinoid-related orphan receptors,ROR)家族,主要调节BMAL1转录和调节CLOCK表达,参与SCN自身节律的调控[4]。
研究发现,多巴胺受体(dopamine receptors,DR)激动剂可以治疗SCN中Per2表达周期延长的昼夜节律紊乱。而且运动、饮食等能通过增强多巴胺的释放活动影响生物的昼夜节律行为[5]。说明多巴胺可能通过SCN中的DR,抑制Per2的表达影响自身节律。
总之,光暗信号、饮食、运动等外界环境因素,通过光暗通路、SCN内的DR影响SCN内在的生物钟。而SCN依据自身节律,通过多种途径调节睡眠与觉醒。
1.2 SCN调控睡眠昼夜节律的解剖基础SCN由下丘脑两个成对小核组成,每个核包含约10 000个神经元,接受来自外部刺激的昼夜节律信号,尤其是光,但也受到其他外部因素的影响,如运动和进餐时间等,是控制昼夜平衡的关键部位[6]。核心或腹侧SCN负责感觉过程,从而可以检测光暗信号,而外壳或背侧SCN则负责将信息传出[7]。
SCN的信号输入通路:光暗检测通路是光暗信息传递到SCN的途径,由特化的固有光敏视网膜神经节细胞(intrinsically photosensitive retinal ganglion cells,ipRGCs)介导,ipRGC是一种特殊的视网膜细胞,含有光色素黑视蛋白,它是转导光暗信号,刺激昼夜节律系统的关键[8]。不同于视杆细胞和视锥细胞,该细胞接受外界光刺激时发生去极化,刺激视网膜下丘脑束(retinal hypothalamic tract,RHT)启动动作电位,传递信号给SCN[6]。DR是G蛋白偶联受体,存在于整个SCN和周围神经系统中。研究发现SCN内的DR通过接受大脑中增多的多巴胺,抑制SCN的神经元活动,进而影响下游的食欲素等系统[5],是SCN感知外界信息的另一种途径。
自SCN始、参与睡眠觉醒调节的中继核团:下丘脑室下区(subparaventricular zone,SPZ)、背内侧下丘脑核(dorsal medial hypothalamus,DMH)是SCN联系VLPO的两个重要的中继核。SPZ是SCN神经投射的主要传出目标,背侧SPZ传递来自SCN控制体温节律的信号,腹侧SPZ对睡眠和运动活动的节律至关重要,其输出本质上与SCN的输出平行并增强SCN的输出信号。DMH同样位于下丘脑,与自主神经应激反应、进食和皮质类固醇的昼夜释放有关,在驱动各种行为昼夜节律(包括睡眠-觉醒节律)方面发挥着作用[9]。下丘脑室旁核(paraventricular nucleus,PVN)是大脑中最重要的自主控制中心之一,在许多稳态反应中发挥作用,其神经元与下丘脑、脑干、边缘区域和前额叶皮层中的多种神经元广泛连接,具有自主作用,包括协调心血管、体温调节、代谢、昼夜节律[10]。
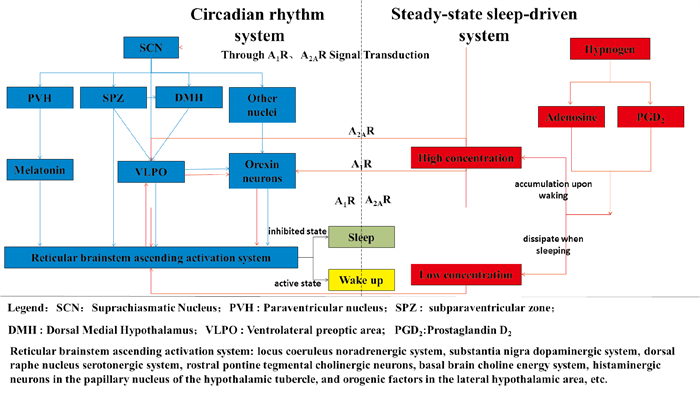
SCN传出、调控睡眠觉醒的解剖通路:一方面,SCN以较稀疏的神经纤维直接投射或经中继至视前区腹外侧部(ventrolateral preoptic area,VLPO)[11],与脑干网状上行激活系统联系,调控睡眠与觉醒[12]。其既可凭较密集的神经纤维,经DMH中继,投射至VLPO;亦可以经SPZ直接投射到VLPO;而且SCN也从SPZ经DMH,再至VLPO[13]。VLPO主要通过调控γ-氨基丁酸的释放来调控失眠与觉醒状态[14]。另一方面,SCN直接支配PVN。从PVN开始,该通路向下传递神经轴,到胸脊髓的中间外侧细胞柱,再到颈上神经节,其节后纤维释放神经递质去甲肾上腺素,作用于松果体β1受体,激活褪黑素合成酶系,使褪黑素的合成和分泌增加,而网状脑干又分布有褪黑素受体,因此,SCN通过褪黑素作用于脑干网状上行系统,影响着睡眠觉醒状态的调节[15]。而且,SCN通过其他核团中继后投射到下丘脑外侧部食欲素神经元,通过其广泛分布于中枢神经系统的受体[16],或食欲素神经元通过投射至VLPO[17],参与觉醒与睡眠状态的调控。此外,SCN通过SPZ中继,可以凭稀疏的神经纤维,直接投射至中缝背核、蓝斑、前蓝斑区、外侧臂旁核等脑干网状上行激活系统联系[13],见Fig 2。
|
| Fig 2 Physiological sleep-wake regulation diagram According to its own rhythm, SCN regulates sleep and wakefulness through four pathways of melatonin, SPZ, VLPO and Orexin neurons. Similarly, various reasons lead to increased adenosine concentration, which can directly act on SCN to regulate sleep and wakefulness through A1R/A2AR signal transduction; it can also directly act on BG and TMN A1R in the brainstem reticular ascending activation system to affect sleep, or act on A1R in orexin neurons, which affects sleep; similarly, adenosine can directly act on A2AR in VLPO to promote sleep, and it can also activate A2AR in nucleus accumbens and olfactory tubercle in the brainstem reticular ascending system, and indirectly act on VLPO to promote sleep. In addition, low concentrations of adenosine can enhance the wakefulness of neurons and promote wakefulness. |
基于其复杂的解剖联系,SCN依据自身节律,通过多种途径参与睡眠觉醒的调控。首先,SCN经SPZ作用脑干网状上行激活系统调节睡眠与觉醒[13]。其次,SCN通过VLPO途径作用于脑干网状上行激活系统调节睡眠觉醒[18],其主要机制为通过VLPO对促醒脑区的抑制发挥促眠作用[19]。另外SCN直接或间接通过食欲素神经元调控睡眠与觉醒[20]。最后,SCN通过褪黑素调节睡眠与觉醒状态[21]。因每条途径包含复杂机制,此处不在详述。
2 睡眠稳态驱动系统 2.1 睡眠稳态驱动系统的提出随着对睡眠调控研究的不断深入,发现单以光暗信号为据,通过SCN调控整个睡眠觉醒周期变化的观点有诸多的不足之处,如正常人白天可以入睡,夜间也可以保持清醒状态,这与昼夜节律系统调控的理论相悖。研究发现,随着清醒持续时间的增加,腺苷、前列腺素D2(prostaglandin D2,PGD2)等促进睡眠的物质增加与生理性睡眠需求的增加相一致,于是,有学者提出来另一个影响睡眠调节的系统,睡眠稳态驱动系统[22]。该系统认为,睡眠的稳态是机体稳态的一部分,睡眠与觉醒的时间比例在一定的范围波动,人体在给定时间段内所需的睡眠总量往往又非常一致,并且独立于昼夜节律系统之外,当睡眠剥夺发生后,需要恢复睡眠的需要进一步说明了这种机制的存在。
2.2 睡眠稳态驱动机制 2.2.1 催眠原对睡眠稳态驱动系统的影响睡眠稳态系统由多个因素驱动,已经确定了一整类称为催眠原的分子,研究发现其会增加稳态睡眠驱动力[22]。核苷腺苷是其中最重要的一种,它在大脑中产生,既作为神经递质,又作为ATP代谢的产物,其促眠的作用,因非特异性腺苷受体拮抗剂——咖啡因而为大家所熟知。研究表明,腺苷随着唤醒时间的增加和睡眠时间的减少,会在大脑中积累,特别是在基底前脑中, 而低浓度和高浓度的腺苷因作用不同的部位而发挥不一样的作用。研究发现,低(纳摩尔)浓度的腺苷已被证明可以增强唤醒神经元传递发挥促醒作用,而高(微摩尔)浓度的腺苷则激活刺激性A2AR来抑制唤醒神经元信息的传递以引起睡意。因此,生理状态下,长期睡眠的缺乏会导致催眠原增多(如腺苷)而引起睡意。
另一种较为典型的物质是PGD2,它是前列腺素H2经前列腺素合成酶的作用形成。研究发现,中枢神经系统中的PGD2有调节睡眠、体温、嗅觉功能、伤害感受等作用[23],主要由脂钙蛋白型前列腺素合成酶产生,两者大量存在于大脑和脑脊液中,而PGD2受体是PGD2调节睡眠最重要的靶点,主要表达在基底前脑的腹侧表面,其位于软脑膜而非脑实质,因此需要一个次级促睡眠信使将软脑膜的睡眠诱导信号,传递至VLPO中促睡眠神经元[22]。研究发现,当PGD2注入基底前脑蛛网膜下腔时,观察到细胞外腺苷水平升高,而PGD2受体中没有这种升高,这表明PGD2受体附近的细胞可能利用腺苷作为次级促眠信使,调节睡眠,而后续的研究也确实证明,PGD2受体刺激A2AR,激活VLPO中的神经元[24],导致睡眠开始,其主要是影响腺苷的释放,发挥稳态睡眠调节的作用。研究发现,PGD2诱导的睡眠能被腺苷A2AR阻断剂所对抗,提示A2AR介导了PGD2的促眠作用[25]。其他几种分子,例如IL-1和TNF-α,已被假设以类似方式作用以参与睡眠稳态的调节[26]。
2.2.2 催眠原调节睡眠的机制催眠原种类虽多,但目前以腺苷与PGD2为研究热点,实际上PGD2通过A2AR实现其促眠作用,故本小节阐述以腺苷为核心的催眠机制。
2.2.2.1 腺苷受体的类型及分布腺苷受体均属于G蛋白偶联受体,A1R和A3R属于G蛋白中的Gi家族,A2AR和A2BR是Gs家族。研究发现,与睡眠相关的包括A1R、A2AR,A1R在大脑皮层、丘脑、海马以及基底神经节(basal ganglia,BG)广泛表达,在下丘脑外侧Orexin和TMN组胺能神经元中的表达也达到一定水平[27];A2AR在前脑区,尤其是纹状体、伏隔核、嗅结节和嗅球中高密度表达。
2.2.2.2 与腺苷相关的睡眠觉醒脑区下丘脑结节乳头体核(tuberomammillary nucleus,TMN)是组胺能神经元集中分布的脑区,其内组胺神经元在觉醒期保持紧张性活动,NREMS期活动减少,REMS期停止放电,被认为是最主要的觉醒调节中枢之一[28]。BG由纹状体、苍白球、丘脑底核和黑质4个主要核团组成,控制动机性行为,参与运动功能、习惯养成和奖赏、成瘾行为等。临床上,帕金森病、亨廷顿氏病、毒品成瘾及抑郁症等均可表现出基底节功能异常,表现出不同程度的睡眠障碍,揭示BG可能参与睡眠调控。VLPO、Orexin神经元经腺苷作用也参与睡眠觉醒的调控,具体内容参照本文相应VLPO、Orexin部分。生理状态下,腺苷随觉醒时间的增加而累积,直接或间接通过分布于相应睡眠觉醒调节脑区的A1R、A2AR发挥促眠作用。
2.2.2.3 腺苷经不同睡眠觉醒脑区的A1R、A2AR发挥不一样的促眠作用研究发现,腺苷作用于基底前脑、下丘脑外侧部和TMN觉醒神经元的A1R发挥抑制作用以促进睡眠; 腺苷也可以经A1R对VLPO或外侧视前区睡眠神经元的抑制作用促进觉醒[29]。在经基底前脑局部给予腺苷或A1R激动剂,可增加NREM;而在侧脑室给予A1R的激动剂却不能明显改变NREM和REM睡眠量[30];腺苷通过作用于下丘脑外侧Orexin、TMN组胺能神经元A1R,对调控睡眠具有较明显的作用[25];此外,A1R基因剔除动物(体内A1R缺失)基础状态或睡眠剥夺后的睡眠觉醒行为均无差异。以上说明腺苷对A1R所在的调控睡眠的脑区表现出明显的脑区依赖性[25],且在睡眠内稳态调节中,A1R并非必需。
腺苷或PGD2激动A2AR,可以使VLPO处c-Fos增加,诱导的NREM睡眠。解剖上从VLPO到TMN存在高度密集的神经投射,主要为GABA和丙甘肽,其抑制TMN神经元,发挥促眠作用。兴奋A2AR,也可以直接增加TMN区GABA释放,抑制组胺能觉醒系统[25]。此外,激活软脑膜或伏隔核神经元上的A2AR,可能也会增强VLPO区的活性,活化VLPO神经元可能抑制多种促觉醒区域,诱发睡眠。目前,更多的证据表明A2AR在腺苷睡眠调节中扮演重要角色。大鼠基底前脑蛛网膜下腔区给予A2AR选择性激动剂CGS21680,能明显增加NREM睡眠量,而给予A1R激动剂仅产生很弱的作用;基因敲除小鼠研究发现,咖啡因可以促进WT和A1R敲除小鼠的觉醒,但并不能增加A2AR敲除小鼠的觉醒水平,表明咖啡因的觉醒作用是阻断A2AR,而非A1R[25],也从侧面反应A2AR在睡眠调节中发挥更为重要作用。
2.2.2.4 睡眠稳态的分子调节机制分子层面,腺苷通过A1R/A2AR信号转导,激活Ca2+-ERK-AP-1和CREB/CRTC1-CRE通路来调节时钟基因Per1和Per2,从而作用于SCN,也可以调控睡眠觉醒[31]。关于稳态睡眠压力系统机制的一个新兴研究领域,可能是蛋白质磷酸化过程。已发现一个蛋白质家族,即睡眠需要指数磷酸化蛋白(sleep need index phosphorylation proteins,SNIPPs),在醒来时会稳定磷酸化,而在睡眠期间会去磷酸化[32]。激酶Sik3已被证明有助于这种磷酸化。这种激酶的组成型活性突变体已被证明可以人为地诱导睡眠压力,从而导致小鼠在非快速眼动睡眠期间具有更高的睡眠时间和delta功率[33]。但整体而言,很少有研究涉及,睡眠-觉醒控制的大脑区域是否以及如何参与稳态睡眠的调节[34]。
3 睡眠昼夜节律系统与睡眠稳态驱动系统之间的相互作用研究发现,这两种机制相互协同配合,共同实现睡眠觉醒状态切换的整体调控[34]。总结两系统调控睡眠觉醒的机制与途径,我们发现其可通过许多交叉融合的部分共同调控睡眠与觉醒。机制层面而言,SCN依据外界信息的输入,在分子水平调节自身的生物种调控睡眠与觉醒,而内稳态系统也可以通过升高的腺苷作用于SCN的Pre1、Pre2影响睡眠觉醒状态。作用途径而言,两者协调配合,均可通过基底前脑、VLPO、Orexin神经元、TMN神经元共同完成睡眠的调节,见Fig 2。
宏观层面而言,稳态睡眠驱动力在清醒状态(通常是白天)由小到大累积;同样,在白天,昼夜节律驱动力也很高并且还在增加,但此时昼夜节律驱动的力度要明显大于稳态睡眠压力,故人可以维持清醒状态。在周期的黑暗阶段开始时,稳态睡眠驱动和昼夜唤醒驱动都很高,相互抵消了两者的影响。然而,在黑暗阶段开始后,昼夜唤醒驱动开始减少,而稳态睡眠驱动保持高位,刺激睡眠状态的开始。在清晨睡眠状态结束时,昼夜唤醒驱动仍然很低,但稳态睡眠驱动低到足以补偿,导致开关再次翻转并开始唤醒状态(如低(纳摩尔)浓度的腺苷发挥的促醒作用)。这种双调控,对正常节律之外的睡眠情况有重要影响[35];例如,在轮班工人中,清晨入睡不是问题,因为昼夜唤醒驱动力低且睡眠压力高。然而,由于昼夜唤醒驱动增加而睡眠压力下降,因此整天保持睡眠可能很困难。
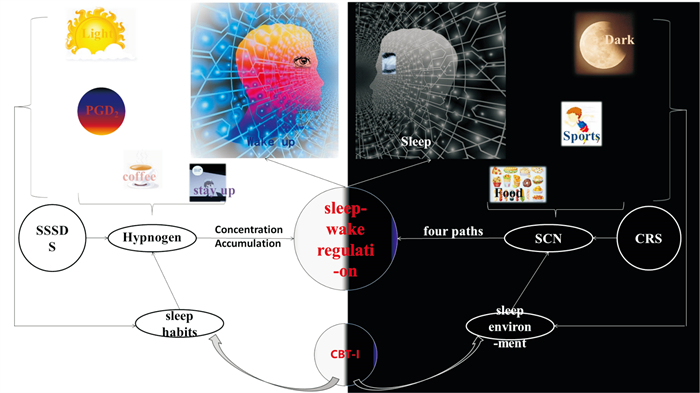
4 小结与展望鉴于睡眠觉醒调节系统复杂的生理联系及神经检测技术尚未十分发达,睡眠觉醒的整体调节机制往往难觅全貌。然而,研究者们通过对各种类型睡眠机制辛勤的探索,发现SCN主导的昼夜节律系统,与各类热门研究的睡眠觉醒调控系统存在解剖上的联系,此外,SCN的略长于24 h的自主节律又与一日24 h的生理行为需求高度吻合,引起大家考虑,SCN在整个睡眠觉醒调控中的重要地位。睡眠稳态的需求驱动,又将内源性的促眠、促醒物质做一整合,回答了昼夜节律系统所不能回答的睡眠中的倒班问题。以上两系统,为失眠的认知行为治疗(cognitive behavioral therapy for insomnia,CBT-I)提供了理论依据。外界24 h的光暗变化、温度、进食等环境因素,在很大程度上影响SCN的自身节律,从而影响着对睡眠觉醒状况的调控;而睡眠习惯(如白天休息时间过长、轮班工作、饮用咖啡等)会通过影响睡眠稳态驱动系统,影响睡眠觉醒的调控。而最新的研究表明,睡眠驱动可以重新配置、唤醒昼夜节律系统,以调节个体一日内睡眠觉醒的分布,这更加突显,睡眠昼夜节律系统与睡眠稳态系统是一个相辅相成的整体,其中环境因素及睡眠习惯在睡眠觉醒调节中有重要意义,见Fig 3。因此,通过CBT-I,改变睡眠环境与习惯,在失眠治疗中十分必要。
|
| Fig 3 Sleep-wake mechanism affected by CBT-I SSDS : Steady-state sleep-driven system; CRS : Circadian rhythm system; CBT-I : Cognitive behavioral therapy for insomnia; SCN : Suprachiasmatic nucleus; PGD2 : Prostaglandin D2 |
| [1] |
Taillard J, Gronfier C, Bioulac S, et al. Sleep in normal aging, homeostatic and circadian regulation and vulnerability to sleep deprivation[J]. Brain Sci, 2021, 11(8): 118-30. |
| [2] |
Von Schantz M, Archer S N. Clocks, genes and sleep[J]. J R Soc Med, 2003, 96(10): 486-9. doi:10.1177/014107680309601004 |
| [3] |
Zhang Z H, Xiong J M, Zhu Y Y, et al. WNK3-PER1 interactions regulate the circadian rhythm in the suprachiasmatic nucleus in rats[J]. Am J Transl Res, 2022, 14(2): 1001-9. |
| [4] |
Adlanmerini M, Krusen B M, Nguyen H C B, et al. REV-ERB nuclear receptors in the suprachiasmatic nucleus control circadian period and restrict diet-induced obesity[J]. Sci Adv, 2021, 7(44): eabh2007-17. doi:10.1126/sciadv.abh2007 |
| [5] |
Grippo R M, Tang Q, Zhang Q, et al. Dopamine signaling in the suprachiasmatic nucleus enables weight gain associated with hedonic feeding[J]. Curr Biol, 2020, 30(2): 196-208. doi:10.1016/j.cub.2019.11.029 |
| [6] |
Steele T A, Stlouis E K, Videnovic A, et al. Circadian rhythm sleep-wake disorders: a contemporary review of neurobiology, treatment, and dysregulation in neurodegenerative disease[J]. Neurotherapeutics, 2021, 18(1): 53-74. doi:10.1007/s13311-021-01031-8 |
| [7] |
Brown M R, Matveyenko A V. Biological timekeeping: scientific background[M]. Circadian Rhythm Sleep-Wake Disorders, Springer, 2020, 12(8): 1-20.
|
| [8] |
Drouyer E, Rieux C, Hut R A, et al. Responses of suprachiasmatic nucleus neurons to light and dark adaptation: relative contributions of melanopsin and rod-cone inputs[J]. J Neurosci, 2007, 27(36): 9623-31. doi:10.1523/JNEUROSCI.1391-07.2007 |
| [9] |
Chou T C, Scammell T E, Gooley J J, et al. Critical role of dorsomedial hypothalamic nucleus in a wide range of behavioral circadian rhythms[J]. Neuroscience, 2003, 23(33): 10691-702. doi:10.1523/JNEUROSCI.23-33-10691.2003 |
| [10] |
Feetham C H, O'brien F, Barrett-Jolley R. Ion channels in the paraventricular hypothalamic nucleus (PVN); emerging diversity and functional roles[J]. Front Physiol, 2018, 9(8): 760-75. |
| [11] |
Pace-Schott E F, Hobson J A. The neurobiology of sleep: Genetics, cellular physiology and subcortical networks[J]. Nat Rev Neurosci, 2002, 3(8): 591-605. doi:10.1038/nrn895 |
| [12] |
Mitchell H A, Weinshenker D. Good night and good luck: norepinephrine in sleep pharmacology[J]. Biochem Pharmacol, 2010, 79(6): 801-9. doi:10.1016/j.bcp.2009.10.004 |
| [13] |
Vujovic N, Gooley J J, Jhou T C, et al. Projections from the subparaventricular zone define four channels of output from the circadian timing system[J]. J Comp Neurol, 2015, 523(18): 2714-37. doi:10.1002/cne.23812 |
| [14] |
李惠敏, 汤琪, 张亚男, 等. 光与睡眠的研究进展[J]. 中风与神经疾病杂志, 2021, 38(12): 1141-3. Li H M, Tang Q, Zhang Y N, et al. Research progress on light and sleep[J]. J Apoplexy Nerv Dis, 2021, 38(12): 1141-3. |
| [15] |
Nikolaev G, Robeva R, Konakchieva R. Membrane melatonin receptors activated cell signaling in physiology and disease[J]. Int J Mol Sci, 2021, 23(1): 119-34. doi:10.3390/ijms23010119 |
| [16] |
王庭槐, 沈霖霖, 武宇明. 生理学[M]. 第九版, 北京: 人民卫生出版社, 2018: 344-8. Wang T H, Shen L l, Wu Y M. Physiology[M]. Ninth Edition, Beijing: People's Health Publishing House, 2018: 344-8. |
| [17] |
Arrigoni E, Fuller P M. The sleep-promoting ventrolateral preoptic nucleus: what have we learned over the past 25 years?[J]. Int J Mol Sci, 2022, 23(6): 119-35. |
| [18] |
Joiner W J. The neurobiological basis of sleep and sleep disorders[J]. Physiology (Bethesda), 2018, 33(5): 317-27. |
| [19] |
张鹏, 李雁鹏, 吴惠涓, 等. 中国成人失眠诊断与治疗指南(2017版)[J]. 中华神经科杂志, 2018, 51(5): 324-35. Zhang P, Li Y P, Wu H J, et al. Guidelines for the diagnosis and treatment of adult insomnia in China (2017 edition)[J]. Chin J Neurol, 2018, 51(5): 324-35. doi:10.3760/cma.j.issn.1006-7876.2018.05.002 |
| [20] |
崔静, 赵维燕, 曹飞, 等. 促食欲素及其受体系统与神经系统疾病[J]. 生理学报, 2019, 71(4): 657-70. Cui J, Zhao W Y, Cao F, et al. Orexin and its receptor system and nervous system diseases[J]. Acta Physiol Sin, 2019, 71(4): 657-70. |
| [21] |
Biggio G, Biggio F, Talani G, et al. Melatonin: from neurobiology to treatment[J]. Brain Sci, 2021, 11(9): 89-98. |
| [22] |
Smith P C, Mong J A. Neuroendocrine control of sleep[J]. Curr Top Behav Neurosci, 2019, 43(7): 353-78. |
| [23] |
Cherasse Y, Aritake K, Oishi Y, et al. The leptomeninges produce prostaglandin D2 involved in sleep regulation in mice[J]. Front Cell Neurosci, 2018, 12(22): 357-66. |
| [24] |
Ahmad A S, Ottallah H, Maciel C B, et al. Role of the L-PGDS-PGD2-DP1 receptor axis in sleep regulation and neurologic outcomes[J]. Sleep, 2019, 42(6): 77-86. |
| [25] |
曲卫敏, 孙宇, 许奇, 等. 腺苷和睡眠觉醒调节[J]. 生物物理学报, 2011, 27(1): 5-17. Qu W M, Sun Y, Xu Q, et al. Adenosine and sleep-wake regulation[J]. Acta Biophysics, 2011, 27(1): 5-17. |
| [26] |
Allada R, Cirelli C, Sehgal A. Molecular mechanisms of sleep homeostasis in flies and mammals[J]. Cold Spring Harb Perspect Biol, 2017, 9(8): 667-75. |
| [27] |
Oishi Y, Huang Z L, Fredholm B B, et al. Adenosine in the tuberomammillary nucleus inhibits the histaminergic system via A1 receptors and promotes non-rapid eye movement sleep[J]. Proc Natl Acad Sci U S A, 2008, 105(50): 19992-7. |
| [28] |
刘天雅, 洪宗元, 曲卫敏, 等. 中枢组胺能神经系统调节睡眠-觉醒机制研究进展[J]. 药学学报, 2011, 46(3): 247-52. Liu T Y, Hong Z Y, Qu W M, et al. Research progress on the mechanism of central histaminergic nervous system regulating sleep-wakefulness[J]. Acta Pharm Sin, 2011, 46(3): 247-52. |
| [29] |
岳小芳, 邱梅红, 曲卫敏, 等. 内源性睡眠促进物质研究进展[J]. 中国临床药理学与治疗学, 2011, 16(6): 672-8. Yue X F, Qiu M H, Qu W M al. Research progress on endogenous sleep-promoting substances[J]. Chin J Clin Pharm Ther, 2011, 16(6): 672-8. |
| [30] |
Urade Y, Eguchi N, Qu W M, et al. Minireview: sleep regulation in adenosine A2A receptor-deficient mice[J]. Neurology, 2003, 61(11 suppl 6): S94-6. |
| [31] |
Jagannath A, Varga N, Dallmann R, et al. Adenosine integrates light and sleep signalling for the regulation of circadian timing in mice[J]. Nat Commun, 2021, 12(1): 2113. |
| [32] |
Wang Z, Ma J, Miyoshi C, et al. Quantitative phosphoproteomic analysis of the molecular substrates of sleep need[J]. Nature, 2018, 558(7710): 435-9. |
| [33] |
Honda T, Fujiyama T, Miyoshi C, et al. A single phosphorylation site of SIK3 regulates daily sleep amounts and sleep need in mice[J]. Proc Natl Acad Sci U S A, 2018, 115(41): 10458-63. |
| [34] |
Yamagata T, Kahn M C, Prius-Mengual J, et al. The hypothalamic link between arousal and sleep homeostasis in mice[J]. Proc Natl Acad Sci U S A, 2021, 118(51): 883-95. |
| [35] |
Pedersen T T, Sunde E, Wisor J, et al. Sleep homeostasis and night work: a polysomnographic study of daytime sleep following three consecutive simulated night shifts[J]. Nat Sci Sleep, 2022, 14(45): 243-54. |

