


2. 山西医科大学药理学教研室,山西 太原 030001;
3. 山西中医药大学中药与食品工程学院,山西 晋中 030619;
4. 山西白求恩医院(山西医学科学院同济山西医院),山西医科大学第三医院,山西 太原 030032
 ,
SHEN Guan-tong1,
HU Xiao-ling2,
ZHU Fei1,
QIN Nan3,
LIAN Ke4,
KANG Jing1,4,
YUE Jing1,4,
SHI Ru-yi1
,
SHEN Guan-tong1,
HU Xiao-ling2,
ZHU Fei1,
QIN Nan3,
LIAN Ke4,
KANG Jing1,4,
YUE Jing1,4,
SHI Ru-yi1

2. Dept of Pharmacology, Shanxi Medical University, Taiyuan 030001, China;
3. College of Pharmaceutical and Food Engineering, Shanxi University of Chinese Medicine, Jinzhong Shanxi 030619, China;
4. Shanxi Bethune Hospital, Shanxi Academy of Medical Sciences, Tongji Shanxi Hospital, Third Hospital of Shanxi Medical University, Taiyuan 030032, China
乳腺癌是威胁全球女性生命健康的最主要的恶性肿瘤之一[1],目前临床上对乳腺癌的主要治疗手段为手术治疗、放疗、化疗[2-3]。其中,乳腺癌的化疗药物种类不足,在化疗过程中对化疗药物的抵抗、肿瘤细胞产生的耐药性、肿瘤发生转移,以及化疗药物价格较为昂贵等都是阻碍有效治疗乳腺癌的重要原因[4]。而中药中所含有的天然活性成分使得其成为潜在治疗癌症的药物,同时,其本身具有成本低且毒性作用较小的优势。因此,青蒿琥酯(artesunate,ART)被用作潜在抗癌药物探究对乳腺癌的治疗,在肿瘤治疗方面具有很大的潜力。
青蒿素长期以来被广泛应用于抗疟疾的治疗[5]。ART是一种在青蒿素基础上合成的衍生物,其水溶性优于青蒿素且更为稳定[6]。研究表明ART因其特有的过氧化桥键结构,不仅可用于抗疟疾,在多种癌症的发展中也具有抑制作用[7]。而ART在乳腺癌中的作用机制尚未完全明确,因此,本研究初步探究ART对乳腺癌细胞MDA-MB-231、MCF-7功能的影响及可能的作用机制。
1 材料与方法 1.1 试剂与材料ART购自Med Chem Express(HY-N0193),使用DMSO(索莱宝科技有限公司)溶解至目标浓度,乳腺癌MDA-MB-231、MCF-7细胞系保存于山西医科大学基础医学院。DMEM高糖培养基(Gibco公司),胎牛血清(FBS,CellMax公司),MTT(索莱宝科技有限公司),细胞凋亡、周期试剂盒(贝博公司),4%多聚甲醛与结晶紫(大连美仑生物公司),基质胶(BD Matrigel,货号356234),培养皿、96孔板、24孔板及其他耗材均购买自Corning公司。
1.2 细胞培养完全培养基为含10% FBS的DMEM高糖培养基。分别将含有30 μmol·L-1 ART、60 μmol·L-1 ART完全培养基处理后MCF-7、MDA-MB-231细胞设置为实验组, 0 μmol·L-1 ART的完全培养基培养细胞为对照组。置于培养箱(温度:37 ℃、CO2含量:5%、湿度:100%)中培养。
1.3 MTT法测定细胞增殖设置实验组用ART培养MCF-7、MDA-MB-231细胞,对照组为0 μmol·L-1 ART培养MCF-7、MDA-MB-231细胞,以每孔2×104细胞铺于96孔板中,细胞贴壁后,每间隔24 h取出一板,每孔加入MTT 20 μL(5 g·L-1),放置培养箱4 h,随后弃掉上清,每孔加入DMSO 200 μL, 放置摇床上,低速震荡10 min,酶标仪测定每孔A值(波长为490 nm)。
1.4 细胞迁移将基础培养基重悬的MCF-7、MDA-MB-231铺入Transwell小室(每室1×105个细胞),下室为含10%FBS的培养基。孵育24 h,使用4%多聚甲醛固定细胞,结晶紫染色,倒置显微镜拍摄并记数。
1.5 细胞侵袭将基质胶与基础培养基按1 ∶ 6稀释后铺于Transwell小室,每室75 μL,待基质胶凝固后,将基础培养基重悬的MCF-7、MDA-MB-231铺入Transwell小室(每室1×105个细胞),下室为含10% FBS的培养基。孵育48 h后,4%多聚甲醛固定细胞15 min,结晶紫染色30 min,倒置显微镜下记数侵袭细胞的数量。
1.6 细胞克隆形成将MCF-7、MDA-MB-231以2.5×103个细胞接种于3.5 cm皿中,培养细胞2~3周,4%多聚甲醛固定细胞15 min,结晶紫染色30 min,使用三蒸水清洗培养皿,干燥后,ImageJ软件计数集落数量。
1.7 细胞周期采用贝博细胞周期试剂盒检测细胞周期,收集细胞沉淀(1×106个细胞),加入1 mL PBS吹匀后,使用75%预冷的乙醇缓慢滴定固定细胞,PI染色,4 ℃避光孵育30 min, 使用流式细胞仪分析对照组与实验组细胞各期细胞含量。
1.8 细胞凋亡采用贝博细胞凋亡试剂盒检测细胞凋亡,收集细胞沉淀,400 μL AnnexinV结合液重悬细胞沉淀(1×106个细胞),加入5 μL AnnexinV-FITC 4 ℃避光孵育15 min、5 μL PI 4 ℃避光孵育5 min,立即在上机进行细胞分选,Flow JO软件分析凋亡细胞比例。
1.9 转录组测序收集ART处理前后的MCF-7、MDA-MB-231细胞沉淀,液氮速冻30 min,将细胞样品送到深圳华大基因科技服务有限公司进行转录组测序。
1.10 Real-Time PCR验证转录组测序结果使用TRIzol法提取对照组和ART处理后的MCF-7、MDA-MB-231细胞的RNA,利用TaKaRa PrimeScriptTMRT Master Mix试剂盒将RNA反转录为cDNA。TaKaRa TB Green PremixE TaqTM Ⅱ进行RealTime PCR(反应条件:95 ℃ 10 min,95 ℃ 15 s,60 ℃ 1 min,40个循环)。所有引物序列均来自NCBI官网,由上海生工合成,详细信息见Tab 1。
| Primer sequences | |
| GAPDH | Forward:5′-GAGTCAACGGATTTGGTCGT-3′ |
| Reverse:5′-TTGATTTTGGAGGGATCTCG-3′ | |
| Skp2 | Forward:5′-ATGCCCCAATCTTGTCCATCT-3′ |
| Reverse:5′-CACCGACTGAGTGATAGGTGT-3′ | |
| CDKN1A | Forward:5′-TGTCCGTCAGAACCCATGC-3′ |
| Reverse:5′-AAAGTCGAAGTTCCATCGCTC-3′ |
基因差异表达的倍数计算(Livak法)
ΔΔCt =[Ct(目的基因, 实验组)-Ct(GAPDH, 实验组)]-[Ct(目的基因,对照组)-Ct(GAPDH, 对照组)]
1.11 统计学分析所有数据均使用SPSS 25.0软件分析,数据表达用x±s,对照组与实验组的差异性,采取独立样本t检验进行统计学分析。
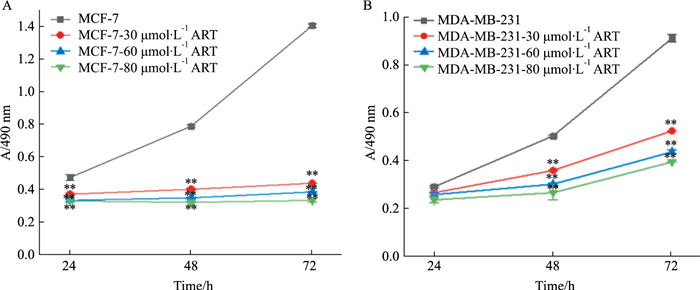
2 结果 2.1 ART可有效抑制MCF-7、MDA-MB-231的增殖通过MTT实验,测定30、60、80 μmol·L-1 ART分别作用24、48、72 h后MCF-7、MDA-MB-231的A值,结果表明ART对两种乳腺癌细胞均具有剂量依赖性和时间依赖性(Fig 1)。ART可有效抑制乳腺癌细胞系的增殖。为降低药物副作用,并且结合药物有效性,故选取浓度为60 μmol·L-1 ART处理MDA-MB-231,30 μmol·L-1 ART处理MCF-7,后续其他实验均按上述浓度进行。
|
| Fig 1 Proliferation of MCF-7 and MDA-MB-231 cells after different concentrations of ART A: Inhibition of the proliferation of MCF-7 after ART treatment; B: Inhibition of the proliferation of MDA-MB-231 after ART treatment. **P < 0.01 vs control group. |
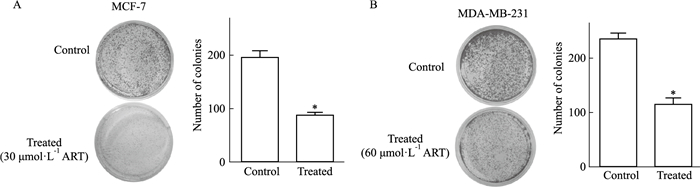
探究ART对乳腺癌细胞系克隆形成能力的影响。结果表明ART处理后的MCF-7、MDA-MB-231细胞,与对照组相比,克隆形成的数量及大小都有所降低且具有统计学意义,ART抑制两种乳腺癌细胞的克隆形成能力(Fig 2)。
|
| Fig 2 Cloning of MCF-7 and MDA-MB-231 inhibited by ART A: Inhibition of the cloning of MCF-7 after ART treatment; B: Inhibition of the cloning of MDA-MB-231 after ART treatment. *P < 0.05 vs control group. |
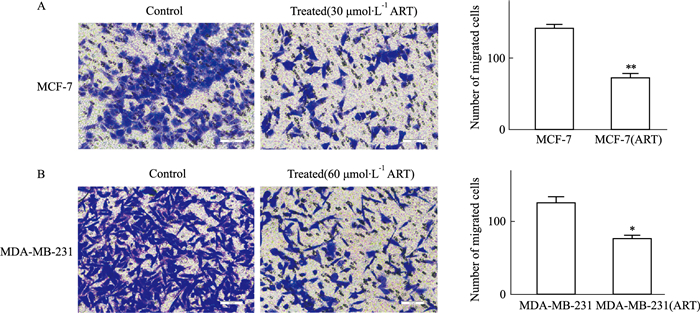
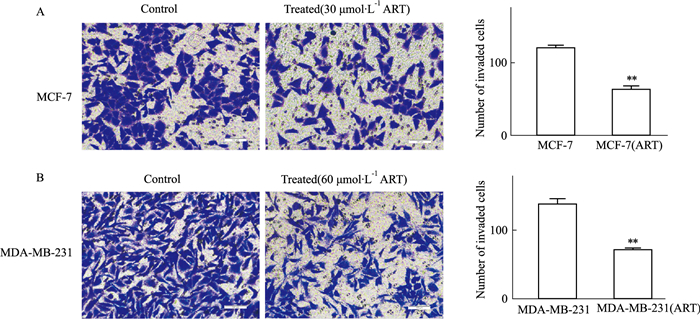
Transwell结果表明,ART作用后的MCF-7、MDA-MB-231细胞与对照组相比, 迁移能力、侵袭能力均明显下降,且差异有显著性(Fig 3,4)。
|
| Fig 3 Migration of MCF-7 and MDA-MB-231 inhibited by ART A: Inhibition of migration of MCF-7 after ART treatment; B: Inhibition of migration of MDA-MB-231 after ART treatment (Scale bars: 100 μm). *P < 0.05, **P < 0.01 vs control group. |
|
| Fig 4 Invasion of MCF-7 and MDA-MB-231 inhibited by ART A: Inhibition of invasion of MCF-7 after ART treatment; B: Inhibition of invasion of MDA-MB-231 after ART treatment (Scale bars: 100 μm). **P < 0.01 vs control group. |
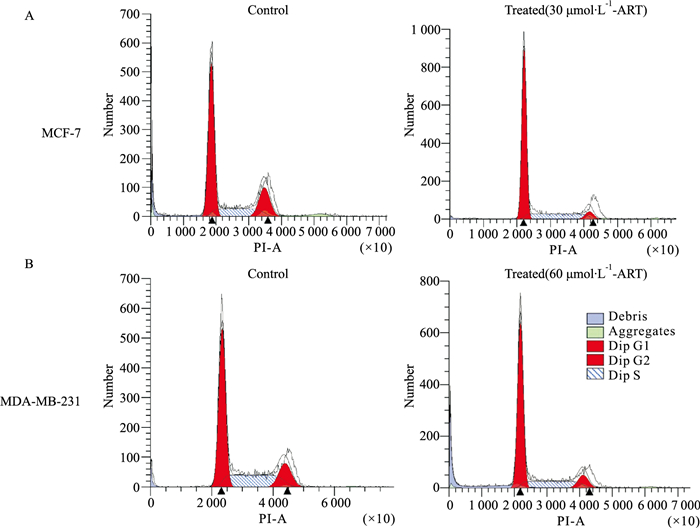
流式细胞术结果表明,与对照组相比,ART处理过后的MCF-7、MDA-MB-231细胞周期均在G0/G1期受阻。ART处理后的MCF-7、MDA-MB-231细胞G0/G1期比例明显增高(MCF-7: 54.47%±0.57% vs 69.95%±0.06%;MDA-MB-231:53.02%±0.1% vs 66.80%±0.43%)(Fig 5,Tab 2)。
|
| Fig 5 Progress of MCF-7 and MDA-MB-231 inhibited by ART A: Inhibition of the progress of MCF-7 after ART treatment; B: Inhibition of the progress of MDA-MB-231 after ART treatment. |
| Group | Cell cycle ratio/% | ||
| G0/G1 | S | G2/M | |
| MCF-7(Control) | 54.47±0.57 | 20.72±0.36 | 20.81±0.93 |
| MCF-7(Treated-30 μmol·L-1ART) | 69.95±0.06** | 24.14±0.14** | 5.91±0.20** |
| MDA-MB-231(Control) | 53.02±0.10 | 31.00±0.11 | 14.98±0.22 |
| MDA-MB-231(Treated-60 μmol·L-1 ART) | 66.80±0.43** | 23.87±0.24** | 9.33±0.24** |
| **P<0.01 vs control group. | |||
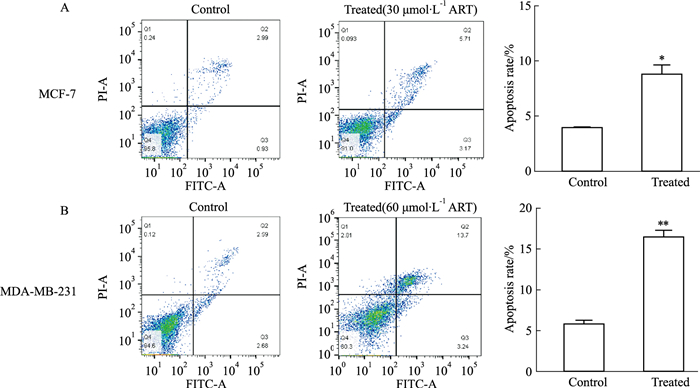
流式细胞术探究ART是否可以诱导乳腺癌细胞MCF-7、MDA-MB-231凋亡的发生,结果如Fig 6所示,ART处理后的乳腺癌细胞的凋亡率,与对照组相比明显增多,ART处理前后MCF-7、MDA-MB-231细胞凋亡率分别为: 3.92% vs 8.88%,5.27% vs 16.94%,差异具有统计学意义。
|
| Fig 6 Apoptosis of MCF-7 and MDA-MB-231 promoted by ART A: Increased rate of apoptosis in MCF-7 after ART treatment; B: Increased rate of apoptosis in MDA-MB-231 after ART treatment. **P < 0.01 vs control group. |
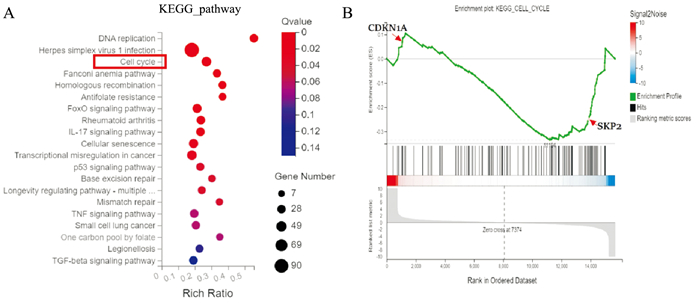
对分别用ART处理前后的MCF-7、MDA-MB-231进行转录组的测序,分析差异基因的表达,KEGG信号通路富集分析结果显示,ART主要通过调控乳腺癌细胞的细胞周期发挥抑制作用,GSEA富集分析结果筛选出ART处理后的MCF-7、MDA-MB-231细胞中Skp2基因的表达差异有显著性,提示ART可能通过影响Skp2的表达,进而参与调控乳腺癌细胞周期的进展, Fig 7。
|
| Fig 7 Analysis of breast cancer cells' differential gene expression before and after ART A: KEGG analysis of breast cancer cells' differential gene expression after ART treatment; B: GSEA analysis of breast cancer cells' differential gene expression after ART treatment. |
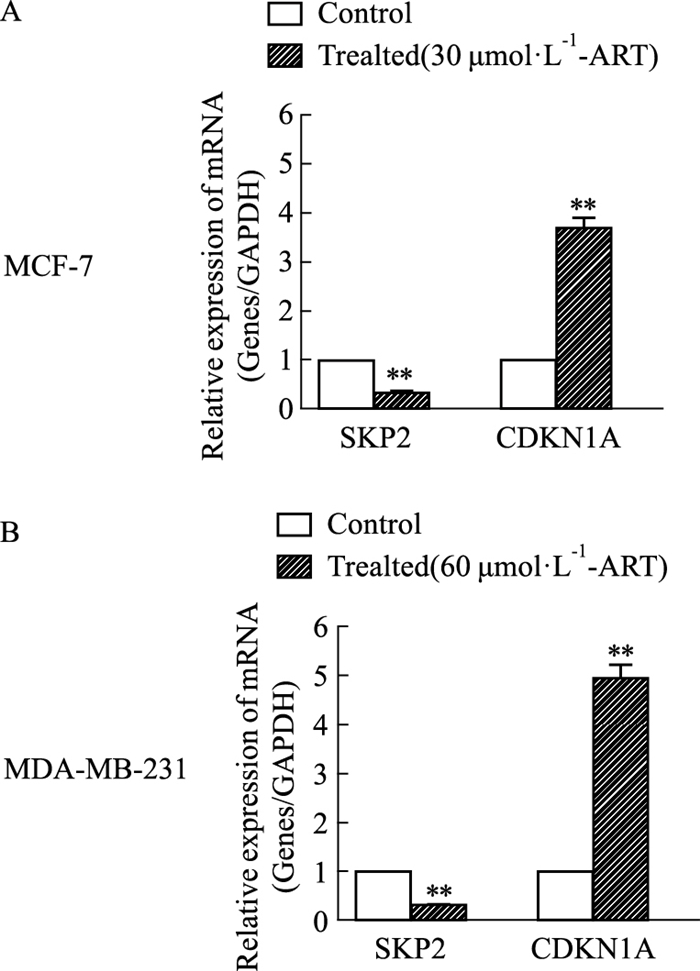
通过qPCR检测ART处理后Skp2、CDKN1A mRNA的表达,结果显示,与ART未处理的MCF-7、MDA-MB-231相比,ART处理后的MCF-7(30 μmol·L-1)、MDA-MB-231(60 μmol·L-1)Skp2基因表达均明显下调,且Skp2下游基因CDKN1A表达上调,差异有统计学意义(Fig 8)。
|
| Fig 8 Expression of Skp2、CDKN1A mRNA in MCF-7 and MDA-MB-231 after ART A: The expressions of Skp2 and CDKN1A in MCF-7 after ART treatment; B: The expressions of Skp2 and CDKN1A in MDA-MB-231 after ART treatment. **P < 0.01 vs control. |
乳腺癌发病率在全球女性癌症中居于首位,也是威胁女性癌症患者生命主要原因之一[8]。然而,乳腺癌化疗药物的应用还有较多的局限性,临床治疗效果有待提高。ART最初用于疟疾的治疗[9]。有研究表明,ART在多种癌症治疗方面具有抑制肿瘤的特性[10]。ART因其具有独特的过氧化桥键结构,当过氧化桥键断裂可产生大量氧自由基[11],杀伤肿瘤细胞[12]。同时,ART在抗疟疾治疗中表现出较好的安全性,因此,ART有望成为乳腺癌化疗药物的更优选择。
本实验研究了抗疟疾药物ART对MCF-7、MDA-MB-231细胞功能的影响以及在乳腺癌中可能发挥的机制。实验结果显示,ART作用后的两种乳腺癌细胞增殖能力、细胞迁移能力、侵袭能力均被ART明显抑制。同时,通过流式细胞术对ART作用前后的乳腺癌的周期及凋亡结果分析表明,ART作用后的乳腺癌细胞周期阻滞于G0/G1期,并且促进乳腺癌细胞凋亡的发生。通过对ART处理前后的乳腺癌细胞进行转录组测序,差异基因富集分析发现ART作用后的乳腺癌细胞差异基因的KEGG通路富集在细胞周期,同时,通过GSEA周期富集筛选出Skp2基因以及下游相关基因CDKN1A[13]。
Skp2是一种RING型泛素化连接酶,介导泛素化降解的途径[14],与细胞周期密切相关[15]。细胞周期蛋白依赖型激酶抑制剂(cyclin-dependent kinase inhibitors,CDKIs)参与调节细胞周期的正常运行[16]。CDKN1A属于CDKIs基因家族,被认为是Skp2的下游基因[17]。本实验结果表明,ART处理后的MCF-7、MDA-MB-231细胞Skp2表达下调且其下游靶基因CDKN1A的表达则上调,与转录组测序结果表达一致,提示ART可能通过影响乳腺癌细胞周期来抑制癌症的发展,这与课题组前期实验中,Skp2调控食管鳞癌细胞周期的结果相一致[18]。本研究结果表明,ART可有效抑制乳腺癌细胞的发展,且具有低成本,毒性较低的优势,提示其可能为乳腺癌药物的开发提供新的研究方向。
| [1] |
Harbeck N, Gnant M. Breast cancer[J]. Lancet, 2017, 389(10074): 1134-50. doi:10.1016/S0140-6736(16)31891-8 |
| [2] |
Maughan K L, Lutterbie M A, Ham P S. Treatment of breast cancer[J]. Am Fam Physician, 2010, 81(11): 1339-46. |
| [3] |
Fan L, Strasser-Weippl-K, Li J J, et al. Breast cancer in China[J]. Lancet Oncol, 2014, 15(7): e279-89. doi:10.1016/S1470-2045(13)70567-9 |
| [4] |
Greenshields A L, Fernando W, Hoskin D W. The anti-malarial drug artesunate causes cell cycle arrest and apoptosis of triple-negative MDA-MB-468 and HER2-enriched SK-BR-3 breast cancer cells[J]. Exp Mol Pathol, 2019, 107: 10-22. doi:10.1016/j.yexmp.2019.01.006 |
| [5] |
John Angus B. An evaluation of rectal artesunate for the pre-hospital management of severe malaria[J]. Expert Opin Pharmacother, 2020, 21(6): 645-51. doi:10.1080/14656566.2020.1718108 |
| [6] |
Efferth T. From ancient herb to modern drug: artemisia annua and artemisinin for cancer therapy[J]. Semin Cancer Biol, 2017, 46: 65-83. doi:10.1016/j.semcancer.2017.02.009 |
| [7] |
Kong Z, Liu R, Cheng Y. Artesunate alleviates liver fibrosis by regulating ferroptosis signaling pathway[J]. Biomed Pharmacother, 2019, 109: 2043-53. doi:10.1016/j.biopha.2018.11.030 |
| [8] |
Yeo S K, Guan J L. Breast cancer: multiple subtypes within a tumor?[J]. Trends Cancer, 2017, 3(11): 753-60. doi:10.1016/j.trecan.2017.09.001 |
| [9] |
孔庆明, 戴方伟, 丁豪杰, 等. 青蒿琥酯抗小鼠血吸虫性肝纤维化的作用[J]. 中国药理学通报, 2019, 35(6): 854-8. Kong Q M, Dai F W, Ding H J, et al. Effects of artesunate on schistosomal liver fibrosis in mice[J]. Chin Pharmacol Bull, 2019, 35(6): 854-8. |
| [10] |
Chen Y, Wang F, Wu P, et al. Artesunate induces apoptosis, autophagy and ferroptosis in diffuse large B cell lymphoma cells by impairing STAT3 signaling[J]. Cell Signal, 2021, 88: 110167. doi:10.1016/j.cellsig.2021.110167 |
| [11] |
Berköz M, Özkan-Yłlma F, ÖZLüER-HUNT A, et al. Artesunate inhibits melanoma progression in vitro via suppressing STAT3 signaling pathway[J]. Pharmacol Rep, 2021, 73(2): 650-63. doi:10.1007/s43440-021-00230-6 |
| [12] |
Zhao F, Vakhrusheva O, Markowitsch S D, et al. Artesunate impairs growth in cisplatin-resistant bladder cancer cells bycell cycle arrest, apoptosis and autophagy induction[J]. Cells, 2020, 9(12): 2643. doi:10.3390/cells9122643 |
| [13] |
Hume S, Grou C P, Lascaux P, et al. The NUCKS1-SKP2-p21/p27 axis controls S phase entry[J]. Nat Commun, 2021, 12(1): 6959. doi:10.1038/s41467-021-27124-8 |
| [14] |
Mikamo M, Kitagawa K, Sakai S, et al. Inhibiting Skp2 E3 Ligase suppresses bleomycin-induced pulmonary fibrosis[J]. Int J Mol Sci, 2018, 19(2): 474. doi:10.3390/ijms19020474 |
| [15] |
Li C, Du L, Ren Y, et al. SKP2 promotes breast cancer tumorigenesis and radiation tolerance through PDCD4 ubiquitination[J]. J Exp Clin Cancer Res, 2019, 38(1): 76. doi:10.1186/s13046-019-1069-3 |
| [16] |
Salamina M, Montefiore B C, Liu M, et al. Discriminative SKP2 interactions with CDK-cyclin complexes support a cyclin A-specific role in p27KIP1 degradation[J]. J Mol Biol, 2021, 433(5): 166795. doi:10.1016/j.jmb.2020.166795 |
| [17] |
De Queiroz R M, Moon S H, Prives C. O-GlcNAc transferase regulates p21 protein levels and cell proliferation through the FoxM1-Skp2 axis in a p53-independent manner[J]. J Biol Chem, 2022, 298(9): 102289. doi:10.1016/j.jbc.2022.102289 |
| [18] |
高媛, 郭敏, 张敏, 等. S期激酶相关蛋白2对食管鳞癌细胞增殖、迁移的影响及其作用机制[J]. 中国生物制品学杂志, 2021, 34(2): 146-51. Gao Y, Guo M, Zhang M, et al. Effect of S-phase kinase associated protein 2 on proliferation and migration of esophageal squamous carcinoma cells and relevant mechanism[J]. Chin J Biol, 2021, 34(2): 146-51. |