


2. 新乡医学院基础医学院,河南 新乡 453003;
3. 新乡医学院药学院,河南 新乡 453003
魏来(1982-),男,博士,副教授,研究方向:药物成瘾机制,通信作者,E-mail: weilai@xxmu.edu.cn
 ,
TU Wan-yu1,
ZHANG Teng-teng1,
YAO Zhi-jun2,
YI Shan-yong1,
ZHAO Ying3,
LUO Guo-sheng1,
JIA Wen-ge1,
LI Chen-chen1,
ZHAO Bin1
,
TU Wan-yu1,
ZHANG Teng-teng1,
YAO Zhi-jun2,
YI Shan-yong1,
ZHAO Ying3,
LUO Guo-sheng1,
JIA Wen-ge1,
LI Chen-chen1,
ZHAO Bin1
 ,
WEI Lai1
,
WEI Lai1

2. School of Basic Medical Science, Xinxiang Medical University, Xinxiang Henan 453003, China;
3. School of Pharmacy, Xinxiang Medical University, Xinxiang Henan 453003, China
药物成瘾是一种以强迫觅药及用药行为为特征的慢性复发性脑疾病,伴有躯体精神依赖、药物耐受及复吸,最终可导致精神障碍、继发性疾病甚至死亡[1]。2022年,世界毒品报告显示,2020年全世界16~64岁人群中约有2.84亿人使用毒品,其中吗啡、海洛因等阿片类毒品的使用人数多达6 130万[2]。由于吗啡等阿片类物质成瘾的发生机制十分复杂,临床上缺乏有效的干预方案。因此,研究吗啡成瘾的神经生物学机制对于开发有针对性的干预靶点具有重要意义。
研究表明[3],吗啡成瘾过程与突触结构和神经可塑性的变化有关,这些神经适应性变化的持续性是由中脑边缘多巴胺系统(mesolimbic dopamine system, MLDS)内基因表达的表观遗传修饰(如组蛋白修饰、DNA甲基化)来调节的。MLDS包括腹侧被盖区(ventral tegmental area, VTA)、伏隔核(nucleus accumbens, NAc)、前额叶皮层(prefrontal cortex, PFC)、杏仁核以及海马等结构。VLO作为PFC的重要组成部分,已被证实参与了吗啡成瘾的形成过程[4]。沉默信息调节因子2相关酶1(silencing information regulator 2 related enzyme 1, SIRT1)是依赖于NAD+的Ⅲ类组蛋白去乙酰化酶家族成员,其通过调控组蛋白和多种非组蛋白(转录因子等)的去乙酰化,调控与成瘾相关的学习记忆、奖赏等过程[5]。研究表明,SIRT1促进神经元轴向伸长和树突分支,参与调节突触可塑性和学习记忆能力,而敲除SIRT1损害了突触可塑性和学习记忆能力[6-7]。药物成瘾的本质是以药物引起的基因表达和突触可塑性改变为基础的病理性记忆,因此,我们推测SIRT1可能在吗啡成瘾中发挥重要作用。
研究表明,细胞外信号调节激酶(extracellular signal-regulated kinase, ERK)、环磷酸腺苷反应元件结合蛋白(cAMP-response element binding protein, CREB)和FosB蛋白参与药物奖赏和学习记忆相关的突触可塑性改变[8]。Gao等[7]研究发现,SIRT1通过含有转录因子YY1的阻遏复合体限制miR-134的表达,敲除SIRT1后miR-134表达升高,通过抑制CREB和BDNF的表达损害突触可塑性及记忆形成。此外,Sun等[9]研究发现,敲除小鼠海马内SIRT1引起突触后密度蛋白95(postsynaptic density protein 95, PSD95)表达降低,通过突触可塑性改变导致认知障碍。以上研究表明,CREB、BDNF、PSD95等分子很有可能是SIRT1参与调节吗啡成瘾记忆的下游关键分子靶点。
EX527是一种选择性SIRT1抑制剂,可有效抑制SIRT1的去乙酰化酶活性。我们前期研究发现,VLO内注射EX527可抑制吗啡诱导大鼠行为敏化的表达,表明EX527可能对吗啡成瘾发挥调节作用[4]。CPP和行为敏化均为研究药物成瘾的经典模型,CPP模型将成瘾性药物的奖赏效应与环境线索配对,动物经过条件性训练后产生与药物相关的条件性记忆(即成瘾记忆),表现出对药物配对环境的偏爱。CPP模型能够评价动物对成瘾性药物的渴求和依赖,并反映成瘾记忆促发觅药渴求和用药行为的过程,是对行为敏化模型的补充。本研究是对前期研究的延伸和进一步验证,通过CPP模型研究VLO内SIRT1在吗啡成瘾中的作用,并探讨SIRT1是否通过CREB/BDNF通路参与行为学改变过程,为寻找吗啡成瘾干预靶点提供理论基础。
1 材料与方法 1.1 实验材料 1.1.1 实验动物SPF级雄性SD大鼠(7周龄)购自于北京斯贝福生物公司,动物许可证号:SCXK(京)2019-0010,在适应饲养环境1周后,即8周龄时开始进行实验。室内温度23℃~26℃,相对湿度50%~70%,光照明暗交替12 h / d,自由饮食和饮水,尽量避免温度变化、噪音以及强光等不良环境刺激。所有动物实验内容尽可能减少动物使用数量并减轻动物的痛苦。
1.1.2 药品与试剂盐酸吗啡(批号171256-201503),中国食品药品检定研究院;EX527(货号E7034),美国Sigma-Aldrich公司;RIPA裂解液(货号P0013B)、PMSF(货号ST506),上海碧云天生物技术公司;磷酸酶抑制剂(货号G2007)、5×蛋白上样缓冲液(货号G2013),武汉赛维尔生物科技公司;180 ku蛋白Marker(货号MP102-01)、BCA蛋白定量试剂盒(货号E112-01)、超敏ECL化学发光试剂盒(货号E411-04),南京诺唯赞生物公司;NC膜(货号66585),美国Santa Cruz Biotechnolongy公司。抗SIRT1(货号#2496)、抗PSD95(货号#3409)、抗c-fos(货号#2250)、抗p-ERK(货号#4370)、抗ERK(货号#4695)、抗CREB(货号#9197)、抗BDNF(货号#47808)、抗β-actin(货号#3700)、抗兔二抗(货号#14708)、抗鼠二抗(货号#7076),美国Cell Signaling Technology公司。
1.1.3 CPP设备CPP实验视频分析系统(上海移数信息科技公司,型号RD1111-CPP)包含左箱、右箱、中间箱以及录像分析系统。左右箱规格均为长330 mm×宽270 mm×高420 mm,顶部有可调节亮度的顶灯和录像系统,中间箱规格为长130 mm×宽100 mm×高420 mm,可通过移动两侧PVC隔板与左右箱相通。CPP左箱内侧壁为白色(白箱),底面有网格状黑色底板,右箱内侧壁为黑色(黑箱),底面有栅栏状黑色底板。
1.2 实验方法 1.2.1 双侧VLO内留置导管应用戊巴比妥钠溶液(2%,3 mL·kg-1)腹腔注射麻醉大鼠,麻醉成功后置于脑立体定位仪操作平台上,将耳杆插入双侧外耳道,固定好门齿,确保整个头部居中且可靠固定。剪去大鼠颅顶头皮,剥离骨膜,暴露颅骨,擦去颅骨表面的血性液体,将前囟点和后囟点垂直高度差控制在±0.1 mm内。参照Paxinos和Watson大鼠脑立体定位图谱[10]计算出VLO的矢状、冠状坐标(前囟前3.2 mm,中线两侧2.0 mm,脑表面下4.6 mm)。在颅骨表面固定两颗微型螺钉,颅骨钻孔,用游丝镊挑破硬脑膜,调整垂直杆,置入导管。用玻璃离子体水门汀、牙托粉涂抹覆盖切口区域及外周皮肤,导管固定后将与导管等长的不锈钢导管内芯插入导管。最后大鼠经腹腔注射青霉素20万U/只/d,连续注射3 d,恢复1周,无运动障碍者进行后续实验。
1.2.2 建立吗啡诱导的CPP模型48只SD大鼠双侧VLO内留置导管后随机分为4组,即DMSO+saline(DS)组、DMSO+morphine(DM)组、EX527+saline(ES)组、EX527+morphine(EM)组,12只/组。所用药物中,盐酸吗啡以5 g·L-1的浓度溶于生理盐水,EX527以5 g·L-1的浓度溶于1% DMSO。
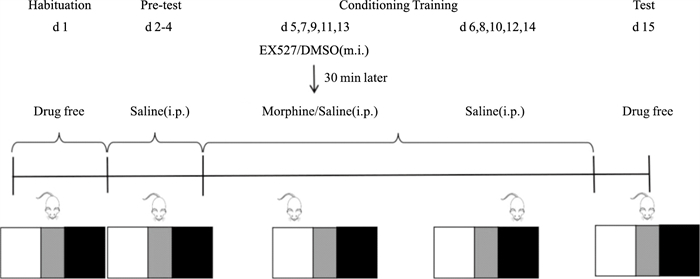
CPP模型的建立(Fig 1):①适应阶段(d 1),将大鼠放入中间箱,自由探索15 min。②前测阶段(d 2~4),大鼠腹腔注射saline(1 mL·kg-1)后放入中间箱,记录15 min内大鼠在左右箱内的停留时间及活动距离,停留时间较少的一侧箱作为伴药箱,另一侧箱作为非伴药箱。③条件性训练阶段(d 5~14),封闭CPP黑白箱。d 5、7、9、11、13,经导管向双侧VLO内微量注射EX527(5 g·L-1, 1 μL)或DMSO(1%, 1 μL),30 min后腹腔注射morphine(1 mL·kg-1, 5 g·L-1)或saline(1 mL·kg-1),放入伴药箱120 min。d 6、8、10、12、14,大鼠腹腔注射saline(1 mL·kg-1),放入非伴药箱120 min。④测试阶段(d 15),取出隔板,将大鼠放入中间箱,记录15 min内大鼠在左右箱内的停留时间及活动距离。大鼠测试阶段伴药箱停留时间减去前测阶段伴药箱平均停留时间为CPP评分。
|
| Fig 1 Procedure of morphine-induced CPP in rats |
行为实验结束后,深度麻醉大鼠,断头法处死,小心剥离整个大脑,参照Paxinos和Watson大鼠脑立体定位图谱[10]于冰上快速分离VLO,经液氮短暂速冻后置于-80 ℃保存。
提取各VLO组织总蛋白,BCA法测定目的蛋白样品浓度,配制SDS-PAGE凝胶,各蛋白样品上样量定为30 μg,电泳条件为:浓缩胶80 V,分离胶120 V。然后将蛋白转印至NC膜上,转印条件为:100 V 90 min。5%脱脂牛奶室温封闭90 min,分别加入兔抗SIRT1(1 ∶ 1 000)、兔抗PSD95(1 ∶ 1 000)、兔抗c-fos(1 ∶ 1 000)、兔抗p-ERK(1 ∶ 2 000)、兔抗ERK(1 ∶ 2 000)、兔抗CREB(1 ∶ 1 000)、兔抗BDNF(1 ∶ 1 000)、鼠抗β-actin(1 ∶ 2 000)4 ℃孵育12 h。TBS-T洗膜,加入对应抗鼠二抗(1 ∶ 5 000)、抗兔二抗(1 ∶ 5 000)室温孵育1 h。TBS-T洗膜,ECL法显影,并使用全自动化学发光系统曝光。通过ImageJ软件计算灰度值,选用β-actin作为内参进行后续统计分析。
1.3 统计学方法实验数据使用SPSS 19.0进行统计分析,以x±s表示,采用t检验和单因素方差分析(One-way ANOVA)进行组间比较。
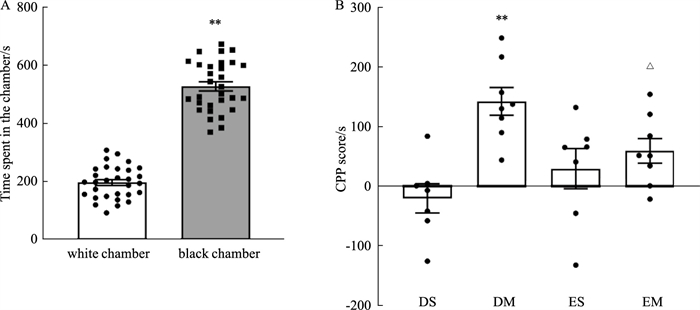
2 结果 2.1 EX527对吗啡诱导大鼠CPP的影响行为学结果显示,在前测阶段,大鼠黑箱内停留时间明显多于白箱在测试阶段(P<0.01),表明大鼠对黑箱存在天然偏爱,因此,我们将非偏爱箱(白箱)与morphine配对进行后续的CPP训练(Fig 2A)。在测试阶段,DM组大鼠CPP评分明显高于DS组(P<0.01),表明吗啡诱导大鼠CPP模型构建成功。在VLO内注射EX527后,EM组大鼠CPP评分较DM组明显降低(P<0.05),且与ES组相比,差异无统计学意义,表明EX527对吗啡诱导CPP具有抑制作用;ES组大鼠CPP评分与DS组相比,差异无统计学意义,表明单独给予EX527不影响大鼠的CPP行为(Fig 2B)。
|
| Fig 2 Effect of EX527 on morphine-induced CPP in rats A: The natural preference of rats for black and white chamber (x±s, n=32); B: Effect of EX527 on CPP score in rats (x±s, n=8). DS represents DMSO+saline; DM represents DMSO+morphine; ES represents EX527+saline; EM represents EX527+morphine. **P < 0.01 vs DS; △P < 0.05 vs DM. |
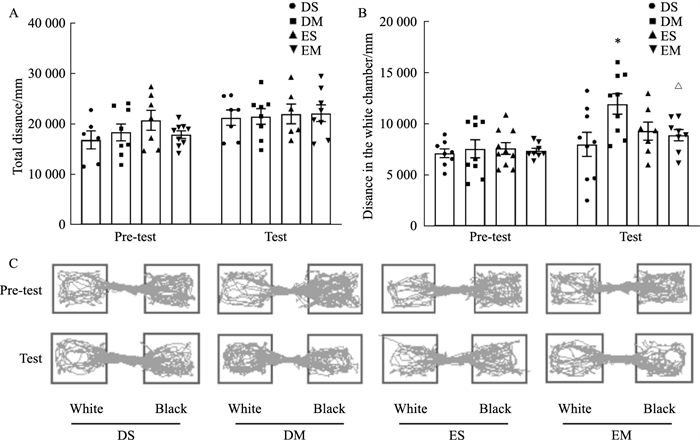
在前测阶段,DS组、DM组、ES组与EM组大鼠活动总距离相比,差异无统计学意义,表明各组大鼠自主活动能力一致;在测试阶段,DS组、DM组、ES组与EM组大鼠活动总距离相比,差异无统计学意义,表明训练阶段吗啡给药不影响测试阶段活动能力(Fig 3A)。在前测阶段,DS组、DM组、ES组与EM组大鼠白箱活动距离相比,差异无统计学意义,表明各组大鼠对白箱的基础偏爱一致;在测试阶段,DM组大鼠白箱活动距离较DS组明显增多(P<0.05),EM组大鼠白箱活动距离较DM组明显减少(P<0.05),ES组白箱活动距离与DS组相比,差异无统计学意义(Fig 3B)。CPP活动轨迹图符合以上结果(Fig 3C)。
|
| Fig 3 Effect of EX527 on total movement distance and movement distance in drug-paired chamber (white chamber) in rats A: The effect of EX527 on total movement distance in rats (x±s, n=8); B: The effect of EX527 on movement distance in drug-paired chamber (white chamber) in rats (x±s, n=8); C: The representative CPP trajectories. DS represents DMSO+saline; DM represents DMSO+morphine; ES represents EX527+saline; EM represents EX527+morphine. *P < 0.05 vs DS; △P < 0.05 vs DM. |
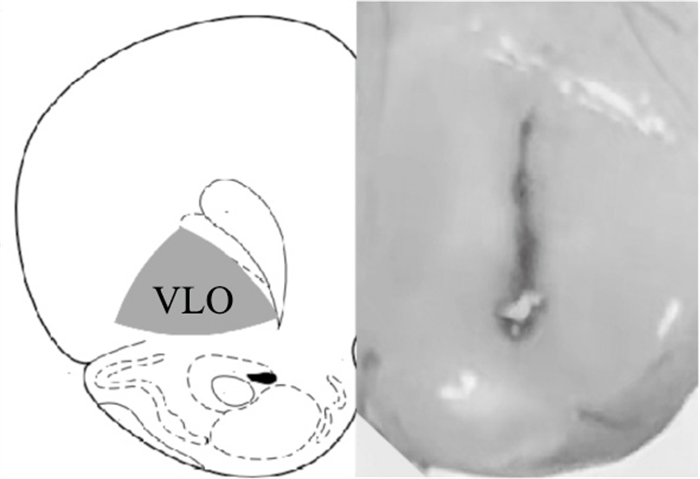
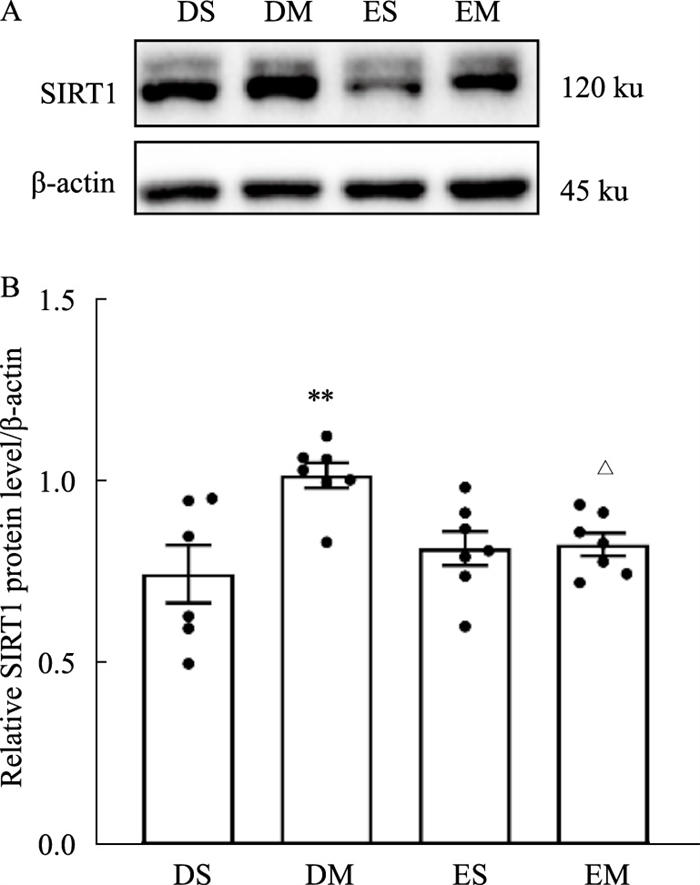
在分离VLO组织时,参照Paxinos和Watson大鼠脑立体定位图谱[10],选取注射位点准确的大鼠数据用于后续分析(Fig 4)。Western blot结果显示,DM组大鼠VLO内SIRT1蛋白表达较DS组明显增高(P<0.01),在VLO内注射EX527后,EM组SIRT1蛋白表达较DM组明显降低(P<0.05),但ES组与DS组之间差异无统计学意义,表明VLO内注射EX527对吗啡诱导CPP形成大鼠SIRT1表达增高有抑制作用,而对正常表达的SIRT1无影响(Fig 5)。
|
| Fig 4 Visual observation of microinjection position in VLO The site of the microinjection of EX527 (right) corresponded to the location of VLO accurately shown in the map (left). |
|
| Fig 5 Effect of EX527 on SIRT1 protein level in VLO A: Detection of protein level of SIRT1 by Western blot; B: Quantification analysis of SIRT1 protein level (x±s, n=6). DS represents DMSO+saline; DM represents DMSO+morphine; ES represents EX527+saline; EM represents EX527+morphine. **P < 0.01 vs DS; △P < 0.05 vs DM. |
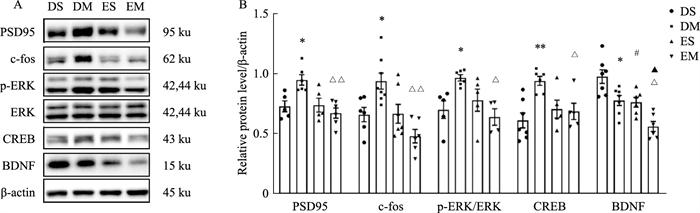
Western blot结果显示,DM组大鼠VLO内PSD95蛋白表达较DS组明显增高(P<0.05),而EM组PSD95蛋白表达较DM组明显降低(P<0.01),但ES组与DS组之间差异无统计学意义;DM组大鼠VLO内c-fos蛋白表达较DS组明显增高(P<0.05),而EM组c-fos蛋白表达较DM组明显降低(P<0.01),但ES组与DS组之间差异无统计学意义;DM组大鼠VLO内p-ERK蛋白表达较DS组明显增高(P<0.05),而EM组p-ERK蛋白表达较DM组明显降低(P<0.05),但ES组与DS组之间差异无统计学意义;DM组大鼠VLO内CREB蛋白表达较DS组明显增高(P<0.01),而EM组CREB蛋白表达较DM组明显降低(P<0.05),但ES组与DS组之间差异无统计学意义。以上结果表明,VLO内注射EX527对吗啡诱导CPP形成大鼠的PSD95、c-fos、p-ERK、CREB表达增高有抑制作用。DM组大鼠VLO内BDNF蛋白表达较DS组明显降低(P<0.05),ES组大鼠VLO内BDNF蛋白表达较DS组明显降低(P<0.05),EM组BDNF蛋白表达较ES组明显降低(P<0.05),EM组BDNF蛋白表达较DM组进一步降低(P<0.05),表明吗啡诱导CPP形成大鼠VLO内BDNF表达降低,VLO内注射EX527进一步抑制了BDNF表达(Fig 6)。
|
| Fig 6 Effect of EX527 on protein level of downstream addictive memory related molecules of SIRT1 in VLO A: Detection of protein level of PSD95, c-fos, p-ERK, CREB and BDNF by Western blot; B: Quantification analysis of PSD95, c-fos, p-ERK, CREB and BDNF protein level (x±s, n=6). DS represents DMSO+saline; DM represents DMSO+morphine; ES represents EX527+saline; EM represents EX527+morphine. *P < 0.05 vs DS, **P < 0.01 vs DS; △P < 0.05 vs DM, △△P < 0.01 vs DM; #P < 0.05 vs DS; ▲P < 0.05 vs ES. |
在临床应用中,吗啡主要作为镇痛药物用于中重度疼痛的治疗,但由于其强大的精神奖赏效应,可以产生强烈的愉悦感和欣快感,滥用后非常容易成瘾。目前临床上仍缺乏有效的治疗措施及药物,探讨吗啡成瘾的神经生物学机制并寻找新的有效干预靶点具有重要研究价值。在本研究中,我们建立了吗啡诱导的CPP大鼠模型,发现吗啡诱导CPP形成大鼠VLO内SIRT1、p-ERK、CREB、c-fos、PSD95蛋白表达增高,BDNF蛋白表达降低。而VLO内微量注射EX527抑制了吗啡诱导CPP形成,EX527对吗啡诱导CPP形成大鼠VLO内SIRT1、p-ERK、CREB、c-fos、PSD95表达增高有抑制作用,并进一步抑制BDNF表达。由于CPP行为学表型能够反映实验动物对成瘾性药物的渴求和依赖,因此,本研究结果提示,EX527可作为吗啡成瘾治疗的潜在药物。
在本研究中,行为学结果显示DM组大鼠CPP评分较DS组明显增高,且两组大鼠之间自主活动能力没有明显差异,表明脑立体定位手术及VLO内注射DMSO均不影响吗啡诱导CPP形成。EM组大鼠CPP评分较DM组明显降低,表明VLO内注射
EX527抑制了吗啡诱导大鼠CPP形成。ES组CPP评分与DS组差异无统计学意义,表明单纯VLO内注射EX527不会影响大鼠的CPP行为。此外,DM组大鼠在测试阶段伴药箱活动距离较DS组明显增多,而EM组大鼠测试阶段伴药箱活动距离较DM组明显减少,表明VLO内注射EX527后大鼠未对伴药箱产生偏爱。Ferguson等[11]研究发现,大鼠NAc内SIRT1过表达促进了吗啡及可卡因诱导CPP形成,而敲除NAc内SIRT1抑制了吗啡及可卡因诱导的奖赏效应。本课题组前期研究表明,大鼠VLO内注射EX527抑制吗啡诱导行为敏化的表达[4]。基于以上研究结果,本研究证实,EX527对吗啡成瘾发挥了潜在的改善作用,该结果与本课题组前期研究中有关EX527对成瘾行为的调节作用具有一致性,是对前期研究的补充和深入验证,为寻找干预吗啡成瘾的新靶点提供理论依据。同时有研究表明,小鼠腹腔注射SIRT1激活剂白藜芦醇能够阻断酒精诱导CPP的形成和复燃,并促进CPP消退[12]。这与本研究结果相悖,可能是由于动物种属、行为学程序以及干预SIRT1活性或表达手段的差异造成的。总之,脑内SIRT1在吗啡成瘾中的作用较为复杂,其相关的调控作用及机制有必要进一步探讨。
研究证实[7, 13],SIRT1的上调通过促进神经营养因子(如BDNF)表达、抗氧化应激、抑制神经炎症等机制改善突触可塑性,保护神经和学习记忆能力,而敲除SIRT1损害了学习记忆和突触可塑性。我们前期研究发现,吗啡诱导行为敏化表达期大鼠VLO内SIRT1表达增高[4]。Ferguson等[11]研究发现,吗啡及可卡因诱导大鼠CPP形成后NAc内SIRT1表达增高。在本研究中,吗啡CPP形成大鼠VLO内SIRT1表达增高,而VLO内注射EX527后SIRT1表达较吗啡CPP形成大鼠降低,提示EX527可能通过抑制VLO内SIRT1阻断吗啡CPP形成。然而,单独给予EX527不影响VLO内SIRT1蛋白表达水平,可能原因是EX527主要通过抑制SIRT1的脱乙酰化酶活性发挥作用,或者EX527仅对SIRT1过表达发挥抑制作用,而对大鼠脑内正常表达的SIRT1无明显影响,具体机制有待进一步研究。
BDNF是脑内调节突触可塑性和重要细胞事件的主要神经营养因子,是神经元活动、学习和记忆形成的基础,与成瘾、抑郁症、焦虑、创伤后应激障碍等许多精神疾病有关。BDNF可通过原肌球蛋白相关激酶B(tropomyosin receptor kinase B, TrkB)受体调节多巴胺的释放和成瘾性药物相关的行为反应,包括依赖、渴求、敏化和复吸等[14]。在吗啡诱导的CPP大鼠模型中,VTA内BDNF和TrkB表达降低,血清中BDNF含量降低[15]。Miyashita等[8]研究表明,敲除小鼠海马内SIRT1引起BDNF表达降低,从而损害了突触可塑性及记忆形成。本研究结果显示,吗啡CPP形成大鼠VLO内BDNF表达降低,VLO内注射EX527进一步降低了BDNF的表达,与之前的研究结果一致。有趣的是,我们前期研究发现,在吗啡诱导大鼠行为敏化表达期VLO内BDNF表达升高[4]。Jorjani等[16]研究表明,吗啡CPP形成大鼠NAc和PFC内BDNF表达增高,NAc和PFC内微量注射BDNF受体拮抗剂ANA-12抑制了吗啡诱导大鼠奖赏记忆的形成,这可能是由行为学程序、给药次数、脑区不同导致的差异。在本研究中,EX527可能通过抑制SIRT1进而影响BDNF的表达参与吗啡成瘾的调节。
在中枢神经系统内,ERK、CREB和c-fos参与多种形式的突触可塑性,如长时程增强,并在吗啡、可卡因等成瘾性药物奖赏效应中发挥重要作用[8]。吗啡作用于MLDS后引起ERK磷酸化激活,ERK启动丝裂原活化蛋白激酶信号级联反应,通过突触可塑性改变,促使成瘾记忆形成。CREB是ERK信号通路的下游靶点,CREB表达增高是神经元激活的重要标志,参与对药物成瘾、学习记忆过程的调节[17]。CREB活化后调节记忆巩固和长时程增强相关基因(c-fos、Arc和BDNF等)的表达。研究表明[18],CREB还通过调节PSD95参与吗啡诱导的突触传递和奖赏行为,PSD95的上调能够促进突触发生和树突分支,对脑发育、突触连接、神经元成熟和学习认知相关突触可塑性至关重要。在本研究中,吗啡CPP形成大鼠VLO内p-ERK、CREB、c-fos和PSD95蛋白表达明显增高,表明吗啡引起了VLO内神经元以及成瘾记忆相关分子的激活。本课题组前期研究发现,VLO内注射EX527通过逆转吗啡引起的p-ERK和BDNF的增高抑制吗啡诱导行为敏化[4]。Xia等[5]和Ferguson等[11]研究发现,NAc内敲除SIRT1通过降低p-ERK、核因子-κB、PSD95以及突触素等分子的表达抑制吗啡及海洛因诱导CPP的形成并减轻戒断症状。在本研究中,VLO内微量注射EX527抑制吗啡诱导CPP大鼠VLO内p-ERK、CREB、c-fos及PSD95表达的增高,这可能是EX527调节吗啡成瘾行为的关键机制。
综上所述,本研究发现吗啡诱导大鼠CPP形成后VLO内SIRT1表达增高,我们选用SIRT1抑制剂EX527对VLO内SIRT1进行干预,EX527通过降低SIRT1脱乙酰化酶活性,抑制吗啡引起的大鼠VLO内PSD95、c-fos、p-ERK、CREB等SIRT1下游分子表达的增高,并进一步抑制BDNF的表达,阻断了吗啡成瘾记忆的形成,进而干预了成瘾行为。本研究证实,VLO内SIRT1在吗啡成瘾中发挥重要作用,而CREB/BDNF通路则是SIRT1调控吗啡成瘾的关键机制。本研究为寻找吗啡成瘾治疗靶点提供了新的证据,对开发新的吗啡成瘾治疗药物及手段具有重要的价值。
| [1] |
Listos J, Lupina M, Talarek S, et al. The mechanisms involved in morphine addiction: An overview[J]. Int J Mol Sci, 2019, 20(17): 4302. doi:10.3390/ijms20174302 |
| [2] |
World Drug Report 2022, New York: United Nations Office On Drugs And Crime, 2022[EB/OL]. https://www.unodc.org/unodc/en/data-and-analysis/world-drug-report-2022.html.
|
| [3] |
Hamilton P J, Nestler E J. Epigenetics and addiction[J]. Curr Opin Neurobiol, 2019, 59: 128-36. doi:10.1016/j.conb.2019.05.005 |
| [4] |
Wei L, Liu B, Yao Z, et al. Sirtuin 1 inhibitor EX527 suppresses morphine-induced behavioral sensitization[J]. Neurosci Lett, 2021, 744: 135599. doi:10.1016/j.neulet.2020.135599 |
| [5] |
Xia B, Li Y, Li R, et al. Effect of Sirtuin-1 on synaptic plasticity in nucleus accumbens in a rat model of heroin addiction[J]. Med Sci Monit, 2018, 24: 3789-803. doi:10.12659/MSM.910550 |
| [6] |
Codocedo J F, Aliard C, Godoy J A, et al. SIRT1 regulates dendritic development in hippocampal neurons[J]. PLoS One, 2012, 7(10): e47073. doi:10.1371/journal.pone.0047073 |
| [7] |
Gao J, Wang W Y, Mao Y W, et al. A novel pathway regulates memory and plasticity via SIRT1 and miR-134[J]. Nature, 2010, 466(7310): 1105-9. doi:10.1038/nature09271 |
| [8] |
Miyashita T, Kikuchi E, Horiuchi J, et al. Long-term memory engram cells are established by c-Fos/CREB transcriptional cycling[J]. Cell Rep, 2018, 25(10): 2716-28. doi:10.1016/j.celrep.2018.11.022 |
| [9] |
Sun Z, Zhao S, Suo X, et al. Sirt1 protects against hippocampal atrophy and its induced cognitive impairment in middle-aged mice[J]. BMC Neurosci, 2022, 23(1): 33. doi:10.1186/s12868-022-00718-8 |
| [10] |
Paxinos G, Watson C. The Rat Brain in Stereotaxic Coordinates[M]. sixth edition, NewYork: Academic press, 2007: 456.
|
| [11] |
Ferguson D, Koo J W, Feng J, et al. Essential role of SIRT1 signaling in the nucleus accumbens in cocaine and morphine action[J]. J Neurosci, 2013, 33(41): 16088-98. doi:10.1523/JNEUROSCI.1284-13.2013 |
| [12] |
Yunusoglu O. Resveratrol impairs acquisition, reinstatement and precipitates extinction of alcohol-induced place preference in mice[J]. Neurol Res, 2021, 43(12): 985-94. doi:10.1080/01616412.2021.1948749 |
| [13] |
Cong L, Lei M Y, Liu Z Q, et al. Resveratrol attenuates manganese-induced oxidative stress and neuroinflammation through SIRT1 signaling in mice[J]. Food Chem Toxicol, 2021, 153: 112283. doi:10.1016/j.fct.2021.112283 |
| [14] |
Liang J, Zheng X, Chen J, et al. Roles of BDNF, dopamine D(3) receptors, and their interactions in the expression of morphine-induced context-specific locomotor sensitization[J]. Eur Neuropsychopharmacol, 2011, 21(11): 825-34. doi:10.1016/j.euroneuro.2010.12.006 |
| [15] |
Rezai M, Hajizadeh M R, Mahmoodi M, et al. Effect of methadone maintenance on expression of BDNF and CREB genes in brain VTA of male morphine treated rats[J]. Cent Nerv Syst Agents Med Chem, 2021, 21(3): 181-6. doi:10.2174/1871524922666211223153555 |
| [16] |
Jorjani H, Joneidi M, Vafaei A A, et al. Microinjection of the BDNF receptor antagonist ANA-12 into the nucleus accumbens and medial-prefrontal cortex attenuates morphine-induced reward memory, and alterations of BDNF levels and apoptotic cells in rats[J]. Pharmacol Biochem Behav, 2021, 201: 173111. doi:10.1016/j.pbb.2021.173111 |
| [17] |
杨根梦, 何翠华, 洪仕君, 等. NR2B/CREB在人参皂苷Rb1调节甲基苯丙胺诱导大鼠条件位置偏爱中的作用[J]. 中国药理学通报, 2020, 36(5): 604-8. Yang G M, He C H, Hong S J, et al. Role of NR2B and CREB in ginsenoside Rb1 regulation of methamphetamine-induced conditioned place preference in rats[J]. Chin Pharmacol Bull, 2020, 36(5): 604-8. |
| [18] |
Ahmad A, Ali T, Park H Y, et al. Neuroprotective effect of fisetin against amyloid-beta-induced cognitive/synaptic dysfunction, neuroinflammation, and neurodegeneration in adult mice[J]. Mol Neurobiol, 2017, 54(3): 2269-85. doi:10.1007/s12035-016-9795-4 |