

2. 安徽中医药大学新安医学教育部重点实验室,安徽 合肥 230038;
3. 安徽中医药大学药学院,安徽 合肥 230012;
4. 安徽中医药大学生命科学学院,安徽 合肥 230012
 ,
CHEN Shi-yu1,2,
WU Xiao-hong1,2,
YE Ming-jun2,3,
ZHU Ting2,3,
ZHU Ji-min2,4,
LI Qing-lin2,3
,
CHEN Shi-yu1,2,
WU Xiao-hong1,2,
YE Ming-jun2,3,
ZHU Ting2,3,
ZHU Ji-min2,4,
LI Qing-lin2,3

2. Key Laboratory of Xin'an Medicine, the Ministry of Education, Anhui University of Chinese Medicine, Hefei 230038, China;
3. School of Pharmacy, Anhui University of Chinese Medicine, Hefei 230012, China;
4. School of Life Sciences, Anhui University of Chinese Medicine, Hefei 230012, China
肺腺癌是一种常见肺癌,因其发病隐蔽,发现时多已失去最佳手术时机,故化疗是其基本治疗手段[1]。临床观察表明,肿瘤患者多存在凝血功能异常,如D-二聚体增高,表现为静脉血栓形成倾向,即高凝状态(hypercoagulable state,HCS)[2]。HCS既促进肿瘤增长,又降低化疗效果[2-3];化疗同期给予抗凝药物可改善患者HCS,增强化疗效果[4-5]。但西药抗凝存在诸多问题,如实验室检测的滞后性、受限于特定肿瘤细胞的类型和分期、抗凝不足易导致血栓形成、抗凝过度则易增加出血风险等[6-7]。由于肿瘤HCS中医辨证为血瘀证,故可采用活血化瘀法干预。桃红四物汤(Taohong Siwu Decotion,TSD)是活血化瘀经方,可有效治疗血瘀证[8-9],推测其可增强顺铂(cisplatin,DDP)这一化疗基本药物的抗肿瘤作用,但是相关研究鲜见。本研究通过动物实验探究了TSD改善肿瘤HCS,增强DDP抑制肺腺癌的效果。
1 材料与方法 1.1 材料 1.1.1 动物与细胞6周龄SPF级的C57小鼠,SCXK(浙)2019-0004,体质量(18~20) g,由浙江子源科技有限公司提供。鼠源肺腺癌细胞系Lewis(Lewis lung carcinoma,LLC)由中国科学院上海细胞研究所惠赠,稳定传至4~5代备用。研究方案获得安徽中医药大学动物伦理委员会的批准。
1.1.2 药物制备TSD各组方药材均为安徽济人药业有限公司赠送,并经安徽中医药大学王玉凤副教授鉴定。按中国中医药出版社第10版《方剂学》中复方配伍比例:桃仁9 g、红花6 g、熟地12 g、当归9 g、白芍9 g、川芎6 g,由安徽中医药大学第一附属医院制剂中心水煎提取浓缩为1.8 kg·L-1并消毒后,4 ℃冰箱冷藏备用。
1.1.3 试剂DDP(国药准字H20040813,规格6 mL:30 mg,批号601220102)购自江苏豪森药业股份有限公司,D-二聚体ELISA试剂盒(批号H416-1-1)购自南京建成生物工程研究所,多克隆抗体Ki67(批号GB111491)、TUNEL(批号G1501)均购自武汉赛维尔生物科技有限公司,Bcl-2(批号381702)、Bax(批号380709)、cleaved Caspase-3(批号341034)、cleaved Caspase-9(批号381336)均购自成都正能技术有限公司。
1.1.4 仪器Donatello脱水机(意大利DIAPATH公司);JB-P5包埋机(武汉俊杰电子有限公司);RM2016病理切片机(上海莱卡仪器有限公司);Eclipse C1正置荧光显微镜(日本尼康公司);DS-U3成像系统(日本尼康公司);Gelview6000plus化学发光成像分析系统(广东BLT生物科技有限公司);多功能酶标仪SpectraMax iD3(美谷分子仪器公司)。
1.2 方法 1.2.1 小鼠肺腺癌细胞移植瘤模型制备与分组于DMEM完全培养基、37 ℃、5% CO2培养箱中培养LLC,收集并制成2×109·L-1单细胞悬液,接种于小鼠右腋皮下0.1 mL(约2×105个)。接种后d 5将造模成功的小鼠随机分为4组:模型(Model)、TSD、DDP、TSD+DDP,另设正常对照组(Normal)。分组后当天给药,按照“人和动物体表面积折算的等效剂量比值表”计算小鼠等效剂量给予TSD,1.6 g·kg-1灌胃给药,1次·d-1,连续14 d;DDP参照临床化疗方案,腹腔注射0.45 mg·kg-1,100 μL,每周3次,连续2周[10]。
1.2.2 模型小鼠一般情况和移植瘤大小观察观察并记录小鼠的毛发、饮食、饮水、精神等情况,于给药d 0、3、7、10、14测量肿瘤体积。末次给药2 h后,将小鼠麻醉,脱颈处死,剥离瘤体并称质量。
1.2.3 HE染色和免疫组化检测瘤组织Ki67表达情况瘤体剥离后,立即放入4% PFA固定,1周后酒精脱水、浸蜡包埋,制作厚度为5~8 μm的连续切片,再经脱蜡、水化、清洗后,常规HE染色,封片后镜下观察肿瘤组织病理改变。免疫组化的切片经脱蜡修复后,加一抗、二抗孵育,经细胞核复染封片后镜下观察Ki67表达情况。
1.2.4 荧光染色法检测肿瘤细胞凋亡情况肿瘤组织切片经脱蜡至水后,滴加蛋白酶K修复,37 ℃孵育22 min;破膜工作液常温孵育20 min,切片稍甩干,滴加buffer后室温平衡10 min;滴加TUNEL反应液,37 ℃避光孵育2 h,PBS洗涤,滴加DAPI染液,避光孵育10 min,再经PBS洗涤,稍甩干,用抗荧光淬灭剂封片。盖好盖玻片,于荧光显微镜下观察细胞凋亡情况,绿色荧光提示为凋亡细胞。
1.2.5 Western blot法检测Bcl-2、Bax、cleaved Caspase-3、cleaved Caspase-9蛋白表达量取部分肿瘤组织,液氮中研磨后加入细胞裂解液,12 000 r·min-1离心20 min取上清液,BCA法蛋白定量后加入上样缓冲液,沸水浴10 min后备用。经电泳、转膜、封闭后,加入一抗,4 ℃摇床孵育过夜,洗膜后加入二抗,常温孵育1 h,暗室中曝光、显影。应用ImageJ分析灰度值,以GAPDH为内参计算蛋白相对表达量。
1.2.6 ELISA法检测小鼠血浆D-二聚体含量小鼠麻醉后,摘眼球取血于抗凝管,提取血浆后,采用ELISA试剂盒检测血浆中D-二聚体含量。
1.2.7 统计学处理采用ImageJ 1.8.0、GraphPad Prism 8.0.2、Adobe Photoshop 7.0.1以及Adobe Illustrator CC 2018等软件进行数据整理与统计分析。定量资料以x±s表示。两组间的比较采用成组样本t检验。各处理组效应的差异先采用单因素方差分析,再以LSD检验进行多重比较。TSD与DDP间的交互作用分析采用析因设计资料的方差分析。
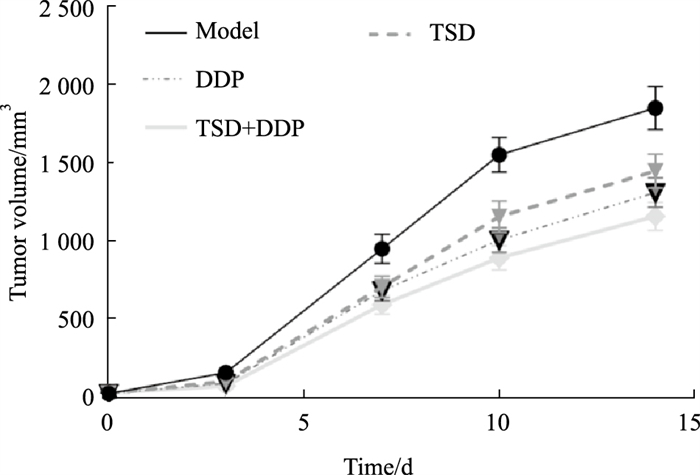
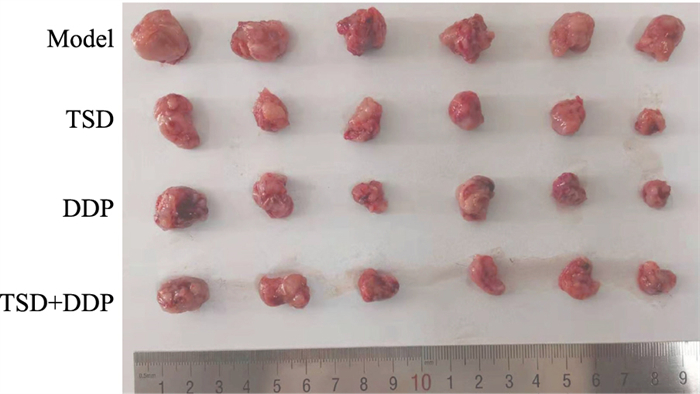
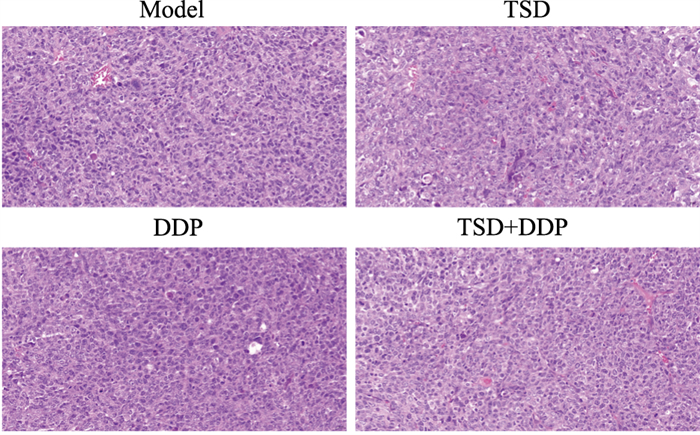
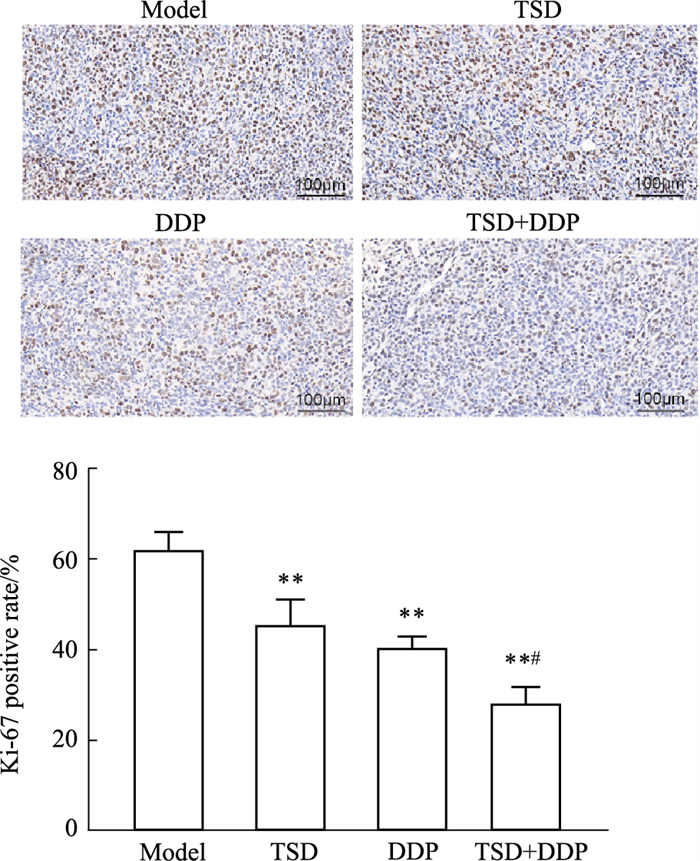
2 结果 2.1 TSD增强DDP对肺腺癌移植瘤增殖的抑制作用成瘤后,模型组小鼠逐渐出现精神萎靡、反应迟钝现象,爪甲口鼻苍白、毛发色淡无光泽;TSD和DDP联用组小鼠上述现象出现延迟且相对较轻。由Fig 1可见,随着干预时间的延长,四组移植瘤体积均呈增长趋势,其中模型组增速最快,TSD和DDP联用组增速相对较慢。移植瘤质量以模型组最大,3个给药组的瘤质量均低于模型组(P < 0.05),但TSD和DDP联用组的瘤质量与单用DDP组的差异未见统计学意义(Fig 2、Tab 1)。瘤组织经HE染色,镜下可见细胞核形状不一、大小不等,符合癌细胞的特征;TSD和DDP联用组以及单用DDP组可见较多的毛细血管(Fig 3)。Ki67可标记增殖周期中的细胞,其阳性率高提示细胞增殖速度快。免疫组化结果显示,TSD和DDP联用组的Ki67表达水平最低(28.3%±3.1%,n=6),且其与单用DDP组(40.3%±2.1%,n=6)间的差异有统计学意义(Fig 4)。进一步分析发现,TSD与DDP对瘤重(F=3.525、P=0.075)和Ki67表达率(F=1.146、P=0.316)都存在交互作用趋势,但差异未见统计学意义(P>0.05)。
|
| Fig 1 Volume change trends of migrated tumors |
|
| Fig 2 Gross morphology of migrated tumors |
| Group | Weight/g |
| Model | 1.87±0.34 |
| TSD | 1.34±0.35* |
| DDP | 1.30±0.33* |
| TSD+DDP | 1.28±0.32* |
| *P < 0.05 vs Model group | |
|
| Fig 3 HE staining results of migrated tumors |
|
| Fig 4 Immunohistochemistry results for Ki67 expression in migrated tumors **P < 0.01 vs Model group, #P < 0.05 vs DDP group. |
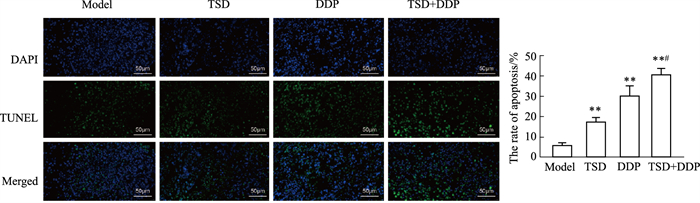
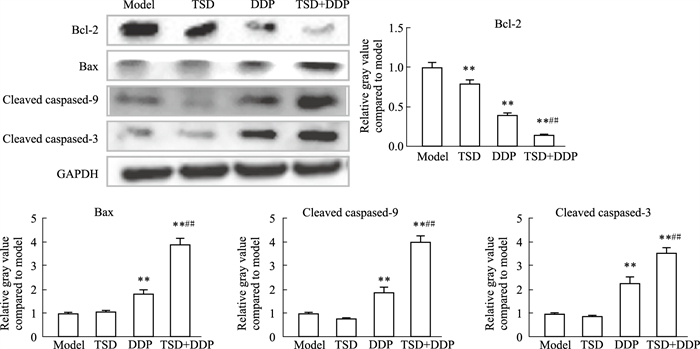
TUNEL染色是原位检测细胞凋亡最敏感、快速、特异的方法。由Fig 5可见,TSD和DDP联用组的TUNEL阳性率(41.0%±3.0%,n=6)最高,与单用DDP组(30.7%±4.5%,n=6)间的差异有统计学意义。进一步采用Western blot法检测瘤组织中凋亡标志蛋白的表达水平,发现各干预组抗凋亡蛋白Bcl-2的表达量较模型组均减低,其中TSD和DDP联用组最低,且与单用DDP组间的差异有统计学意义;而各干预组促凋亡蛋白Bax、cleaved Caspase 9和cleaved Caspase 3的表达量较模型组均明显增加,其中TSD和DDP联用组最高,且与单用DDP组间的差异有统计学意义(Fig 6)。进一步分析TSD与DDP在促进肺腺癌细胞凋亡上是否存在交互作用,发现二者对4种凋亡蛋白的表达量均呈现出差异有统计学意义的交互作用(P < 0.05)。
|
| Fig 5 TUNEL staining results of migrated tumors **P < 0.01 vs Model group, #P < 0.05 vs DDP group. |
|
| Fig 6 Related expression level of four apoptosis-related proteins in migrated tumors measured via Western blot **P < 0.01 vs Model group, ##P < 0.01 vs DDP group. |
D-二聚体是经典的血栓标志物。本研究采用ELISA法检测了各组小鼠血浆中的D-二聚体含量,发现模型组的D-二聚体含量明显高于正常组,也高于各干预组;其中TSD和DDP联用组和单用DDP组均较低,且差异有统计学意义(Tab 2)。
| Group | D-dimer/μg·L-1 |
| Normal | 124.50±22.77 |
| Model | 457.70±88.25* |
| TSD | 123.30±53.06## |
| DDP | 269.80±35.92# |
| TSD+DDP | 188.50±28.46 & |
| *P < 0.05 vs Normal group,#P < 0.05,##P < 0.01 vs Model group; & P < 0.05 vs DDP group. | |
《素问·阴阳应象大论》曰:“所谓血实者宜决之”。临床观察发现气滞血瘀为肺癌的主要证型[11-12],故治则上多以活血化瘀为主[13]。现代医学也发现,肿瘤患者特别是中晚期的恶性肿瘤患者,血液HCS现象明显,肺腺癌也不例外[14]。HCS除增加严重肺栓塞和静脉血栓栓塞风险,还能帮助肿瘤细胞逃避免疫杀伤,阻碍化疗药物与肿瘤细胞的有效接触,降低癌细胞对化疗药的敏感性[2-3, 15]。
本研究采用动物实验,首先观察了干预对移植瘤大小的影响,发现TSD和DDP联用,既可减弱移植瘤体积的增长速度,又可以降低移植瘤的重量;但联用组与单用DDP组的抑瘤作用差异无统计学意义。然后,从分子水平观察干预对肿瘤细胞增殖的影响,发现TSD和DDP联用组移植瘤组织的Ki67表达水平低于单用DDP组。接着,采用荧光染色和免疫印迹技术观察了干预对肿瘤细胞凋亡的影响,发现TSD和DDP联用组移植瘤组织的凋亡标志分子TUNEL以及促凋亡蛋白Bax、cleaved Caspase 9和cleaved Caspase 3的表达量均明显高于单用DDP组,而抗凋亡蛋白Bcl-2的表达量则较单用DDP组低。最后,检测比较了干预对模型鼠血液凝血状态的影响,发现TSD和DDP联用组模型鼠血浆的D-二聚体表达水平较单用DDP组低。研究结果提示,TSD可能增强了DDP对肺腺癌移植瘤的抑制作用,表现为抑制癌细胞增殖,促进癌细胞凋亡。
TSD增加DDP化疗效果的作用可能与其改善血液HCS,使得DDP更容易与癌细胞发生有效接触,进而为DDP发挥抑瘤作用有关;同时,TSD也可能提高了NK细胞活性以及CD3+、CD4+、CD4+/CD8+等T淋巴细胞表达量等,而增强机体的免疫功能[16]。类似的,田虎等[13]研究发现,中医药干预HCS疗效确切,既可改善肿瘤患者HCS提高肿瘤疗效,又可预防低分子肝素等西药引起的不良事件。于弘等[11]报道中药与放化疗等西医手段有协同作用,中西医结合可提高肺癌治疗效果。黄燕花等[17]研究发现,阿司匹林可促进5-氟尿嘧啶(5-fluorouracil,5-FU)对食管癌的治疗作用,包括抑制癌细胞增殖并促进癌细胞凋亡。而阿司匹林增强化疗的作用可能与其抑制血小板活化,进而降低肿瘤HCS等有关[18]。徐兴远[15]研究发现低分子肝素也可增强结直肠癌对5-FU的敏感性,提高Ⅲ期结直肠癌患者的3年无疾病生存率及总体生存率等。这些结果都与本研究的结果相似。
本研究还发现两个有趣的现象:①TSD单用也可抑制肺腺癌增殖;这可能与TSD改善血液高凝状态的同时,增加了机体免疫细胞和免疫分子与肿瘤细胞接触的机会有关[16],具体机制有待进一步研究。②TSD与DDP在抑制肿瘤细胞增殖上的交互作用接近,但未达到有统计学意义的标准(P=0.075),可能与样本量较小有关;然而,它们在促进肿瘤细胞凋亡上表则现出明显的交互作用(P < 0.05),这可能与DDP的抑瘤作用机制主要是破坏DNA,从而促进肿瘤细胞凋亡有关。本研究也存在一些局限性:仅构建一种肺腺癌移植瘤模型,这使得本研究结果的外推受限;干预后仅观察2周,随访时间可能会影响干预效应的充分展现;D-二聚体可能不足以全面反映血液的凝血状态,但作为经典的血栓标志物,D-二聚体单用也可有效反映肺癌患者化疗期间的凝血状态[2]。
综上可见,本研究采用同源肺腺癌移植小鼠模型,探究了DDP和中医活血化瘀经方TSD联用的抗肿瘤作用,发现TSD可能通过降低肿瘤HCS,增强了DDP对肺腺癌移植瘤的抑制作用,但具体作用机制还有待进一步研究。
( 致谢: 感谢安徽中医药大学王玉凤老师、安徽中医药大学第一附属医院制剂中心、安徽济人药业有限公司 )
| [1] |
Miller K D, Nogueira L, Mariotto A B, et al. Cancer treatment and survivorship statistics, 2019[J]. CA Cancer J Clin, 2019, 69(5): 363-85. doi:10.3322/caac.21565 |
| [2] |
Antoniou D, Pavlakou G, Stathopoulos G P, et al. Predictive value of D-dimer plasma levels in response and progressive disease in patients with lung cancer[J]. Lung Cancer, 2006, 53(2): 205-10. doi:10.1016/j.lungcan.2006.03.015 |
| [3] |
Versteeg H H, Spek C A, Peppelenbosch M P, et al. Tissue factor and cancer metastasis: The role of intracellular and extracellular signaling pathways[J]. Mol Med, 2004, 10(1-6): 6-11. doi:10.2119/2003-00047.Versteeg |
| [4] |
蔡夏水, 刘芯, 张还珠. 177例恶性肿瘤患者预防性抗凝治疗的疗效分析[J]. 广州医科大学学报, 2022, 50(1): 75-9. Cai X S, Liu X, Zhang H Z. Therapeutic efficacy of prophylactic anticoagulation therapy in 177 patients with malignant tumors[J]. Academic J Guangzhou Med Univ, 2022, 50(1): 75-9. |
| [5] |
Kiziltunc Ozmen H, Simsek M. Serum IL-23, E-selectin and sICAM levels in non-small cell lung cancer patients before and after radiotherapy[J]. J Int Med Res, 2020, 48(5): 300060520923493. |
| [6] |
Rayes R F, Mouhanna J G, Nicolau I, et al. Primary tumors induce neutrophil extracellular traps with targetable metastasis promoting effects[J]. JCI Insight, 2019, 5(16): e128008. |
| [7] |
Ren J H, He J Y, Zhang H J, et al. Platelet TLR4-ERK5 axis facilitates NET-mediated capturing of circulating tumor cells and distant metastasis after surgical stress[J]. Cancer Res, 2021, 81(9): 2373-85. doi:10.1158/0008-5472.CAN-20-3222 |
| [8] |
Ma Q, Li P L, Hua Y L, et al. Effects of Tao-Hong-Si-Wu decoction on acute blood stasis in rats based on a LC-Q/TOF-MS metabolomics and network approach[J]. Biomed Chromatogr, 2018, 32(4): 10. |
| [9] |
韩岚, 梁杰, 张艳艳, 等. 桃红四物汤对产后血瘀大鼠血清NO、子宫组织VEGF的表达及对PI3K/Akt信号通路的影响[J]. 中华中医药杂志, 2016, 31(5): 1625-9. Han L, Liang J, Zhang Y Y, et al. Effects of Taohong Siwu decoction on the VEGF, NO expression and PI3K/Akt pathway alterations in uterine tissue of postpartum rats with blood stasis syndrome[J]. Chin J Tradit Chin Med Pharm, 2016, 31(5): 1625-9. |
| [10] |
李白坤. 从瘀论治桃红四物汤干预肺腺癌细胞驯化血小板构筑转移前生态位的作用与机制[D]. 合肥: 安徽中医药大学, 2021. Li B K. Effects and mechanism of Taohong Siwu decoction in regulating the construction of premetastatic niche by lung adenocarcinoma cells educated platelets based on treating blood stasis[D]. Hefei: Anhui Univ Chin Med, 2021. |
| [11] |
于弘, 胡倩, 周光飚. 肺癌中医证型与用药规律的研究[J]. 中成药, 2022, 44(7): 2273-8. Yu H, Hu Q, Zhou G B. Study on traditional Chinese medicine syndromes and medication rules of lung cancer[J]. Chin Tradit Patent Med, 2022, 44(7): 2273-8. doi:10.3969/j.issn.1001-1528.2022.07.036 |
| [12] |
郭雯, 冯贞贞, 王露, 等. 基于文献的肺癌常见中医证候研究[J]. 中医杂志, 2021, 62(16): 1447-54. Guo W, Feng Z Z, Wang L, et al. Literature-based analysis of common traditional Chinese medicine syndromes of lung cancers[J]. J Tradit Chin Med, 2021, 62(16): 1447-54. |
| [13] |
田虎, 田思胜. 恶性肿瘤血液高凝状态的中医药治疗[J]. 中医杂志, 2019, 60(7): 572-5. Tian H, Tian S S. Traditional Chinese medicine intervention for high blood coagulation in malignant tumors[J]. J Tradit Chin Med, 2019, 60(7): 572-5. |
| [14] |
李晓晓, 马云飞, 李光达, 等. 恶性肿瘤血液高凝状态的发病机制及中西医治疗进展[J]. 世界中西医结合杂志, 2019, 14(11): 1619-23. Li X X, Ma Y F, Li G D, et al. The pathogenesis of blood hypercoagulability in malignant tumors and the progress of traditional Chinese and Western medicine treatment[J]. World J Integr Tradit West Med, 2019, 14(11): 1619-23. |
| [15] |
徐兴远. 低分子肝素对结直肠癌患者预后的影响及相关机制的研究[D]. 上海: 复旦大学, 2014. Xu X Y. Effect of low molecular weight heparin on survival in patients with colorectal cancer and its mechanisms[D]. Shanghai: Fudan Univ, 2014. |
| [16] |
焦艺博, 朱丽瑶, 刘征辉. 桃红四物汤对结肠癌术后患者疼痛及免疫功能影响研究[J]. 辽宁中医杂志, 2022, 49(11): 105-8. Jiao Y B, Zhu L Y, Liu Z H. Study on the effect of Taohong Siwu decoction on pain and immune function in patients with colon cancer after operation[J]. Liaoning J Tradit Chin Med, 2022, 49(11): 105-8. |
| [17] |
黄燕花, 王鲁妮, 刘泽, 等. 阿司匹林通过抑制β-catenin/EMT信号通路促进5-FU诱导食管癌细胞凋亡[J]. 中国药理学通报, 2020, 36(5): 655-9. Huang Y H, Wang L N, Liu Z, et al. Aspirin promotes apoptosis of esophageal cancer cells induced by 5-FU through inhibiting β-catenin/EMT signaling pathway[J]. Chin Pharmacol Bull, 2020, 36(5): 655-9. |
| [18] |
Hao W M, Shen Y X, Feng M X, et al. Aspirin acts in esophageal cancer: A brief review[J]. J Thorac Dis, 2018, 10(4): 2490-7. |