

动脉粥样硬化(atherosclerosis,AS)是一种慢性多因素疾病,与心血管疾病的发生、发展密切相关,其中内皮功能障碍是导致As的始动因素[1]。NLRP3炎症小体是由受体蛋白(NLRP3)、凋亡相关斑点样蛋白(ASC)和半胱氨酸天冬氨酸特异蛋白酶1前体(pro-caspase-1)组成的多蛋白复合物,激活后参与IL-1β和IL-18的活化与释放,并介导细胞焦亡[2]。细胞焦亡又称细胞炎性坏死,是一种程序性细胞死亡,由GasderminD蛋白(GSDMD)介导。研究表明[3],在NLRP3炎症小体激活后,受损的内皮细胞释放大量炎症介质,并诱导内皮功能障碍发生,最终促进As进展。同时[4-5],内皮细胞中激活的NLRP3炎症小体通过介导GSDMD活化,引起细胞膜孔的形成,进而发生细胞焦亡,从而加速内皮细胞丢失并导致心血管疾病。NLRP3炎症小体介导的pro-caspase-1激活是诱发细胞焦亡和炎症反应的关键机制之一[6]。因此,抑制pro-caspase-1的激活,可以有效降低细胞炎症和细胞焦亡的发生,从而改善内皮功能障碍,为治疗心血管疾病提供作用靶点。
灯盏花乙素(scutellarin,Scu)是一种天然黄酮类活性成分,具有抗炎[7-8]、抗癌[9-10]、抗氧化[11-12]等多种药理作用。研究表明[13-14],Scu对肺上皮细胞、心肌细胞中NLRP3、pro-caspase-1、ASC的表达具有调节作用,通过抑制NLRP3炎症小体激活,显著减少炎症因子活化水平并改善细胞焦亡。基于上述研究,探索Scu对血管内皮细胞炎症损伤和细胞焦亡的改善作用,将为筛选动脉粥样硬化治疗药物提供潜在目标。因此,该文以人脐静脉内皮细胞(human umbilical vein endothelial cells,HUVECs)为对象,通过LPS+ATP诱导建立炎症模型,探讨Scu对内皮细胞炎症损伤和细胞焦亡的调节作用和分子机制,为进一步临床实验提供理论依据。
1 材料与方法 1.1 材料 1.1.1 细胞原代人脐静脉内皮细胞(HUVCEs)购自ScienCell公司。
1.1.2 药品与试剂Scu(0329)购自上海瑞楚生物科技有限公司;Endothelial cell medium(ECM,1001)购自Sciencell technology;脂多糖(lipopolysaccharide,LPS)(L2880)和腺苷5′-三磷酸二钠盐水合物(ATP)(A2383)购自美国Sigma公司;pan-caspase抑制剂Z-YVAD-FMK(HY-P1009)购自MCE公司;3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(MTT)(103)购自美国Solarbio公司;乳酸脱氢酶(lactate dehydrogenase,LDH)检测试剂盒(A020-2)购自南京建成生物工程研究所;NLRP3抗体(DF7438)、caspase-1抗体(AF5418)、cleaved-caspase-1(Asp296),p20抗体(AF4005)和GSDMD抗体(AF4013)购自Affinity公司;ASC抗体(YT0365)购自Immunoway公司。caspase-1和GAPDH的qRT-PCR引物购自Invitrogen公司。
1.1.3 主要仪器HF240型二氧化碳培养箱(上海力申科学仪器有限公司);SW-CJ-2F单人双面净化工作台(苏州净化设备有限公司);Nikon ECLIPSE TS100-F(日本尼康公司);JT74-2晶体管鼓风电热恒温箱(浙江余姚低塘恒温箱厂);ELX800型酶联免疫检测仪(美国GE公司);CFX型凝胶成像系统、Mini-Protean Tetra电泳槽、Power Pace Basic基础电源、Trans-Blot转印槽(美国Bio-Rad公司)。
1.2 方法 1.2.1 原代细胞培养复苏后将HUVCEs细胞培养于ECM培养基中(双抗占总体积1%、血管内皮生长因子占总体积1%、胎牛血清占总体积5%),放置于含5% CO2、温度为37 ℃的恒温培养箱中,每隔1 d更换1次培养基,通过显微镜观察,当细胞占瓶底90%后进行传代。4~7代HUVCEs可收集用于实验。
1.2.2 实验分组及处理本研究分为药效和抑制剂两部分,药效实验分组为:Control组、LPS+ATP组(2.5 mg·L-1 LPS+2.5 mmol·L-1 ATP)、LDG组(0.2 μmol·L-1 Scutellarin+2.5 mg·L-1 LPS+2.5 mmol·L-1 ATP)、MDG组(1 μmol·L-1 Scutellarin+2.5 mg·L-1 LPS+2.5 mmol·L-1 ATP)、HDG组(5 μmol·L-1 Scutellarin+2.5 mg·L-1 LPS+2.5 mmol·L-1 ATP)。除Control组外,各组给予不同浓度的Scu预保护1 h后,加入LPS进行5.5 h活化,再加入ATP共同孵育0.5 h,结束后根据实验设计进行相应处理。抑制剂实验分组为:Control组、LPS+ATP组(2.5 mg·L-1 LPS+2.5 mmol·L-1 ATP)、HDG组(5 μmol·L-1 Scutellarin+2.5 mg·L-1 LPS+2.5 mmol·L-1 ATP)、YVAD组(1 μmol·L-1 Z-YVAD-FMK)、LAY组(1 μmol·L-1 Z-YVAD-FMK+2.5 mg·L-1 LPS+2.5 mmol·L-1 ATP)、LAYH组(1 μmol·L-1 Z-YVAD-FMK+5 mmol·L-1 Scutellarin+2.5 mg·L-1 LPS+2.5 mmol·L-1 ATP)。除Control组外,各组给予Scu或Z-YVAD-FMK预保护1 h后,加入LPS进行5.5 h活化,再加入ATP共同孵育0.5 h,结束后根据实验设计进行相应处理。
1.2.3 MTT实验检测细胞活力以1×105个·L-1密度的细胞接种于96孔板中,依据分组处理细胞后,采用MTT法检测细胞活力。计算公式:细胞存活率/%=实验组OD值/对照组OD值×100%。
1.2.4 乳酸脱氢酶(LDH)释放实验检测细胞的毒性损伤以1×105个·L-1密度的细胞接种于96孔板中,依据分组处理细胞并收集各组上清液,经离心后根据LDH检测试剂盒使用说明书进行操作,检测各组细胞上清液中LDH的含量。
1.2.5 酶联免疫吸附剂测定(enzyme-linked immunosorbent assay,ELISA)检测炎症因子的释放以1×108个·L-1密度的细胞接种于96孔板中,依据分组处理细胞并收集各组上清液,经离心后根据ELISA检测试剂盒使用说明书进行操作,检测各组细胞上清液中IL-1β、IL-18、HMGB-1的含量。
1.2.6 免疫印迹(Western blot,WB)法检测相关蛋白表达依据分组处理细胞后收集细胞,加入细胞裂解液(PMSF 1% ∶ RIPA 99%),冰上裂解30 min后提取总蛋白,采用BCA蛋白浓度检测进行定量。经10% SDS-PAGE电泳后,采用湿转法将已分离的蛋白转移0.22 μm PVDF膜上,5%脱脂奶粉室温封闭2 h,加入目标一抗后置于4 ℃冰箱孵育过夜。1×TBST洗膜3次,加入二抗室温孵育2 h。通过CFX型凝胶成像系统进行显影和数据分析。
1.2.7 qRT-PCR(quantitative real time PCR)法检测相关mRNA表达分组处理细胞后收集细胞,根据TransZol Up Plus RNA Kit试剂盒使用说明书提出总mRNA,利用超微量紫外分光光度仪测定mRNA浓度。根据TransScript Frist-Strand cDNA Synthesis SuperMix试剂盒使用说明书,以mRNA为模板,合成cDNA。用目的基因设计引物,利用Universal Hood Ⅱ型实时荧光定量PCR系统进行扩增和检测。PCR引物序列见Tab 1,其中GAPDH为内参。
| Gene | Forward primer(5′ to 3′) | Reverse primer (5′ to 3′) |
| caspase-1 | TCACTGCTTCGGACATGACT | GGCCTGGATGATGATCACCT |
| GAPDH | CAGGAGGCATTGCTGATGAT | GAAGGCTGGGGCTCATTT |
所有实验独立(n≥3),实验数据均采用x±s表示,采用GraphPad Prism7软件进行统计学处理。采用单因素方差分析和t检验对数据进行组间分析比较。
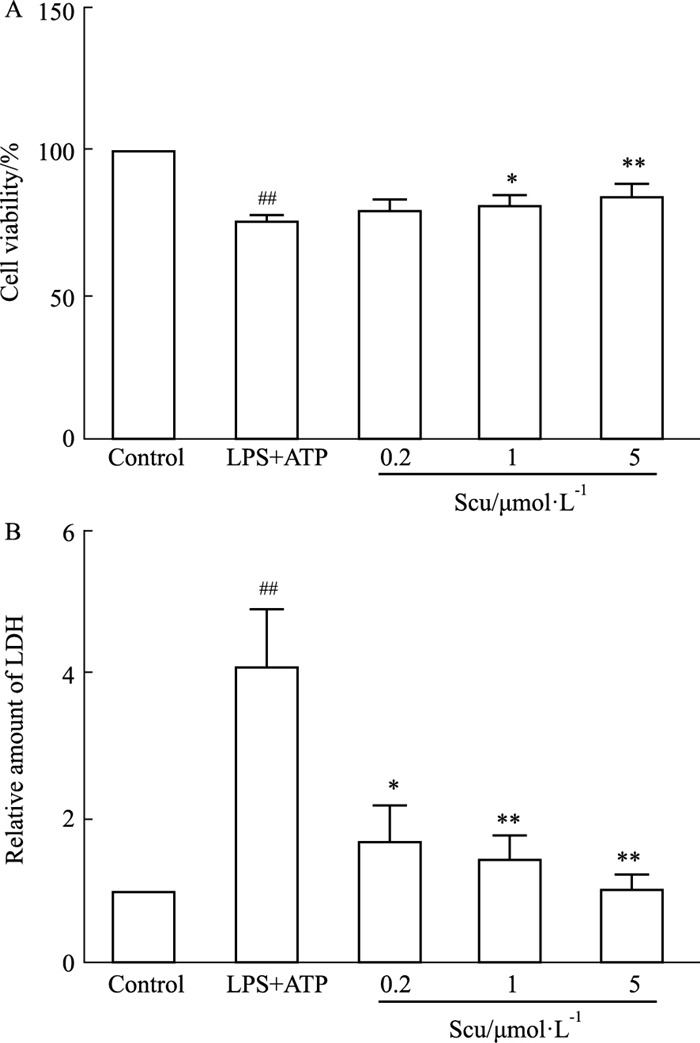
2 结果 2.1 Scu对LPS+ATP诱导细胞毒性损伤的影响MTT实验结果发现,与Control组比较,LPS+ATP组可明显降低细胞活力(P<0.01)。与LPS+ATP组比较,给予Scu预保护后,细胞活性随给药浓度提升而增加,其中HDG组最显著(P<0.01),如Fig 1A所示。
|
| Fig 1 Effect of Scu on LPS+ATP induced cytotoxic injury (x±s, n=3, 5) A.Cell viability enhanced by Scu; B.Inhibitory effect of Scu on LDH release rate after cell injury; ##P < 0.01 vs Control; *P < 0.05, **P < 0.01 vs LPS+ATP |
检测细胞上清中LDH含量,与Control组比较,LPS+ATP组细胞上清中LDH含量显著增加(P<0.01);与LPS+ATP组比较,给予Scu预保护后,LDH含量逐渐降低,其中HDG组最明显(P<0.01),如Fig 1B所示。结果说明,Scu可浓度依耐性改善LPS+ATP诱导的内皮细胞毒性损伤。
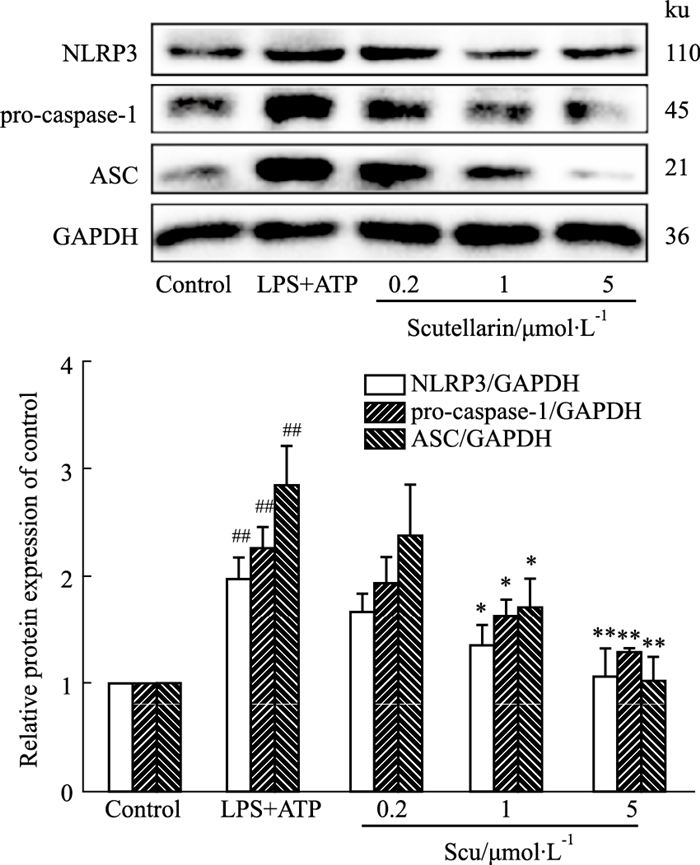
2.2 Scu对NLRP3炎症小体组成蛋白NLRP3、ASC和pro-caspase-1表达的影响与Control组比较,LPS+ATP组细胞中NLRP3、ASC和pro-caspase-1的表达明显增加(P<0.01);与LPS+ATP组比较,给予Scu预保护后,细胞中NLRP3、ASC和pro-caspase-1的表达梯度减少,其中HDG组最明显(P<0.01),如Fig 2所示。结果说明Scu呈剂量依赖性抑制内皮细胞中炎症小体的产生。
|
| Fig 2 Effect of Scu on expression of NLRP3 inflammasome related proteins including NLRP3, ASC and pro-caspase-1 (x±s, n=3) ##P < 0.01 vs Control; *P < 0.05, **P < 0.01 vs LPS+ATP |
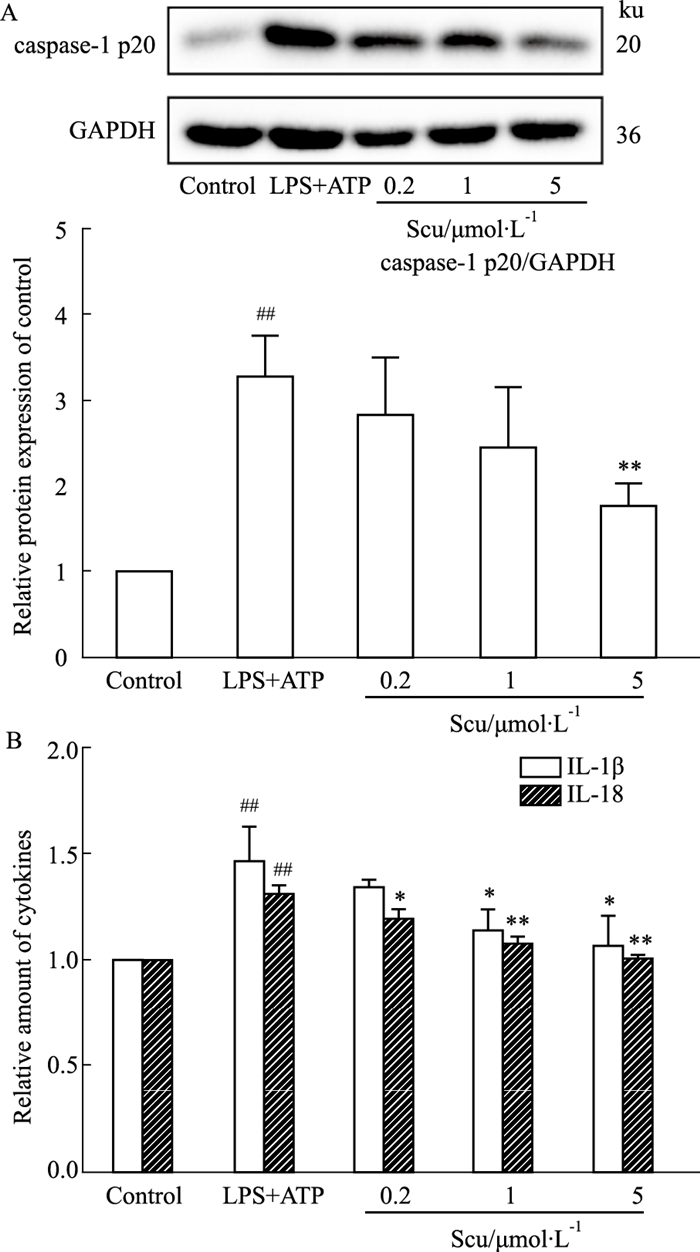
内源性刺激因子ATP可以诱导细胞内NLRP3炎症小体的活化,caspase-1 p20的产生和成熟的IL-1β、IL-18释放是NLRP3炎症小体活化的标志。通过western blot法对细胞中caspase-1 p20检测,与Control组比较,LPS+ATP组的caspase-1 p20表达增加(P<0.01);与LPS+ATP组比较,给予Scu预保护后呈浓度依赖性减少(P<0.05),如Fig 3A所示。通过ELISA法检测细胞上清中IL-1β、IL-18含量,与Control组比较,LPS+ATP组的IL-1β、IL-18含量增加(P<0.01);与LPS+ATP组比较,给予Scu预保护后呈浓度依赖性减少(P<0.05),如Fig 3B所示。结果说明,Scu通过降低caspase-1p20的产生和IL-1β、IL-18的释放,抑制LPS+ATP诱导内皮细胞中NLRP3炎症小体的活化。
|
| Fig 3 Effect of Scu on LPS+ATP induced NLRP3 inflammasome activation (x±s, n=3) ##P < 0.01 vs Control; *P < 0.05, **P < 0.01 vs LPS+ATP |
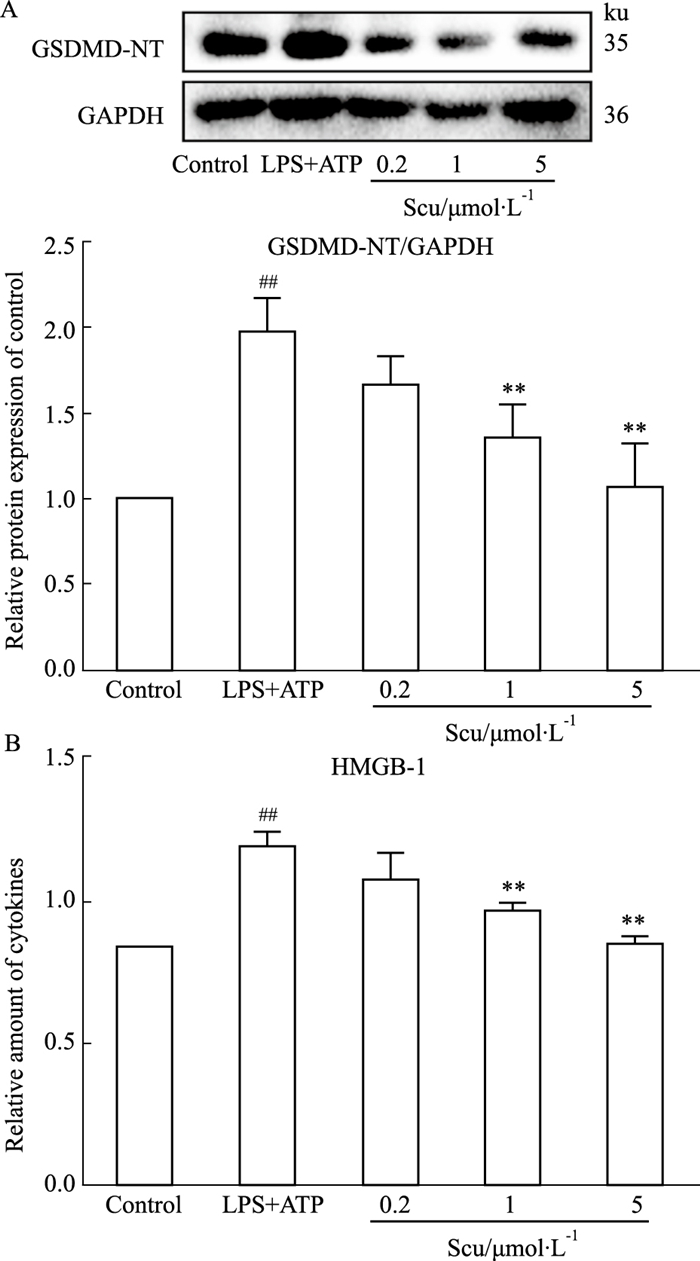
NLRP3炎症小体活化可介导焦亡效应蛋白GSDMD-NT的产生,诱使细胞发生焦亡并向胞外释放HMGB-1。通过Western blot法对细胞中GSDMD-NT检测,与Control组比较,LPS+ATP组的GSDMD-NT表达增加(P<0.01);与LPS+ATP组比较,给予Scu预保护后呈浓度依赖性减少,其中HDG组最明显(P<0.01),如Fig 4A所示。通过ELISA法检测细胞上清中HMGB-1含量,与Control组比较,LPS+ATP组的HMGB-1含量增加(P<0.01);与LPS+ATP组比较,给予Scu预保护后呈浓度依赖性减少,其中HDG组最明显(P<0.01),如Fig 4B所示。结果说明,Scu通过降低GSDMD-NT的产生和HMGB-1的释放,抑制LPS+ATP诱导的内皮细胞焦亡。
|
| Fig 4 Effect of Scu on LPS+ATP induced pyroptosis (x±s, n=3) ##P < 0.01 vs Control; **P < 0.01 vs LPS+ATP |
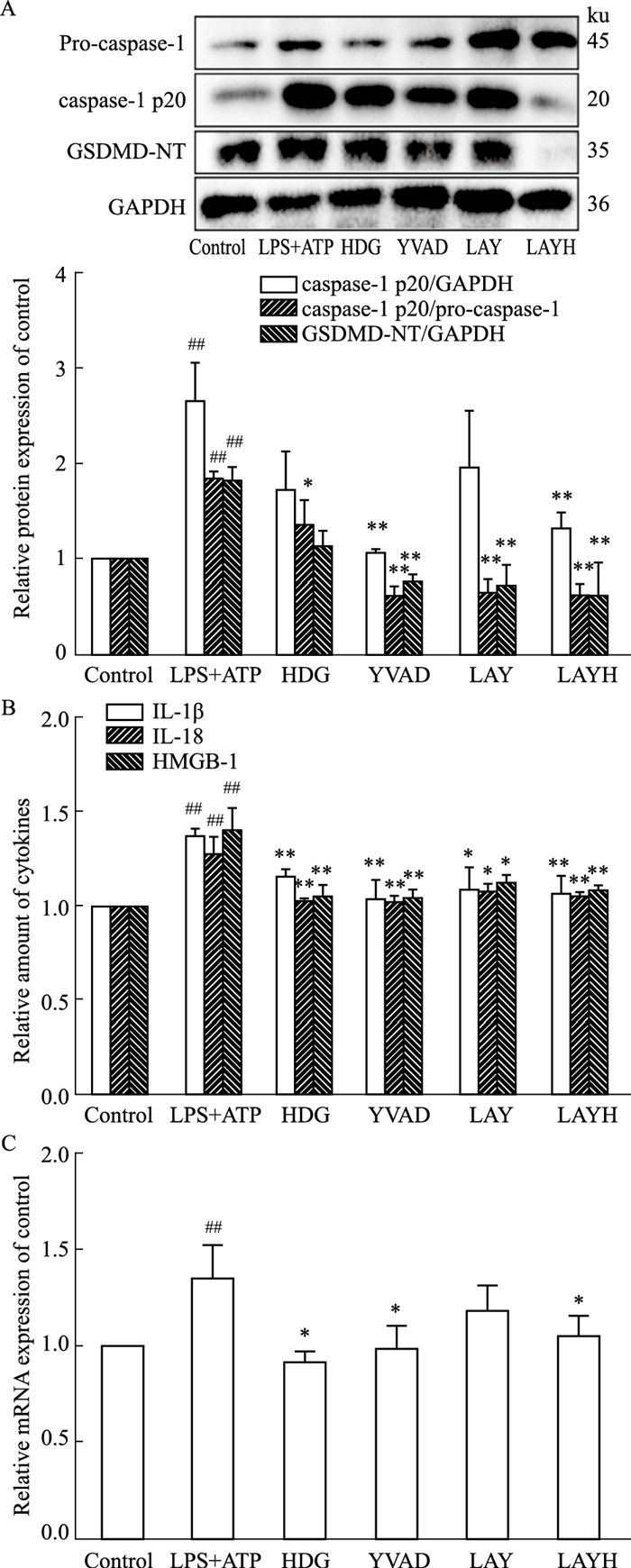
pro-caspase-1的活化可以介导IL-1β、IL-18的成熟释放和GSDMD-NT的生成,从而引起细胞炎症损伤和焦亡的发生。pan-caspase抑制剂Z-YVAD-FMK可以抑制pro-caspase-1的活化,以caspase-1 p20/ pro-caspase-1比值体现。通过Western blot法对细胞中pro-caspase-1、caspase-1 p20、GSDMD-NT检测,与LPS+ATP组比较,LAY组和LAYH组的caspase-1 p20/ pro-caspase-1比值均降低(P<0.05),且二者差异无显著性(P>0.05),如Fig 5A所示。与LPS+ATP组比较,LAY组和LAYH组的GSDMD-NT表达均降低(P<0.05),且二者无差异(P>0.05),如Fig 5A所示。与LPS+ATP组比较,LAY组caspase-1p20表达无显著差异,LAYH组表达降低(P<0.05),如Fig 5A所示。通过ELISA法检测细胞上清中IL-1β、IL-18、HMGB-1含量,与LPS+ATP组比较,LAY组和LAYH组的含量表达均降低(P<0.05)且二者无差异(P>0.05),如Fig 5B所示。通过PCR检测caspase-1mRNA表达水平,与LPS+ATP组比较,LAY组无差异,LAYH组表达降低(P<0.05),Fig 5C所示。结果说明,通过抑制pro-caspase-1的生成和活化,Scu对LPS+ATP诱导HUVECs的炎症损伤和细胞焦亡发挥改善作用。
|
| Fig 5 Scu improved inflammation and pyroptosis in LPS+ATP induced HUVECs by inhibiting activation of pro-caspase-1 (x±s, n=3) ##P < 0.01 vs Control; *P < 0.05, **P < 0.01 vs LPS+ATP |
NLRP3炎症小体参与内皮细胞损伤的发生和发展过程[15],并通过介导细胞焦亡进一步诱导心血管疾病的发生[16]。研究表明[17],当细胞中NLRP3炎性小体途径被激活,相关蛋白NLRP3、ASC、pro-caspase-1表达增加。随着炎症小体被组装活化,结构改变的NLRP3炎性小体诱导pro-caspase-1激活。Pro-caspase-1激活是细胞炎症反应和焦亡的关键环节,一方面,激活的caspase-1对Gasdermin D进行剪切,形成含有Gasdermin D氮端活性结构域的多肽(GSDMD-NT)。这种反应会导致内皮细胞膜破裂,内容物释放并引起炎症反应,同时内皮的完整性丧失。另一方面,pro-IL-1β和pro-IL-18被激活的caspase-1裂解为成熟的IL-1β和IL-18,并将它们释放到细胞外,招募炎症细胞并导致炎症细胞积聚,从而放大炎症。本研究结果显示,与LPS+ATP组比较,Scu组能降低内皮细胞中NLRP3、ASC、pro-caspase-1表达,表明其对NLRP3炎性小体生成具有抑制作用。同时减少IL-1β、IL-18、HMGB-1的释放和降低细胞焦亡相关蛋白GSDMD-NT的表达,表明对NLRP3炎性小体诱导的内皮细胞炎症损伤和细胞焦亡具有改善作用。和Scu /Z-YVAD-FMK联用组相比,Scu组对pro-caspase-1活化无差异,但能减少caspase-1 mRNA的表达,进一步说明Scu可以同时抑制pro-caspase-1的蛋白生成和活化。
综上所述,Scu能改善血管内皮细胞损伤,其机制是通过下调NLRP3/caspase-1通路,减少IL-1β、IL-18、HGBM-1的释放,改善内皮细胞的炎症损害,同时抑制GSDMD活化,减弱细胞焦亡的发生,从而达到进一步减轻内皮细胞损伤的作用。
| [1] |
Barquera S, Pedroza-Tobías A, Medina C, et al. Global overview of the epidemiology of atherosclerotic cardiovascular disease[J]. Arch Med Res, 2015, 46(5): 328-38. doi:10.1016/j.arcmed.2015.06.006 |
| [2] |
黄芷棋, 宁一博, 贺润铖, 等. NLRP3炎性小体与糖尿病心肌病的发生发展[J]. 中国药理学通报, 2021, 37(4): 463-7. Huang Z Q, Ning Y B, He R C, et al. NLRP3 inflammasome and development of diabetic cardiomyopathy[J]. Chin Pharmacol Bull, 2021, 37(4): 463-7. doi:10.3969/j.issn.1001-1978.2021.04.005 |
| [3] |
Bäck M, Yurdagul A J, Tabas I, et al. Inflammation and its resolution in atherosclerosis: Mediators and therapeutic opportunities[J]. Nat Rev Cardiol, 2019, 16(7): 389-406. |
| [4] |
Gimbrone MA Jr, García-Cardeña G. Endothelial cell dysfunction and the pathobiology of atherosclerosis[J]. Circ Res, 2016, 118(4): 620-36. doi:10.1161/CIRCRESAHA.115.306301 |
| [5] |
Qian Z, Zhao Y, Wan C, et al. Pyroptosis in the initiation and progression of atherosclerosis[J]. Front Pharmacol, 2021, 12: 652963. doi:10.3389/fphar.2021.652963 |
| [6] |
Chen R, Sun G, Yang L, et al. Salvianolic acid B protects against doxorubicin induced cardiac dysfunction via inhibition of ER stress mediated cardiomyocyte apoptosis[J]. Toxicol Res (Camb), 2016, 5(5): 1335-45. doi:10.1039/C6TX00111D |
| [7] |
Wang W, Li J, Li F, et al. Scutellarin suppresses cartilage destruction in osteoarthritis mouse LPS+ATP by inhibiting the NF-κB and PI3K/Akt signaling pathways[J]. Int Immunopharmacol, 2019, 77: 105928. doi:10.1016/j.intimp.2019.105928 |
| [8] |
Xu L, Chen R, Zhang X, et al. Scutellarin protects against diabetic cardiomyopathy via inhibiting oxidative stress and inflammatory response in mice[J]. Ann Palliat Med, 2021, 10(3): 2481-93. doi:10.21037/apm-19-516 |
| [9] |
Xiong L L, Du R L, Xue L L, et al. Anti-colorectal cancer effects of scutellarin revealed by genomic and proteomic analysis[J]. Chin Med, 2020, 15: 28. doi:10.1186/s13020-020-00307-z |
| [10] |
Liu F, Zu X, Xie X, et al. Scutellarin suppresses patient-derived xenograft tumor growth by directly targeting Akt in esophageal squamous cell carcinoma[J]. Cancer Prev Res (Phila), 2019, 12(12): 849-60. doi:10.1158/1940-6207.CAPR-19-0244 |
| [11] |
Wu H, Jia L. Scutellarin attenuates hypoxia/reoxygenation injury in hepatocytes by inhibiting apoptosis and oxidative stress through regulating Keap1/Nrf2/ARE signaling[J]. Biosci Rep, 2019, 39(11): BSR20192501. doi:10.1042/BSR20192501 |
| [12] |
Gao L, Tang H, Zeng Q, et al. The anti-insulin resistance effect of scutellarin may be related to antioxidant stress and AMPKα activation in diabetic mice[J]. Obes Res Clin Pract, 2020, 14(4): 368-74. doi:10.1016/j.orcp.2020.06.005 |
| [13] |
Peng L, Wen L, Shi Q F, et al. Scutellarin ameliorates pulmonary fibrosis through inhibiting NF-κB/NLRP3-mediated epithelial-mesenchLAYal transition and inflammation[J]. Cell Death Dis, 2020, 11(11): 978. doi:10.1038/s41419-020-03178-2 |
| [14] |
Xu L J, Chen R C, Ma X Y, et al. Scutellarin protects against myocardial ischemia-reperfusion injury by suppressing NLRP3 inflammasome activation[J]. Phytomedicine, 2020, 68: 153169. doi:10.1016/j.phymed.2020.153169 |
| [15] |
Pober J S, Sessa W C. Evolving functions of endothelial cells in inflammation[J]. Nat Rev Immunol, 2007, 7(10): 803-15. |
| [16] |
Patel P, Karch J. Regulation of cell death in the cardiovascular system[J]. Int Rev Cell Mol Biol, 2020, 353: 153-209. |
| [17] |
Ji N, Qi Z, Wang Y, et al. Pyroptosis: A new regulating mechanism in cardiovascular disease[J]. J Inflamm Res, 2021, 14: 2647-66. |

