

2. 南京大学医学院附属鼓楼医院药学部,江苏 南京 210008;
3. 南京中医药大学药学院,江苏 南京 210023;
4. 南京临床药学中心,江苏 南京 210008
梅洪梁(1990-),硕士,主管药师,研究方向:药理学和临床药学,共同通信作者,E-mail:liulidemao@126.com
2. Department of Pharmacy, Nanjing Drum Tower Hospital, The Affiliated Hospital of Nanjing University Medical School, Nanjing 210008, China;
3. School of Pharmacy, Nanjing University of Chinese Medicine, Nanjing 210023, China;
4. Nanjing Medical Center for Clinical Pharmacy, Nanjing 210008, China
糖尿病是一种有着持续高血糖症状的代谢性疾病[1]。机体的慢性高血糖状态是导致血管内皮功能异常的重要因素,最终可能导致血管病变,引起眼、肾脏、神经和心血管系统的并发症[2],给患者造成身体和经济上的负担,因此了解血管病变发生的机制及时防治糖尿病血管病变是改善糖尿病并发症的有效途径。血管内皮细胞(vasuclar endothelial cell,VEC)是心血管系统的第一层屏障[3],在血管病变中起着关键作用。血糖浓度过高诱导VEC发生氧化应激,使其分泌的细胞因子水平失调,引起细胞损伤和组织病变[4]。细胞内低水平的自噬可以降解部分氧化应激产生的代谢废物和受损的细胞器。而高血糖状态下,内皮细胞的自噬水平无法降解持续产生的多余代谢废物,过量活性氧累积、炎症体激活,多种细胞器功能受损,最终结果即是细胞死亡,血管病变开始发生。因此,靶向自噬治疗以减轻糖尿病血管病变有重要意义。
香菇多糖(lentinan,LNT)是从中药香菇中提取的活性成分,符合糖尿病血管病变的治疗法则。有研究显示LNT能调控自噬[5],减轻活性氧(reactive oxygen species,ROS)和过量一氧化氮(nitric oxide,NO)对膈肌线粒体的损伤[6]。
但目前尚未见LNT对VEC保护作用的相关研究。基于此,本研究以高糖(high concentration of glucose,HG)诱导人脐静脉内皮细胞(human umbilical vein endothelial cells,HUVECs)制备糖尿病状态下VEC损伤的病理模型[7],研究在HG损伤条件下LNT对HUVEC的保护作用以及相关机制,为糖尿病血管病变的防治提供新思路。
1 材料与方法 1.1 细胞HUVEC购自江苏恩莫阿赛生物技术有限公司。
1.2 药物纯度98%的LNT粉末购自北京索莱宝科技有限公司(批号SL8730)。
1.3 试剂香菇多糖粉末(纯度98%,北京索莱宝科技有限公司,货号:SL8730);纯度50%的无菌葡萄糖注射液(北京雷根生物技术有限公司,批号0615A20);DMEM无糖培养液、DMEM高糖培养液、胎牛血清(FBS)、胰酶、PBS(美国Gibco公司,批号分别为8120075、8114146、1619679、2186956、8120233);BCA试剂盒、ROS检测试剂盒、超氧化物歧化酶(superoxide dismutase,SOD)试剂盒、丙二醛(malondialdehyde,MDA)试剂盒、SDS-PAGE凝胶试剂盒(上海碧云天生物技术有限公司,批号分别为120219200629、213620200912、102620201202、073120201204、PA667);TUNEL试剂盒(美国Everbright公司,批号323D0101);兔源GAPDH抗体、兔源诱导型一氧化氮合酶(iNOS)抗体、兔源T-p38 MAPK抗体(武汉三鹰生物技术有限公司,批号00074988、00085538、00076424);兔源p-p38 MAPK抗体(美国Affinity公司,批号79d6101);辣根过氧化物(HRP)标记的山羊抗兔IgG二抗(英国Abcam公司,批号GR313248-1);CCK-8试剂盒(上海翌圣生物科技有限公司,批号C0001261)。
1.4 仪器MCO-15AC型CO2细胞培养箱(日本Sanyo公司);Synergy H1型多功能微孔板检测仪(美国BioTek公司);TDZ4-WS台式低速离心机(中国湘仪集团);SW-CJ-1F型超净工作台(苏州安泰空气技术有限公司);微孔板恒温振荡器(杭州奥盛仪器有限公司);荧光倒置显微镜(德国Carl Zeiss公司);307352型电泳仪、化学发光成像系统(美国Bio-Rad公司), Thermo NanoDrop One/One c超微量紫外分光光度计, ABI7500实时荧光定量PCR仪。
1.5 细胞培养在37 ℃、5% CO2条件下应用DMEM高糖培养基培养HUVEC,培养基中含10% FBS、100 kU·L-1青霉素、100 mg·L-1链霉素。每隔1~2 d换液,实验采用对数生长期的细胞(融合度70%~80%)进行。
1.6 药物工作液的配制 1.6.1 LNT工作液取LNT 20 mg,溶解于8 mL DMEM无糖培养基配制成浓度为25 g·L-1的母液,于4 ℃下保存;使用前,用DMEM无糖培养基稀释至相应浓度的工作液。
1.6.2 HG溶液的配制取2.592 mL葡萄糖溶液,稀释于25 mL无糖DMEM培养基中,配制成浓度为240 mmol·L-1的HG母液,于4 ℃下保存,使用时按需用DMEM无糖培养基稀释至相应浓度的工作液。
1.7 CCK-8法检测HUVEC活力 1.7.1 HG对HUVEC活力的影响取处于对数生长期的HUVEC,胰酶消化后以含FBS的高糖DMEM培养基制备细胞悬液,将细胞以每孔约5 000个接种于96孔板,每孔细胞悬液体积为100 μL。HUVEC培养8~12 h贴壁后,随机分为空白对照组和HG不同浓度处理组(40、80、120、160 mmol·L-1),再设置一组添加DMEM培养基,不含细胞的A0组,每组重复6个孔。弃去原先孔板中的培养基,无菌PBS洗涤后,各组加入含不同浓度HG且无FBS的DMEM培养基,空白对照组和A0组加入无糖无FBS的DMEM培养基。继续培养24 h后,弃去上清液,每孔加入含10%CCK-8的DMEM单培100 μL。2 h后应用酶标仪于波长450 nm处检测光密度(OD值),将空白对照组的OD值设置为细胞活力100%,计算各组的相对细胞活力。实验重复6次,取平均值。
1.7.2 LNT对HUVEC活力的影响细胞培养和种板方法同上,设置空白对照组和LNT不同质量浓度处理组(50、100、200、400、800 mg·L-1),以及A0组(含培养基但不含细胞)加入LNT后培养24 h,检测方法同上。实验重复6次,取平均值。
1.7.3 HG诱导损伤条件下,LNT对HUVEC活力的影响细胞培养和种板方法同上,设置6个实验组:空白对照组、HG损伤模型组、HG+LNT低剂量组(200 mg·L-1)、HG+LNT中剂量组(400 mg·L-1)、HG+LNT高剂量组(800 mg·L-1)、以及A0组,加药后培养24 h,检测方法同上。实验重复6次,取平均值。
1.8 DCFH-DA探针法检测HUVEC胞内ROS水平设置5个实验组:空白对照组、HG损伤模型组、HG+LNT低剂量组(200 mg·L-1)、HG+LNT中剂量组(400 mg·L-1)、HG+LNT高剂量组(800 mg·L-1),将HUVEC细胞按2×108·L-1接种于6孔板,加药培养24 h后,弃去上清,无菌PBS洗涤后加入DCFH-DA稀释试剂(按1 ∶ 1 000用不含血清的DMEM培养基稀释),DCFH-DA工作浓度为10 μmol·L-1,置于细胞培养箱中37 ℃孵育20~30 min。用无血清的培养基洗涤3次后,在荧光显微镜下观察各处理组荧光强度,荧光强度与胞内ROS水平呈正比。应用ImageJ 1.8.0软件分析图像,将空白对照组的荧光强度设置为100%。实验重复6次,取平均值。
1.9 黄嘌呤氧化酶法、硫代苯巴比妥酸法检测HUVEC的SOD、MDA水平分组方法同“1.8”,加药培养24 h后,裂解细胞,按照试剂盒说明书操作。实验重复6次,取平均值。
1.10 MDC染色法检测HUVEC的自噬水平设置6个实验组:空白对照组、HG损伤模型组、HG+LNT低剂量组(200 mg·L-1)、HG+LNT中剂量组(400 mg·L-1)、HG+LNT高剂量组(800 mg·L-1)、雷帕霉素(rapamycin,RAPA)阳性对照组。将HUVEC细胞按2×108个·L-1接种于6孔板,HG诱导损伤后,分别加入200、400、800 mg·L-1LNT处理,阳性药对照组加100 nmol·L-1 RAPA。24 h后,加入50 μmol·L-1 MDC孵育20 min,荧光显微镜观察拍照。应用ImageJ 1.8.0软件分析图像,将空白对照组的荧光强度设置为100%。实验重复6次,取平均值。
1.11 PCR法检测HUVEC自噬相关基因Beclin-1表达水平设置分组同1.10。细胞培养种板方法同上,给药培养24 h后,加入TRIzol和氯仿进行mRNA提取,将mRNA逆转录成cDNA,进行浓度测定后点板上机检测自噬相关的基因Beclin-1,引物序列见Tab 1。
| Gene | Forward (5′-3′) | Reverse (5′-3′) |
| Beclin-1 | CAAGATCCTGGACCGTGTCA | TGGCACTTTCTGTGGACATCA |
| GAPDH | TGCTGGTGCTGAGTATGTCG | GCATGTCAGATCCACAACGG |
细胞种板培养方法同上,各组细胞加药培养24 h后,弃去上清,用PBS清洗后,在6孔板中加入含苯甲基磺酰氟(PMSF)的RIPA裂解液90 μL。冰上充分裂解后,在4 ℃,12 000 r·min-1条件下离心20 min,取上清总蛋白液进行BCA法定量。将各组蛋白浓度调至统一后,100 ℃水浴锅中煮10 min,将蛋白变性。上样时各组取等量样本,进行SDS-PAGE分离后转移至聚偏二氟乙烯(PVDF)膜,室温下5%脱脂牛奶封闭2 h。加入一抗4 ℃孵育过夜。用三羟甲基氨基甲烷盐酸盐(TBST)溶液洗涤5次,每次10 min,随后孵育二抗,于室温孵育1 h。TBST清洗5次后采用ECL显影液显色,于化学发光成像系统成像。应用ImageJ 1.8.0软件分析图像的灰度值,以GAPDH为内参计算所测蛋白的表达水平。实验重复3次,取平均值。
1.13 统计学方法采用SPSS 23.0软件统计分析数据。计量资料用x±s表示,单因素方差分析,两组间比较用t检验。
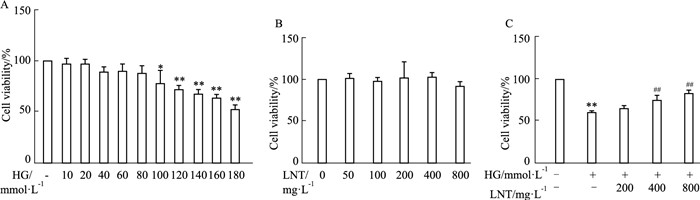
2 结果 2.1 CCK-8实验确定HG、LNT作用的最佳浓度 2.1.1 HG作用浓度筛选不同浓度HG培养液作用于HUVEC后,与对照组相比,当HG的工作浓度为120 mmol·L-1时,HUVEC开始出现活力明显下降(P<0.01),如Fig 1A所示;HG工作浓度达到180 mmol·L-1时,HUVEC活力下降程度约为正常对照组的一半(P <0.01)。这提示120 mmol·L-1的HG能引起适度的HUVEC损伤,后续实验选取120 mmol·L-1作为HG诱导HUVEC损伤的工作浓度。
|
| Fig 1 Activity of HUVECs (x±s, n=6) A: Effects of different concentrations of HG on relative activity of HUVECs; B: Effects of different concentrations of LNT on relative activity of HUVECs; C: Effects of different concentrations of LNT on activity of HUVECs under HG induced injury. *P<0.05, **P<0.01 vs control; ##P<0.01 vs HG. |
仅用LNT处理HUVEC并不影响细胞活力,这提示LNT对HUVEC不存在明显的细胞毒性,见Fig 1B。
2.1.3 LNT提高HG损伤下的细胞活力与空白对照组相比,仅用120 mmol·L-1的HG处理HUVEC降低了细胞活力(P<0.01);应用不同浓度LNT与HG共处理HUVEC时,与HG单独处理组相比,当LNT浓度达到400 mg·L-1和800 mg·L-1时,能明显改善HG诱导的HUVEC活力下降(P<0.01),见Fig 1C。这说明对于HG诱导的HUVEC活力下降,LNT能起到一定的改善作用。
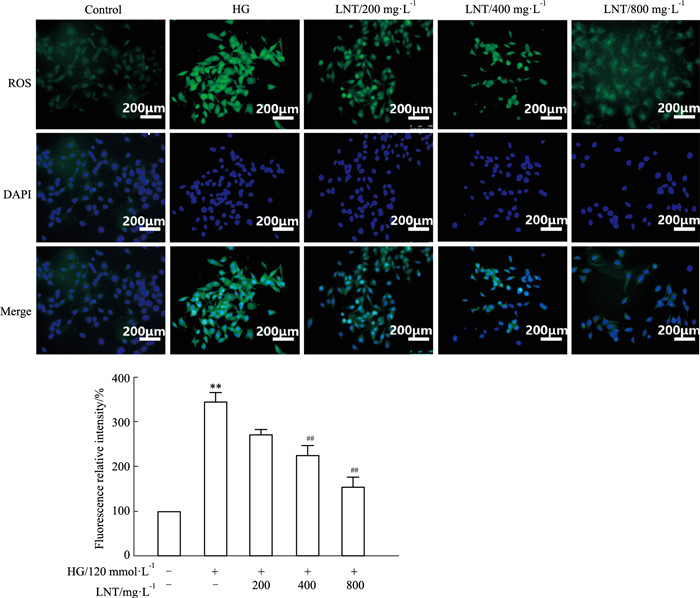
2.2 LNT抑制HG诱导ROS的产生与空白对照组相比,HG的处理增加了HUVEC胞内ROS水平(P<0.01)。同时与HG损伤组进行比较,LNT剂量依赖性地缓解HG引起的ROS增加,400 mg·L-1作用后差异有统计学意义(P<0.05),见Fig 2。这说明LNT可有效改善HG诱导的HUVEC胞内ROS堆积。
|
| Fig 2 Effects of LNT on intracellular ROS level of HUVECs induced by HG (x±s, n=6) **P<0.01 vs control; ##P<0.01 vs HG. |
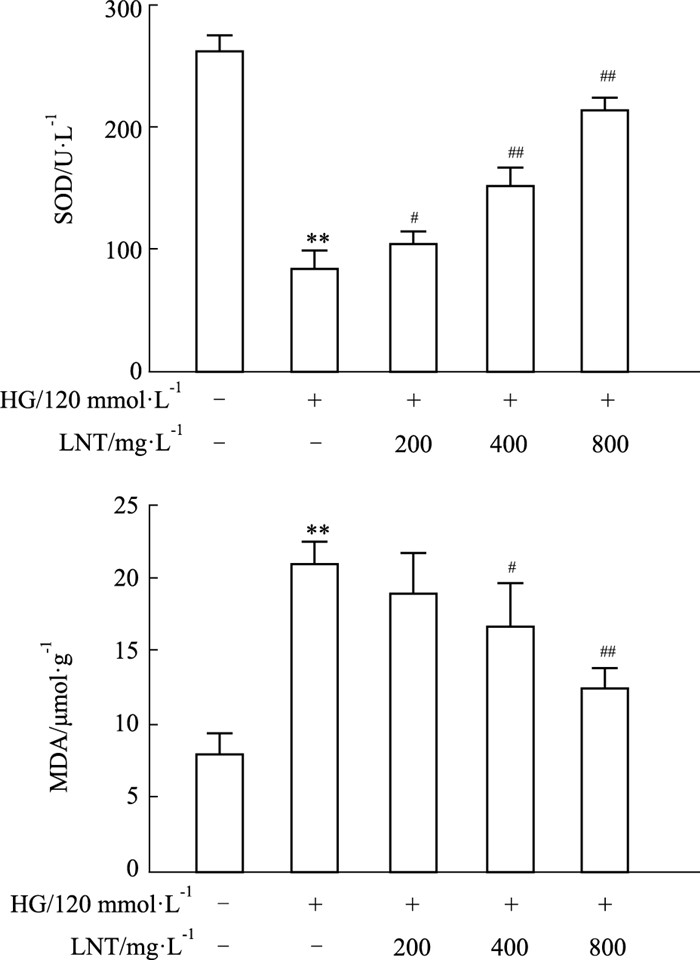
120 mmol·L-1的HG可明显降低HUVEC胞内SOD含量(P<0.01),增加MDA含量(P<0.01)。不同剂量LNT的处理能明显改善HG诱导的SOD降低,并呈剂量依赖性。同时400 mg·L-1的LNT即可有效降低HG引起的MDA水平增加(P<0.01),见Fig 3。
|
| Fig 3 SOD and MDA level of HUVECs (x±s, n=6) A. Effects of LNT on intracellular SOD level of HUVECs in HG induced injury; B. Effects of LNT on intracellular MDA level of HUVECs in HG induced injury. **P<0.01 vs control; #P<0.05, ##P<0.01 vs HG. |
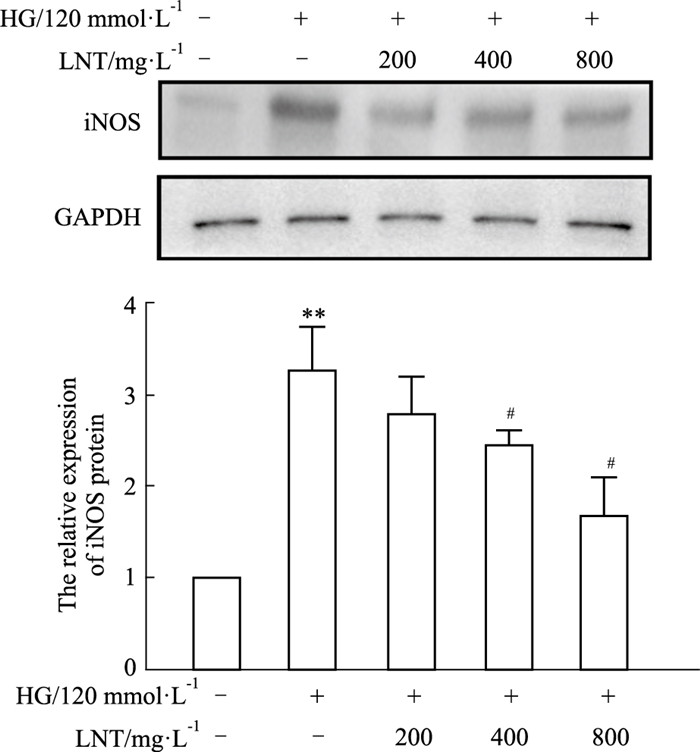
与空白对照组相比,HG的处理明显增强了HUVEC的iNOS蛋白表达(P<0.01),400 mg·L-1(P<0.05)和800 mg·L-1(P<0.01)的LNT能有效抑制HG引起的iNOS表达增加,见Fig 4。结果说明, LNT能通过减少ROS堆积和iNOS表达改善HG引起的HUVEC胞内氧化应激。
|
| Fig 4 Effects of LNT on iNOS protein expression in HG treated HUVECs (x±s, n=3) **P<0.01 vs control; #P<0.05 vs HG. |
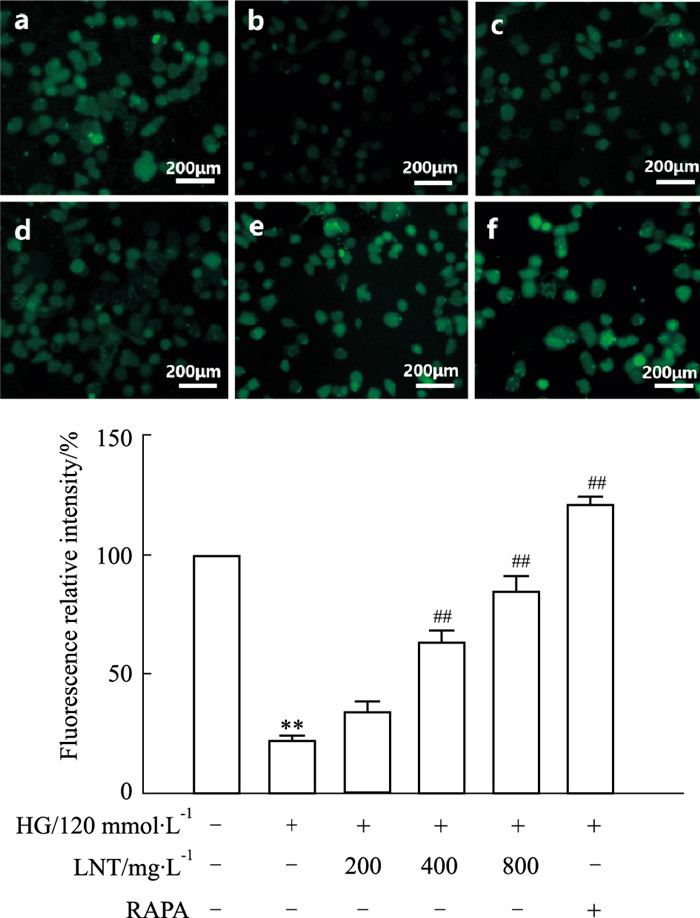
与对照组比较,120 mmol·L-1的HG可明显降低HUVEC胞内自噬水平(P<0.05)。400 mg·L-1、800 mg·L-1LNT都明显增加MDC染色标记的荧光颗粒水平,见Fig 5。RAPA是自噬诱导剂,此处用作为阳性参照。
|
| Fig 5 Effects of LNT on intracellular autophagy level of HUVECs in HG induced injury (x±s, n=6) a. Control; b. HG; c. LNT 200 mg·L-1; d. LNT 400 mg·L-1; e. LNT 800 mg·L-1; f. RAPA.**P<0.01 vs control, ##P<0.01 vs HG. |
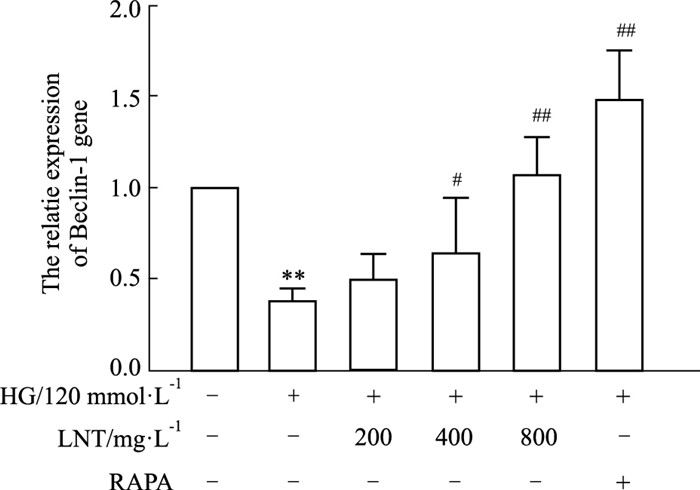
与空白对照组相比,HG的处理明显降低了HUVEC的Beclin-1基因表达(P<0.01),400 mg·L-1(P<0.05)和800 mg·L-1(P<0.01)的LNT能增加Beclin-1基因表达,见Fig 6。
|
| Fig 6 Effect of LNT on expression of HUVEC Beclin-1 gene treated with HG (x±s, n=6) **P<0.01 vs control; #P<0.05, ##P<0.01 vs HG. |
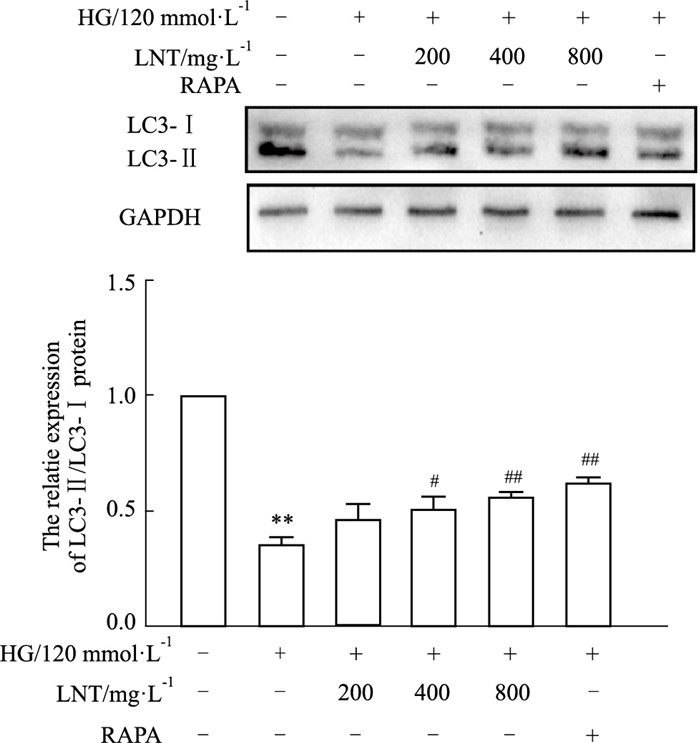
与空白对照组相比,HG的处理明显降低了HUVEC的LC3II/LC3I的蛋白表达(P<0.001),400 mg·L-1(P<0.05)和800 mg·L-1(P<0.01)的LNT能有效提高HG引起的LC3II/LC3I表达减少,见Fig 7。这部分结果说明LNT能提高HG诱导损伤下,细胞内的自噬水平。
|
| Fig 7 Effects of LNT on LC3 protein expression in HG treated HUVECs (x±s, n=3) **P<0.01 vs control; #P<0.05, ##P<0.01 vs HG. |
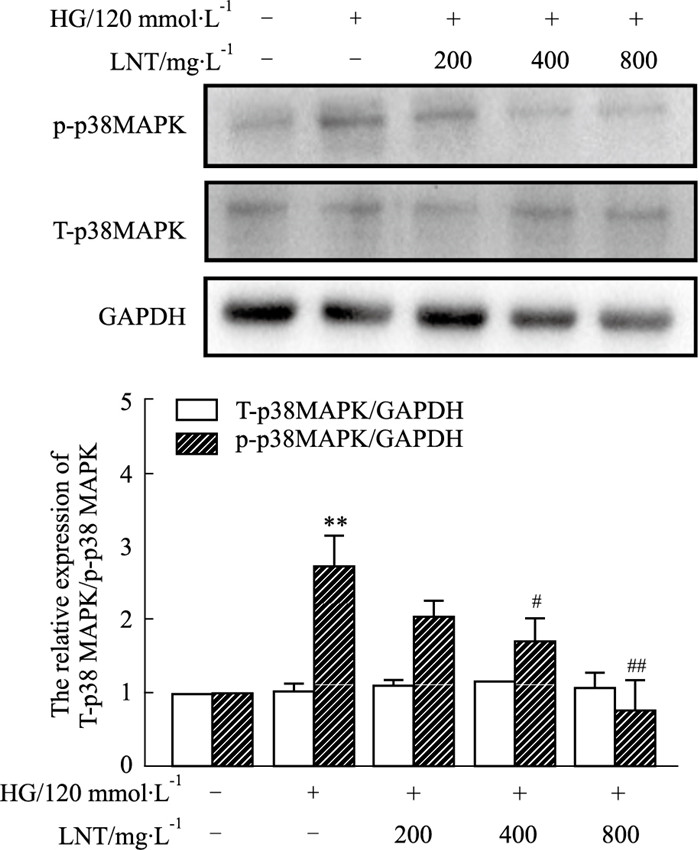
对于HUVEC,HG的刺激可增强p38 MAPK的磷酸化(P<0.001),LNT的处理能剂量依赖性地改善HG诱导的p38 MAPK磷酸化,200 mg·L-1的剂量即差异有显著性(P<0.01),见Fig 8。这部分结果说明,LNT改善HG诱导的HUVEC氧化应激状态,可能与抑制p38 MAPK信号通路的磷酸化相关。
|
| Fig 8 Effects of LNT on p-p38 protein expression in HG treated HUVECs (x±s, n=3) **P<0.01 vs control; #P<0.05, ##P<0.01 vs HG. |
糖尿病是一个全球性的健康问题,已成为全球十大死亡原因之一,其患者多死于并发症,其中最常见的是血管病变,因此防治糖尿病血管病变是改善糖尿病并发症的有效途径。
糖尿病属于中医的“消渴”范畴,在疾病早期,常表现为阴虚肝旺、气阴两虚、阴虚燥热、热伤气阴等症候。在疾病中晚期,出现血管病变等并发症,其主要病机特征多为气虚血瘀、经络闭阻。因此,中医治疗糖尿病及其血管病变,常采用调整脏腑、补虚泻实、标本兼治的治疗法则[8]。药食两用药材香菇具有补虚扶正、益气健脾的功效,不仅和糖尿病的治疗理论相符,还和自噬在传统中医理论中的“补虚泻实”相符合。
近年来,中医药对疾病的诊治作用在国内外得到广泛关注和推广,关于多糖类物质药理作用的研究有所增多,然而,LNT对于糖尿病血管病变的防治作用和机制尚不明确。本研究通过体外细胞实验,探究LNT对HUVEC的保护效应。研究结果首次证实了在HG的损伤处理下,LNT对HUVEC的活力有改善作用。
正常生理情况下iNOS蛋白表达量较低,有损伤因素刺激时iNOS表达上调并产生大量NO,可诱导ROS形成,进一步引起脂质过氧化[9-10]。脂质过氧化会使MDA生成增加,胞内ROS和MDA水平呈明显正相关[11]。SOD活性反映细胞清除ROS的能力,是一种重要的抗氧化酶[12-13]。
在生理条件下,对于细胞内的多余代谢物,胞内维持着一种保守的降解途径—自噬。此过程通过自噬体的双膜囊泡将大量细胞质、细胞器(如线粒体和过氧化物酶体)感染因子等在内的代谢废物传递到溶酶体中降解,缓和炎症反应,防止细胞死亡,保护细胞免受饥饿和相关压力[14]。而II型糖尿病是一种常见的与氧化应激相关的多因素疾病,通过活性氧的形成导致高血糖和高脂血症引起的细胞损伤和胰岛素抵抗[15]。在糖尿病状态下,血管内皮细胞的自噬水平不能维持多余代谢废物的清除,代谢废物过度堆积,内皮细胞最终无法维持正常生理功能,血管病变开始发生。
丝裂原活化蛋白激酶(mitogen-activated protein kinases,MAPK)属于高度保守的丝氨酸/苏氨酸蛋白激酶家族,包含3种亚家族:c-Jun的N末端激酶(c-Jun N-terminal kinases,JNK)、细胞外信号调节激酶(extracellar signal-regulated kinases,ERK)以及p38[16]。不仅与胞内氧化应激状态密切相关,还作为mTOR下游的关键靶点调控着自噬[17]。且调节许多蛋白质、酶和转录因子的活性,参与细胞对外部刺激的生物反应,有研究表明,氧化应激在血管内皮损伤的发病机制中起着重要作用,ROS可通过多种途径诱导p38 MAPK持续活化[18],活化后参与调控,使细胞内的自噬过程受到抑制,ROS的清除能力下降,二者互相促进、恶性循环,进而造成细胞损伤和活力下降。
本研究发现,HG诱导HUVEC胞内p38 MAPK磷酸化增加,自噬水平受到抑制。LNT作用后可增加HG损伤下细胞内的自噬水平。通过调控自噬可以降低HG引起的HUVEC胞内iNOS蛋白表达、减少ROS和MDA水平,改善HG诱导的SOD水平降低,缓解胞内氧化应激。同时p38 MAPK的磷酸化水平也降低,以上作用均为剂量依赖性。这提示对于HG引起的HUVEC活力下降,LNT可以通过ROS/p38 MAPK通路调控自噬来改善细胞损伤,减缓血管病变的发生。
综上所述,LNT可能作为防治糖尿病血管病变的候选药物,从而为延缓糖尿病并发症的发生发展,提高糖尿病病人的生活质量提供可能性。但自噬的调控是多途径的,LNT是否仅通过ROS/p38 MAPK通路调控自噬尚不明确,HG刺激HUVEC条件下,LNT对其它自噬相关信号通路的影响尚未阐明,后续本课题组将在此基础上进一步深入探究。
| [1] |
Furuyama K, Chera S, Van G L, et al. Diabetes relief in mice by glucose-sensing insulin-secreting human alpha-cells[J]. Nature, 2019, 567(7746): 43-8. doi:10.1038/s41586-019-0942-8 |
| [2] |
Kaur R, Kaur M, Singh J. Endothelial dysfunction and platelet hyperactivity in type 2 diabetes mellitus: Molecular insights and therapeutic strategies[J]. Cardiovasc Diabetol, 2018, 17(1): 121. doi:10.1186/s12933-018-0763-3 |
| [3] |
Kruger-genge A, Blocki A, Franke R P, et al. Vascular endothelial cell biology: An update[J]. Int J Mol Sci, 2019, 20(18): 4411. doi:10.3390/ijms20184411 |
| [4] |
Knapp M, Tu X, Wu R. Vascular endothelial dysfunction, a major mediator in diabetic cardiomyopathy[J]. Acta Pharmacol Sin, 2019, 40(1): 1-8. doi:10.1038/s41401-018-0042-6 |
| [5] |
Zhang Y, Liu Y, Zhou Y, et al. Lentinan inhibited colon cancer growth by inducing endoplasmic reticulum stress-mediated autophagic cell death and apoptosis[J]. Carbohyd Polym, 2021, 267: 118154. doi:10.1016/j.carbpol.2021.118154 |
| [6] |
Chen J, Raymond K. β-glucans in the treatment of diabetes and associated cardiovascular risks[J]. Vasc Health Risk Man, 2008, 4(6): 1265-72. |
| [7] |
宋晓妹, 杨红, 龙秋双, 等. 1, 8-桉叶油素调节自噬改善高糖诱导的内皮细胞损伤[J]. 中国药理学通报, 2021, 37(4): 472-7. Song X M, Yang H, Long Q S, et al. 1, 8-Cineole improves endothelial cell injury induced by high glucose via regulating autophagy[J]. Chin Pharmacol Bull, 2021, 37(4): 472-7. doi:10.3969/j.issn.1001-1978.2021.04.007 |
| [8] |
张嘉悦, 高天舒. 2型糖尿病湿热证型的中医治疗探析[J]. 中医药临床杂志, 2019, 31(1): 192-5. Zhang J Y, Gao T S. Discussion on TCM treatment of damp-heat syndrome of type 2 diabetes[J]. Clin J Tradit Chin Med, 2019, 31(1): 192-5. |
| [9] |
Anavi S, Tirosh O. iNOS as a metabolic enzyme under stress conditions[J]. Free Radic Biol Med, 2020, 146: 16-35. doi:10.1016/j.freeradbiomed.2019.10.411 |
| [10] |
Gliozzi M, Scicchttano M, Bosco F, et al. Modulation of nitric oxide synthases by oxidized LDLs: Role in vascular inflammation and atherosclerosis development[J]. Int J Mol Sci, 2019, 20(13): 3294. doi:10.3390/ijms20133294 |
| [11] |
Mbaveng A T, Noulala C G T, Samba A R M, et al. The alkaloid, soyauxinium chloride, displays remarkable cytotoxic effects towards a panel of cancer cells, inducing apoptosis, ferroptosis and necroptosis[J]. Chem Biol Interact, 2021, 333: 109334. doi:10.1016/j.cbi.2020.109334 |
| [12] |
Ai Z X, Wu Y O, Yu M, et al. Theaflavin-3, 3'-Digallate suppresses RANKL-induced osteoclastogenesis and attenuates ovariectomy-induced bone loss in mice[J]. Front Pharmacol, 2020, 11: 803. doi:10.3389/fphar.2020.00803 |
| [13] |
Sakamoto T, Hirotaka I. Hydrogen peroxide produced by superoxide dismutase SOD-2 activates sperm in Caenorhabditis elegans[J]. J Biol Chem, 2017, 292(36): 14804-13. doi:10.1074/jbc.M117.788901 |
| [14] |
Bento C F, Renna M, Ghislat G, et al. Mammalian autophagy: How does it work[J]. ? Annu Rev Biochem, 2016, 85: 685-713. |
| [15] |
Wang Y, Li YB, Yin JJ, et al. Autophagy regulates inflammation following oxidative injury in diabetes[J]. Autophagy, 2013, 9(3): 272-7. doi:10.4161/auto.23628 |
| [16] |
Lu M, Wang Y, Zhan X. The MAPK pathway-based drug therapeutic targets in pituitary adenomas[J]. Front Endocrinol (Lausanne), 2019, 10: 330. |
| [17] |
Gong L, LeiI Y, Liu Y, et al. Vaccarin prevents ox-LDL-induced HUVEC EndMT, inflammation and apoptosis by suppressing ROS/p38 MAPK signaling[J]. Am J Transl Res, 2019, 11(4): 2140-54. |
| [18] |
Pu Y, Zhang S, Zhou R, et al. IL-17A up-regulates expression of endothelial tissue factor in liver cirrhosis via the ROS/p38 signal pathway[J]. Biochem Biophy Res Commun, 2016, 470(1): 41-7. |

