

2. 安徽医科大学基础医学院,安徽 合肥 230032;
3. 中国科学技术大学附属第一医院产科,安徽 合肥 230032;
4. 安徽医科大学第一附属医院新生儿科,安徽 合肥 230032
周南(1995-),男,硕士生,研究方向:生物化学与分子生物学,共同第一作者,E-mail: 1069165164@qq.com。
2. School of Basic Medical Sciences, Anhui Medical University, Hefei 230032, China;
3. Dept of Obstetrics, The First Affiliated Hospital of USTC, Hefei 230032, China;
4. Dept of Neonatology, The First Affiliated Hospital of Anhui Medical University, Hefei 230032, China
内质网(endoplasmic reticulum, ER)是蛋白质折叠、翻译后修饰以及分泌性蛋白和膜蛋白转运的场所。环境和/或宿主的诸多因素可以造成ER应激,继而触发未折叠蛋白反应(unfolded protein reponse, UPR)[1]。此时细胞会产生一系列的保护反应,通过抑制蛋白的翻译、降解错误折叠蛋白以及促进错误蛋白的重新折叠,从而恢复ER的稳态。但如果错误折叠蛋白超出了ER的清除能力,便会诱发持续的ER应激,导致细胞凋亡,甚至细胞死亡[2]。
肠黏膜屏障是机体抵挡外来侵袭的一道重要防线。由于各种急慢性刺激,如病原菌入侵、缺血再灌注、膳食代谢物和毒素的影响等,均可导致肠上皮屏障的损伤,造成肠源性感染诱发肠道炎症,继而引起肠上皮细胞凋亡或坏死,甚至发展为全身炎症反应综合征,直至患者死亡[2]。研究表明,多种细胞因子及其介导的信号传导途径参与肠道炎症的发生和发展。其中,杯状细胞、潘氏细胞等具有强大分泌功能的肠上皮细胞,其蛋白质合成和加工的负荷较重,对ER应激尤为敏感。近年来的研究表明,ER应激参与肠上皮屏障功能的调节,是肠道炎症发生的重要发病机制之一[5-6]。
中脑星形胶质细胞源性神经营养因子(mesencephalic astrocyte-derived neurotrophic factor, MANF)是一个高度保守的可溶性蛋白,分子量约为18 ku。运用微阵列技术筛选与ER应激相关的基因发现,MANF是对ER应激最为敏感的基因[7]。之后,多项研究均证明MANF在ER应激相关疾病中具有明确的保护作用[8-12]。脑缺血可触发ER应激并增强MANF的表达,重组人MANF可促进神经元的增殖,防止神经元凋亡[8-9]。ER应激相关蛋白在胰腺细胞特异性MANF缺陷小鼠中表达上调,重组MANF能促进胰腺β细胞的增殖,可能成为糖尿病再生治疗的潜在靶点[10]。此外,我们前期的研究还表明,炎症可以触发ER应激,促进MANF定位于细胞核,干扰p65与其靶基因启动子结合,抑制NF-κB通路激活,从而抑制炎性滑膜细胞增殖[11]。MANF还可以通过抑制NF-κB/Snail信号通路,在肝脏ER应激与炎症的关系中发挥重要作用,可能是肝癌的潜在治疗靶点[12]。
但是MANF在肠道炎症中的作用尚无报道。由于MANF与ER应激密切相关,且ER应激是肠道炎症发生发展的重要分子机制之一。本实验拟在正常人小肠上皮细胞系FHs 74 Int中过表达MANF,并用ER应激诱导剂TM或TNF-α刺激,探究MANF对ER应激诱导的肠道上皮细胞损伤的保护作用。
1 材料与方法 1.1 材料 1.1.1 细胞株及质粒细胞系FHs 74 Int购自北纳生物公司;pEGFP-C2-MANF质粒为安徽医科大学沈玉先教授课题组惠赠;pEGFP-C2载体质粒为本课题组保存。
1.1.2 试剂转染试剂Lipofectamine 2000、ECL发光液(美国Thermo Fisher Scientific公司);DMEM培养基(美国HyClone公司);Tunicamycin(上海生工);TNF-α(美国MCE公司);MANF、cleaved caspase-3、CHOP、Bip、β-actin抗体(英国Abcam公司);Bcl-2、Bax抗体(中国proteintech公司);CCK8试剂盒(上海碧云天);PE Annexin Ⅴ凋亡检测试剂盒(美国BD公司)。
1.1.3 仪器超净工作台(江苏苏静集团);电泳仪、凝胶成像系统(美国BIO-RAD公司);CytoFLEX分析流式细胞仪(美国Beckman Coulter公司)
1.2 方法 1.2.1 MANF过表达正常人小肠上皮细胞FHs 74 Int细胞参照Lipofectamine 2000说明书将MANF-GFP质粒转染FHs 74 Int细胞,同步转染空载体GFP为对照。转染24 h后荧光显微镜观察各组转染效率。
1.2.2 免疫印迹法(Western blot)用裂解液裂解细胞,提取总蛋白,金属浴煮沸样品10 min,上样15 μL至SDS-PAGE胶电泳,槽式湿转法转移蛋白至NC膜,封闭缓冲液封闭1 h后分别用MANF、Bip、CHOP、cleaved-caspase-3、β-actin等抗体于4 ℃冰箱过夜,二抗在室温条件下孵育1 h后蛋白显影。
1.2.3 CCK8检测细胞增殖将FHs 74 Int细胞按相应组别接种于96孔培养板中,按说明书加入CCK8溶液,孵育1 h,上机测定OD值。
1.2.4 流式细胞术(flow cytometry)检测细胞凋亡分别收集相应组别的FHs 74 Int细胞。以1 000 r·min-1转速收集细胞沉淀,PBS清洗2遍。将10×Binding buffer用双蒸水稀释成1×Binding buffer,用1×Binding buffer将FHs 74 Int细胞重悬为1×109 L-1细胞悬液。吸取100 μL加入流式管中,按照说明书添加5 μL的PE Annexin Ⅴ和7-AAD至各组样品管,用移液器充分混匀后,室温避光孵育15 min,上机前补加400 μL 1×Binding buffer用于检测。
1.2.5 统计学方法使用Graph Pad Prism8.4软件进行统计学分析,实验结果以x±s来表示,两组以上数据组间比较采用One-way ANOVA。
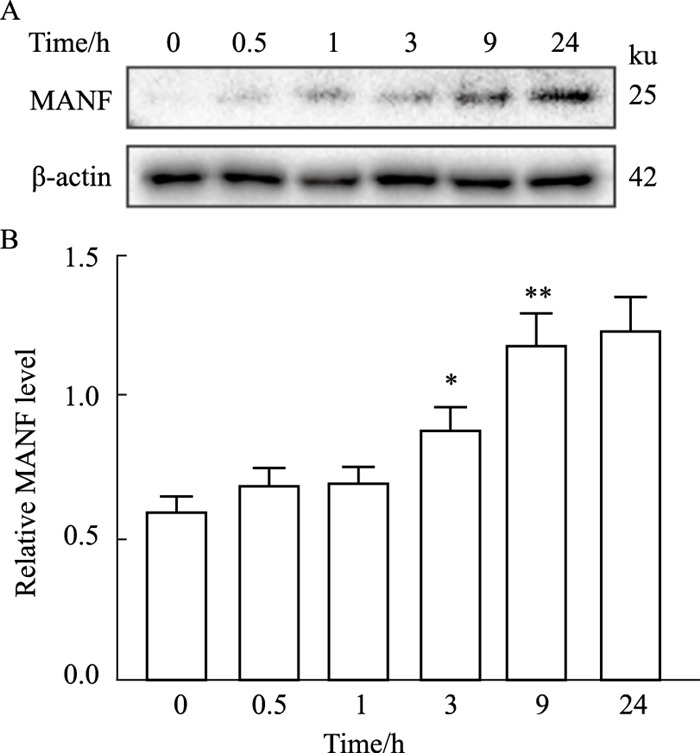
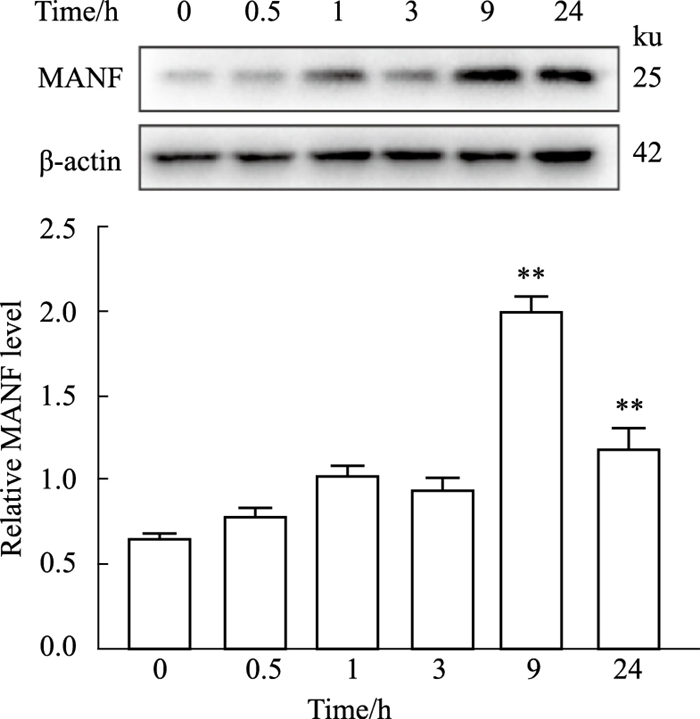
2 结果 2.1 ER应激可诱导小肠上皮细胞内MANF表达增多在正常人小上皮细胞FHs 74 Int细胞培养基中给予ER应激诱导剂TM (2 mg·L-1) 或TNF-α (0.785 μg·L-1)刺激后,MANF分别从加药后3 h(Fig 1)和9 h(Fig 2)开始表达增多,并呈时间依赖关系。提示肠上皮细胞内发生ER应激的早期即可以诱导MANF的表达。
|
| Fig 1 TM induced MANF expression in intestinal epithelial cells (x±s, n=3) A: MANF protein levels at indicated time points were assessed by Western blot; B: The gray value was detected for A, *P < 0.05, **P < 0.01 vs 0 h. |
|
| Fig 2 TNF-α induced MANF expression in intestinal epithelial cells (x±s, n=3) A: MANF protein levels at indicated time points were assessed by Western blot; B: The gray value was detected for A, **P < 0.01 vs 0 h. |
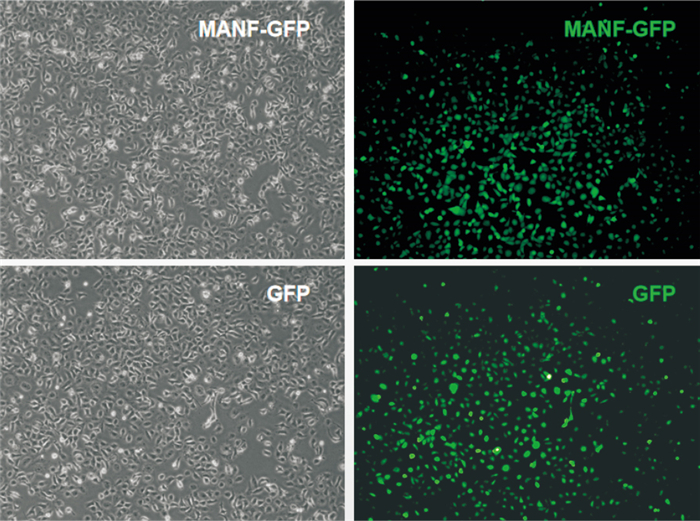
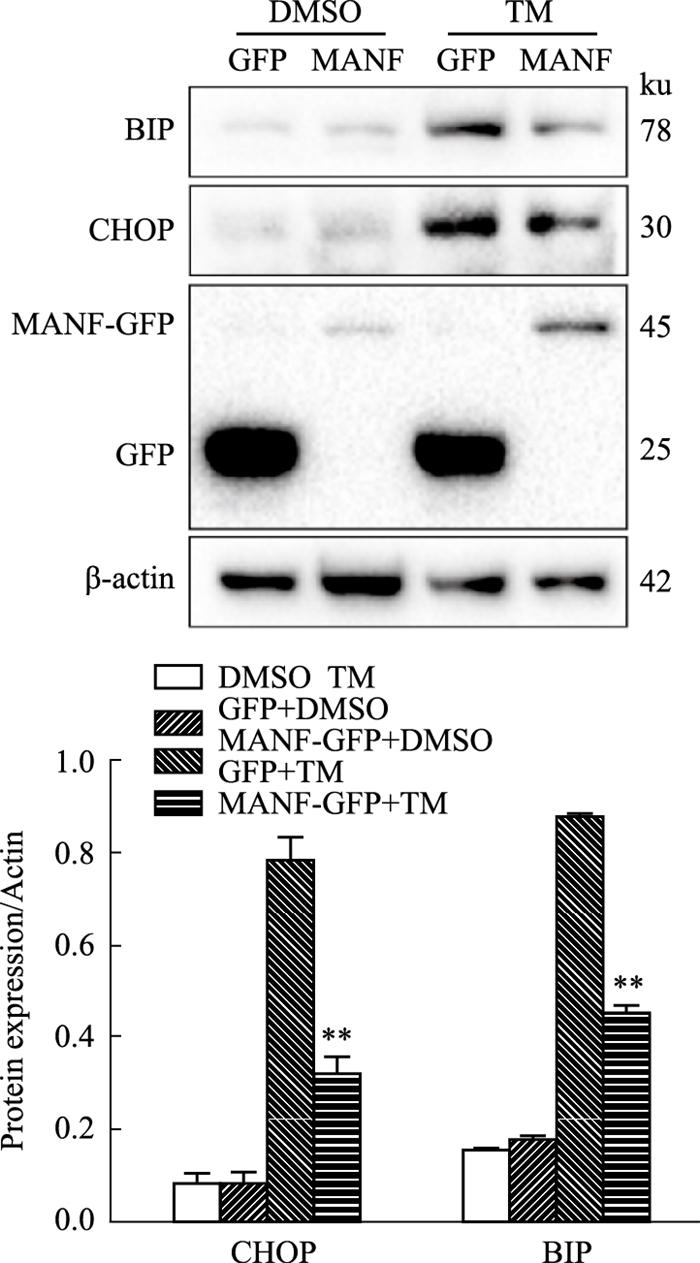
分别将MANF-GFP与空载体GFP质粒转染FHs 74 Int细胞,观察到绿色荧光,提示外源性MANF在小肠上皮细胞中成功表达(Fig 3)。转染后16 h,用TM刺激细胞24 h后观察ER应激指标。结果显示,过表达MANF可以减少TM刺激后的ER应激相关蛋白Bip、CHOP的表达(Fig 4),提示MANF具有抑制ER应激的作用。
|
| Fig 3 Successful expression of exogenous MANF in intestinal epithelial cells Cell status was observed under a microscope (Left panel), and the expression of green fluorescent protein was observed under a fluorescence microscope (right panel) (magnification 200×). |
|
| Fig 4 MANF protected intestinal epithelial cells from ER stress(x±s, n=3) A: ER stress related proteins were detected via Western blot; B: The gray value was detected for A, **P < 0.01 vs GFP+TM. |
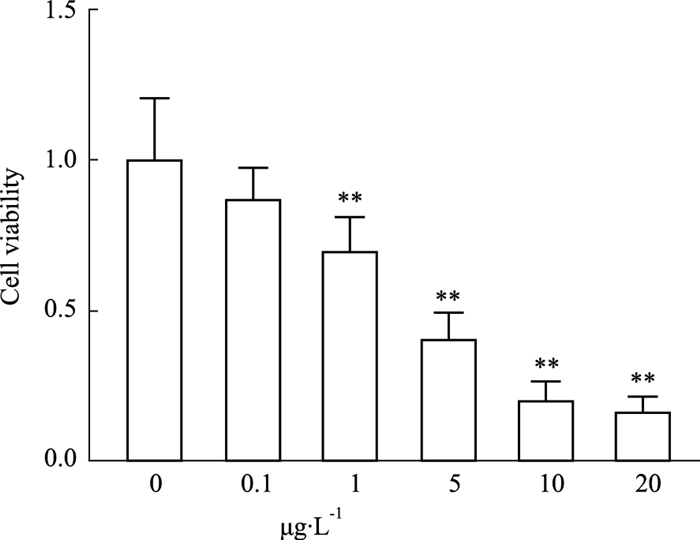
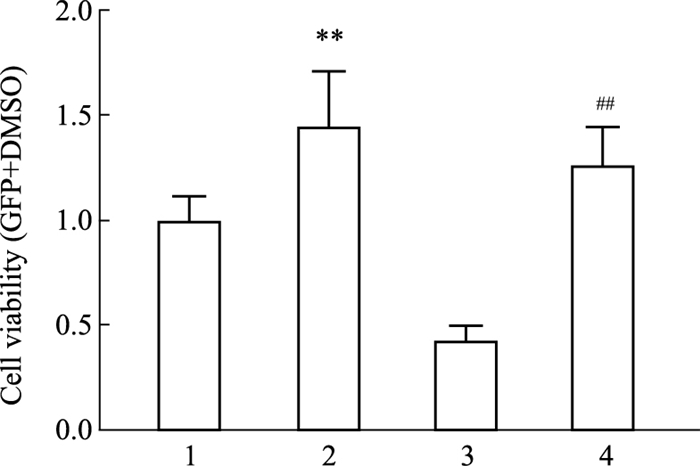
用TM诱导肠上皮细胞发生ER应激后,CCK8细胞增殖实验发现细胞增殖能力减弱,并呈现剂量依赖性关系(Fig 5)。过表达MANF后可明显提高小肠上皮细胞的增殖活性(Fig 6)。结果表明肠上皮细胞中过表达MANF可以促进细胞增殖。
|
| Fig 5 ER stress had effects on proliferation of intestinal epithelial cells(x±s, n=3) The CCK8 assay showed that TM inhibited cell viability in a dose-dependent manner. **P < 0.01 vs control. |
|
| Fig 6 MANF promoted proliferation of intestinal epithelial cells 1:GFP+DMSO; 2:MANF-GFP+DMSO; 3:GFP+TM; 4:MANF-GFP+TM. The influence of MANF on intestinal epithelial cell proliferation was detected by CCK8 assay. **P < 0.01 vs GFP+DMSO; ##P < 0.01 vs GFP+TM. |
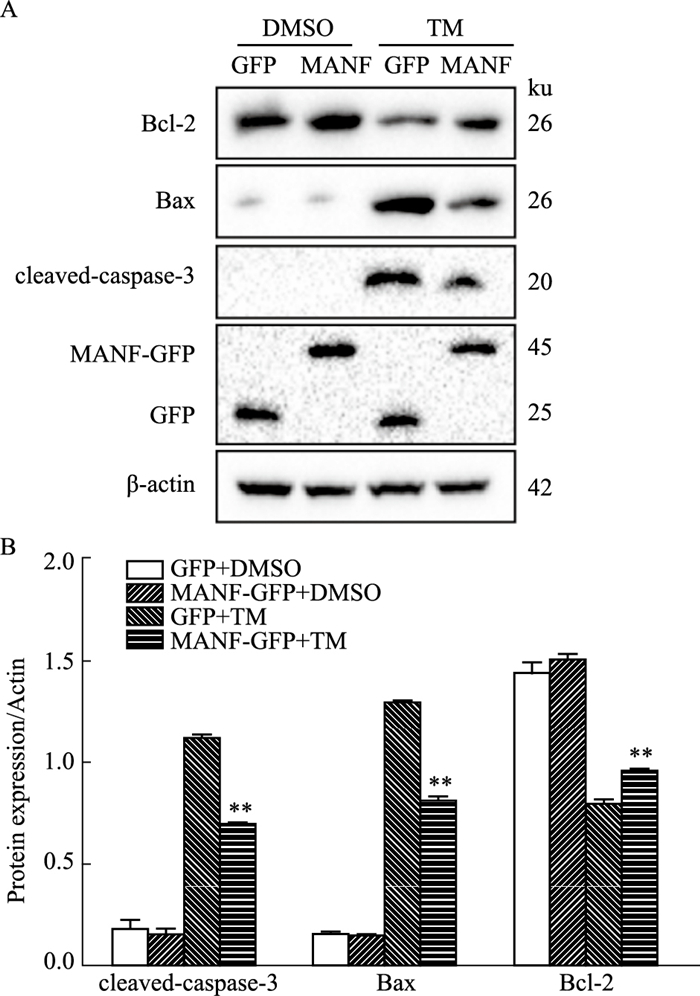
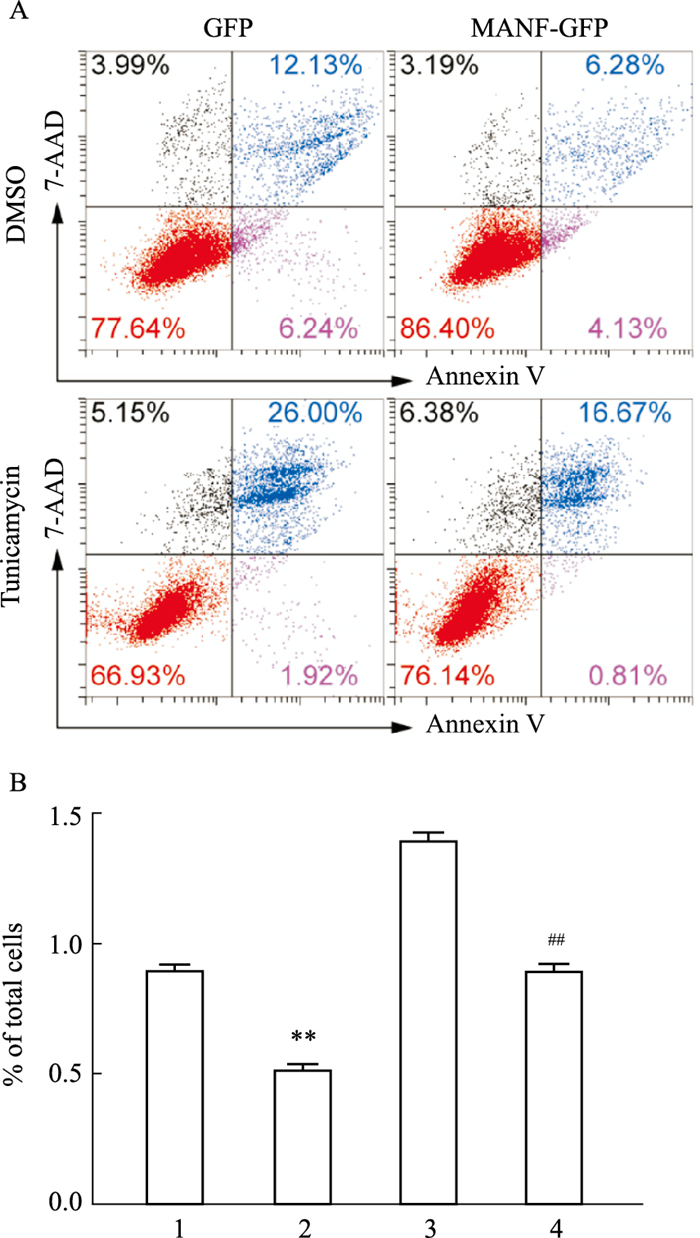
Western blot结果显示,转染MANF-GFP质粒可以显著降低TM诱导后FHs 74 Int细胞中促凋亡蛋白cleaved-caspase-3和Bax的生成,提高抗凋亡蛋白Bcl-2的表达(Fig 7);flow cytometry显示,TM刺激后,GFP组发生凋亡的细胞比例(27.9±0.535 4),高于MANF-GFP组发生凋亡的细胞比例(17.93±0.495 7)(Fig 8)。结果表明过表达MANF可以抑制ER应激诱导的小肠上皮细胞的凋亡。
|
| Fig 7 MANF inhibited TM-induced ER stress-mediated apoptosis(x±s, n=3) A: The expression of apoptosis-related proteins was detected by Western blot; B: The gray value was detected for A. **P < 0.01 vs GFP+TM. |
|
| Fig 8 MANF inhibited TM-induced ER stress-mediated apoptosis (x±s, n=3) A: Representative flow cytometry density plots of apoptosis rates of intestinal epithelial cells; B: Statistical bar chart of A. 1:GFP+DMSO; 2:MANF-GFP+DMSO; 3:GFP+TM; 4:MANF-GFP+TM. **P < 0.01 vs GFP+DMSO; ##P < 0.01 vs GFP+TM. |
功能失调的ER应激和UPR是肠道炎症的发病原因之一。因此,以减轻ER应激为靶点的药物可能是治疗肠炎的有效选择[13]。本研究表明,MANF可以明显抑制小肠上皮细胞内的ER应激,促进肠上皮细胞的增殖能力并减少其凋亡。
MANF是一种对ER应激敏感的可溶性分泌蛋白[7]。在脑缺血的早期即可上调表达,甚至早于ER应激的标志性蛋白CHOP[8]。本研究发现,诱导FHs 74 Int细胞发生ER应激后,内源性的MANF分别从TM处理后3 h和TNF-α处理后9 h开始表达增多,再次证明ER应激早期即可以诱导MANF的表达。
有研究表明[14-15],MANF的表达上调是对ER应激的适应性反应,MANF的表达有助于缓解UPR。UPR信号转导作用主要依赖PERK、IRE1和ATF6 3种ER跨膜蛋白。在稳态情况下,Bip结合并封闭上述3个信号分子,使其保持于非激活的状态,并稳定在ER膜上。但Bip和非折叠蛋白有更强的亲和力,当ER中滞留非折叠蛋白时,Bip则会同其结合,并释放PERK、IRE1和ATF6,继而激活UPR的3条信号通路。PERK和ATF6均可诱导CHOP的表达,故一般认为Bip和CHOP均为ER应激的标志蛋白[1, 16]。本研究发现,给予ER应激诱导剂后,Bip和CHOP的表达增多。相较转染空载体的对照组,MANF可以明显抑制ER应激相关蛋白Bip和CHOP的表达,表明MANF发挥抑制ER应激的作用。
当ER应激持续加重,则会通过激活caspase-12和CHOP途径诱导细胞的凋亡。ER应激可以激活caspase-12,继而切割caspase-9,使caspase-3激活,导致细胞凋亡[17]。在肠炎模型中,与全身缺失CHOP的小鼠相比,野生型小鼠肠黏膜中有大量凋亡细胞,提示CHOP基因表达上调加重了细胞凋亡和结肠炎的发生[18]。在本研究中,我们用Bcl-2, Bax和cleaved-caspase-3以及Annexin Ⅴ和7-AAD凋亡流式检测来表征细胞凋亡的水平,发现MANF可以抑制ER应激诱导的细胞凋亡。同时我们还观察到ER应激抑制肠上皮细胞增殖,并呈现剂量依赖的关系,提示ER应激越严重,对上皮细胞的增殖抑制作用越明显,但过表达MANF可明显缓解此现象。
以上结果提示,MANF在肠上皮细胞发生ER应激的早期即可明显上调,并具有抑制ER应激,促进肠上皮细胞增殖,抑制其凋亡的保护作用。从而发挥肠黏膜屏障保护和抑制肠道炎症的潜在治疗作用。然而MANF影响ER应激发生的具体分子机制尚待阐明。本研究为MANF促进肠上皮细胞功能修复提供一定的理论依据。
| [1] |
Todd D J, Lee A H, Glimcher L H. The endoplasmic reticulum stress response in immunity and autoimmunity[J]. Nat Rev Immunol, 2008, 8(9): 663-74. doi:10.1038/nri2359 |
| [2] |
Eugene S P, Reddy V S, Trinath J. Endoplasmic reticulum stress and intestinal inflammation: A perilous union[J]. Front Immunol, 2020, 11: 543022. doi:10.3389/fimmu.2020.543022 |
| [3] |
Kaser A, Blumberg R S. Endoplasmic reticulum stress and intestinal inflammation[J]. Mucosal Immunol, 2010, 3(1): 11-6. doi:10.1038/mi.2009.122 |
| [4] |
Hosomi S, Grootjans J, Tschurtschenthaler M, et al. Intestinal epithelial cell endoplasmic reticulum stress promotes mult1 up-regulation and nkg2d-mediated inflammation[J]. J Exp Med, 2017, 214(10): 2985-97. doi:10.1084/jem.20162041 |
| [5] |
Wang R, Moniruzzaman M, Wong K Y, et al. Gut microbiota shape the inflammatory response in mice with an epithelial defect[J]. Gut Microbes, 2021, 13(1): 1-18. |
| [6] |
Stengel S T, Fazio A, Lipinski S, et al. Activating transcription factor 6 mediates inflammatory signals in intestinal epithelial cells upon endoplasmic reticulum stress[J]. Gastroenterology, 2020, 159(4): 1357-74 e1310. doi:10.1053/j.gastro.2020.06.088 |
| [7] |
Apostolou A, Shen Y, Liang Y, et al. Armet, a upr-upregulated protein, inhibits cell proliferation and er stress-induced cell death[J]. Exp Cell Res, 2008, 314(13): 2454-67. doi:10.1016/j.yexcr.2008.05.001 |
| [8] |
Yu Y Q, Liu L C, Wang F C, et al. Induction profile of manf/armet by cerebral ischemia and its implication for neuron protection[J]. J Cereb Blood Flow Metab, 2010, 30(1): 79-91. doi:10.1038/jcbfm.2009.181 |
| [9] |
Yang W, Shen Y, Chen Y, et al. Mesencephalic astrocyte-derived neurotrophic factor prevents neuron loss via inhibiting ischemia-induced apoptosis[J]. J Neurol Sci, 2014, 344(1-2): 129-38. doi:10.1016/j.jns.2014.06.042 |
| [10] |
Danilova T, Belevich I, Li H, et al. Manf is required for the postnatal expansion and maintenance of pancreatic beta-cell mass in mice[J]. Diabetes, 2019, 68(1): 66-80. doi:10.2337/db17-1149 |
| [11] |
Chen L, Feng L, Wang X, et al. Mesencephalic astrocyte-derived neurotrophic factor is involved in inflammation by negatively regulating the nf-kappab pathway[J]. Sci Rep, 2015, 5: 8133. doi:10.1038/srep08133 |
| [12] |
Liu J, Wu Z, Han D, et al. Mesencephalic astrocyte-derived neurotrophic factor inhibits liver cancer through small ubiquitin-related modifier (sumo)ylation-related suppression of nf-kappab/snail signaling pathway and epithelial-mesenchymal transition[J]. Hepatology, 2020, 71(4): 1262-78. doi:10.1002/hep.30917 |
| [13] |
You Y D, Deng W H, Guo W Y, et al. 4-phenylbutyric acid attenuates endoplasmic reticulum stress-mediated intestinal epithelial cell apoptosis in rats with severe acute pancreatitis[J]. Dig Dis Sci, 2019, 64(6): 1535-47. doi:10.1007/s10620-018-5437-1 |
| [14] |
Albert K, Airavaara M. Neuroprotective and reparative effects of endoplasmic reticulum luminal proteins-mesencephalic astrocyte-derived neurotrophic factor and cerebral dopamine neurotrophic factor[J]. Croat Med J, 2019, 60(2): 99-108. doi:10.3325/cmj.2019.60.99 |
| [15] |
马钰泱, 狄泽敏, 曹晴, 等. 佐剂性关节炎大鼠滑膜及血清中manf的表达及其与炎症的相关性[J]. 中国药理学通报, 2018, 34(4): 537-43. Ma Y Y, Di Z M, Cao Q, et al. Expression characterization of MANF during course of rat adjuvant arthritis and its relationship with inflammation[J]. Chin Pharmacol Bull, 2018, 34(4): 537-43. doi:10.3969/j.issn.1001-1978.2018.04.020 |
| [16] |
Rees W D, Stahl M, Jacobson K, et al. Enteroids derived from inflammatory bowel disease patients display dysregulated endoplasmic reticulum stress pathways, leading to differential inflammatory responses and dendritic cell maturation[J]. J Crohns Colitis, 2020, 14(7): 948-61. doi:10.1093/ecco-jcc/jjz194 |
| [17] |
Fu H Y, Okada K, Liao Y, et al. Ablation of c/ebp homologous protein attenuates endoplasmic reticulum-mediated apoptosis and cardiac dysfunction induced by pressure overload[J]. Circulation, 2010, 122(4): 361-9. doi:10.1161/CIRCULATIONAHA.109.917914 |
| [18] |
Namba T, Tanaka K, Ito Y, et al. Positive role of ccaat/enhancer-binding protein homologous protein, a transcription factor involved in the endoplasmic reticulum stress response in the development of colitis[J]. Am J Pathol, 2009, 174(5): 1786-98. doi:10.2353/ajpath.2009.080864 |

