

韩冰(1989-),男,博士,讲师,研究方向:中药学,通信作者,E-mail:hanbing7525@163.com
结肠癌作为常见的消化道恶性肿瘤,发病率逐年增加,且其死亡率更是高居恶性肿瘤第四位[1]。西医对于结肠癌的治疗手段单一,以手术、放疗和化疗为主,后期副作用较大。中医对结肠癌的认识在古今有两种不同的看法,《黄帝内经》将结肠癌命名为“积证”,主要原因是卫气停留于结肠不能返回,积液久停,合而为肠瘤,以气滞为主要原因[2]。现代中医认为,癌毒源于内,在肠道瘀结,脏腑通降失常,无力抗癌毒,以血瘀为主[3-4]。中医对于结肠癌的治疗复方有多种,如四君子汤、加味乌梅汤、黄芩汤等[5]。丹参饮符合古今病因辩证,丹参有活血祛瘀之功,檀香具行气温中之效,可能对结肠癌的治疗有一定效果。
丹参饮由中药丹参(Salvia miltiorrhiza Bge)、檀香(Santalum album L)和砂仁(Amomum villosum Lour)组成,具有活血行气止痛的功效,主治气滞血瘀证,目前临床上主要用于心血管和胃肠道系统的治疗[6]。王程等[7]建立CT-26结肠癌肝转移小鼠模型,丹参饮(1 g生药/mL)干预该模型可抑制结肠癌转移,其机制可能与抑制肝脏肿瘤中端粒酶的表达有关。王学良[8]采用丹参饮干预结肠癌肝转移小鼠模型,发现丹参饮对肿瘤转移过程有明显的抑制作用,其作用机制与调节NF-κB和EGFR的表达有关。尽管当下对丹参活性成分的研究较多,但对中药复方丹参饮的研究较少。网络药理学利用网上平台大数据分析,通过药物有效成分对应靶点和疾病靶点,构建中药-成分-靶点-疾病网络关系,并以分子对接检验结合效果,进而分析潜在的治疗机制。
1 材料与方法 1.1 丹参饮活性成分和结肠癌靶点筛选丹参饮作用靶点筛选:在中药系统药理学数据库与分析平台(Traditional Chinese Medicine Systems Pharmacology Database and Analysis Platform,TCMSP)中查找,得到复方丹参饮中丹参、檀香、砂仁的所有有效活性成分,以生物利用度OB值≥30%,类药性DL≥0.18为筛选条件,分选出中药复方丹参饮的主要活性成分。以TCMSP数据库查找丹参饮各味药的相关作用靶点,再通过Uniprot数据库(http//www.Uniprotorg/)将target name转化为symbol name。
结肠癌作用靶点筛选:在GeneCards数据库(https://www.genecards.org/)中查找Colon Cancer疾病相关靶点,以得分≥1.0为筛选条件,得到相应疾病靶点。
1.2 药物与疾病相关靶点交集的构建为了进一步剖析复方丹参饮与结肠癌的关系,依托R4.0.2软件,绘制丹参饮与结肠癌靶点的韦恩图。再以共同靶点为筛选条件,找出丹参饮中主要的相关活性成分。并以Cytoscape3.7.0软件为依托,结合上述得到的各靶点、疾病以及中药有效成分的关系,构建中药-活性成分-靶点-疾病的网络关系图。
1.3 PPI蛋白互作网络关系图的构建在STRING数据库(http://string-db.org/)中,将疾病和中药成分共有的靶点导入进行搜索,物种选择为“Homo sapiens”,隐藏蛋白网络中游离的节点,设置最低互作分值为0.4,构建靶点蛋白的可视化互作网络图。
1.4 GO功能与KEGG通路富集分析通过Biocondoctor数据库(http://www.bioconductor.org/)下载安装基因本体论富集分析(Gene Ontology,GO)和信号通路富集分析(Kyoto Encyclopedia of Genes and Genomes,KEGG)的语言包到R4.0.2软件,然后依托R4.0.2绘制出GO功能和KEGG通路富集气泡图、柱状图以及相应的信号通路图。
1.5 重要靶点和主要活性成分的分子对接通过PDB数据库(http://www.rcsb.org/)下载通路中重要蛋白AKT1的3D蛋白结构,通过Pubchem数据库(https://pubchem.ncbi.nlm.nih.gov/)下载主要活性成分木犀草素(Luteolin)和丹参酮ⅡA(Tanshinone ⅡA)的3D结构,通过Sybyl X2.0软件进行Surflex-Dock分析,Total score为输出构象的总打分函数, 涉及碰撞打分(crash)、极化打分(polar)。本文将Total score打分高于5.000的输出构象判定为较好的输出构象,并用Pymol软件处理对接结果。
2 结果 2.1 丹参饮中活性成分与靶点筛选通过TCMSP数据库平台,查找得到丹参饮的所有化学成分。其中丹参有202个化学成分,檀香有70个,砂仁有165个。以OB>30%,DL>0.18为筛选条件过滤,共得到丹参饮中药物的活性成分78个,其中丹参65个,檀香3个,砂仁10个(Tab 1)。
| Molecule name | OB (%) | DL |
| Salvia miltiorrhiza | ||
| Przewalskin B | 110.32 | 0.44 |
| (2R)-3-(3, 4-Dihydroxyphenyl)-2-[(Z)-3-(3, 4-dihydroxyphenyl) acryloyl]oxy-propionic acid | 109.38 | 0.35 |
| (Z)-3-[2-[(E)-2-(3, 4-Dihydroxyphenyl)vinyl]-3, 4-dihydroxy-phenyl]acrylic acid | 88.54 | 0.26 |
| (6S)-6-Hydroxy-1-methyl-6-methylol-8, 9-dihydro-7H-naphtho [8, 7-g]benzofuran-10, 11-quinone | 75.39 | 0.46 |
| Formyltanshinone | 73.44 | 0.42 |
| Miltionone Ⅱ | 71.03 | 0.44 |
| Epidanshenspiroketallactone | 68.27 | 0.31 |
| (6S)-6-(Hydroxymethyl)-1, 6-dimethyl-8, 9-dihydro-7H-naphtho [8, 7-g]benzofuran-10, 11-dione | 65.26 | 0.45 |
| Prolithospermic acid | 64.37 | 0.31 |
| 2-(4-Hydroxy-3-methoxyphenyl)-5-(3-hydroxypropyl)-7-methoxy- 3-benzofurancarboxaldehyde | 62.78 | 0.40 |
| Przewaquinone B | 62.24 | 0.41 |
| Digallate | 61.85 | 0.26 |
| Danshenol B | 57.95 | 0.56 |
| Danshenol A | 56.97 | 0.52 |
| Przewaquinone C | 55.74 | 0.40 |
| Isocryptotanshi-none | 54.98 | 0.39 |
| Neocryptotanshinone | 52.49 | 0.32 |
| Tanshinaldehyde | 52.47 | 0.45 |
| Cryptotanshinone | 52.34 | 0.40 |
| Danshenspiroketallactone | 50.43 | 0.31 |
| Isotanshinone Ⅱ | 49.92 | 0.40 |
| Tanshinone IIA | 49.89 | 0.40 |
| Miltionone Ⅰ | 49.68 | 0.32 |
| Deoxyneocryptotanshinone | 49.40 | 0.29 |
| (E)-3-[2-(3, 4-Dihydroxyphenyl)-7-hydroxy-benzofuran-4-yl]acrylic acid | 48.24 | 0.31 |
| 6-o-Syringyl-8-o-acetyl shanzhiside methyl ester | 46.69 | 0.71 |
| Tanshinone Ⅵ | 45.64 | 0.30 |
| Salvianolic acid G | 45.56 | 0.61 |
| Isoimperatorin | 45.46 | 0.23 |
| Dihydrotanshinone Ⅰ | 45.04 | 0.36 |
| Manool | 45.04 | 0.20 |
| Miltirone Ⅱ | 44.95 | 0.24 |
| 3α-Hydroxytanshinone ⅡA | 44.93 | 0.44 |
| Poriferasterol | 43.83 | 0.76 |
| Dehydrotanshinone IIA | 43.76 | 0.40 |
| Sclareol | 43.67 | 0.21 |
| Salvianolic acid J | 43.38 | 0.72 |
| Przewaquinone E | 42.85 | 0.45 |
| Tanshindiol B | 42.67 | 0.45 |
| (6S, 7R)-6, 7-Dihydroxy-1, 6-dimethyl-8, 9-dihydro-7H-naphtho [8, 7-g]benzofuran-10, 11-dione | 41.31 | 0.45 |
| 2-Isopropyl-8-methylphenanthrene-3, 4-dione | 40.86 | 0.23 |
| Przewaquinone F | 40.31 | 0.46 |
| Baicalin | 40.12 | 0.75 |
| Microstegiol | 39.61 | 0.28 |
| α-amyrin | 39.51 | 0.76 |
| Neocryptotanshinone Ⅱ | 39.46 | 0.23 |
| Dan-shexinkum D | 38.88 | 0.55 |
| Miltirone | 38.76 | 0.25 |
| 1, 2, 5, 6-Tetrahydrotanshinone | 38.75 | 0.36 |
| Dihydrotanshinlactone | 38.68 | 0.32 |
| Przewalskin A | 37.11 | 0.65 |
| Methylenetanshinquinone | 37.07 | 0.36 |
| Poriferast-5-en-3β-ol | 36.91 | 0.75 |
| Miltipolone | 36.56 | 0.37 |
| Luteolin | 36.16 | 0.25 |
| Sugiol | 36.11 | 0.28 |
| C09092 | 36.07 | 0.25 |
| 1-Methyl-8, 9-dihydro-7H-naphtho[5, 6-g]benzofuran-6, 10, 11-trione | 34.72 | 0.37 |
| NSC 122421 | 34.49 | 0.28 |
| 4-Methylenemiltirone | 34.35 | 0.23 |
| 5, 6-Dihydroxy-7-isopropyl-1, 1-dimethyl-2, 3-dihydrophenanthren-4-one | 33.77 | 0.29 |
| Salvilenone Ⅰ | 32.43 | 0.23 |
| 3-β-Hydroxymethyllenetanshiquinone | 32.16 | 0.41 |
| Salviolone | 31.72 | 0.24 |
| Salvilenone | 30.38 | 0.38 |
| Santalum album | ||
| Isorhamnetin | 49.60 | 0.31 |
| Luteolin | 36.16 | 0.25 |
| Isovitexin | 31.29 | 0.72 |
| Amomum villosum | ||
| Stigmasta-5, 22-dien-3-β-yl acetate | 46.44 | 0.86 |
| Icosa-11, 14, 17-trienoic acid methyl ester | 44.81 | 0.23 |
| Stigmasterol | 43.83 | 0.76 |
| Sitosteryl acetate | 40.39 | 0.85 |
| Methyl icosa-11, 14-dienoate | 39.67 | 0.23 |
| Poriferast-5-en-3β-ol | 36.91 | 0.75 |
| β-Sitosterol | 36.91 | 0.75 |
| 24-Ethylcholest-4-en-3-one | 36.08 | 0.76 |
| (5S, 8S, 9S, 10R, 13R, 14S, 17R)-17-[(1R, 4R)-4-ethyl-1, 5-Dimethylhexyl]-10, 13-dimethyl-2, 4, 5, 7, 8, 9, 11, 12, 14, 15, 16, 17-dodecahydro-1H-cyclopenta[a]phenanthrene-3, 6-dione | 33.12 | 0.79 |
| Vitamin E | 32.29 | 0.70 |
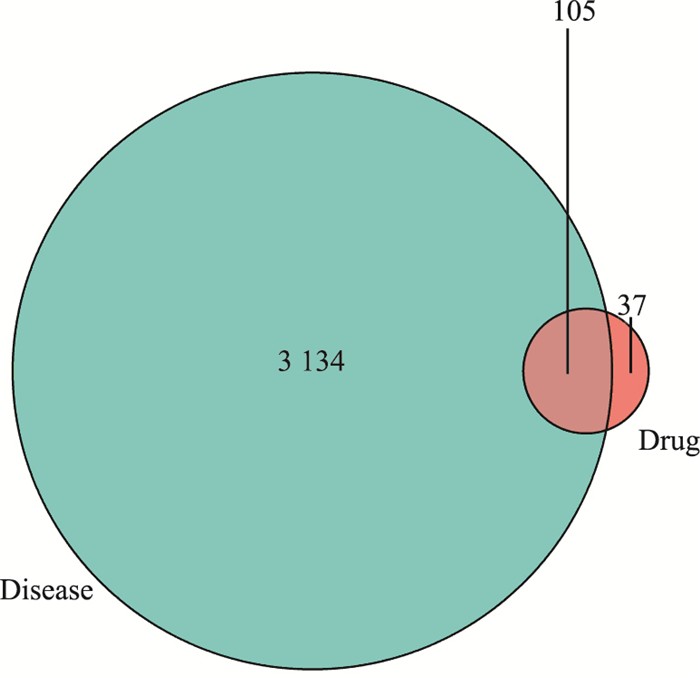
将TCMSP数据库中丹参饮有效成分对应的靶点蛋白通过Uniprot数据库进行转化,共得到基因靶点142个。利用GeneCards数据库,以得分>1为筛选条件,得到3 239个结肠癌靶点。利用R4.0.2软件,绘制丹参饮-结肠癌靶点韦恩图(Fig 1),获得中药有效成分和疾病共同靶点105个,根据靶点筛选获得含有相应靶点的中药有效成分69个。
|
| 图 1 The Venn diagram of Danshen decoction and colon cancer targets |
将疾病和复方中共有靶点作为研究对象,再将相应靶点与复方中的有效成分和单味药对应关系,有效成分与相关靶点关系,以及靶点与疾病关系导入Cytoscape3.7.0软件。对药物及其对应的有效成分,靶点以及疾病进行优化,获得中药-成分-靶点-疾病网络关系。该网络由178个节点,888条边组成,其中木犀草素是丹参和檀香的共有成分,重要性最强。在丹参中,与靶点关联度居前三的是丹参酮ⅡA、丹参新醌D和二氢丹参内酯。在檀香中,除木犀草素外,与靶点关联最强的是异鼠李素。在砂仁中,β-谷甾醇作为丹参和砂仁的共有成分,其与靶点关联度最强,其次是豆甾醇。总结来说,木犀草素和丹参酮ⅡA与靶点相互作用最多,研究价值相对较大。
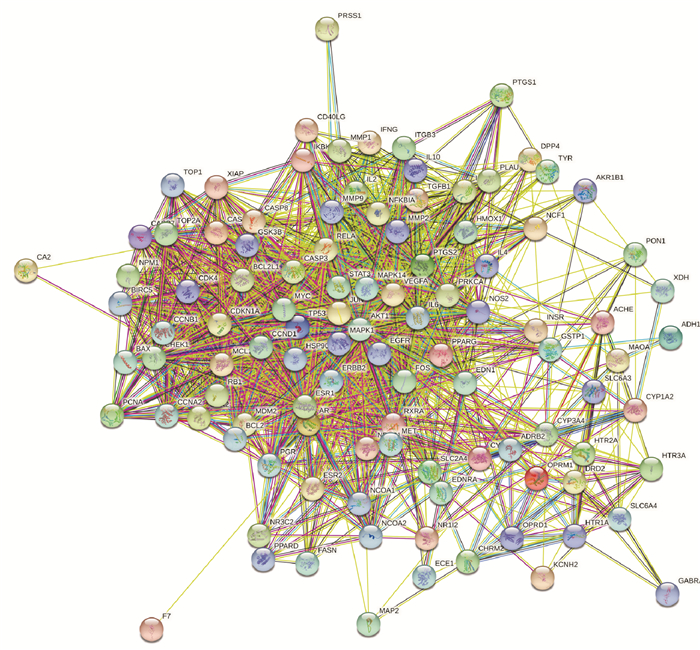
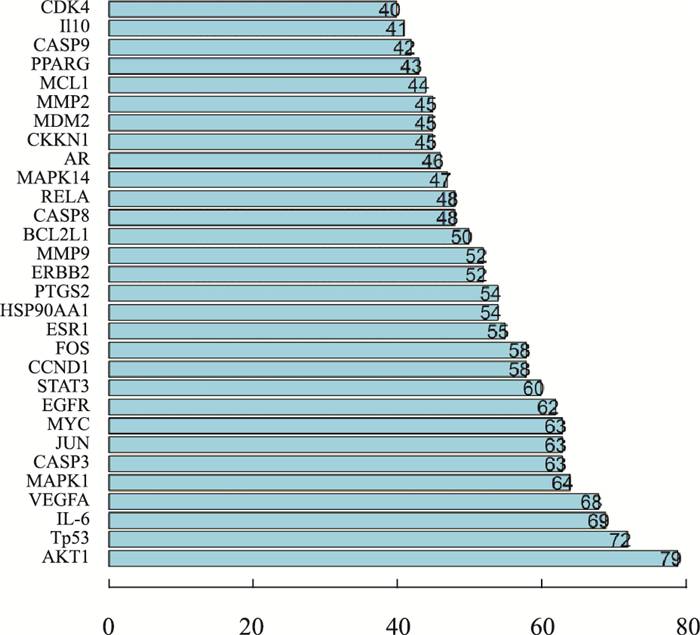
2.4 PPI蛋白相互作用网络构建在STRING数据库中输入药物和共有的105个有效靶点,设置物种为“Homo sapiens”,得到PPI蛋白相互作用网络关系图(Fig 2)。并分选出链接节点最多的20个靶点基因,根据其连线数做出蛋白互作网络核心基因的柱状图(Fig 3)。其中主要受影响的靶点基因有AKT1、Tp53、IL-6等,这为探寻中药复方丹参饮治疗结肠癌的机制提供深远的参考价值。
|
| 图 2 PPI protein interaction network diagram |
|
| 图 3 Core gene of protein interaction network |
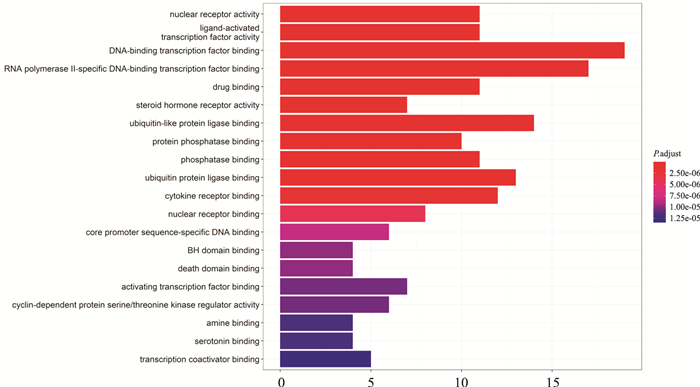
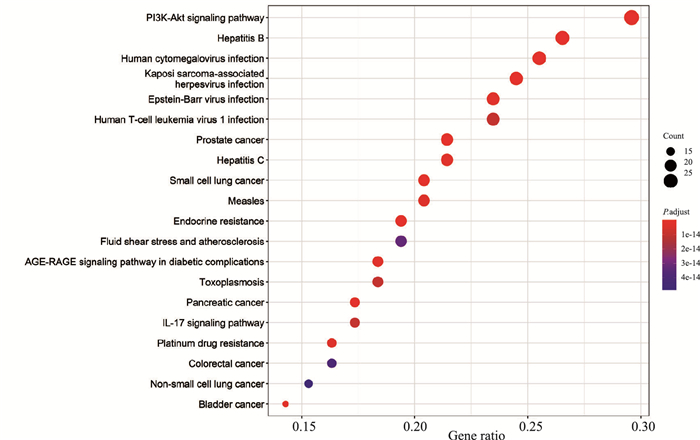
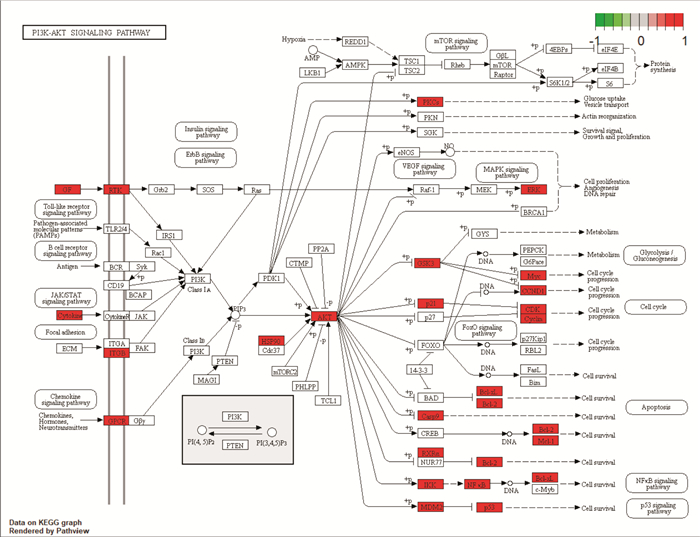
以Biocondoctor数据库中GO和KEGG相应的语言包,依托R语言,得出主要的GO功能柱状图(Fig 4)和KEGG富集通路气泡图(Fig 5)。其中GO功能分析结果从高到低为DNA-binding transcription factor binding、RNA polymerase Ⅱ-specific DNA-binding transcription factor binding、ubiquitin-like protein ligase binding、ubiquitin protein ligase binding、cytokine receptor binding。KEGG通路富集分析结果从高到低为PI3K/AKT signaling pathway、Hepatitis B、Human cytomegalovirus infection、Kaposi sarcoma-associated herpesvirus infection。同时以PI3K/AKT信号通路为主要影响对象,得出相应通路蛋白变化情况的通路图(Fig 6)。根据中药-成分-靶点-疾病网络关系、PPI蛋白互作和KEGG通路富集的结果,选择AKT1作为后续分子对接的靶点蛋白。
|
| 图 4 The bar diagram of GO function analysis |
|
| 图 5 The bubble diagram of KEGG pathway |
|
| 图 6 Map of PI3K/AKT signaling pathway |
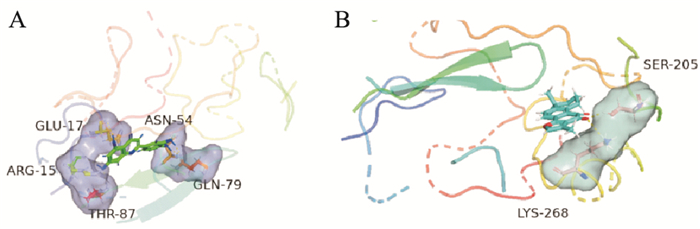
利用SybylX2.0软件,将木犀草素和丹参酮ⅡA分别与AKT1进行分子对接,发现木犀草素与AKT1对接的Total score、crash、polar分别为8.649 2、-0.945 2、6.543,有强烈的结合活性。丹参酮ⅡA与AKT1对接的Total score、crash、polar分别为5.250 7、-0.107 8、1.294 7。通过Pymol软件将分子对接结果优化,如图可知木犀草素和AKT1中的GLU-17、ARG-15、THR-87、ASN-54和GLN-79这5个氨基酸存在较强的氢键作用(Fig 7A)。丹参酮ⅡA与AKT1中的LYS-268和SER-205两个氨基酸有较强的氢键作用(Fig 7B)。说明木犀草素和丹参酮ⅡA对丹参饮药效作用的发挥有重要影响,为研究丹参饮对结肠癌的作用机制提供了理论参考。
|
| 图 7 The docking diagram of AKT1 with Luteolin (A) and Tanshinone ⅡA (B) |
近年来,随着人们饮食多脂化和人口老龄化的加剧,结肠癌的发病率逐年提升。值得注意的是,我国城镇化的发展对结肠癌的发病率同样影响重大。城市人群脂肪相对摄入量远高于农村,因此其发病率高于农村人群[9]。本研究结合结肠癌的古今病因辨证,预测丹参饮可能对结肠癌起着一定的治疗作用。结合网络药理学,将丹参饮的有效化学成分和疾病的对应靶点进行整合,建立有效的中药-成分-靶点-疾病网络关系,并通过PPI蛋白互作确定主要核心靶点蛋白,依托R语言完成通路的预测,最后用分子对接确定结果的有效程度。
其中,PPI蛋白互作结果中核心蛋白主要包括AKT1、Tp53、IL-6、VEGFA、MAPK1、CASP3、JUN、MYC、EGFR、STAT3、CCND1、TOS等。Häggblad等[10]通过研究AKT1、AKT2和AKT1/2基因敲除的结肠癌细胞,发现AKT1和AKT2敲除可以减弱肿瘤细胞的转移和生长。证实核心蛋白AKT1在结肠癌中的重要作用,说明丹参饮可能通过调节上述核心蛋白发挥抗结肠癌活性,然而还需要后续进一步的体内外验证。
从中药-活性成分-靶点-疾病网络关系中可以发现木犀草素和丹参酮ⅡA是丹参饮中的重要活性成分,进一步通过分子对接证实其与关键蛋白AKT1具有相互作用。Kang等[11]发现木犀草素可以抑制转录抑制因子DNA甲基转移酶的表达,降低Nrf2启动子区域的甲基化,增加5-甲基胞嘧啶双加氧酶与Nrf2启动子的结合,确定了木犀草素抗结肠癌的作用机制。此外,Cyanidin-3-葡萄糖氯化物与木犀草素可协同抑制结肠癌和乳腺癌细胞的生长[12]。Xue等[13]发现丹参酮IIA对人结肠癌细胞增殖、凋亡和迁移的影响与下调mTOR和VEGF表达有关。另有学者[14]发现丹参酮IIA可以抑制COX-2的表达,激活Wnt/β-catenin信号通路,进而下调VEGF的表达水平,最终抑制结肠癌细胞生长。从中可以看出木犀草素和丹参酮ⅡA对结肠癌细胞有显著的抑制作用,而目前关于两者靶向AKT1的抗肿瘤机制鲜有报道,因此可能是潜在的候选抗结肠癌药物。
此外,KEGG通路分析发现PI3K/AKT信号通路可能是丹参饮治疗结肠癌的关键信号通路。Bishnupuri等[15]发现结肠肿瘤上皮中PI3K/AKT信号激活显著促进β-catenin核转位、细胞增殖和抗凋亡。Ma等[16]发现成纤维细胞来源的趋化因子可以促进结肠癌细胞分泌趋化因子CXCL6和CXCL12,并通过PI3K/AKT/mTOR信号通路,协同调节肿瘤转移,因此阻断该途径是结肠癌患者潜在的抗转移治疗靶点之一。此外,趋化因子CXCL12调节PTEN表达,并通过PI3K/AKT信号调节结肠癌细胞的增殖和侵袭能力[17],暗示PTEN或PI3K功能的修饰是抑制结肠癌侵袭性扩散的原因所在。人参皂苷Rh2诱导结肠癌细胞SW480凋亡也与抑制PI3K/AKT/GSK-3β信号通路有关,其机制可能是通过激活p53和caspase-3活化,下调Bcl-2/Bax比例[18]。总结以上研究可知,PI3K/AKT信号通路可能是丹参饮治疗结肠癌的关键通路。
综上所述,丹参饮具有活血行气、祛湿止痛的功效,其对结肠癌的治疗或许可以起到一定的积极意义,作用机制可能与调节PI3K/AKT信号通路有关。在世界文化交流日益频繁的大背景下,在中西医结合治疗的大潮流下,中药多靶点、多途径给药的优势彰显无遗。随着各种癌症发病率的日益增多,中药的地位日益显著。然而,对于疾病的攻克和治疗,仍然需要广大研究者的努力探究和挖掘。
| [1] |
张滔, 胡玲, 唐加峰, 等. 二甲双胍激活AMPK/p53调节尿素循环抑制结肠癌HCT116细胞增殖[J]. 中国药理学通报, 2020, 36(10): 1361-7. Zhang T, Hu L, Tang J F, et al. Metformin activates AMPK/p53 to regulate urea cycle and inhibits proliferation of colon cancer HCT116 cells[J]. Chin Pharmacol Bull, 2020, 36(10): 1361-7. doi:10.3969/j.issn.1001-1978.2020.10.007 |
| [2] |
程海波, 周仲瑛, 李柳, 等. 基于癌毒病机理论的中医肿瘤临床辨治体系探讨[J]. 中医杂志, 2015, 56(23): 1989-92. Cheng H B, Zhou Z Y, Li L, et al. Discussion on system of clinical syndrome differentiation on Chinese medicine oncology based on pathogenesis theory of cancerous toxin[J]. J Tradit Chin Med, 2015, 56(23): 1989-92. |
| [3] |
高小明. 八珍汤加减对结肠癌术后气血两虚型患者辅助化疗减毒作用的临床研究[D]. 福建: 福建中医药大学, 2015. Gao X M. The clinical research of attenuated about Ba Zhen Tang subtraction adjuvant chemotherapy in patients with colon cancer postoperative deficiency of Qi and Blood[D]. Fujian: Fujian Univ Tradit Chin Med, 2015. |
| [4] |
秦洁. 健脾益气, 补肾填精方联合奥沙利铂+CF/5-FU方案治疗大肠癌的临床研究[D]. 南京: 南京中医药大学, 2009. Qin J. Clinical study of strengthen the spleen to reinforcing Qi, tonify kidney to nourishing essence prescription with L-OHP+CF/5-FU chemotherapy in the treatment of patients with colorectal tumor[D]. Nanjing: Nanjing Univ Tradit Chin Med, 2009. |
| [5] |
张科, 李春耕. 中医药治疗结肠癌基础研究进展[J]. 国际中医中药杂志, 2020, 42(9): 936-8. Zhang K, Li C G. Progress of the basic research on traditional Chinese medicine treating colon cancer[J]. Int J Tradit Chin Med, 2020, 42(9): 936-8. doi:10.3760/cma.j.cn115398-20190130-00224 |
| [6] |
孔令雷, 杜冠华. 丹参饮的现代研究进展[J]. 中药药理与临床, 2019, 35(3): 197-200. Kong L L, Du G H. The progress of research on Danshen Yin[J]. Pharmacol Clin Chin Mater Med, 2019, 35(3): 197-200. |
| [7] |
王程, 杨运高, 王学良. 活血化瘀经典方剂对小鼠大肠癌肝转移模型端粒酶及p53、c-erbB-2、Bcl-2基因表达的影响[J]. 第一军医大学学报, 2004(7): 758-60. Wang C, Yang Y G, Wang X L. Expressions of hTERT, p53, c-erbB-2 and Bcl-2 in colonic adenocarcinoma mouse models with liver metastases: effects of classical traditional Chinese medicine prescriptions for promoting circulation and removing blood stasis[J]. J First Mil Med Univ, 2004(7): 758-60. |
| [8] |
王学良. 抵当汤对小鼠结肠癌细胞脾种植肝转移模型影响的实验研究[D]. 广州: 第一军医大学, 2004. Wang X L. Experimental study on effect of Didangtang to the model of CT-26 cell spleen transplant and liver metastasis of mice colorectal cancer[D]. Guangzhou: First Mil Med Univ, 2004. |
| [9] |
林燕, 马蕾, 布力布·吉力斯汉, 等. 中医药辅助治疗结肠癌的应用研究进展[J]. 中国药师, 2018, 21(9): 1637-40. Lin Y, Ma L, Bulibu J, et al. Application of traditional Chinese medicine in the adjuvant treatment of colon cancer[J]. China Pharm, 2018, 21(9): 1637-40. |
| [10] |
Häggblad Sahlberg S, Mortensen A C, Haglöf J., et al. Different functions of AKT1 and AKT2 in molecular pathways, cell migration and metabolism in colon cancer cells[J]. Int J Oncol, 2017, 50(1): 5-14. doi:10.3892/ijo.2016.3771 |
| [11] |
Kang K A, Piao M J, Hyun Y J, et al. Luteolin promotes apoptotic cell death via upregulation of Nrf2 expression by DNA demethylase and the interaction of Nrf2 with p53 in human colon cancer cells[J]. Exp Mol Med, 2019, 51(4): 1-14. |
| [12] |
Yin H, Wang L, Wu M, et al. Cyanidin-3-O-glucoside chloride acts synergistically with luteolin to inhibit the growth of colon and breast carcinoma cells[J]. Pharmazie, 2019, 74(1): 54-61. |
| [13] |
Xue J, Jin X, Wan X, et al. Effects and mechanism of tanshinone ⅡA in proliferation, apoptosis, and migration of human colon cancer cells[J]. Med Sci Monit, 2019, 25: 4793-800. doi:10.12659/MSM.914446 |
| [14] |
Ma S, Lei Y, Zhang L, et al. Research on the inhibiting effect of tanshinone ⅡA on colon cancer cell growth via COX-2-Wnt/β-catenin signaling pathway[J]. J BUON, 2018, 23(5): 1337-42. |
| [15] |
Bishnupuri K S, Alvarado D M, Khouri A N, et al. IDO1 and kynurenine pathway metabolites activate PI3K-Akt signaling in the neoplastic colon epithelium to promote cancer cell proliferation and inhibit apoptosis[J]. Cancer Res, 2019, 79(6): 1138-50. doi:10.1158/0008-5472.CAN-18-0668 |
| [16] |
Ma J, Sun X W, Su H, et al. Fibroblast-derived CXCL12/SDF-1α promotes CXCL6 secretion and co-operatively enhances metastatic potential through the PI3K/Akt/mTOR pathway in colon cancer[J]. World J Gastroenterol, 2017, 23(28): 5167-78. doi:10.3748/wjg.v23.i28.5167 |
| [17] |
Ma J, Sun X, Wang Y, et al. Fibroblast-derived CXCL12 regulates PTEN expression and is associated with the proliferation and invasion of colon cancer cells via PI3k/Akt signaling[J]. Cell Commun Signal, 2019, 17(1): 119. doi:10.1186/s12964-019-0432-5 |
| [18] |
石雪萍, 李静, 冉建华, 等. 人参皂苷Rh2调控PI3K/AKT/GSK-3β信号通路诱导人结肠癌细胞凋亡[J]. 中国药理学通报, 2017, 33(1): 114-9. Shi X P, Li J, Rang J H, et al. Ginsenoside Rh2 induced human colorectal cancer cell apoptosis through PI3K/AKT/GSK-3β pathway[J]. Chin Pharmacol Bull, 2017, 33(1): 114-9. doi:10.3969/j.issn.1001-1978.2017.01.020 |

