

2. 中国人民解放军联勤保障部队第九四〇医院,甘肃 兰州 730050
贾正平(1957-),男,博士,教授,博士生导师,研究方向:抗高原缺氧研究,通讯作者,E-mail:pharmapaper@163.com
2. PLA Joint Logistic Support Hospital 940 Hospital, Lanzhou 730050, China
氟西汀是目前临床常用的抗抑郁药,其作用机制是作为选择性5-羟色胺再摄取抑制剂来抑制神经元对5-羟色胺的再摄取。最近有学者报道,氟西汀还具有神经保护作用,Zhao等[1]发现氟西汀处理的抑郁症大鼠神经元凋亡减少,凋亡蛋白Bax、cleaved caspase-3水平下调;Zeng等[2]报道氟西汀通过PI3K/Akt/Fox03a和PKA/CREB信号通路对抗皮质酮所致的PC12细胞损伤发挥保护作用;Hu等[3]发现氟西汀可改善脑缺血小鼠的记忆障碍,其可能机制是氟西汀可以促进细胞实验中海马神经干细胞的存活,增加海马回和齿状回区神经细胞增殖,抑制细胞凋亡。
课题组在前期抗高原缺氧损伤研究中发现,由模拟高原环境引起的大鼠高原脑水肿模型中脑组织5-羟色胺转运蛋白(serotonin transporter, SERT)蛋白和基因表达量均显著上升,预先服用抗高原缺氧损伤药物后,不但高原脑水肿发病情况明显减轻,而且SERT的表达量也显著下降。用体外培养PC12细胞可以模拟这一过程。我们为此提出假说:SERT高表达也许是缺氧环境引起高原脑水肿的重要原因,抑制其高表达可能预防高原脑水肿。由于氟西汀是SERT抑制剂,故我们推测应用氟西汀有可能获得抗缺氧损伤效果。本实验首先考察了氟西汀对PC12细胞缺氧损伤的保护作用,得到了理想的结果,初步证明本假说的科学性,现报道如下。
1 材料与方法 1.1 材料 1.1.1 主要仪器CO2细胞培养箱(Thermo公司,美国);缺氧处理小室(STEMCELL,加拿大);氧浓度检测仪(EST-10,CSE,美国);荧光倒置相差显微镜(IX3-SVR,Olympus,日本);免疫印迹分析仪(1703930,Bio-Rad,美国);高分辨活细胞成像系统(Delta Vision Ultra,Cytiva,美国)。
1.1.2 细胞株PC12细胞(ATCC CRL-1721.1TM),购自美国模式培养物集存库(American type culture collection, ATCC)。
1.1.3 药物与试剂盐酸氟西汀(Y110140,MCE,美国);F-12K培养基(21127022,Gibco,美国);马血清(04-004-1,ABI,以色列);胎牛血清(10099-141,Gibco,美国);CCK-8(BA00208,博奥森生物,中国);乳酸脱氢酶(A020-2-2,LDH)、丙二醛(A003-4-1,MDA)、超氧化物歧化酶(A001-3-2,SOD)和过氧化氢酶(A007-1-1,CAT)试剂盒购于南京建成生物;MAP2 (ab32454)、Bax (ab170114)、Bcl-2 (ab196495) 和caspase-3(ab13847)抗体购自英国Abcam公司;RIPA裂解液(R0020)、4×缓冲液(P1015)、SDS-PAGE凝胶制备试剂盒(P1200)、ECL等购于北京索莱宝公司。
1.2 实验方法 1.2.1 细胞培养取对数生长期的PC12细胞,0.25%的胰酶消化,用含15%马血清、2.5%胎牛血清的F-12K培养基培养,每隔2-3 d更换一次培养液。
1.2.2 免疫荧光染色将细胞传代接种于铺有细胞爬片的6孔板中,待细胞贴壁并长满80%皿底后进行缺氧及加药处理,之后弃掉培养液,用PBS洗片,加入预冷的4%多聚甲醛固定10 min,洗片,加入0.1% Triton X-100透膜10 min,洗片,加入免疫荧光封闭液封闭1 h,弃封闭液,不洗,直接加入MAP2一抗,4 ℃冰箱过夜,次日洗片后,加入二抗,4 ℃冰箱避光孵育过夜,d3早晨从冰箱取出,洗掉二抗后,DAPI孵育15 min,避光封片,放置阴暗环境下晾干,用活细胞工作站观察染色情况。
1.2.3 缺氧损伤模型的建立待培养于中皿的PC12细胞长至接近融合后,将其转入缺氧盒中,通入94% N2、1% O2和5% CO2的混合气,氧浓度降至1%后开始计时,18 h后观察细胞形态并进行各项指标的检测。
1.2.4 药物处理准确称取盐酸氟西汀3.457 9 mg,融入100 μL DMSO后得到浓度为0.1 mol· L-1的盐酸氟西汀母液,逐级稀释,吸10 μL上级浓度,加入到90 μL的DMSO中,得到浓度分别为10-2、10-3、10-4和10-5 mol·L-1溶液,放入-20 ℃保存待用。用培养基稀释时,需现配现用。
1.2.5 细胞活力检测采用CCK-8试剂盒。将对数生长期的细胞接种至96孔板,细胞浓度为每孔1×104个细胞。待细胞贴壁后,加入盐酸氟西汀,使其终浓度为10、1、0.1和0.01 μmol·L-1,每个浓度设6个复孔。将缺氧对照组和加药组放入缺氧盒中缺氧处理18 h后,加入CCK-8,放入培养箱继续培养1 h,在450 nm波长下测定吸光度(A)。根据A值高低筛选出盐酸氟西汀作用的最佳药物浓度。
1.2.6 氧化产物含量和抗氧化酶活性检测从培养箱中取出培养皿,收集培养液用于检测LDH活性。培养皿弃掉剩余培养基,用预冷的PBS洗细胞3次,大皿细胞加800 μL裂解液,中皿加300 μL裂解液,冰上裂解20 min,吸上清至1.5 mL的离心管中,4 ℃低温离心机中,12 000 r·min-1离心15 min,取上清,分别检测MDA含量和SOD、CAT酶活性,蛋白浓度采用BCA法检测。
1.2.7 Western blot检测相关蛋白的表达从培养箱中取出细胞操作同上。在细胞裂解液中加入4×缓冲液,100 ℃沸水煮15 min,制备好的蛋白样品-80 ℃备用。按每孔20 μg上样,以5%浓缩胶、12%分离胶的SDS-PAGE分离蛋白,湿法将蛋白转至PVDF膜上后,用5%脱脂牛奶封闭2 h后,孵一抗Bcl-2(1 ∶ 1 000)、Bax(1 ∶ 500)、caspase-3(1 ∶ 2 000)、β-actin (1 ∶ 4 000),在常温下摇床孵育1 h后放入4 ℃冰箱过夜,洗膜,加入二抗,室温孵育2 h,洗膜,化学发光法显色,灰度值用ImageJ 6.0软件分析。
1.3 统计学处理量化结果均用x±s表示,采用SPSS 25.0统计软件对各组之间进行统计学分析,多组间比较采用单因素方差分析。
2 结果 2.1 PC12细胞的鉴定MAP2是神经元的特异性标记物,可作为神经元的标志性蛋白。本实验使用绿色荧光标记的anti-MAP2抗体检测PC12细胞的MAP2表达情况。结果PC12细胞染色呈阳性(Fig 1),表明该PC12细胞为神经元样细胞。

|
| Fig 1 MAP2 protein expression in PC12 cells in vitro (×60) (A): MAP2 protein expression by immunofluorescence staining; (B): Nuclear DAPI; (C): Merge MAP2 and DAPI |
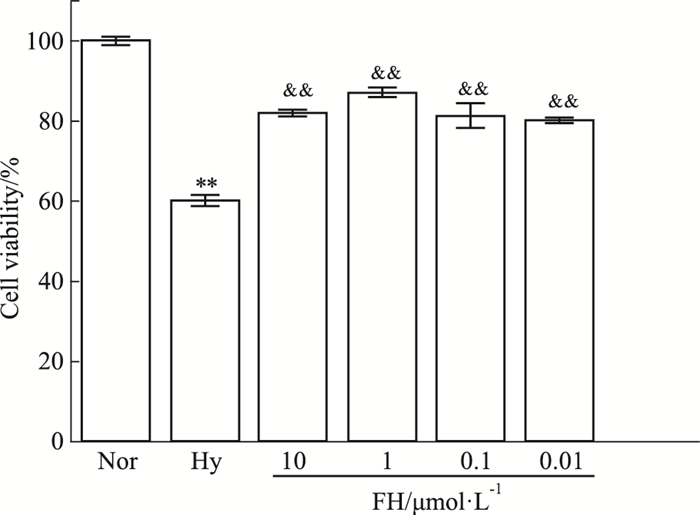
与常氧对照(Normoxia,Nor) 组相比(设定细胞存活率为100%),缺氧模型(Hypoxia,Hy) 组的细胞存活率活力仅为60%,低于Nor组(P<0.01),表明细胞缺氧模型建立成功。盐酸氟西汀(Fluoxertine hydrochloride,FH) 各组均高于模型组(P<0.01),以10-6 mol·L-1最高,之后逐渐下降,说明在该浓度下细胞存活率最高,因此后续实验均在该浓度下进行,见Fig 2。
|
| Fig 2 Effect of fluoxetine on cell viability of PC12 cells in hypoxia condition (x±s, n=4) **P<0.01 vs Nor group; &&P<0.01 vs Hy group. |
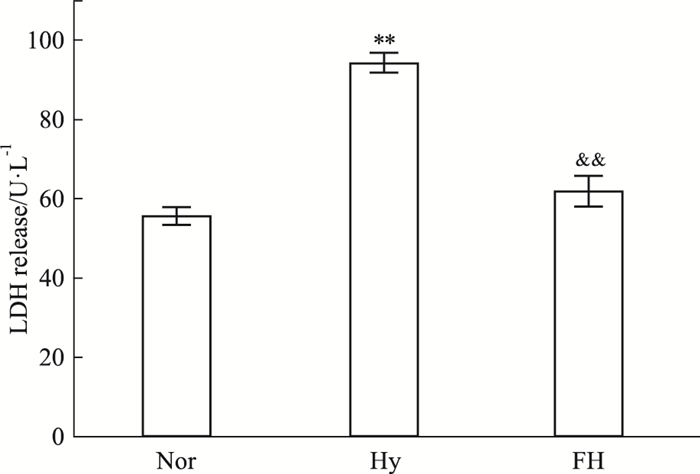
LDH是公认的细胞损伤标志物。与Nor组相比,Hy组培养基中LDH含量明显升高(P<0.01),表明缺氧导致PC12细胞膜损伤,细胞内的LDH外泄到细胞培养液中。而与Hy组比,经盐酸氟西汀处理后,LDH水平降低(P<0.01),说明盐酸氟西汀能够维持细胞膜的完整性,减轻缺氧对PC12细胞的损伤,见Fig 3。
|
| Fig 3 Effect of fluoxetine hydrochloride on hypoxia-induced LDH leakage in PC12 cells (x±s, n=4) **P<0.01 vs Nor group; &&P<0.01 vs Hy group. |
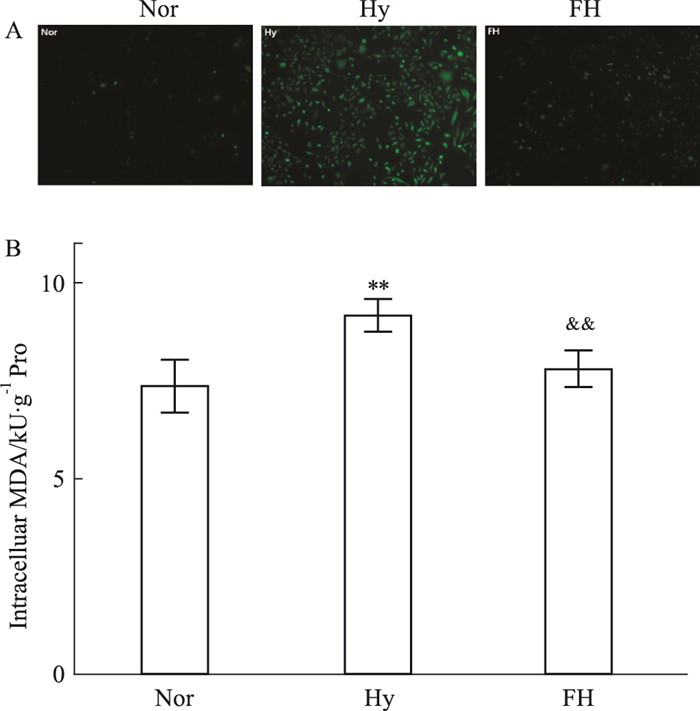
活性氧(reactive oxygen species,ROS)和丙二醛(Malondialdehyde,MDA)是最主要的氧化损伤指标。如Fig 4A所示,ROS染色后发绿色荧光,与Nor组相比,Hy组胞内ROS含量明显增高,而FH组的ROS表达量没有明显增加,低于Hy, 而与Nor组差异无统计学意义。MDA含量的变化与ROS相同, 如图Fig 4B。以上结果说明氟西汀可以有效缓解缺氧导致的胞内氧化损伤。
|
| Fig 4 Effect of fluoxetine hydrochloride on ROS and MDA content level in PC12 cells under hypoxia (×40, x±s, n=4) **P<0.01 vs Nor group; &&P<0.01 vs Hy group. |
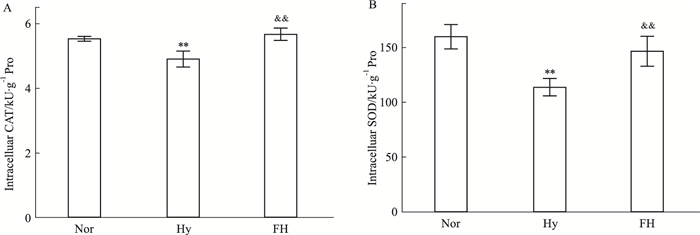
与Nor组相比,Hy组的CAT活性显著降低(P<0.01),但FH组并没降低,且显著高于Hy组(P<0.01),而与Nor组处于同一水平(Fig 5A)。SOD活性的变化与CAT相似(Fig 5B),表明盐酸氟西汀能够抵御缺氧造成的氧化损伤,显著提高抗氧化酶活性。
|
| Fig 5 Effect of fluoxetine hydrochloride on CAT content and SOD level in PC12 cells under hypoxia (x±s, n=4) **P<0.01 vs Nor group; &&P<0.01 vs Hy group. |
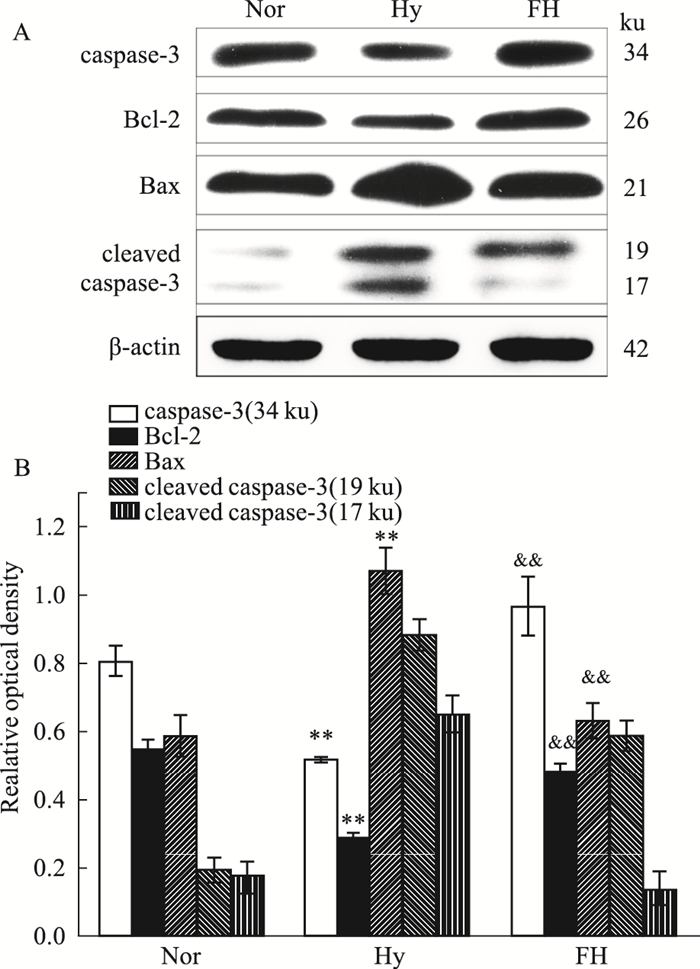
与Nor组比较,Hy组中促凋亡蛋白Bax的表达量增加(P<0.01),而抗凋亡蛋白Bcl-2和caspase-3下降。FH组与Hy组相比,促凋亡蛋白表达量下降而抗凋亡蛋白表达量上升(P<0.01), 表明盐酸氟西汀抑制缺氧导致的细胞凋亡(Fig 6)。
|
| Fig 6 Effect of fluoxetine on expression of apoptosis-related protein hypoxia condition **P < 0.01 vs Nor group; &&P < 0.01 vs Hy group. |
我国虽然拥有960万平方米的陆地面积,但高原地区面积占国土面积的26.04%。高原地区氧含量稀薄,人在急进高原时,大脑不能适应高原地区氧含量的急剧变化,会由于供氧不足而出现视觉、记忆力、思维和注意力不同程度下降的症状,即发生所谓高原反应[4]。研究预防和治疗高原反应对于在高原地区开展国防和经济建设具有重大意义。目前市场上可供选择的的抗高原缺氧药物非常匮乏,美国FDA唯一批准的乙酰唑胺副作用较多,而中药红景天资源有限。因此,寻找新的疗效好、副作用少的抗高原缺氧药物是当务之急。
PC12细胞是大鼠肾上腺髓质嗜铬瘤细胞,与神经元细胞具有相近的形态、结构和功能[5-6],是体外实验中模拟神经元功能的重要细胞株,我们利用实验室已经建立成熟稳定的PC12缺氧损伤模型[7-8]研究发现,缺氧时PC12细胞内的LDH、ROS和MDA含量都相对增加,其中LDH的增加表明细胞在缺氧环境中受到损伤,ROS和MDA的增加表明缺氧后胞内发生氧化性损伤,抗氧化酶SOD和CAT活性的降低表明细胞抵抗氧化损伤的能力下降。氟西汀能够抑制LDH、ROS和MDA的增加,提高SOD和CAT活性,表明其缓解了缺氧对PC12细胞造成的氧化性损伤。低氧导致PC12细胞中cleaved caspase-3和Bax的表达升高,Bcl-2的表达降低。氟西汀治疗可抑制这种变化趋势,减少细胞凋亡,改善PC12细胞在缺氧环境下的生存状态。
虽然氟西汀是临床常用的抗抑郁药,但近年来的许多实验研究证明,其对神经细胞损伤具有保护作用。氟西汀对于皮质酮造成的PC12细胞损伤的保护作用可能是通过提高FoxO3a、Akt和CREB表达及其磷酸化水平[9]。氟西汀对神经干细胞具有保护作用,其机制是上调神经营养因子的转录和翻译,促进神经干细胞活化为星形胶质细胞,进而促进受损神经元组织的修复[10]。氟西汀具有抗炎作用,其作用机制可能是激活迷走神经抗炎途径,从而减轻周围神经组织和大脑中的炎症反应。氟西汀和西酞普兰的抗炎作用归因于5-羟色胺依赖性和5-羟色胺非依懒性。本课题组在后续研究中发现,缺氧损伤后细胞内的5-羟色胺含量较常氧对照组升高,而给予盐酸氟西汀后,5-羟色胺含量下降。说明氟西汀极有可能通过影响胞内5-羟色胺的含量来发挥其抗缺氧损伤活性。
综上所述,本实验首次发现氟西汀对体外培养缺氧细胞具有保护作用,其机制可能与氟西汀对胞内5-羟色胺含量的调节作用有关,但详细机制还有待于进一步研究。本实验结果提示氟西汀除作为抗抑郁药外,还具有开发为抗缺氧损伤新药的潜力,这也为抗高原缺氧药物的研发提供了一条新思路。
| [1] |
Zhao Y, Shang P, Wang M, et al. Neuroprotective effects of fluoxetine against chronic stress-induced neural inflammation and apoptosis: involvement of the p38 activity[J]. Front Physiol, 2020, 11: 351. doi:10.3389/fphys.2020.00351 |
| [2] |
Zeng B, Li Y, Niu B, et al. Involvement of PI3K/Akt/FoxO3a and PKA/CREB signaling pathways in the protective effect of fluoxetine against corticosterone-induced cytotoxicity in PC12 cells[J]. J Mol Neurosci, 2016, 59(4): 567-78. doi:10.1007/s12031-016-0779-7 |
| [3] |
Hu H M, Li B, Wang X D, et al. Fluoxetine is neuroprotective in early brain injury via its anti-inflammatory and anti-apoptotic effects in a rat experimental subarachnoid hemorrhage model[J]. Neurosci Bull, 2018, 34(6): 951-62. doi:10.1007/s12264-018-0232-8 |
| [4] |
Gudbjartsson T, Sigurdsson E, Gottfredsson M, et al. High altitude illness and related diseases-a review[J]. Laeknabladid, 2019, 105(11): 499-507. |
| [5] |
杨泽霖, 洪桂祝, 张小琴, 等. 红景天苷对CoCl2诱导PC12细胞低氧损伤的神经保护作用[J]. 中国药理学通报, 2019, 35(4): 530-4. Yang Z L, Hong G Z, Zhang X Q, et al. Neuroprotective effect of salidroside on CoCl2-induced hypoxia injury in PC12 cells[J]. Chin Pharmacol Bull, 2019, 35(4): 530-4. doi:10.3969/j.issn.1001-1978.2019.04.017 |
| [6] |
景临林, 杨颖, 武柠子, 等. 黄芩素-7-甲醚对缺氧致PC12细胞损伤的保护作用[J]. 中国现代应用药学, 2018, 35(6): 787-92. Jing L L, Yang Y, Wu N Z, et al. Protective effect of negletein against hypoxia induced injury on PC12 cells[J]. Chin J Mod Appl Pharm, 2018, 35(6): 787-92. |
| [7] |
Zeng B, Li Y, Niu B, et al. Involvement of PI3K/Akt/FoxO3a and PKA/CREB signaling pathways in the protective effect of fluoxetine against corticosterone-induced cytotoxicity in PC12 cells[J]. J Mol Neurosci, 2016, 59(4): 567-78. doi:10.1007/s12031-016-0779-7 |
| [8] |
强晓菲. 氟西汀促进脑神经功能修复的机制研究[D]. 石家庄: 河北医科大学, 2013. Qiang X F. The research of Fluoxetine's mechanism on promote the repairation of cranial nerve function[D]. Shijiazhuang: Hebei Med Univ, 2013. |
| [9] |
Ondicova K, Tillinger A, Pecenak J, et al. The vagus nerve role in antidepressants action: Efferent vagal pathways participate in peripheral anti-inflammatory effect of fluoxetine[J]. Neurochem Int, 2019, 125: 47-56. doi:10.1016/j.neuint.2019.02.003 |
| [10] |
Di Rosso M E, Palumbo M L, Genaro A M. Immunomodulatory effects of fluoxetine: A new potential pharmacological action for a classic antidepressant drug[J]. Pharmacol Res, 2016, 109: 101-7. doi:10.1016/j.phrs.2015.11.021 |

