


杜冠华(1956-),男,博士,研究员,博士生导师,研究方向:心脑血管药理学,通讯作者,E-mail: dugh@imm.ac.cn
肺动脉高压(pulmonary artery hypertension,PAH)是一种慢性进行性疾病,可能是多种不明病因引起的原发性疾病,也可能是心肺功能异常相关疾病的并发症,其病因复杂,发病率和死亡率高[1-2];PAH定义为静息时通过右心导管测量的平均肺动脉压≥ 3.325 kPa,肺毛细血管楔压≤ 1.995 kPa。PAH以肺动脉增生、血管重构和血管收缩为关键特征,随着肺血管阻力及肺动脉压的进行性升高,最终导致右心衰竭和死亡。
肺动脉平滑肌细胞(pulmonary artery smooth muscle cell,PASMC)、肺血管内皮细胞和肺成纤维细胞是构成肺血管壁的主要细胞,这些细胞结构和功能的异常变化是导致血管重构和血管收缩的主要原因[3]。与PAH血管重构的特定特征包括肺远端小动脉的肌肉化、内皮细胞的功能失调、PASMC的增殖和凋亡、血管周围炎症以及细胞外基质(extracellular matrix,ECM)蛋白的沉积[4]。尽管近年来在药物治疗方面有所进步,但是PAH患者的生存率仍低下。
随着“组学”研究的进展,基于核糖核酸(ribonucleic acid,RNA)的PAH分子机制逐渐被发现。进一步研究PAH的发病机制及尝试新的治疗方法逆转血管重构进而阻断PAH进展,可能将有助于提高患者的生活质量及生存率。
1 circRNA的生物学特性环状RNA(circular RNA,circRNA)是非编码RNA家族的新成员,其特征是共价闭环结构而没有5′末端帽或3′末端多聚(A)尾。最初,circRNA被认为是正常剪接过程的无功能副产物;随着第二代测序的出现,人们发现circRNA广泛分布于各种细胞类型的稳定实体中,并以物种、组织、疾病和发育阶段特异性的方式表达[5]。
circRNA具有多种生物学功能。位于细胞核中的circRNA可能参与转录的调控和选择性剪接[6];circRNA还可以被翻译成蛋白质;其中,最被广泛研究的功能是其作为微小RNA(microRNA,miRNA)海绵发挥作用的能力。circRNA分子富含miRNA应答元件,可通过与miRNA发生海绵作用,减轻miRNA对靶基因的抑制效果,上调靶基因的表达。相较于其他类型的内源性RNA(competitive endogenous RNA,ceRNA),circRNA在细胞中表达量高且稳定性强,并具有更多与miRNA结合的位点,能够更加快速、稳定地结合或释放大量miRNA,高效发挥其调控miRNA的作用,比线性的ceRNA更具有突出的ceRNA活性。circRNA也可能是细胞外miRNA海绵,其可能存在病毒miRNA的结合位点,进而与病毒miRNA结合,破坏免疫应答[7]。研究circRNA这一独特的功能为我们对PAH等心血管疾病潜在的分子生物学机制的理解,以及新型诊断生物标志物和创新治疗策略的可能性提供新的方向。
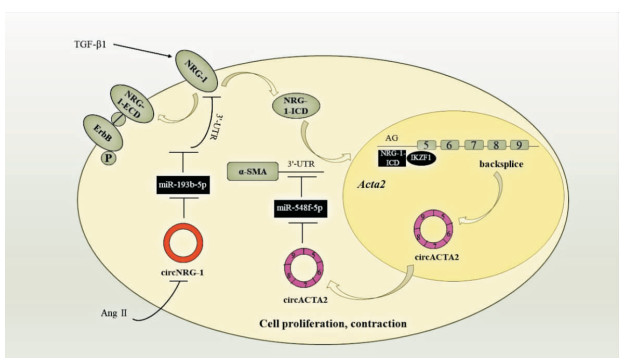
2 circRNA参与PAH形成 2.1 circRNA参与PAH形成的NRG-1相关信号通路神经调节蛋白-1(neuregulin-1,NRG-1)在血管的生理病理学中起着重要作用。研究发现,在血管平滑肌细胞(vascular smooth muscle cell,VSMC)中,转化生长因子-β1(transforming growth factor-β1,TGF-β1)可以诱导大量表达的NRG-1被蛋白水解酶切割,释放其表皮细胞生长因子样序列的细胞外结构域(extracellular domain,NRG-1-ECD)和高度保守的细胞内结构域(intracellular domain,NRG-1-ICD)来调节VSMC表型。首先,NRG-1在血管内皮细胞和VSMC中表达,其受体定位于底层VSMC中[8];其次,NRG-1-ECD是一种生物活性片段,可与ErbB家族受体酪氨酸激酶结合以激活靶细胞中的ErbB信号传导[9];第三,TGF-β1和血小板衍生的生长因子(platelet-derived growth factor,PDGF)是影响VSMC分化的2种关键细胞因子[10],分别增加和减少NRG-1-ICD的表达[11](Fig 1)。
|
| Fig 1 NRG-1 could be cleaved into NRG-1-ECD and NRG-1-ICD under the stimulation of TGF-β1 to regulate the VSMC phenotype. In nucleus, NRG-1-ICD induced the formation of circACTA2 and up-regulated the expression of α-SMA; in cytoplasm, NRG-1-ECD reduced the phosphorylation level of ErbB receptor NRG-1: Neuregulin-1; TGF-β1: Transforming growth factor-β1; Ang Ⅱ: Angiotensin Ⅱ; α-SMA: smooth muscle actin α; IKZF1: IKAROS family zinc finger 1; VSMC: vascular smooth muscle cell. |
NRG-1/ErbB信号传导是调节血管重构的重要潜在机制。Grant等[12]指出,调节ErbB信号通路可导致细胞凋亡增加和克隆形成生存的丧失,并且细胞增殖也已被证明与PAH有关。在血管重构的早期阶段,低浓度的血管紧张素Ⅱ(angiotensin Ⅱ,Ang Ⅱ)可能会抑制小鼠VSMC中circNRG-1的表达。下调的circNRG-1充当miR-193b-5p的海绵或ceRNA,显著提高miR-193b-5p的水平;miR-193b-5p通过靶向其3′-非翻译区(untranslated regions,UTR)抑制VSMC中NRG-1的表达[8]。NRG-1-ECD的低表达通过降低ErbB受体的磷酸化水平,降低VSMC的凋亡基因cleaved-caspase-3和bax,并增加抗凋亡基因bcl-2的表达水平,从而抑制细胞凋亡[8]。而NRG-1过表达可以逆转Ang Ⅱ对VSMC凋亡的抑制作用。
2.1.2 circACTA2/miR-548f-5p/α-SMA平滑肌α-肌动蛋白(smooth muscle actin α,α-SMA/Acta2)是VSMC收缩机制的关键组成部分,对血管壁稳态所需的肌动蛋白细胞骨架动力学至关重要。α-SMA表达的细微变化可能会对正常的血管功能产生影响,并促进血管疾病的进展。在VSMC的细胞质中,NRG-1-ICD通过与α-SMA相互作用,参与丝状肌动蛋白的形成,参与细胞骨架的组成,增强VSMC的收缩[11];而NRG-1-ICD被TGF-β1刺激后转移到细胞核中[11],通过募集锌指转录因子-IKZF1并形成稳定的转录复合物,该复合物与Acta2基因的第一个内含子相互作用,诱导circACTA2形成[13]。充当海绵结合miR-548f-5p的circACTA2与靶向α-SMA信使RNA(messenger RNA,mRNA)3′UTR的miR-548f-5p相互作用,减轻miR-548f-5p的抑制作用,上调α-SMA的表达,从而促进VSMC中的应力纤维形成、细胞收缩和内膜增生[11, 13]。同时,α-SMA在细胞质中以更高的水平表达并与NRG-1-ICD相互作用。
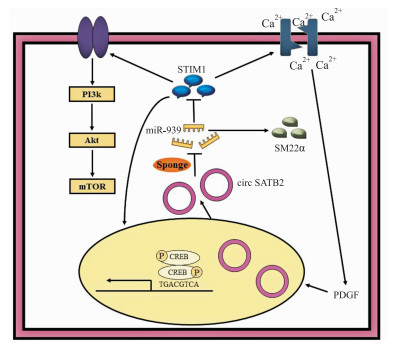
2.2 circRNA参与PAH形成的STIM1相关信号通路PDGF刺激可以上调circ-SATB2和基质相互作用分子1(stromal interaction molecule 1,STIM1)的表达,但抑制miR-939的表达。miR-939在circ-SATB2(由SATB2基因产生)上具有多个结合位点,STIM1是miR-939的重要靶基因。研究发现,circ-SATB2与VSMC的表型调节密切相关,在增殖型VSMC中circ-SATB2被上调,而在收缩型VSMC中被下调。增殖型VSMC中上调的circ-SATB2充当miR-939海绵,抑制miR-939的转录活性并上调STIM1的表达[14](Fig 2)。但circ-SATB2线性序列不能阻断miR-939对STIM1表达的抑制作用。
|
| Fig 2 circ-SATB2 was up-regulated and the expression of STIM1 was up-regulated in the proliferative VSMC, which inhibited the expression of SM22α. STIM1 was closely related to the proliferation and differentiation of VSMC. STIM1 could promote Akt/mTOR pathway activation, significantly increase SOCE, activate CREB phosphorylation, and promote cell proliferation and migration STIM1: Stromal interaction molecule 1; SOCE: store-operated calcium entry; CREB: cAMP response element binding protein; SM22α: smooth muscle 22alpha. |
STIM1与VSMC的增殖分化密切相关。STIM1的过表达可以促进Akt/mTOR途径的活化,导致VSMC生长速度加快,促进其增殖和PAH形成[14]。研究证明,STIM1和Orai1是高度Ca2+选择性SOCE电流I(CRAC)的基本成分;VSMC中敲除STIM1或Orai1的蛋白后,钙库调控钙离子通道(store-operated calcium entry,SOCE)显著降低,可显著抑制Ang Ⅱ介导的Ca2+流入、VSMC增殖和对PDGF的趋化性迁移[15]。此外,针对STIM1的RNA干扰还可以通过抑制环磷酸腺苷应答元件结合蛋白的磷酸化,抑制VSMC增殖和新内膜形成[14]。
平滑肌22α(smooth muscle 22 alpha,SM22α)蛋白,又称转凝蛋白,是收缩型VSMC重要的骨架相关蛋白,是VSMC分化标志物。研究发现,过表达circ-SATB2可以抑制SM22α的表达,并促进细胞的增殖和迁移[14]。而miR-939具有相反的作用,可以促进细胞凋亡并抑制细胞增殖和迁移,靶向circ-SATB2的小干扰RNA具有类似的作用。
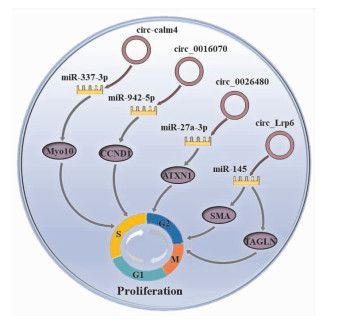
2.3 circRNA参与PAH形成的细胞周期调控通路研究发现,circ-calm4、circ_0016070、circ_0026480和circ_Lrp6等circRNA可以通过调节细胞周期来调节PASMC的增殖和新内膜增生(Fig 3)。
|
| Fig 3 circRNA could regulate VSMC proliferation by regulating cell cycle. circ-calm4/miR-337-3p, circ_0016070/miR-942-5p, circ_0026480/miR-27a-3p, and circ_Lrp6/miR-145 regulated cell cycle by targeting Myo10, CCND1, ATXN1, SMA, and TAGLN, respectively Myo10: Myosin 10; CCND1: Cyclin D1; ATXN1: Ataxin1; SMA: Smooth muscle actin; TAGLN: Transgelin. |
肌球蛋白10(myosin 10, Myo10)是细胞骨架的组成成分,为细胞运动、胞内物质传输、胞质分裂、有丝分裂等提供所需的力,可以调节细胞间信号传递、指导向化性迁移和细胞形状改变等。在小鼠低氧肺组织中,通过生物信息学和实时荧光定量PCR的筛选显示,钙调蛋白4基因(指定为circ-calm4)的可变剪接产生的circRNA明显升高;上调的circ-calm4可以作为miR-337-3p的海绵,吸附并抑制miR-337-3p与Myo10 mRNA的3′-UTR结合,明显提高Myo10的表达水平[16],进而通过调节细胞周期来调节PASMC的增殖。而miR-337-3p抑制缺氧性PASMC的增殖。
2.3.2 circ_0016070/miR-942-5p/CCND1细胞周期蛋白D1(cyclin D1, CCND1)充当“有丝分裂传感器”,调节细胞周期进程,控制细胞从G1到S期的转变。研究发现,CCND1通过促进G1/S期过渡而参与结缔组织生长因子(connective tissue growth factor,CTGF)的功能,从而促进PASMC的增殖和PAH的发生[1]。气管内给予CCND1或CTGF短发夹RNA(short hairpin RNA,shRNA)可明显逆转PAH患者的病情进展。
CCND1被鉴定为miR-942的候选靶基因,miR-942模拟物可以抑制野生型CCND1 3′UTR;circ_0016070通过使miR-942-5p海绵化,增强CCND1的表达[1],减少G1/G0期停滞的细胞数量,进而增加细胞活力,促进PASMC的体内外增殖,与PAH中的血管重构相关。
2.3.3 circ_0026480/miR-27a-3p/ATXN1紫杉醇1(Ataxin1, ATXN1)可使微管稳定,并抑制细胞的有丝分裂和诱导细胞凋亡,有效抑制细胞的增殖。在慢性血栓栓塞性肺动脉高压(chronic thromboembolic pulmonary hypertension,CTEPH)患者外周血样本中发现,circ_0026480的表达被下调,海绵化吸附的miR-27a-3p减少,从而增加miR-27a-3p的表达水平;而ATXN1是上调的miR-27a-3p的靶基因[17],ATXN1的表达降低会促进细胞增殖等。
2.3.4 circ_Lrp6/miR-145/SMA/TAGLN脂蛋白受体6(lipoprotein receptor 6,Lrp6)是在血管中高度表达并与血管病变相关的基因,circ_Lrp6由Lrp6的选择性剪接而成。在鼠类和人类血管疾病中发现,circ_Lrp6与miR-145结合与未结合的比例在调节VSMC表型等血管发病机理中起作用。一项研究发现,病毒转染circ_Lrp6 shRNA可预防小鼠颈动脉内膜增生[10]。当circ_Lrp6沉默时,可以释放被吸附的与增殖分化表型相关的miR-145,降低VSMC分化标志物平滑肌肌动蛋白(smooth muscle actin,SMA)和转胶蛋白(transgelin,TAGLN)的表达,导致细胞迁移能力明显降低,同时降低细胞周期S期中VSMC的百分比,从而抑制其增殖[10]。而circ_Lrp6的过表达能抑制miR-145的表达,恢复受RNA水平调节的miR-145靶标的表达,例如SMA、TAGLN1和赖氨酰氧化酶,从而重建原发性VSMC的增殖能力以及迁移和分化状态。
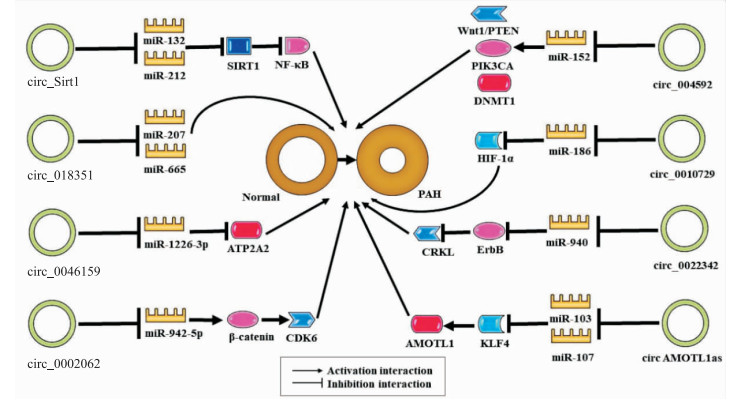
2.4 circRNA参与PAH形成的血管炎症相关通路炎症在PAH形成的肺血管重构中发挥重要作用,如引起内皮细胞功能紊乱、PASMC增殖及成纤维细胞肌化;损伤的血管细胞及活化的血小板可进一步产生炎症因子,正反馈促进血管炎症反应,进一步加重PAH的进程[18]。研究发现,circ_0029642和circ-Sirt1等circRNA介导了PAH的发生, 见Fig 4。
|
| Fig 4 circ_0029642 and circ-Sirt1 mediated PAH by participating in vascular inflammation-related pathways; circ_0022342, circ_0002062, circ_004592 and circ_018351 participated in pulmonary vascular remodeling through mediating cancer-related pathways; in addition, circRNA via HIF-1, ATP2A2, KLF4 and AMOTL1 key molecules had important regulatory effects on PAH formation SIRT1: sirtuin1; CDK6: Cyclin dependent kinase 6; CRKL: CRK like proto-oncogene; HIF-1: Hypoxia-inducible factor 1; KLF4: Kruppel-like factor 4. |
先心病伴PAH患者的肺血管内皮细胞在高血流及高血压所产生的剪切力的作用下, 内皮细胞损伤,导致血小板黏附及激活凝血途径和炎症反应,从而导致内皮细胞中RNA编码酶-腺苷脱氨酶1(adenosine to inosine acting on RNA enzyme 1,ADAR1)升高[19],与circRNA呈负相关的ADAR1导致circ_0029642的表达降低。circ_0029642是由位于13号染色体的CRYLl基因编码的,具有促进细胞代谢,抑制细胞增殖的作用。下调的circ_0029642吸附miRNA的海绵作用减弱, 导致miRNA(如miR-410)升高,最终导致内皮细胞增殖,肺血管重构[19]。
2.4.2 circ-Sirt1/miR-132/212/SIRT1circ-Sirt1(circ_0093887)由沉默信息调节因子2相关酶1(sirtuin1,SIRT1)基因外显子2~7共价闭合环化而成,参与VSMC炎症反应和新内膜增生。核因子κB(nuclear factor kappa-B,NF-κB)的激活,包括核易位和翻译后修饰,是VSMC炎症表型的标志和关键步骤。circ-Sirt1在收缩型VSMC中高表达;在VSMC的细胞质中,circ-Sirt1以序列依赖性方式与肿瘤坏死因子α(tumor necrosis factor α,TNF-α)诱导的核易位直接相互作用形成circ-Sirt1-NF-κBp65失活复合物。同时,过表达的circ-Sirt1还可以作为miR-132/212的miRNA海绵,干扰SIRT1 mRNA,并促进宿主基因SIRT1的表达[20]。升高的SIRT1与核NF-κBp65相互作用,并通过对TNF-α响应而使p65脱乙酰化来抑制NF-κB的转录活性,从而抑制VSMC的炎症表型转换,改善损伤诱导的血管炎症和新内膜形成[21]。而在炎症刺激和新内膜增生状态下circ-Sirt1在收缩型VSMC中的表达下调[20]。
2.5 circRNA参与PAH形成的癌症相关信号通路当受到病毒感染或理化因素刺激时,癌基因被激活而异常表达,其表达产物一般为生长因子或生长因子受体,进而导致细胞过度增生甚至癌变。circ_0022342、circ_0002062、circ_004592和circ_018351等circRNA通过介导癌症途径参与肺血管重构(Fig 4)。
2.5.1 circ_0022342/miR-940/CRKLPAH患者血液样本中circ_0022342表达下调;下调的circ_0022342可以充当miR-940海绵,上调miR-940的表达,而降低ErbB受体的磷酸化水平,导致CRK样原癌基因(CRK like proto-oncogene,CRKL)的表达上调[22]。研究发现,过表达的CRKL可以促进细胞增殖和PAH的发生。
2.5.2 circ_0002062/miR-942-5p/CDK6在CTEPH患者中,表达下调的circ_0002062可以充当miRNA海绵,上调miR-942-5p的表达[22]。miR-942可以通过直接抑制TLE1、GSK3β和sFRP4基因的表达来激活Wnt/β-catenin通路,而细胞周期蛋白依赖性激酶6(cyclin dependent kinase 6, CDK6)富集的与此类癌症相关的途径和轴突引导可能与CTEPH相关。
2.5.3 circ_004592/miR-152miR-152是一种肿瘤抑制因子,可以通过靶向Wnt1、PIK3CA、DNMT1和PTEN基因来抑制细胞的增殖、侵袭和迁移。生物信息学工具分析显示,在缺氧诱导的PAH小鼠肺组织中,上调的circ_004592可抑制miR-742-3p、miR-6373、miR-880-5p、miR-298-3p和miR-152-3p的表达水平,促进miRNA的靶向基因的表达,进而调控肿瘤通路、PI3K-Akt信号传导通路和肌动蛋白骨架等,促进增殖,并抑制肺动脉中内皮细胞、PASMC和成纤维细胞的衰老和凋亡[23]。
2.5.4 circ_018351/miR-207/665PAH小鼠肺组织中下调的circ_018351可以增加miR-6992-3p、miR-5133、miR-6936-5p、miR-7015-3p、miR-207和miR-665的表达水平,降低miRNA靶向基因的表达,进而调控癌症途径、PI3K-Akt信号传导途径、肌动蛋白细胞骨架、癌症中的蛋白聚糖和MAPK信号传导途径,抑制内皮细胞、PASMC和成纤维细胞的凋亡,进一步增加肺血管的压力[23]。
2.6 circRNA参与PAH形成的其他相关信号通路除上述信号传导通路外,circRNA通过缺氧诱导因子1(hypoxia-inducible factor 1,HIF-1)、ATP酶肌浆/内质网Ca2+转运2(ATP2A2)、Kruppel样因子4(Kruppel-like factor 4,KLF4)、血管抑素结合蛋白样蛋白1(angiomotin like protein 1,AMOTL1)等关键分子对PAH的形成也有着重要调节作用(Fig 4)。
2.6.1 circ_0010729/miR-186/HIF-1αHIF-1由HIF-1α和HIF-1β两个亚基组成。HIF-1α与缺氧诱导的细胞凋亡密切相关,可以调控一些对细胞适应性有着重要影响的miRNA,同时miRNA也可以作用于HIF-1α[24]。在缺氧诱导的人血管内皮细胞中,circ_0010729明显上调。功能获得实验证明circ_0010729的表达增加,可以使miR-186海绵化,导致miR-186的下游靶基因HIF-1α表达增加,进而显著促进增殖和迁移活性,并抑制细胞凋亡[25]。
2.6.2 circ_0046159/miR-1226-3p/ATP2A2ATP2A2是一种钙泵,维持细胞内钙离子信号传导,基因突变后细胞间黏附功能受损;气管内递送基因ATP2A2的雾化导致较低的肺血管阻力,并有较好的长期生存趋势[26]。而miR-1226可以促进细胞凋亡。PAH患者外周血样本中circ_0046159的表达显著增加,通过海绵miR-1226-3p,降低miR-1226-3p的表达,并上调靶基因ATP2A2的表达来增加PASMC的收缩、迁移,并抑制其凋亡,从而参与PAH的发展[17]。
2.6.3 circ AMOTL1as/miR-103/107/KLF4/AMOTL1KLF4是含有3个锌指结构的转录因子,参与不同的细胞信号通路,参与细胞的增殖分化,在血管重构过程发挥重要的转录调控作用。研究发现[27],circ AMOTL1as存在多个与miR-103/107种子序列结合的位点。在血管内膜损伤后,作为海绵体的circ AMOTL1as表达明显下调,释放出所吸附的miR-103/107,进而抑制下游靶基因KLF4的表达。研究还发现,Hippo信号通路是一条细胞抑制生长性信号通路,其关键蛋白——AMOTL1的基因启动子上存在多个KLF4结合位点。下调的KLF4能降低AMOTL1基因的转录,解除对增殖相关基因的抑制,进而促进VSMC的增殖、迁移和血管重构。此外,下调的KLF4还能降低circ AMOTL1as基因的表达,导致circ AMOTL1as-miR-103/107-KLF4形成反馈调节[27]。
文中circRNA作为ceRNA对信号通路和肺血管重构的作用列于Tab 1。
| circRNA | miRNA | Target | Target cell | Target signaling pathway | circRNA expression level in PAH(up↑/down↓) | Role on signaling pathway(activate↑/inhibit↓) |
| circNRG-1[8] | miR-193b-5p | NRG-1 | VSMC | ErbB | ↓ | ↓ |
| circACTA2[11] | miR-548f-5p | α-SMA | VSMC | TGF-β1 | ↑ | ↑ |
| circSATB2[14] | miR-939 | STIM1/SM22a | VSMC | PDGF/Akt/mTOR SOCE/CREB | ↑ | ↑ |
| circ-calm4[16] | miR-337-3p | Myo10 | PASMC | Cell cycle | ↑ | —— |
| circ_0016070[1] | miR-942-5p | CCND1 | PASMC | CTGF/G1/S phase of cell cycle | ↑ | ↑ |
| circ_0026480[17] | miR-27a-3p | ATXN1 | PASMC | Cell cycle | ↓ | —— |
| circ_Lrp6[10] | miR-145 | SMA/TAGLN | VSMC | S-phase of cell cycle | ↑ | ↑ |
| circ_0029642[19] | miR-410 | —— | VEC | ADAR1 | ↓ | ↓ |
| circ-Sirt1[20] | miR-132/212 | SIRT1 | VSMC | TNF-α | ↓ | ↓ |
| circ_0002062[22] | miR-942-5p | CDK6 | VSMC | Wnt/β-catenin | ↓ | ↑ |
| circ_0022342[22] | miR-940 | CRKL | VSMC | ErbB | ↓ | ↓ |
| circ_004592[23] | miR-152 | Wnt1、PIK3CA DNMT1、PTEN |
VEC、VF PASMC | Tumor pathway | ↑ | ↑ |
| circ_018351[23] | miR-207/665 | —— | VEC、VF PASMC | Tumor pathway | ↑ | ↓ |
| circ_0010729[25] | miR-186 | HIF-1a | VEC | —— | ↑ | —— |
| circ_0046159[17] | miR-1226-3p | ATP2A2 | PASMC | —— | ↑ | —— |
| circ AMOTL1as[27] | miR-103/107 | KLF4/AMOTL1 | VSMC | Hippo | ↓ | ↓ |
| “——”: There are no reports of circRNA-regulated targets or target signaling pathways involved in pulmonary vascular remodeling | ||||||
circRNA由于其独特的功能,目前已成为心血管领域的前瞻性研究方向。Li等[28]提出心脏相关的circ_000203作为内源性miR-26b-5p和miR-140-3p海绵,上调转录因子Gata4的表达,加剧心脏肥大和心功能损伤;主动脉瘤患者组织中circ-000595的表达水平更高,敲除circ-000595可以上调miR-19a的表达,减弱缺氧诱导的人主动脉平滑肌细胞凋亡[14]。此外,circRNA的组织特异性和稳定性使其有可能成为一种良好的生物标志物。据报道,circSERPINE2和circ_Atp9b可作为骨关节炎生物标志物[29];circ_100338、circ_102958、circ-MYLK、circHIPK3和circDLGAP4、circHECTD1、CIRC-Ankib1和circZNF609在诊断和治疗恶性肿瘤及神经系统疾病中是很有价值的生物标志物。不仅如此,人造circRNA海绵也具有广泛的潜在应用价值。Jost等[30]设计了靶向miR-122的人造circRNA海绵,其可以有效抑制丙肝病毒细胞培养系统中病毒蛋白的产生。
综上所述,circRNA充当miRNA海绵,通过与miRNA相互作用从而调控miRNA靶基因的表达,这丰富了人们对动物自然进化的认知,颠覆了RNA仅仅是DNA与编码蛋白之间的平凡使者的传统理念。circRNA与PAH的形成密切相关,通过与关联的miRNA相互作用,在PAH等心血管疾病的发生和发展中起着关键的调节作用,有望成为新型的PAH临床诊断标志物,在防治领域展现出光明的应用前景。
| [1] |
Zhou S, Jiang H, Li M, et al. Circular RNA hsa_circ_0016070 is associated with pulmonary arterial hypertension by promoting PASMC proliferation[J]. Mol Ther Nucleic Acids, 2019, 18(6): 275-84. |
| [2] |
梁宇, 杜冠华. 抗肺动脉高压药物研究进展[J]. 中国药理学通报, 2019, 35(7): 902-6. Liang Y, Du G H. Research progress of anti-pulmonary hypertension drugs[J]. Chin Pharmacol Bull, 2019, 35(7): 902-6. |
| [3] |
Kylhammar D, Radegran G. The principal pathways involved in the in vivo modulation of hypoxic pulmonary vasoconstriction, pulmonary arterial remodelling and pulmonary hypertension[J]. Acta Physiol (Oxf), 2017, 219(4): 728-56. doi:10.1111/apha.12749 |
| [4] |
Schermuly R T, Ghofrani H A, Wilkins M R, Grimminger F. Mechanisms of disease: pulmonary arterial hypertension[J]. Nat Rev Cardiol, 2011, 8(8): 443-55. doi:10.1038/nrcardio.2011.87 |
| [5] |
Liu J, Liu T, Wang X, He A. Circles reshaping the RNA world: from waste to treasure[J]. Mol Cancer, 2017, 16(1): 58. doi:10.1186/s12943-017-0630-y |
| [6] |
Han B, Chao J, Yao H. Circular RNA and its mechanisms in disease: From the bench to the clinic[J]. Pharmacol Ther, 2018, 187(7): 31-44. |
| [7] |
Memczak S, Jens M, Elefsinioti A, et al. Circular RNAs are a large class of animal RNAs with regulatory potency[J]. Nature, 2013, 495(7441): 333-8. doi:10.1038/nature11928 |
| [8] |
Sun Y, Zhang S, Yue M, et al. Angiotensin Ⅱ inhibits apoptosis of mouse aortic smooth muscle cells through regulating the circNRG-1/miR-193b-5p/NRG-1 axis[J]. Cell Death Dis, 2019, 10(5): 362. doi:10.1038/s41419-019-1590-5 |
| [9] |
Parodi E M, Kuhn B. Signalling between microvascular endothelium and cardiomyocytes through neuregulin[J]. Cardiovasc Res, 2014, 102(2): 194-204. |
| [10] |
Hall I F, Climent M, Quintavalle M, et al. Circ_Lrp6, a circular RNA enriched in vascular smooth muscle cells, acts as a sponge regulating miRNA-145 function[J]. Circ Res, 2019, 124(4): 498-510. doi:10.1161/CIRCRESAHA.118.314240 |
| [11] |
Sun Y, Yang Z, Zheng B, et al. A novel regulatory mechanism of smooth muscle alpha-actin expression by NRG-1/circACTA2/miR-548f-5p axis[J]. Circ Res, 2017, 121(6): 628-35. doi:10.1161/CIRCRESAHA.117.311441 |
| [12] |
Grant S, Qiao L, Dent P. Roles of ERBB family receptor tyrosine kinases, and downstream signaling pathways, in the control of cell growth and survival[J]. Front Biosci, 2002, 7(2): d376-89. |
| [13] |
Weiser-Evans M C M. Smooth muscle differentiation control comes full circle: The circular noncoding RNA, circActa2, functions as a miRNA sponge to fine-tune alpha-SMA expression[J]. Circ Res, 2017, 121(6): 591-3. doi:10.1161/CIRCRESAHA.117.311722 |
| [14] |
Mao Y Y, Wang J Q, Guo X X, et al. Circ-SATB2 upregulates STIM1 expression and regulates vascular smooth muscle cell proliferation and differentiation through miR-939[J]. Biochem Biophys Res Commun, 2018, 505(1): 119-25. |
| [15] |
Hou X, Chen J, Luo Y, et al. Silencing of STIM1 attenuates hypoxia-induced PASMCs proliferation via inhibition of the SOC/Ca2+/NFAT pathway[J]. Respir Res, 2013, 14(1): 2. doi:10.1186/1465-9921-14-2 |
| [16] |
Zhang J, Li Y, Qi J, et al. Circ-calm4 serves as an miR-337-3p sponge to regulate Myo10 (myosin 10) and promote pulmonary artery smooth muscle proliferation[J]. Hypertension, 2020, 75(3): 668-79. |
| [17] |
Miao R, Gong J, Zhang C, et al. Hsa_circ_0046159 is involved in the development of chronic thromboembolic pulmonary hypertension[J]. J Thromb Thrombolysis, 2020, 49(3): 386-94. doi:10.1007/s11239-019-01998-4 |
| [18] |
葛晓月, 张卫芳, 胡长平. 炎症在动脉性肺动脉高压病理生理过程中的作用[J]. 中南医学科学杂志, 2017, 45(4): 325-30. Ge X Y, Zhang W F, Hu C P. Role of inflammation in the pathophysiology of arterial pulmonary hypertension[J]. J Chin Cen Sou Med Sci, 2017, 45(4): 325-30. |
| [19] |
彭文林.循环环状RNA hsa_circ_0029642与成人先心病肺动脉高压的初步研究[D].重庆: 第三军医大学, 2017. Peng W L. Preliminary study of circulating circular RNA hsa_circ_0029642 and pulmonary hypertension in adults with congenital heart disease[D]. Chongqing: Third Military Med Univ, 2017. http://cdmd.cnki.com.cn/Article/CDMD-90031-1017235660.htm |
| [20] |
Kong P, Yu Y, Wang L, et al. circ-Sirt1 controls NF-kappaB activation via sequence-specific interaction and enhancement of SIRT1 expression by binding to miR-132/212 in vascular smooth muscle cells[J]. Nucleic Acids Res, 2019, 47(7): 3580-93. doi:10.1093/nar/gkz141 |
| [21] |
Jia Y, Zheng Z, Wang Y, et al. SIRT1 is a regulator in high glucose-induced inflammatory response in RAW264.7 cells[J]. PLoS One, 2015, 10(3): e0120849. doi:10.1371/journal.pone.0120849 |
| [22] |
Miao R, Wang Y, Wan J, et al. Microarray expression profile of circular RNAs in chronic thromboembolic pulmonary hypertension[J]. Medicine (Baltimore), 2017, 96(27): e7354. doi:10.1097/MD.0000000000007354 |
| [23] |
Wang J, Zhu M C, Kalionis B, et al. Characteristics of circular RNA expression in lung tissues from mice with hypoxiainduced pulmonary hypertension[J]. Int J Mol Med, 2018, 42(3): 1353-66. |
| [24] |
陈颖, 于浩滢, 孙岚, 杜冠华. 血管平滑肌细胞表型转化中microRNA调控信号传导通路的研究进展[J]. 药学学报, 2018, 53(4): 487-94. Chen Y, Yu H Y, Sun L, Du G H. Research progress of microRNA-regulated signal transduction pathway in vascular smooth muscle cell phenotypic transformation[J]. Acta Pharm Sin, 2018, 53(4): 487-94. |
| [25] |
Dang R Y, Liu F L, Li Y. Circular RNA hsa_circ_0010729 regulates vascular endothelial cell proliferation and apoptosis by targeting the miR-186/HIF-1alpha axis[J]. Biochem Biophys Res Commun, 2017, 490(2): 104-10. |
| [26] |
Watanabe S, Ishikawa K, Plataki M, et al. Safety and long-term efficacy of AAV1.SERCA2a using nebulizer delivery in a pig model of pulmonary hypertension[J]. Pulm Circ, 2018, 8(4): 2045894018799738. |
| [27] |
杨展, 郑斌, 孙艳, 等.环状RNAcircAMOTL1as与KLF4形成反馈环路在血管重塑过程中的机制研究[C].中国生物化学与分子生物学会, 2016, 116. Yang Z, Zheng B, Sun Y, et al. Study on the mechanism of circular RNA circAMOTL1as and KLF4 forming a feedback loop during vascular remodeling[C]. Chin Soci of Biochem and Mole Bio, 2016, 116. |
| [28] |
Li H, Xu J D, Fang X H, et al. Circular RNA circRNA_000203 aggravates cardiac hypertrophy via suppressing miR26b-5p and miR-140-3p binding to Gata4[J]. Cardiovasc Res, 2019, cvz215. PMID: 31397837
|
| [29] |
Shen S, Wu Y, Chen J, et al. CircSERPINE2 protects against osteoarthritis by targeting miR-1271 and ETS-related gene[J]. Ann Rheum Dis, 2019, 78(6): 826-36. doi:10.1136/annrheumdis-2018-214786 |
| [30] |
Jost I, Shalamova L A, Gerresheim G K, et al. Functional sequestration of microRNA-122 from hepatitis C virus by circular RNA sponges[J]. RNA Biol, 2019, 15(8): 1032-9. |

