

2. 朝阳市第二医院药剂科,辽宁 朝阳 122000
2. Dept of Pharmacy, the Second Hospital, Chaoyang City, Chaoyang Liaoning 122000, China
糖尿病心肌病是糖尿病患者主要的心脏并发症,心肌间质纤维化为其主要病理改变,也是引起糖尿病心室重塑导致心力衰竭的关键原因;其表现为心肌间质细胞增殖及表型转分化,细胞外基质(extracellular matrix,ECM)过度沉积等。Wnt/β-catenin信号通路是参与细胞生长、增殖的重要途径,与肺、肝脏及肾脏等多脏器纤维增生性疾病的发生密切相关[1-3];Wnt/β-catenin通路的激活也参与了糖尿病心脏重构的病理过程[4]。目前,针对Wnt/β-catenin通路抑制剂的研究已成为防治纤维化相关疾病药物研究的重要靶点。丹酚酸B(salvianolic acid B,Sal B)是用于心血管系统疾病的传统中药丹参的主要活性成分,基础研究发现[5, 6]其对多种心血管损伤具有一定保护作用,如心肌缺血/再灌注损伤、2型糖尿病小鼠心肌病变等。但有关Sal B对糖尿病心肌纤维化的具体作用目前尚不明确,本研究通过体外培养心肌成纤维细胞(cardiac fibroblasts,CFs),高糖诱导模拟糖尿病高糖状态,基于Wnt/β-catenin信号通路,观察Sal B对高糖诱导CFs增殖及转分化的影响,探讨Sal B对糖尿病心肌间质纤维化的作用及可能机制,为传统中药防治糖尿病心肌病变提供理论依据。
1 材料与方法 1.1 材料 1.1.1 动物、药品与试剂1~3 d龄新生SD大鼠乳鼠(锦州医科大学实验动物中心提供),动物使用许可证号:SCXK(辽)2016-0004。Sal B(美仑MB6598);Wnt/β-catenin通路抑制剂XAV939(APEX BIO A1877)。DMEM培养基(Mediatech公司);增强型CCK-8试剂盒(上海尚宝生物科技有限公司);α-SMA抗体(博士德公司WL02509);β-catenin抗体(abcam公司ab32572);p-GSK 3β抗体(abcam公司ARG51777)。
1.1.2 仪器CO2孵箱(三洋公司);相差显微镜(Olympus公司);Mini-REPOTEANⅡ型电泳槽、电泳仪、Semi-dry Transfer cell(Bio-Red公司);TGL-16G高速冷冻离心机(日立公司);Biocell 2010酶标仪(Anthos Labtec Instruments公司);数显气浴恒温震荡器(江苏CHA-SA);化学发光凝胶系统分析仪(美国UVP公司);Leica 4000B正置荧光显微镜(德国Leica公司)。
1.2 方法 1.2.1 CFs分离与培养新生SD大鼠乳鼠,♀ ♂不拘,体积分数75%的乙醇消毒,取出心脏,冷PBS冲洗2次,放于冷培养基中,剪约1 mm3组织碎块,加入0.25%胰酶37 ℃水浴中进行消化。将消化的上清加至含10%胎牛血清的培养基中终止消化。将收集的细胞1 000×g离心10 min,弃去上清。向沉淀中加入含10%胎牛血清的培养基,吹打均匀,制成细胞悬液。剩余组织继续按上述操作消化至组织消化完全,之后将细胞悬液均匀接种于培养瓶中,放入37 ℃、5% CO2孵箱。差速贴壁90 min后,弃去培养液,PBS冲洗细胞3次,更换新的培养基。细胞生长近融合状态时0.25%胰酶消化传代,本实验使用2~3代细胞。
1.2.2 CCK-8检测细胞增殖将对数生长期的CFs胰酶消化后,用培养液制成单个细胞悬液计数,以每孔300个细胞接种至96孔板,每孔100 μL,贴壁培养24 h,吸去上清,加无血清培养基,血清饥饿24 h。分别进行:①不同浓度葡萄糖对CFs增殖的作用:分为正常对照组(Control,含5.5 mmol·L-1葡萄糖)和葡萄糖组(含10、20、25、30、50 mmol·L-1葡萄糖);②高糖诱导CFs增殖的时间效应:分为Control组,高糖组(HG组,含25 mmol·L-1葡萄糖),作用时间分为12 h、24 h、48 h;③Sal B对高糖诱导CFs增殖的作用:分为Control组、HG组(25 mmol·L-1)、HG+ Sal B(12.5、25、50 μmol·L-1)、高渗透压对照组(MG组,含5.5 mmol·L-1葡萄糖+19.5 mmol·L-1甘露醇)。按上述不同的处理因素作用48 h,每组设6复孔。每孔加入CCK-8试剂10 μL,轻轻摇晃96孔板后放入37 ℃ 5% CO2培养箱中继续培养1 h,取出96孔板置于酶标仪上,490 nm测定各孔吸光度OD值。
1.2.3 分组及药物处理实验分为:① Control组(含5.5 mmol·L-1葡萄糖),②MG组(含5.5 mmol·L-1葡萄糖+19.5 mmol·L-1甘露醇),③ HG组(含25 mmol·L-1葡萄糖),④ HG + Sal B组(25 μmol·L-1 Sal B预处理细胞1 h,加25 mmol·L-1葡萄糖),⑤ HG+XAV939组(1 μmol·L-1 XAV939预处理细胞1 h,加25 mmol·L-1葡萄糖),⑥ XAV939组(1 μmol·L-1),⑦ Sal B组(25 μmol·L-1)。
1.2.4 苦味酸天狼猩红染色取出药物作用后的24孔培养板,弃掉培养基,PBS清洗3次,4%多聚甲醛室温固定15 min。PBS清洗3次,0.5%的聚乙二醇辛基苯基醚(Triton-X-100)破膜20 min,PBS清洗3次,天狼猩红染液染色1 h,苏木素染液复染细胞核5 min,倒置显微镜下观察并拍照。
1.2.5 免疫荧光法各组CFs加不同条件培养基药物处理24 h后,吸去培养液,冷PBS漂洗3次;新鲜配制4%多聚甲醛室温固定30 min,PBS漂洗3次;0.3% Triton X-100作用30 min,PBS漂洗3次;室温山羊血清工作液封闭60 min;滴加α-SMA一抗溶液,4 ℃孵育过夜;PBS漂洗,异硫氰酸荧光素(FITC)标记的二抗室温孵育1 h,PBS漂洗,用含DAPI的抗淬灭封片剂封片,荧光显微镜观察及拍照。
1.2.6 Western blot各组CFs加不同条件培养基药物处理24 h后,冷PBS冲洗3次,立即放入预冷的裂解液中,每隔5 min震荡20 s,4 ℃ 12 000×g离心,取上清,BCA法进行蛋白质定量。每个泳道蛋白上样量为20 μg,行SDS-PAGE凝胶电泳,观察Marker移动情况。电泳后将凝胶中的蛋白质转移至硝酸纤维素膜上,室温封闭1 h,分别加兔抗大鼠α-SMA一抗、兔抗大鼠β-catenin一抗、兔抗大鼠p-GSK 3β一抗、兔抗大鼠GSK 3β一抗,4 ℃孵育过夜。次日早上取出膜,TBST洗膜3次,每次10 min,将膜放入山羊抗兔二抗(1 :1 000)中,室温孵育1 h。TBST洗膜3次,每次10 min,行ECL化学发光显影。利用Visionworks 6.3.3图像采集及分析软件对蛋白带进行分析。实验重复3次。
1.2.7 统计学方法实验数据用表示,SPSS 18.0软件进行统计学分析。采用One-way ANOVA和LSD-t检验进行两两比较。
2 结果 2.1 不同浓度葡萄糖对CFs增殖的作用CCK-8结果(Tab 1)显示,不同浓度(5.5、10、20、25、30、50 mmol·L-1)葡萄糖诱导CFs 24 h,25、30、50 mmol·L-1葡萄糖诱导,CFs增殖率明显增加,实验中25 mmol·L-1高糖诱导时细胞增殖率已经达到196 %(P < 0.01),本实验确定高糖诱导浓度为25 mmol·L-1。
| Group | Concentration /mmol·L-1 |
OD490 | Proliferation rate/% |
| Control | 5.5 | 0.276±0.016 | 100.00 |
| HG | 10 | 0.278±0.020 | 100.79 |
| 20 | 0.291±0.038 | 105.50 | |
| 25 | 0.541±0.277** | 196.07 | |
| 30 | 0.572±0.226** | 207.56 | |
| 50 | 0.571±0.321** | 207.25 | |
| **P < 0.01 vs control | |||
根据Tab 1结果,应用25 mmol·L-1葡萄糖作用12、24及48 h,结果(Tab 2)显示,作用24 h时CFs增殖率最高,达到204.6%(P < 0.01),本实验确定高糖作用时间为24 h。
| Group | Time /h |
OD490 | Proliferation rate/% |
| Control | 12 | 0.267±0.026 | 100.00 |
| HG | 12 | 0.294±0.022 | 110.11 |
| Control | 24 | 0.304±0.019 | 100.00 |
| HG | 24 | 0.623±0.019** | 204.60 |
| Control | 48 | 0.397±0.027 | 100.00 |
| HG | 48 | 0.503±0.044** | 126.80 |
| **P < 0.01 vs control | |||
B对CFs增殖的影响CCK-8结果(Tab 3)显示,与Control组相比,MG组CFs无明显变化,提示高渗透压对CFs增殖无明显影响,而25 mmol·L-1高糖作用可促进CFs增殖(P < 0.01);与HG组相比,经不同剂量(12.5、25、50 μmol·L-1)Sal B干预,对CFs增殖均出现抑制作用(P < 0.05),25 μmol·L-1差异具有极显著性(P < 0.01),后续实验选取Sal B的给药浓度为25 μmol·L-1。
| Group | Concentration /mmol·L-1 |
OD490 | Proliferation rate/% |
| Control | 0.307±0.021 | 100.00 | |
| MG | 0.306±0.029 | 99.78 | |
| HG | 0.595±0.010** | 193.71 | |
| HG+Sal B | 12.5 | 0.560±0.033# | 182.15 |
| 25 | 0.374±0.023## | 121.60 | |
| 50 | 0.363±0.009## | 118.18 | |
| **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs HG | |||
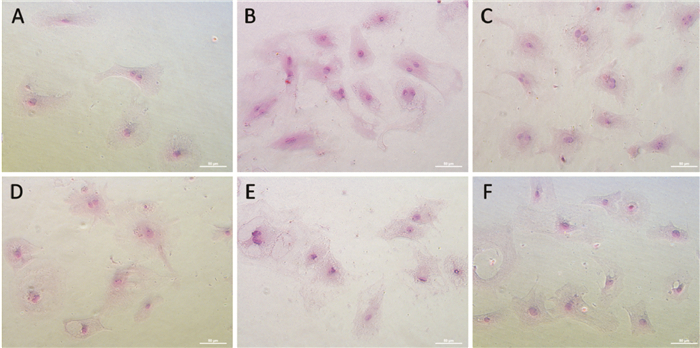
天狼猩红染色(Fig 1)显示:倒置显微镜下,胶原纤维为粉红色,细胞核为紫红色。与Control组相比,HG组细胞数量增多,红色胶原面积明显增加。与HG组相比,经Sal B以及XAV939预处理后,红色胶原面积减少,细胞间隙变大;单独应用Sal B及XAV939对CFs胶原纤维表达无明显影响。表明Sal B可通过抑制Wnt/β-catenin信号途径减少高糖诱导CFs胶原沉积。
|
| 图 1 Effects of Sal B on expression of collagen fiber in CFs induced by high glucose(400×) A:Control group; B:HG group; C:HG + Sal B group; D:HG + XAV939 group; E:XAV939 group; F:Sal B group |
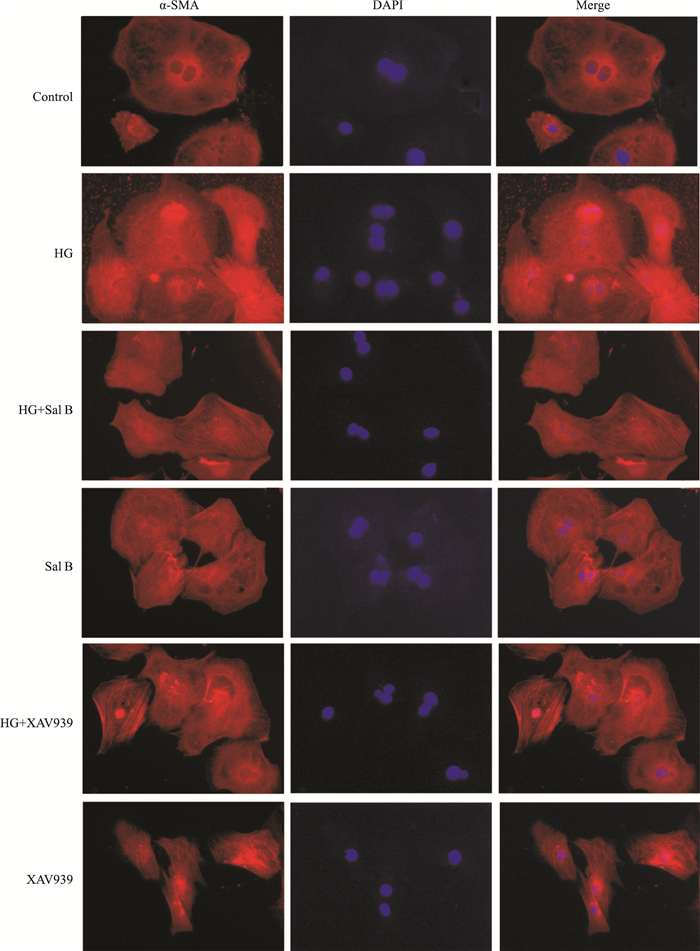
免疫荧光(Fig 2)显示:红色荧光代表α-SMA,蓝色荧光为细胞核,与Control组相比,HG组细胞红色荧光明显增强;与HG组相比,经Sal B(25 μmol·L-1)以及XAV939预处理后,红色荧光强度明显减弱;单独Sal B组及单独XAV939组与Control组相比荧光强度变化不明显。
|
| 图 2 Effect of Sal B on expression of α-SMA in CFs induced by high glucose(400 ×) |
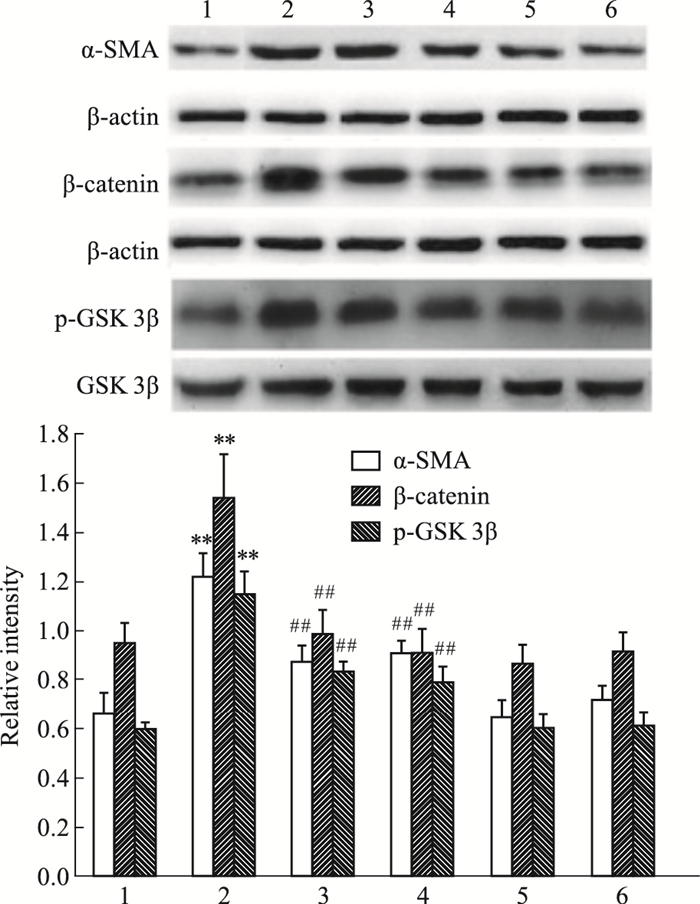
Western blot(Fig 3)显示:与Control组相比,HG组α-SMA蛋白表达明显增加(P < 0.01);与HG组相比,HG+XAV939组与HG+Sal B组α-SMA蛋白水平降低(P < 0.01),HG+XAV939组降低更为明显;单独Sal B组及单独XAV939组与Control组相比无明显变化。α-SMA为肌成纤维细胞的标志性蛋白,提示高糖可诱导CFs转分化为肌成纤维细胞,Sal B以及抑制Wnt/β-catenin信号可阻止高糖诱导CFs转分化程度。
|
| 图 3 Effects of Sal B on expression of α-SMA, β-catenin and p-GSK 3β in CFs induced by high glucose(x±s, n=3) 1:Control group; 2:HG group; 3:HG + Sal B group; 4:HG + XAV939 group; 5:XAV939 group; 6:Sal B group; **P < 0.01 vs Control group; ##P < 0.01 vs HG group |
Western blot(Fig 3)显示:与Control组相比,HG组β-catenin、p-GSK 3β蛋白表达明显增加(P < 0.01);与HG组相比,HG+XAV939组与HG+Sal B组β-catenin、p-GSK 3β蛋白水平降低(P < 0.01),HG+XAV939组降低更为明显;单独Sal B组及单独XAV939组与Control组相比无明显变化。表明Sal B可通过下调β-catenin、p-GSK 3β表达抑制高糖诱导CFs增殖及转分化程度。
3 讨论CFs是心肌间质的主要细胞成分,糖尿病状态下CFs增殖可合成大量胶原,ECM合成增加,导致心肌间质纤维化。然而,单纯CFs增殖不足以完成纤维化进程,CFs转分化(即CFs转分化为肌成纤维细胞)则是心肌间质纤维化进展的关键所在,转分化作用可导致ECM合成级联放大,从而加重心肌间质纤维化及心脏重构的病理进程[7]。α-SMA是肌成纤维细胞特征性标志物,本研究中应用高糖(25 mmol·L-1葡萄糖)诱导,CFs增殖率显著升高,α-SMA表达增加,胶原纤维增多;证实高糖可诱导CFs增殖转分化为肌成纤维细胞,特征性α-SMA表达增加,与Tao等[8]报道一致。实验中经Sal B(25 μmol·L-1)预处理后,明显抑制了CFs增殖及胶原纤维沉积,α-SMA表达明显减少,提示Sal B对高糖诱导CFs增殖及转分化有一定的抑制作用。
Wnt/β-catenin信号通路是调控组织器官发育的重要途径,参与细胞增殖、迁移及间质转化等过程。其中β-catenin在细胞内的数量与状态对该途径起决定作用,β-catenin在胞质中积累后进入细胞核,是Wnt信号传递的重要环节,β-catenin异常激活参与纤维增生疾病的发生发展[9]。刘理静等[1]研究显示,高糖可通过激活β-catenin引起肺成纤维细胞增殖及胶原合成。也有研究显示,持续血糖可通过激活Wnt/β-catenin/TCF7L2通路,使β-catenin活化参与糖尿病心肌病的病理生理过程[4, 10]。本研究中,高糖(25 mmol·L-1葡萄糖)诱导,CFs内β-catenin表达明显增加,经Sal B及XAV939预处理后,β-catenin表达明显减少。提示Sal B可抑制高糖诱导CFs增殖转分化,其作用与下调β-catenin表达有关。
正常情况下,β-catenin受多种蛋白调控,GSK 3β为其负向调节因素。当无Wnt配体时,GSK 3β的调控作用使胞质内β-catenin处于较低水平;当有Wnt配体时,Wnt配体与膜上Frizzled及LRP5/6受体结合,形成复合物,激活胞内的Dsh,从而抑制GSK 3β活性,阻止胞质内β-catenin的降解;当GSK 3β的N端9位丝氨酸被磷酸化后,p-GSK 3β增加,降低了GSK 3β活性,从而导致胞质β-catenin过度表达[11]。有学者在小鼠肾间质纤维化的研究中发现,p-GSK 3β水平与β-catenin表达同步增加[12];Liu等[13]发现,Wnt/β-catenin信号通路在糖尿病诱导的心肌损伤中被激活,推测其与糖尿病诱导的心肌病变的发生有关。本研究中,高糖诱导CFs内p-GSK 3β与β-catenin亦出现同步增加;经Sal B及Wnt/β-catenin通路抑制剂XAV939预处理后,p-GSK 3β、β-catenin表达出现同步下调;提示GSK 3β磷酸化,可上调β-catenin表达,使α-SMA表达增多,促进高糖诱导CFs增殖及转分化;Sal B可通过下调p-GSK 3β、β-catenin表达抑制高糖诱导CFs细胞增殖及转分化过程。
综上所述,高糖作用CFs可上调p-GSK 3β与β-catenin表达,促进CFs增殖、转分化;Sal B可有效抑制高糖诱导CFs增殖及转分化作用,其机制与抑制Wnt/β-catenin信号通路有关。
| [1] |
Liu L J, Qian H, Hu K, et al. miR-27a-3p inhibited synthesis of Col Ⅰ and Col Ⅲ in pulmonary fibroblasts through Wnt3a /β-catenin signaling pathway[J]. Chin Pharmacol Bull, 2019, 35(2): 229-34. |
| [2] |
Miao C G, Yang Y Y, He X, et al. Wnt signaling in liver fibrosis: progress, challenges and potential directions[J]. Biochimie, 2013, 95(12): 2326-35. doi:10.1016/j.biochi.2013.09.003 |
| [3] |
Tan R J, Zhou D, Zhou L, et al. Wnt/β-catenin signaling and kidney fibrosis[J]. Kidney Int Suppl, 2014, 4(1): 84-90. doi:10.1038/kisup.2014.16 |
| [4] |
邱晓霞, 李逸朗, 梁关凤, 等. 经典Wnt/β-catenin /TCF7L2信号通路在1型糖尿病心肌病中的作用[J]. 中国药理学通报, 2019, 35(8): 1104-9. Qiu X X, Li Y L, Liang G F, et al. Effect of activated canonical Wnt/β-catenin /TCF7L2 signaling pathway in type 1 diabetic cardiomyopathy[J]. Chin Pharmacol Bull, 2019, 35(8): 1104-9. doi:10.3969/j.issn.1001-1978.2019.08.014 |
| [5] |
陈俞材, 方莲花, 杜冠华. 丹参水溶性化合物抗心肌缺血作用的研究进展[J]. 中国药理学通报, 2015, 31(2): 162-5. Chen Y C, Fang L H, Du G H. Research advances in protective effects of water soluble compounds in Salvia miltiorrhiza against myocardial ischemia[J]. Chin Pharmacol Bull, 2015, 31(2): 162-5. doi:10.3969/j.issn.1001-1978.2015.02.004 |
| [6] |
臧慧梅, 苏磊, 陈家政, 等. 丹酚酸B通过PPARα抑制2型糖尿病小鼠心肌肥厚[J]. 中国药理学通报, 2018, 34(1): 97-102. Zang H M, Su L, Chen J Z, et al. Salvianolic acid B ameliorates cardiac hypertrophy in T2DM mice by activating PPARα[J]. Chin Pharmacol Bull, 2018, 34(1): 97-102. doi:10.3969/j.issn.1001-1978.2018.01.021 |
| [7] |
Shinde A V, Humeres C, Frangogiannis N G, et al. The role of α-smooth muscle actin in fibroblast-mediated matrix contraction and remodeling[J]. Biochim Biophys Acta Mol Basis Dis, 2017, 1863(1): 298-309. doi:10.1016/j.bbadis.2016.11.006 |
| [8] |
Tao H, Yang J J, Shi K H, et al. Wnt signaling pathway in cardiac fibrosis: New insights and directions[J]. Metabolism, 2016, 65(2): 30-40. doi:10.1016/j.metabol.2015.10.013 |
| [9] |
Haidari M, Zhang W, Willerson J T, et al. Disruption of endothelial adherens junctions by high glucose is mediated by protein kinase C-β-dependent vascular endothelial cadherin tyrosine phosphorylation[J]. Cardiovasc Diabetol, 2014, 15(13): 105. |
| [10] |
Guo Y, Gupte M, Umbarkar P, et al. Entanglement of GSK-3β, β-catenin and TGF-β1 signaling network to regulate myocardial fibrosis[J]. J Mol Cell Cardiol, 2017, 110: 109-20. doi:10.1016/j.yjmcc.2017.07.011 |
| [11] |
Aumiller V, Balsara N, Wilhelm J, et al. Wnt /β-catenin signaling induces IL-1β expression by alveolar epithelial cells in pulmonary fibrosis[J]. Am J Respir Cell Mol Biol, 2013, 49(1): 96-104. doi:10.1165/rcmb.2012-0524OC |
| [12] |
Jiang M Q, Wang L, Cao A L, et al. Huang Qi Decoction improves renal tubulointerstitial fibrosis in mice by inhibiting the up-regulation of Wnt/β-Catenin signaling pathway[J]. Cell Physiol Biochem, 2015, 36(2): 655-69. doi:10.1159/000430128 |
| [13] |
Liu X, Liang E, Song X, et al. Inhibition of Pin1 alleviates myocardial fibrosis and dysfunction in STZ-induced diabetic mice[J]. Biochem Biophys Res Commun, 2016, 479(1): 109-15. doi:10.1016/j.bbrc.2016.09.050 |

