


2. 贵阳妇幼保健院围产期保健科, 贵州 贵阳 550004;
3. 贵州医科大学地方病与少数民族疾病教育部重点实验室, 贵州省医学分子生物重点实验室, 贵州 贵阳 550004;
4. 贵州中医药大学基础医学院, 贵州 贵阳 550004
 ,
MOU Deng-feng1,
WANG Qi1,
ZHENG Dan2,
QI Xiao-lan3,
GUAN Zhi-zhong3,
YU Yan-ni1,
LOU Di-dong4
,
MOU Deng-feng1,
WANG Qi1,
ZHENG Dan2,
QI Xiao-lan3,
GUAN Zhi-zhong3,
YU Yan-ni1,
LOU Di-dong4

2. Perinatal Health Care Section, Guiyang Maternal and Child Health Hospital, Guiyang 550004, China;
3. Key Lab of Endemic and Minority Diseases of Ministry of Education, Guizhou Medical University, Key Lab of Medical Molecular Biology of Guizhou Province, Guiyang 550004, China;
4. School of Basic Medicine, Guizhou University of Traditional Chinese Medicine, Guiyang 550004, China
甲基苯丙胺(methamphetamine, METH)因毒性较低、起效较快、作用持久, 并趋向低龄化, 已严重危害到公共卫生安全和社会安全。探索METH致神经细胞的神经毒性机制, 获取治疗和预防METH神经毒性的方法已迫在眉睫。研究认为, 线粒体病理过程与METH致细胞损伤密切相关, 包括线粒体氧化还原平衡[1]、线粒体自噬[2]、线粒体钙管理[3]、线粒体能量合成[4]和线粒体促凋亡因子释放[5]。线粒体过度分裂产生新的线粒体, 新生线粒体膜电位较低、线粒体DNA(mitochondrial DNA, mtDNA)含量低[1, 6], 这些受损的线粒体不能产生足够的ATP来促进细胞新陈代谢, 而且释放出促凋亡因子进入细胞质/细胞核, 以启动线粒体凋亡途径[7-8]。例如, 在内皮氧化损伤中, 线粒体分裂损害线粒体DNA转录和复制, 并因此抑制线粒体呼吸复合物的表达[6], 导致ATP消耗。我们前期研究发现, METH可诱导体外培养人神经母细胞瘤细胞(human neuroblastoma cells, SH-SY5Y cells)增殖能力减弱, 线粒体膜电位(mitochondrial membrane potential, MMP)水平下降, 线粒体超微结构改变, 线粒体趋向分裂, 启动线粒体自噬, 并发现线粒体融合蛋白1(mitofusin 1, Mfn1)和线粒体分裂蛋白1(fisson 1, Fis1)蛋白表达异常, 这些线粒体形态与功能改变可能与Mfn1和Fis1调节的线粒体动力学有关。为进一步探索METH诱导SH-SY5Y细胞毒性损伤与Fis1之间的相互关系, 本研究拟通过沉默Fis1基因, 下调Fis1蛋白表达后, 检测和观察METH诱导SH-SY5Y细胞增殖能力、MMP水平和线粒体超微结构, 探讨Fis1在METH诱导体外培养SH-SY5Y细胞增殖能力、线粒体膜电位和超微结构变化中的作用。
1 材料与方法 1.1 细胞SH-SY5Y细胞, 购于Sigma公司。
1.2 试剂与仪器METH(美国Cerilliant公司, 标准品编号:M-009, 纯度:99.9%); siRNA(上海吉玛制药技术有限公司); 脂质体LipofectamineTM 3000(美国Invitrogen公司); JC-1线粒体膜电位检测试剂盒(上海碧云天生物技术有限公司); 胎牛血清(美国BI公司); 兔抗人Fis1单克隆抗体(美国Abmart公司); 兔抗人β-actin抗体(美国Gene Tex公司)。恒温细胞培养箱、ND2000型超微量紫外分光光度计(美国Thermo公司); ELX800UV酶标仪、化学发光成像系统(美国Bio-Rad公司); DMi8型倒置显微镜(德国Leica公司); H-7650型透射电镜(日本Hitachi公司); AllegraX-30R高速冷冻离心机(美国Beckman公司)。
1.3 细胞培养、转染及METH处理将体外培养SH-SY5Y细胞冻存管迅速放入37 ℃恒温水浴箱中, 轻轻摇动融化后移入培养瓶中, 并加入4 mL的完全培养基(90%高糖DMEM培养基+10%灭活胎牛血清+1%双抗), 轻柔匀速吹打细胞制成单细胞悬液, 放入37 ℃、5% CO2恒温培养箱中培养。次日更换培养基, 继续放入恒温箱中培养。待培养瓶中细胞贴壁长至80%~90%时, 将细胞按1×106·mL-1的密度接种于6孔培养板。待细胞贴壁生长至70%~80%进行转染, 转染实验按照说明书严格操作。分组:未沉默组(0 mmol·L-1 METH、1.0 mmol·L-1 METH、2.0 mmol·L-1 METH); 沉默阴性组(0 mmol·L-1 METH+siRNA-NC、1.0 mmol·L-1 METH+siRNA-NC、2.0 mmol·L-1 METH+siRNA-NC), siRNA-NC非特异性序列:5′-UUCUCCGA ACGUGUCACGUTT-3′, 5′-ACGUGACACGUUCGGAGA ATT-3′; 沉默组(0 mmol·L-1 METH+siRNA-Fis1、1.0 mmol·L-1 METH+siRNA-Fis1、2.0 mmol·L-1 METH+siRNA-Fis1), siRNA-Fis1特异性序列:5′- GCUGUGUCCAAGUCCAAAUTT-3′, 5′-AUU UG GACUUGGACACAGC TT- 3′。METH诱导未沉默组、沉默阴性组和沉默组24 h, 浓度和时间选择参照文献[9]和细胞增殖-毒性检测实验(CCK-8)结果。
1.4 CCK-8法检测细胞增殖将siRNA-Fis1和siRNA-NC分别转染后的细胞消化、吹打成单细胞悬液, 按1×104个/孔接种于96孔培养板中, 放入37 ℃、5% CO2恒温培养箱中培养。待细胞贴壁长至60%~70%时, 换含有METH(0、1.0、2.0 mmol·L-1)的培养液培养, 未沉默组、沉默阴性组和沉默组的每个浓度做6个复孔, METH诱导24 h后, 向每孔加入10 μL CCK-8溶液, 将96孔板放入37 ℃、5% CO2恒温培养箱中孵育3 h后, 用酶标仪测定在450 nm处的吸光度(OD)值, 并计算细胞存活率。细胞存活率/%=(实验组OD值-空白组OD值)/(对照组OD值-空白组OD值)×100%。
1.5 Western blot法检测Fis1蛋白表达水平使用RIPA裂解细胞提取总蛋白, 超微量紫外分光光度计检测各样本蛋白浓度。经12%聚丙烯酰胺凝胶电泳分离蛋白(浓缩胶电泳80 V, 分离胶电泳120 V)、转膜(100 V, 45 min。)、室温封闭2 h后, 一抗Fis1(1 :2 000)、β-actin(1 :5 000)4 ℃孵育过夜, 二抗(1 :10 000)室温孵育1 h。将PVDF膜与超敏发光液(ECL)试剂反应1 min后, 使用化学发光成像系统扫描PVDF膜, ImageJ软件分析Fis1蛋白条带, 使用β-actin蛋白条带校正。
1.6 MMP检测采用JC-1法, 按照试剂盒说明书操作。使用倒置荧光显微镜观察METH诱导SH-SY5Y细胞24 h后的各组细胞的红、绿荧光, 计算机采集荧光图像, 使用ImageJ软件重叠红绿荧光, 将合成荧光的光密度比值作为膜电位表达水平值。
1.7 透射电镜观察体外培养SH-SY5Y细胞线粒体超微结构收集细胞; 将细胞固定于2.5%戊二醛溶液中4 h(4 ℃), 0.1 mol·L-1 PBS漂洗; 1%锇酸溶液后固定2 h(4 ℃), 0.1 mol·L-1 PBS漂洗; 丙酮脱水; Epon812树脂包埋; 切片; 醋酸铀、硝酸铅染色; 在H-7650型透射电镜下, 根据观察内容不一选择不同的放大倍数进行超微结构观察和拍照; 每个样本随机拍片9张, 同时避免同一细胞重复拍照。将类圆形(短轴/长轴≥0.7)线粒体定义为小球状线粒体, 短轴/长轴<0.7的线粒体定义为棒状线粒体, 并排除因为图片质量模糊等原因不能明确定义形态的线粒体。计数每组样本中棒状线粒体数和小球状线粒体数, 小球状线粒体数与棒状线粒体数比值代表线粒体分裂水平。
1.8 统计学处理运用SPSS 24.0统计软件分析数据, 计量资料数据采用单因素方差分析, 用x±s表示, 方差齐时进一步两两比较采用LSD-t分析, 方差不齐时组间两两比较采用Dunnett′s T3检验; 计数资料数据采用χ2检验, 多重比较, 进一步两两比较检验水准需要进行Bonferroni校正(α’=α/比较次数)。
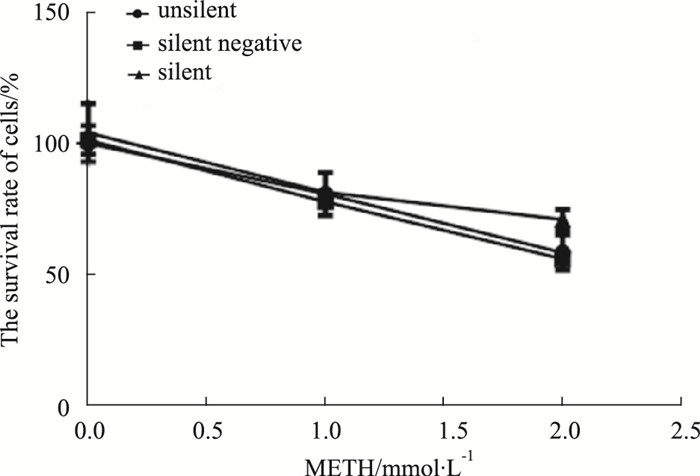
2 结果 2.1 CCK-8法检测结果如Fig 1所示, 使用METH(0、1.0、2.0 mmol·L-1)诱导体外培养SH-SY5Y细胞24 h后, SH-SY5Y细胞存活率随METH浓度的增加而减小(P<0.05), METH抑制SH-SY5Y细胞增殖。且在2.0 mmol·L-1 METH诱导下, 沉默组细胞存活率明显高于未沉默组和沉默阴性组(P<0.05)。
|
| Fig 1 Effect of METH on survival rate of SH-SY5Y cells cultured in vitro |
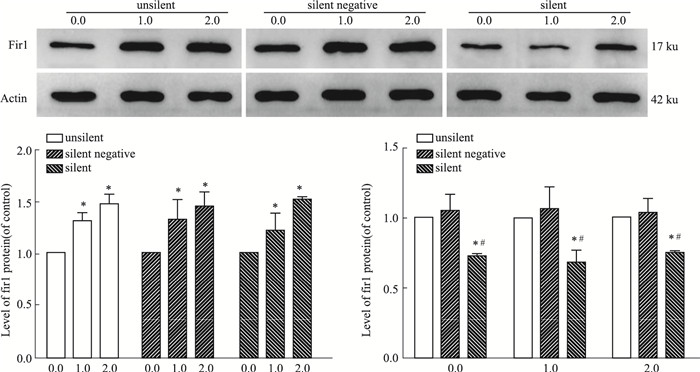
如Fig 2所示, 未沉默组、沉默阴性组和沉默组中, 各组组内与对照组(0 mmol·L-1 METH)比较, 1.0和2.0 mmol·L-1 METH诱导SH-SY5Y细胞, Fis1蛋白表达水平分别升高31%、47%, 32%、45%, 22%、51%(P<0.05);与未沉默组相同浓度比较, 沉默组Fis1蛋白表达水平分别降低27%、32.5%、25%(P<0.05);与沉默阴性组相同浓度比较, 沉默组Fis1蛋白表达水平分别降低31%、36%、28%(P<0.05)。
|
| Fig 2 Expression of Fis1 protein in SH-SY5Y cells (x±s, n=3)) *P < 0.05 vs control; #P < 0.05 vs silent negative group |
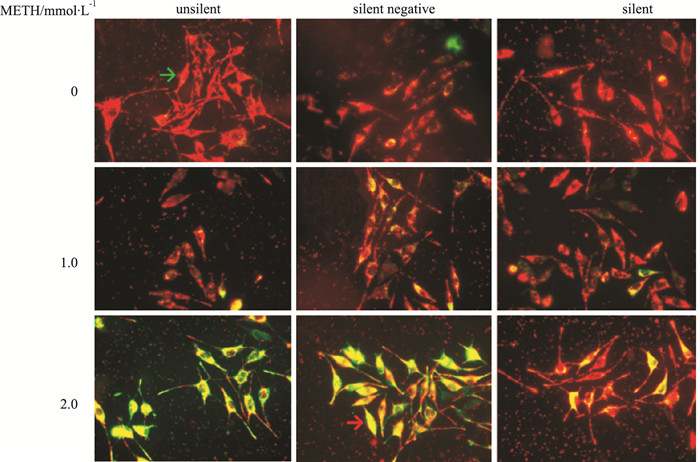
如Tab 1、Fig 3所示, 未沉默组、沉默阴性组和沉默组中, 各组组内与对照组(0 mmol·L-1 METH)比较, 1.0和2.0 mmol·L-1 METH诱导SH-SY5Y细胞, MMP水平降低(P<0.05), 荧光显微镜下, 随METH浓度增加, SH-SY5Y细胞红色荧光减弱, 绿色荧光增强; 与未沉默组和沉默阴性组相同浓度比较, 沉默组MMP水平升高(P<0.05), 红色荧光增强。
| METH/mmol·L-1 | 24 h | ||
| Unsilent groups | Silent negative groups | Silent groups | |
| 0 (controls) | 0.95±0.07 | 0.92±0.06 | 0.91±0.05 |
| 1.0 | 0.68±0.02* | 0.70±0.01* | 0.82±0.02* |
| 2.0 | 0.43±0.04* | 0.45±0.01* | 0.64±0.01* |
| *P<0.05 vs control | |||
|
| Fig 3 MMP in SH-SY5Y cells cultured in vitro detected by red-green overlapping fluorescence (×400) Green arrows indicate the normal MMP, while red arrows indicate the decreased MMP. |
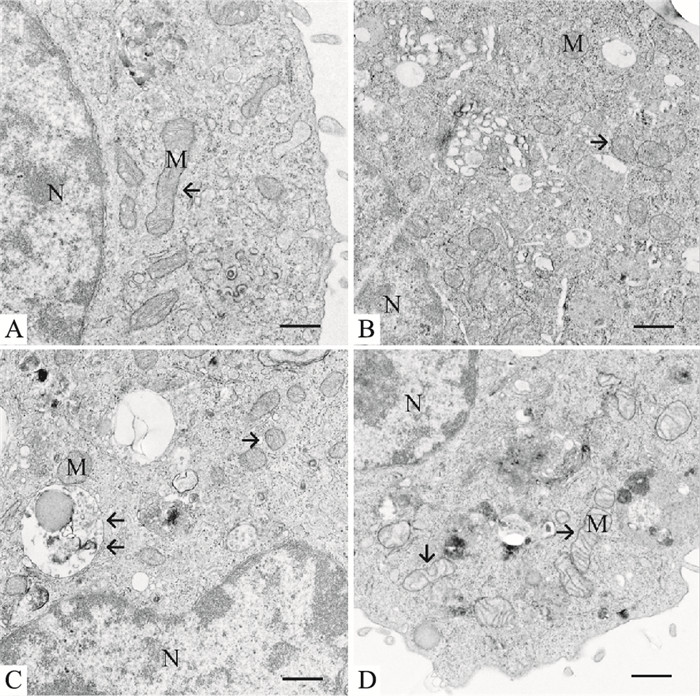
如Tab 2、Fig 4所示, 与对照组(0 mmol·L-1 METH)比较, 未沉默组、沉默阴性组和沉默组在2.0 mmol·L-1 METH诱导24h后, 透射电镜观察见各组线粒体小球状结构增加, 线粒体分裂水平明显增高(P<0.01);与未沉默组和沉默阴性组比较, 沉默组线粒体分裂水平差异无显著性(P>0.01)。未沉默组和沉默阴性组中部分线粒体呈现出空泡化, 损伤严重, 同时在沉默阴性组中发现自噬溶酶体, 沉默组中个别棒状结构的线粒体内外膜完整, 线粒体嵴清晰可见。
| METH/mmol·L-1 | Number of mitochondria | ||
| Small globular (A) | Rod-like (B) | A/B | |
| 0 (controls) | 37 | 45 | 0.82 |
| 2.0 | 78 | 27 | 2.89** |
| 2.0(+siRNA-NC) | 131 | 49 | 2.67** |
| 2.0(+siRNA-Fis1) | 100 | 46 | 2.17** |
| **P<0.01 vs control | |||
|
| Fig 4 Observation of mitochondrial ultrastructure of SH-SY5Y cells by TEM (scale bar= 5 μm) A: Control groups, mitochondria elliptical rod-like structure, normal and clear; B: Unsilent groups: mitochondrial globular structure increased significantly (arrow); C: Silent negative groups: mitochondrial globular structure increased significantly (arrow); D: Silent groups, mitochondrial globular structure decreased, rod structure increased (arrow). M: mitochondria; N: nuclei. |
METH俗称“冰毒”, 具有极强的精神兴奋和致幻作用, METH长期滥用已严重危害社会安全, 探明METH的神经毒性机制可为预防和治疗METH的神经毒性作用探寻高效、便捷的靶点。Parameyong等[9]研究认为, METH通过诱导线粒体分裂途径, 引起SH-SY5Y细胞线粒体动力学紊乱, 参与线粒体碎裂成小球状结构。此外, MMP的下降是线粒体膜损伤和细胞凋亡的早期指标, 此过程与线粒体不断的分裂有关[10]。线粒体分裂过度或融合不足都会导致线粒体碎裂, 降低呼吸作用和能量生产, 增加神经元损伤和细胞凋亡的可能性[11]。Fis1的过度表达可以导致线粒体分裂, 造成线粒体功能障碍, 导致细胞凋亡, 药物抑制分裂可以减轻细胞凋亡[12]。我们前期实验也发现[13], METH可诱导体外培养SH-SY5Y细胞增殖能力减弱, MMP水平下降, 线粒体超微结构改变, 线粒体趋向分裂, 启动线粒体自噬, 并发现Mfn1和Fis1蛋白表达异常, 这些线粒体形态与功能改变可能与Mfn1和Fis1调节的线粒体动力学有关。为了进一步研究Fis1在METH诱导SH-SY5Y细胞损伤中的重要作用, 本实验通过基因干扰法, 沉默Fis1基因, 探讨Fis1在METH诱导SH-SY5Y细胞损伤中的作用。
实验发现, CCK-8实验中, 未沉默组、沉默阴性组和沉默组随着METH浓度增加, 细胞存活率均减小(P<0.05), 表明METH对体外培养SH-SY5Y细胞具有毒性作用; 且未沉默组和沉默阴性组细胞存活率减小趋势相近, 表明沉默试剂对细胞无毒性作用或毒性作用微小, 不足以降低细胞存活率, 排除沉默试剂对细胞毒性的干扰; 同时发现, 2.0mmol·L-1 METH诱导SH-SY5Y细胞24 h后, 与未沉默组和沉默阴性组比较, 沉默组对应细胞存活率明显提高(P<0.05), 表明沉默Fis1基因可以减轻细胞损伤, 提高细胞增殖能力。进一步研究发现, 体外培养SH-SY5Y细胞经METH诱导24h后, 未沉默组、沉默阴性组和沉默组组内的MMP水平随METH的浓度增高呈现降低趋势(P<0.05), 但与未沉默组和沉默阴性组相同浓度相比, 沉默组MMP水平呈现上升趋势(P<0.05), MMP得以恢复或接近正常水平, 表明沉默Fis1基因对稳定MMP水平起到重要作用。透射电镜下观察见对照组线粒体多呈现棒状结构, 线粒体内外膜结构良好, 线粒体嵴清晰、正常; 未沉默组和沉默阴性组线粒体多为小球状结构, 部分空泡化, 并再次观察到自噬现象, 和前期实验现象基本一致[13]; 沉默组中个别棒状结构的线粒体内外膜保持良好, 线粒体嵴清晰可见, 虽然与未沉默组和沉默阴性组比较, 统计球状小泡结构/棒状结构(A/B)无明显统计学意义, 但A/B值下降仍很明显; 这也部分表明沉默Fis1基因可以抑制Fis1蛋白表达, 从而可能减弱线粒体过度分裂, 线粒体损伤程度得以减轻。沉默Fis1基因, Fis1蛋白表达水平下调, 透射电镜下观察线粒体超微结构部分改善, MMP水平上升, 细胞增殖能力增强。我们推测, 沉默Fis1基因抑制Fis1蛋白表达后, 线粒体分裂功能下降, 稳定线粒体膜结构, 提高MMP水平, 降低METH对体外培养SH-SY5Y细胞的神经毒性作用, 可恢复细胞增殖功能。
综上所述, 沉默Fis1基因, 可下调Fis1蛋白表达, 可降低线粒体分裂水平和线粒体膜损伤, 部分恢复SH-SY5Y细胞增殖能力。线粒体功能紊乱可能是METH诱导体外培养SH-SY5Y细胞神经毒性的重要机制之一, Fis1可能在METH诱导体外培养SH-SY5Y细胞线粒体形态与功能紊乱中起关键作用。
| [1] |
Zhou H, Shi C, Hu S, et al. BI1 is associated with microvascular protection in cardiac ischemia reperfusion injuryvia repressing Syk-Nox2-Drp1-mitochondrial fission pathways[J]. Angio-genesis, 2018, 21(3): 599-615. |
| [2] |
Jin Q, Li R, Hu N, et al. DUSP1 alleviates cardiac ischemia/reperfusion injury by suppressing the Mff-required mitochondrial fission and Bnip3-related mitophagy via the JNK pathways[J]. Redox Biol, 2018, 14: 576-87. doi:10.1016/j.redox.2017.11.004 |
| [3] |
Zhu H, Jin Q, Li Y, et al. Melatonin protected cardiac microvascular endothelial cells against oxidative stress injury via suppression of IP3R-[Ca2+]c/VDAC-[Ca2+]m axis by activation of MAPK/ERK signaling pathway[J]. Cell stress chaperones, 2018, 23(1): 101-13. doi:10.1007/s12192-017-0827-4 |
| [4] |
Yan H, Qiu C, Sun W, et al. Yap regulates gastric cancer survival and migration via SIRT1/ Mfn2/mitophagy[J]. Oncol Rep, 2018, 39(4): 1671-81. |
| [5] |
Li H, He F, Zhao X, et al. YAP inhibits the apoptosis and migration of human rectalcancer cells via suppression of JNK-Drp1-mitochondrial fission-HtrA2/Omi pathways[J]. Cell Physiol Biochem, 2017, 44(50): 2073-89. |
| [6] |
Zhou H, Hu S, Jin Q, et al. Mff-dependent mitochondrial fission contributes to the pathogenesis of cardiac microvasculature ischemia/reperfusion injuryvia induction of mROS-mediated cardiolipin oxidation and HK2/VDAC1 disassociation-involved mPTP opening[J]. J Am Heart Assoc, 2017, 6(3): e005328. |
| [7] |
Yan H, Xiao F, Zo uJ, et al. NR4A1-induced increase in the sensitivity of a human gastric cancer line to TNFalpha-mediated apoptosis is associated with the inhibition of JNK/Parkin-dependent mitophagy[J]. Int J Oncol, 2018, 52(2): 367-78. |
| [8] |
Zhao Q, Ye M, Yang W, et al. Effect of Mst1 on endometriosis apoptosis and migration: role of Drp1-related mitochondrial fission and Parkin-required mitophagy[J]. Cellular Physiology and Biochemistry, 2018, 45(3): 1172-90. doi:10.1159/000487450 |
| [9] |
Parameyong A, Charngkaew K, Govitrapong P, et al. Melatonin attenuates methamphetamine-induce disturbances in mitochondrial dynamics and degeneration in neuroblastoma SH-SY5Y cells[J]. Journal of Pineal Research, 2013, 55(3): 313-23. doi:10.1111/jpi.12078 |
| [10] |
Desagher S, Martinou JC. Solange Desagher and Jean-Claude Martinou: Executioners of cell death[J]. Trends Cell Biol, 2016, 26(8): 560-2. doi:10.1016/j.tcb.2016.05.010 |
| [11] |
Gan X, Huang S, Wu L, et al. Inhibition of ERK-DLP1 signaling and mitochondrial division alleviates mitochondrial dysfunction in Alzheimer's disease cybrid cell[J]. Biochim Biophys Acta, 2014, 1842(2): 220-31. doi:10.1016/j.bbadis.2013.11.009 |
| [12] |
Serasinghe M N, Yoon Y. The mitoehondrial outer membrane protein hFisl regulates mitoehondrial morphology and fission through self-interaction[J]. Exp Cell Res, 2008, 314(19): 3494-507. doi:10.1016/j.yexcr.2008.09.009 |
| [13] |
牟登峰, 郑丹, 王琪, 等. 甲基苯丙胺对体外培养SH-SY5Y细胞线粒体膜电位、超微结构及Mfn1、Fis1蛋白表达的影响[J]. 中国药理学通报, 2019, 35(7): 935-9. Mou D F, Zheng D, Wang Q, et al. Effects of METH on mitochondrial membrane potential, ultrastructure and expression of Mfn1 and Fis1 protein in SH-SY5Y cells cultured in vitro[J]. Chin Pharmacol Bull, 2019, 35(7): 935-9. doi:10.3969/j.issn.1001-1978.2019.07.010 |