

2. 锦州医科大学基础医学院解剖学教研室,辽宁 锦州 121001
2. Dept of Anatomy, Foundation Institute of Jinzhou Medical University, Jinzhou Liaoning 121001, China
阿尔茨海默病(Alzheimer’s disease, AD)为一种年龄相关的神经退行性疾病,是最常见的痴呆类型。目前认为AD发病伴随着严重自噬损害,主要表现为自噬底物降解受阻,自噬溶酶体堆积[1],细胞中β淀粉样蛋白(β-amyloid,Aβ)、tau蛋白等自噬体内待降解的物质堆积,引起细胞毒性损害,导致AD的发生[2]。
荭草苷(orientin)是一种碳苷类黄酮化合物,为荭草、竹叶、金莲花的主要活性成分。研究表明,荭草苷能够改善Aβ以及噪音诱导的痴呆小鼠的认知功能[3-4]。但荭草苷改善痴呆鼠认知功能的机制尚不清楚。本研究拟初步探讨荭草苷通过改善APP/PS1转基因小鼠自噬功能,从而改善认知功能,寻找潜在的AD防治药物。
1 材料与方法 1.1 材料 1.1.1 实验动物7月龄SPF级APPswe/PS1△E9双转基因♀小鼠16只,同月龄的♀C57BL/6J小鼠8只,购自中国医科大学动物实验中心,许可证号:SYXK(辽)2008-005。
1.1.2 药物与试剂荭草苷(纯度≥98%),购自成都曼思特;Aβ抗体,购自CST;LC3、Beclin-1抗体,购自武汉三鹰;p62、组织蛋白酶D(Cathepsin D)抗体,购自沈阳万类生物;DAB、通用SP试剂盒,购自北京中杉金桥。
1.1.3 仪器Morris水迷宫(安徽正华生物);显微镜(日本Olympus);电泳仪、凝胶成像系统(美国Bio-Rad)。
1.2 方法 1.2.1 动物分组与处理将16只APP/PS1转基因小鼠随机分为转基因对照组(transgenic control group, Tg)和荭草苷处理组(Tg+Ori),每组8只;8只同月龄C57BL/6J小鼠作为非转基因对照组(non-transgenic control group, NT)。荭草苷组连续30 d每天腹腔注射生理盐水稀释的荭草苷(10 mg·kg-1),Tg和NT组给予同剂量的生理盐水。由于转基因鼠不易获得,因此本课题未设置荭草苷多个剂量组,仅初步探讨荭草苷的药理作用,未探索最佳给药剂量。
1.2.2 水迷宫行为学检测给药结束24 h后,进行Morris水迷宫实验,实验分为定位航行和空间探索实验两部分,实验过程参照Vorhees等[5]方法。
1.2.3 取材小鼠行为学检测结束后,以水合氯醛麻醉,生理盐水左心室灌注后断头取脑,一半置于多聚甲醛中行后固定,用于免疫组化染色;另一半取海马,置于-80 ℃低温冰箱储存,用于免疫印迹检测。
1.2.4 免疫组化检测Aβ的表达小鼠脑经石蜡包埋、切片后,脱蜡至水,抗原修复,阻断内源性过氧化物酶,血清封闭,Aβ抗体(1 :800)4 ℃孵育过夜,生物素化二抗、辣根酶标记卵白素孵育,DAB显色,苏木精复染,脱水透明封片后,显微镜下观察摄片。
1.2.5 免疫印迹检测海马自噬相关蛋白表达海马组织剪碎后,以RIPA缓冲液和超声裂解细胞,BCA法蛋白定量,SDS-PAGE电泳,转膜,封闭2 h,p62、LC3、Cathepsin D、Beclin-1抗体(1 :500)4 ℃孵育过夜,二抗孵育2 h,ECL发光。
1.2.6 统计学分析以软件SPSS 16.0进行统计学分析,多组比较用F检验。方差齐,两两比较用q检验,方差不齐用Dunnett检验。
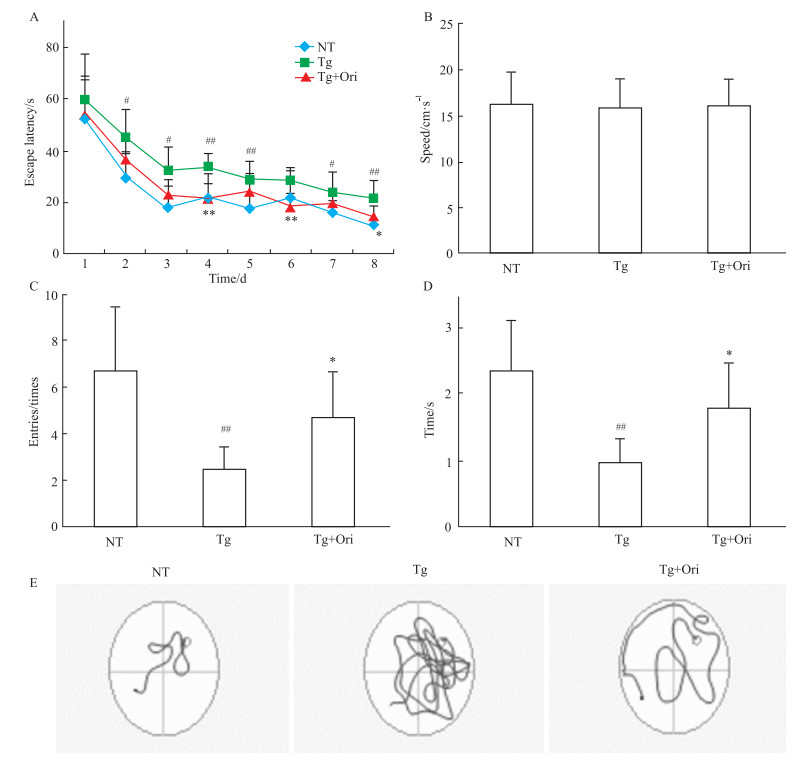
2 结果 2.1 荭草苷改善APP/PS1转基因小鼠空间学习和记忆功能如Fig 1A所示,各组小鼠逃避潜伏期随训练天数的增加,均有逐渐下降的趋势。与NT组相比,Tg组小鼠逃避潜伏期延长(P < 0.01);与Tg相比,Tg+Ori组逃避潜伏期缩短(P < 0.05)。各组小鼠的游泳速度无差异(Fig 1B)。表明转基因小鼠空间学习能力受损,荭草苷能够改善转基因小鼠空间学习能力。
|
| Fig 1 Cognition of APP/PS1 mice improved by orientin treatment (x±s, n=8) A: Spatial learning and memory were assessed by the measurement of escape latency; B: Swimming speed was assessed; C, D: The number of times entered the target zone and the time spent in it during 120 s probe trail; E: Representative swimming paths on day 8 of training. #P < 0.05, ##P < 0.01 vs NT; *P < 0.05, **P < 0.01 vs Tg. |
如Fig 1C、1D所示,与NT组相比,Tg组小鼠穿过平台象限的次数和所处时间均减少(P < 0.01);与Tg组相比,Tg+Ori组小鼠穿过平台象限的次数和所处时间均增加(P < 0.05)。表明转基因小鼠记忆能力降低,荭草苷能够改善转基因小鼠空间记忆能力。
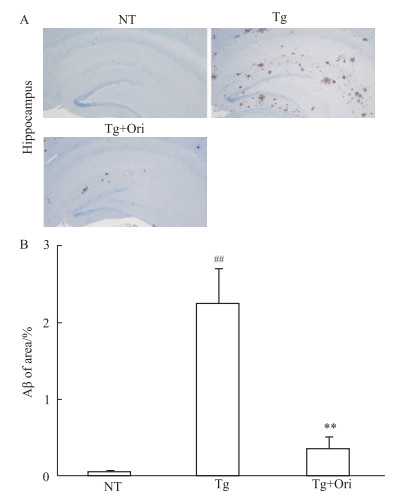
2.2 荭草苷改善APP/PS1转基因小鼠海马Aβ沉积Fig 2的Aβ免疫组化染色结果显示,与NT组相比,Tg组小鼠海马出现大量的Aβ阳性染色区域(P < 0.01);与Tg组相比,荭草苷组小鼠Aβ阳性染色所占面积百分比降低(P < 0.01)。表明Tg小鼠表现为海马Aβ沉积,荭草苷能够减少转基因小鼠海马Aβ沉积。
|
| Fig 2 Amyloid plaques of APP/PS1 mice reduced by orientin treatment (x±s, n=4) A:Brain sections were stained with an anti-Aβ antibody (×400); B: The relative area occupied by Aβ was measured ##P < 0.01 vs NT; **P < 0.01 vs Tg. |
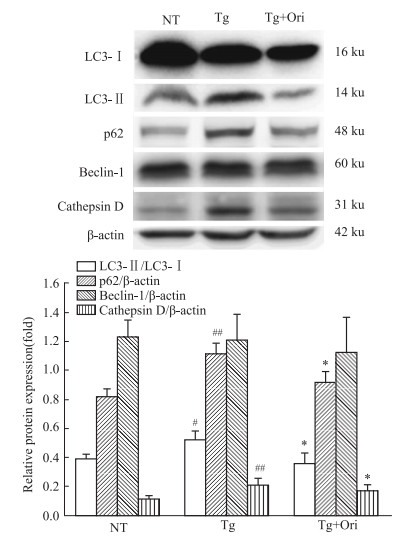
为了探究荭草苷对小鼠自噬的影响,检测自噬典型标记物LC3、p62、Beclin-1和Cathepsin D的表达。如Fig 3所示,与NT组相比,Tg组LC3-Ⅱ/LC3-Ⅰ的比值、p62、Cathepsin D表达升高(P < 0.05,P < 0.01);与Tg组相比,荭草苷组LC3-Ⅱ/LC3-Ⅰ的比值、p62、Cathepsin D表达降低(P < 0.05)。组间Beclin-1表达无差异。提示转基因小鼠自噬体堆积,荭草苷能够调控转基因小鼠自噬,促进自噬底物降解。
|
| Fig 3 Effects of orientin on autophagy related proteins in hippocampus of APP/PS1 mice (x±s, n=4) #P < 0.05, ##P < 0.01 vs NT; *P < 0.05 vs Tg |
目前AD确切的病因和致病机制仍不清楚,Aβ瀑布理论仍然是最广为接受的发病机制假说[6]。APP/PS1转基因小鼠是把人源性的APPswe和PS1△E9基因敲入到小鼠基因组中,能够较好地模拟AD患者的临床表现和病理改变[7-8],是研究AD的可靠模型。研究表明,荭草苷具有抗衰老、抗炎、抗抑郁、抗氧化应激、增强自噬[9]、抑制凋亡等作用[10],这些均与AD的发病密切相关。因此,荭草苷可能是一个潜在的多靶点作用的AD防治药物,但荭草苷治疗AD的确切机制仍不是很清楚。认知功能障碍是AD最重要的临床表现。本研究提示,荭草苷能够减少APP/PS1转基因小鼠脑Aβ沉积,从而改善学习记忆功能。
自噬是存在于真核细胞生物中保守的细胞内物质降解方式,能够选择性吞噬降解细胞内受损细胞器、易聚集蛋白、病原体等有害物质,并释放营养成分,维持细胞内稳态。近期研究表明,包括AD在内的表现为蛋白异常聚集的神经退行性疾病,其发病往往伴随着脑部自噬损害,主要表现为自噬内容物降解受阻、自噬溶酶体堆积[1]。LC3是典型的自噬标志物之一,在自噬体形成和成熟中起着重要作用,自噬体形成过程中,胞质型LC3酶解形成LC3-Ⅰ,LC3-Ⅰ与磷脂酰乙醇胺(phosphatidylethanolamine,PE)结合,转变为存在于自噬体的膜型LC3-Ⅱ,LC3-Ⅱ蛋白表达能够反映细胞内成熟自噬体的数量,LC3-Ⅱ/LC3-Ⅰ的比值反映自噬水平的变化[11]。对小鼠海马LC3检测结果提示,Tg组小鼠海马LC3-Ⅱ表达(结果未列出)及LC3-Ⅱ/LC3-Ⅰ的比值均升高,提示转基因AD小鼠海马自噬体数量增加,自噬处于高水平。p62能够识别、连接待降解自噬内容物,并通过与LC3-Ⅱ的连接,将自噬内容物募集到自噬体内[12]。p62检测结果表明,组间p62变化趋势和LC3-Ⅱ/LC3-Ⅰ的结果一致,表现为Tg组p62表达升高,荭草苷组p62表达下降。LC3-Ⅱ/LC3-Ⅰ和p62下降的原因可能是自噬诱导降低或(和)自噬溶酶体降解增加。为了明确自噬水平降低的原因,分别对自噬诱导及降解相关蛋白Beclin-1和Cathepsin D进行检测。Beclin-1在调控自噬体生成中起着不可或缺的作用[13],其蛋白表达能够反映自噬诱导水平。本实验结果表明,各组间Beclin-1蛋白表达无差异,提示各实验组动物的自噬诱导无差异,即荭草苷组LC3-Ⅱ/LC3-Ⅰ和p62的下降可能并非自噬诱导水平下降所致。Cathepsin D是人体内唯一天冬氨酸蛋白水解酶,通过降解自噬溶酶体和内吞体中未折叠或氧化性聚集蛋白,在维持神经元细胞内稳态中起着不可替代的作用。Cathepsin D有3种构型:存在于高尔基复合物的分子质量为53 ku的无活性的前体蛋白,转运至内吞体后修饰成为分子质量为48 ku的具有酶活性的单链蛋白中间体,以及进一步转运至溶酶体并修饰成为分子质量为31 ku的具有酶活性的成熟双链结构[14]。本实验结果提示,Tg组成熟型Cathepsin D、LC3-Ⅱ和p62均升高,与Lee等[15]的研究结果一致,荭草苷组均表现为降低,提示APP/PS1小鼠海马未降解的自噬溶酶体增多,荭草苷能够促进自噬内容物降解,改善转基因AD小鼠脑部自噬溶酶体底物堆积。
本实验结果表明,荭草苷能促进APP/PS1转基因小鼠脑自噬底物降解、减少自噬体堆积,进而减少脑内Aβ沉积,从而改善学习记忆障碍。因此,荭草苷可能是一个潜在的多靶点作用的AD防治药物。
( 致谢: 本实验在锦州医科大学生命科学院公共实验平台完成,感谢王宇教授的指导和帮助 )
| [1] |
Bordi M, Berg M J, Mohan P S, et al. Autophagy flux in CA1 neurons of Alzheimer hippocampus: increased induction overburdens failing lysosomes to propel neuritic dystrophy[J]. Autophagy, 2016, 12(12): 2467-83. doi:10.1080/15548627.2016.1239003 |
| [2] |
Menzies F M, Fleming A, Caricasole A, et al. Autophagy and neurodegeneration: pathogenic mechanisms and therapeutic opportunities[J]. Neuron, 2017, 93(5): 1015-34. doi:10.1016/j.neuron.2017.01.022 |
| [3] |
Yu L, Wang S, Chen X, et al. Orientin alleviates cognitive deficits and oxidative stress in Aβ1-42-induced mouse model of Alzheimers disease[J]. Life Sci, 2015, 121: 104-9. doi:10.1016/j.lfs.2014.11.021 |
| [4] |
Wang S, Yu Y, Feng Y, et al. Protective effect of the orientin on noise-induced cognitive impairments in mice[J]. Behav Brain Res, 2016, 296: 290-300. doi:10.1016/j.bbr.2015.09.024 |
| [5] |
Vorhees C V, Williams M T. Morris water maze: procedures for assessing spatial and related forms of learning and memory[J]. Nat Protoc, 2006, 1(2): 848-58. doi:10.1038/nprot.2006.116 |
| [6] |
Hardy J, Allsop D. Amyloid deposition as the central event in the aetiology of Alzheimers disease[J]. Trends Pharmacol Sci, 1991, 12(10): 383-8. |
| [7] |
Kurt M A, Davies D C, Kidd M, et al. Neurodegenerative changes associated with beta-amyloid deposition in the brains of mice carrying mutant amyloid precursor protein and mutant presenilin-1 transgenes[J]. Exp Neurol, 2001, 171(1): 59-71. |
| [8] |
Kurt M A, Davies D C, Kidd M, et al. Hyperphosphorylated tau and paired helical filament-like structures in the brains of mice carrying mutant amyloid precursor protein and mutant presenilin-1 transgenes[J]. Neurobiol Dis, 2003, 14(1): 89-97. |
| [9] |
刘立亚, 王慧晔, 黄秀兰. 基于细胞自噬的荭草苷抗心肌缺血/再灌注损伤的机制研究[J]. 中国药理学通报, 2016, 32(4): 542-7. Liu L Y, Wang H Y, Huang X L. Mechanism of anti-myocardial ischemia/reperfusion injury of orientin based on autophagy[J]. Chin Pharmacol Bull, 2016, 32(4): 542-7. doi:10.3969/j.issn.1001-1978.2016.04.020 |
| [10] |
Lam K Y, Ling A P, Koh R Y, et al. A review on medicinal properties of orientin[J]. Adv Pharmacol Sci, 2016, 2016: 4104595. |
| [11] |
Schaaf M B, Keulers T G, Vooijs M A, Rouschop K M. LC3/GABARAP family proteins: autophagy-(un)related functions[J]. FASEB J, 2016, 30(12): 3961-78. doi:10.1096/fj.201600698R |
| [12] |
Bjrky G, Lamark T, Brech A, et al. p62/SQSTM1 forms protein aggregates degraded by autophagy and has a protective effect on huntingtin-induced cell death[J]. J Cell Biol, 2005, 171(4): 603-14. doi:10.1083/jcb.200507002 |
| [13] |
Bento C F, Renna M, Ghislat G, et al. Mammalian autophagy: how does it work[J]. Annu Rev Biochem, 2016, 85: 685-713. doi:10.1146/annurev-biochem-060815-014556 |
| [14] |
Vidoni C, Follo C, Savino M, et al. The role of Cathepsin D in the pathogenesis of human neurodegenerative disorders[J]. Med Res Rev, 2016, 36(5): 845-70. |
| [15] |
Lee J K, Jin H K, Park M H, et al. Acid sphingomyelinase modulates the autophagic process by controlling lysosomal biogenesis in Alzheimers disease[J]. J Exp Med, 2014, 211(8): 1551-70. doi:10.1084/jem.20132451 |

