

2. 厦门大学药学院,福建 厦门 361102
2. School of Pharmaceutical Sciences, Xiamen University, Xiamen Fujian 361102, China
糖尿病是一种多因素引起的内分泌代谢紊乱性疾病,可分为1型、2型、妊娠糖尿病和其它特殊类型糖尿病[1]。胰岛素抵抗和高血糖是2型糖尿病的主要特征,器官减少对葡萄糖的摄取、代谢[2]。因此,寻找胰岛素增敏剂来对抗胰岛素抵抗,从而治疗2型糖尿病[3]。噻唑烷二酮(thiazolidinedione,TZD)介导过氧化物酶体增殖物激活受体γ(peroxisome proliferator-activated receptor γ,PPARγ)的激活,导致胰岛素敏感性明显提高[4-5]。PPARγ对葡萄糖、脂质代谢和炎症过程发挥较大作用[6-7]。PPARγ对胰岛素应答性葡萄糖摄取和增强葡萄糖转运体的表达有重要意义[8-9]。PPARγ2在脂肪细胞中表达,且促进分化[10]。3T3-L1前脂肪细胞分化后,得到的新的成熟脂肪细胞能加快对葡萄糖的吸收。胰岛素或胰岛素类似物在培养基中与细胞内不同的酶和受体作用,可以激活细胞和细胞核中的许多信号通路,从而进一步促进成熟脂肪细胞摄取、运输、消耗葡萄糖,最终使细胞培养基中葡萄糖浓度降低。综上所述,3T3-L1前脂肪细胞分化模型已被用于降血糖活性筛选[11-12]。
泽泻[Alisma orientale(Sam.) Juzep.]利水渗湿、泄热、化浊降脂,现代研究表明,泽泻水、醇提物均可改善高脂饲喂小鼠胰岛素抵抗模型的糖耐量[13],但具体药效物质基础尚不明确。23-乙酰泽泻醇B是泽泻中的特征成分之一,属于化学结构分类中三萜类化合物,具有促进HepG2细胞葡萄糖摄取活性[13]。因此,本研究旨在探索23-乙酰泽泻醇B是否具有抗糖尿病的潜力。采用链脲佐菌素(streptozotocin,STZ)和烟酰胺腹腔注射诱导的2型糖尿病小鼠模型[14],测定23-乙酰泽泻醇B降低血糖活性;应用3T3-L1脂肪细胞葡萄糖吸收模型,检测23-乙酰泽泻醇B对葡萄糖吸收的影响;通过3T3-L1前脂肪细胞分化模型,评估23-乙酰泽泻醇B对分化的作用和改善胰岛素抵抗的能力。在本研究中使用TZD类中的罗格列酮作为阳性对照药。
1 材料 1.1 药物与试剂胰岛素、葡萄糖、STZ、烟酰胺、罗格列酮、油红O染色和Harris苏木精染色液,购自美国Sigma-Aldrich公司;23-乙酰泽泻醇B(C32H50O5,纯度>98%),购自成都瑞芬思有限公司;葡萄糖荧光示踪剂2-[N-(7-硝基苯-2-氧代-1,3-重氮基-4-基)氨基]-2-脱氧-D-葡萄糖(2-[N-(7-nitrobenz-2-oxa-1, 3-diazol-4-yl)amino]-2-deoxy-D-glucose,2-NBDG),购自美国Molecular Probes公司;其他化学试剂均为分析级。
1.2 实验动物5~6周龄C57BL/6 ♂小鼠,体质量20~23 g,购自上海斯莱克实验动物有限公司,动物合格证号为2015000501745。每笼随机8只,饲养在室温(22±2)℃、湿度(50±5)%和12 h/12 h明暗光循环条件下。适应2周后,按照国家动物实验标准开始实验。
1.3 细胞3T3-L1前脂肪细胞,购自美国菌种保存中心。
1.4 仪器血糖仪(罗氏诊断产品上海有限公司);流式细胞仪(美国Becton Dickinson公司)。
2 方法 2.1 2型糖尿病模型的建立♂ C57BL/6小鼠禁食,次日腹腔注射240 mg·kg-1烟酰胺,15 min后腹腔注射100 mg·kg-1 STZ,2 d后再次注射相同剂量的烟酰胺和STZ。3周后,与空白对照组相比,血糖明显升高则可证实已造成高血糖,2型糖尿病模型成功建立。每日称量,并记录建模期间和灌胃给药期间小鼠体质量。
2.2 测定血糖值腹腔注射烟酰胺和STZ后,每7 d采血(5~10 μg)1次,即分别在d 0(注射前)、7、14、21,用血糖测定仪测定血糖浓度。
2.3 口服葡萄糖耐受试验(oral glucose tolerance test,OGTT)小鼠注射STZ和烟酰胺后的d 21禁食过夜,d 22进行OGTT。2型糖尿病模型组、阳性对照药罗格列酮组及23-乙酰泽泻醇B不同剂量组分别按小鼠体质量给予生理盐水、10 mg·kg-1罗格列酮、23-乙酰泽泻醇B(5、10、20 mg·kg-1)2 h后,再灌胃葡萄糖溶液(2.0 g·kg-1)。第0 min和灌胃葡萄糖后的第30、60、120 min尾静脉收集血液,并测定血糖水平。
2.4 灌胃给予23-乙酰泽泻醇B对空腹血糖和OGTT的影响空白对照组和模型组小鼠每日灌胃生理盐水、阳性对照组灌胃罗格列酮10 mg·kg-1,试药组分别灌胃23-乙酰泽泻醇B(5、10、20 mg·kg-1),持续3周。在d 0和给药后d 7、14、21,测定各组小鼠血糖值,小鼠在灌胃后的d 21禁食过夜,于d 22进行OGTT。
2.5 细胞培养小鼠3T3-L1前脂肪细胞用含10%胎牛血清的DMEM培养基,于5% CO2细胞培养箱37 ℃培养,第5~9代的细胞用于实验。
2.6 流式细胞仪分析细胞葡萄糖吸收情况参照文献[11]测定23-乙酰泽泻醇B对葡萄糖吸收的影响。每孔1×104个细胞将分化的3T3-L1脂肪细胞接种到96孔板培养24 h后,再用含30 mmol·L-1 D-葡萄糖(高糖条件)和1 μmol·L-1胰岛素的无血清DMEM培养,对照组不加任何药物处理,阳性对照组和试药组分别用罗格列酮(1、10 μmol·L-1)和23-乙酰泽泻醇B(1、10 μmol·L-1)与10 μmol·L-1 2-NBDG处理1 h后,收集细胞,并悬浮在500 μL预冷的无血清培养基中,在4 ℃条件下待流式细胞仪分析。记录流式细胞仪FL1通道中每组细胞的葡萄糖荧光示踪剂2-NBDG的荧光强度。用罗格列酮(1、10 μmol·L-1)、23-乙酰泽泻醇B(1、10 μmol·L-1)不加10 μmol·L-1 2-NBDG的条件下单独处理细胞1 h,作为背景值,以避免假阳性。相对荧光强度减去背景值用于数据分析。
2.7 油红O染色参照文献方法[11],首先将3T3-L1前脂肪细胞按4×103细胞/孔接种到96孔板中培养24 h,然后换成含10%胎牛血清和1 μmol·L-1胰岛素的DMEM培养基,对照组不加任何药物处理,阳性对照组加入罗格列酮(1、10 μmol·L-1)培养3 d,23-乙酰泽泻醇B组加入23-乙酰泽泻醇B(1、10 μmol·L-1)培养3 d。细胞培养12 d后,经10%福尔马林溶液固定1 h,依次用油红O溶液2 h、Harris苏木精染色液染色15 min后,用60%异丙醇清洗3次,将未与细胞结合的染料移除,最后于显微镜下(×400)拍摄染色情况。
2.8 统计学处理所有数据均以x±s表示。用SPSS 13.0软件进行单因素方差分析(ANOVA)、Dunnett′s或最小显著差异(LSD)检验。
3 结果 3.1 2型糖尿病小鼠模型造模后的空腹血糖值、OGTT、体质量变化在腹腔注射烟酰胺和STZ后的d 21,小鼠的血糖值明显高于空白对照组小鼠血糖值,提示造模成功。d 22对模型组和空白对照组进行OGTT,2型糖尿病模型小鼠灌胃葡萄糖溶液后的第30、60、120 min对应的血糖值,均明显高于空白对照组,提示造模成功。2型糖尿病模型建立期间,模型组、空白对照组的小鼠体质量差异无显著性。
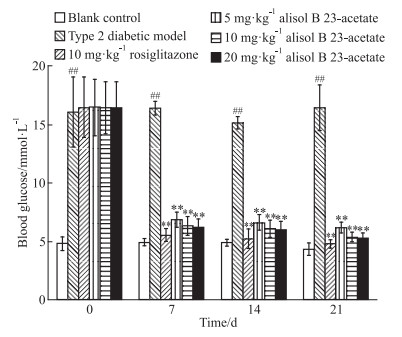
3.2 23-乙酰泽泻醇B对2型糖尿病小鼠血糖的影响阳性对照组每日灌胃罗格列酮10 mg·kg-1,d 7、14、21的血糖值与2型糖尿病模型组相比明显降低。每日按小鼠体质量分别灌胃23-乙酰泽泻醇B(5、10 mg·kg-1),持续给药3周,在给药后的d 7、14、21,与2型糖尿病模型组小鼠相比,血糖值呈明显下降的趋势(Fig 1)。23-乙酰泽泻醇B 10 mg·kg-1剂量组比5 mg·kg-1组显示出更好的降血糖活性,而20 mg·kg-1剂量组降血糖趋势并未比10 mg·kg-1剂量组明显。
|
| Fig 1 Effect of alisol B 23-acetate at different doses on blood glucose (x±s, n=8) **P < 0.01 vs type 2 diabetic model group; ##P < 0.01 vs blank control group |
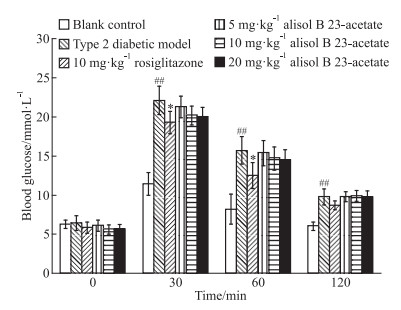
与模型组比较,罗格列酮10 mg·kg-1组使2型糖尿病小鼠在OGTT中第30、60 min的血糖值明显降低,而23-乙酰泽泻醇B(5、10、20 mg·kg-1)组在OGTT中仅在一定程度上对血糖值呈现出降低的趋势(Fig 2)。
|
| Fig 2 Effect of alisol B 23-acetate at different doses on OGTT (x±s, n=8) *P < 0.05 vs type 2 diabetic model group; ##P < 0.01 vs blank control group |
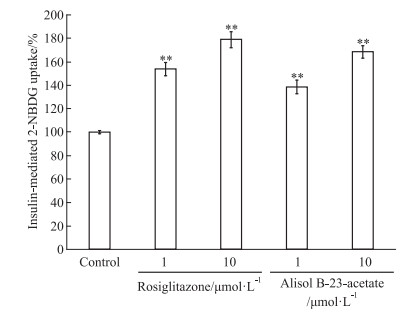
为研究23-乙酰泽泻醇B在高糖(30 mmol·L-1)条件下,是否提高葡萄糖吸收,采用分化的3T3-L1脂肪细胞模型进行葡萄糖荧光示踪剂2-NBDG吸收实验。罗格列酮(1、10 μmol·L-1)在高糖条件下明显增加胰岛素刺激的3T3-L1脂肪细胞对2-NBDG的吸收。23-乙酰泽泻醇B(1、10 μmol·L-1)也明显提高了胰岛素介导的脂肪细胞对2-NBDG的吸收。23-乙酰泽泻醇B(10 μmol·L-1)促进脂肪细胞吸收2-NBDG的活性与阳性对照药罗格列酮相似(Fig 3)。提示在高浓度葡萄糖环境下,23-乙酰泽泻醇B提高分化的3T3-L1脂肪细胞吸收胰岛素刺激的2-NBDG活性。
|
| Fig 3 Effect of alisol B-23-acetate on insulin-stimulated glucose uptake in adipocytes under high concentration glucose condition (x±s,n=8) **P < 0.01 vs control(2-NBDG and insulin co-treated high-concentration glucose group) |
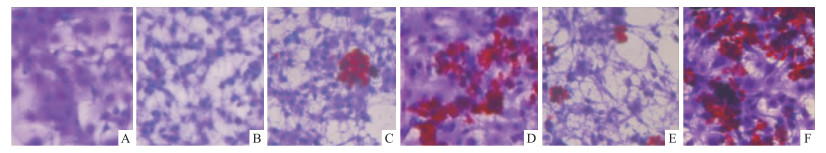
油红O染料可与细胞中的甘油三酯反应,使脂肪细胞呈现红色。大量的脂肪滴出现在细胞中,表明新的成熟脂肪细胞的形成。如Fig 4所示,与对照组相比,23-乙酰泽泻醇B(1、10 μmol·L-1)和罗格列酮(1、10 μmol·L-1)均能促进分化。
|
| Fig 4 Effect of alisol B 23-acetate on differentiation in 3T3-L1 pre-adipocytes (×400) A: Pre-adipocytes; B: Control cells (differentiated 3T3-L1 adipocytes); C: 1 μmol·L-1 rosiglitazone; D: 10 μmol·L-1 rosiglitazone; E: 1 μmol·L-1 alisol B 23-acetate; F: 10 μmol·L-1 alisol B 23-acetate. |
灌胃泽泻乙酸乙酯提取物降低2型糖尿病小鼠空腹血糖值和口服葡萄糖耐量实验期间的血糖值,但具体的有效成分尚不明确[15]。研究表明,泽泻三萜类成分23-乙酰泽泻醇B具有促进HepG2细胞葡萄糖摄取活性[13],很可能是其降糖药效物质基础之一。因此,本实验探讨了泽泻的特征化学成分23-乙酰泽泻醇B对2型糖尿病小鼠降糖活性的影响。模型组空腹血糖值和OGTT期间血糖明显高于空白对照组,提示造模成功。罗格列酮10 mg·kg-1给药21 d后的血糖值明显低于2型糖尿病组小鼠;23-乙酰泽泻醇B(5、10、20 mg·kg-1)组给药3周后,与模型组相比,也降低了血糖值。进行OGTT以确认对胰岛素的敏感性,2型糖尿病模型组小鼠在灌胃葡萄糖溶液后的第30、60、120 min时,血糖值明显高于空白对照组。罗格列酮10 mg·kg-1组在OGTT的第30、60 min时,使2型糖尿病小鼠血糖值下降, 23-乙酰泽泻醇B组也在第30、60 min对血糖值有一定程度的降低。以上结果提示,23-乙酰泽泻醇B和罗格列酮均可降低OGTT期间的血糖值,提示二者均能使胰岛素抵抗程度降低。因此,23-乙酰泽泻醇B降低血糖值,可一定程度地改善胰岛素抵抗。
23-乙酰泽泻醇B(1、10 μmol·L-1)均能明显促进脂肪细胞吸收胰岛素刺激的葡萄糖,提示23-乙酰泽泻醇B可能作为治疗2型糖尿病的候选药物,但其作用机制尚需深入研究。
在3T3-L1前脂肪细胞分化模型中,23-乙酰泽泻醇B(1、10 μmol·L-1)均能促进分化过程。在分化过程中,产生新的成熟的脂肪细胞可能与胰岛素或胰岛素类似物作用,从而激活细胞和细胞核中的信号通路,增强成熟脂肪细胞对葡萄糖的吸收。因此,推测23-乙酰泽泻醇B降血糖活性、提高糖吸收可能与其促进分化有关。
本文报道了23-乙酰泽泻醇B的降血糖活性,提示23-乙酰泽泻醇B可能是泽泻降血糖作用的药效物质。综合23-乙酰泽泻醇B促进分化、提高糖吸收、降低2型糖尿病小鼠空腹血糖值和OGTT过程中的血糖值的结果分析,推测23-乙酰泽泻醇B的降血糖活性可能是由于其激活PPARγ,并增加其在脂肪细胞中表达,促进前脂肪细胞分化,提高胰岛素敏感性,从而促进胰岛素应答性葡萄糖吸收和改善胰岛素抵抗,最终使葡萄糖浓度降低。然而,上述推测尚需进一步研究和验证,详细的药理作用及作用机制尚需深入研究。
| [1] |
李吉萍, 袁野, 张文友. 西洋参茎叶皂苷对糖尿病大鼠氧化损伤和血管内皮功能的影响[J]. 中国药理学通报, 2017, 33(12): 1698-702. Li J P, Yuan Y, Zhang W Y. Influence of Panax quinquefolium saponins on oxidative damage and function of vascular endothelium in diabetic rats[J]. Chin Pharmacol Bull, 2017, 33(12): 1698-702. doi:10.3969/j.issn.1001-1978.2017.12.014 |
| [2] |
Hardie D G. Role of AMP-activated protein kinase in the metabolic syndrome and in heart disease[J]. FEBS Lett, 2008, 582(1): 81-9. doi:10.1016/j.febslet.2007.11.018 |
| [3] |
Prasad C N, Anjana T, Banerji A, et al. Gallic acid induces GLUT4 translocation and glucose uptake activity in 3T3-L1 cells[J]. FEBS Lett, 2010, 584(3): 531-6. doi:10.1016/j.febslet.2009.11.092 |
| [4] |
Saltiel A R, Olefsky J M. Thiazolidinediones in the treatment of insulin resistance and type II diabetes[J]. Diabetes, 1996, 45(12): 1661-9. doi:10.2337/diab.45.12.1661 |
| [5] |
Olefsky J M, Saltiel A R. PPAR γ and the treatment of insulin resistance[J]. Trends Endocrinol Metab, 2000, 11(9): 362-8. doi:10.1016/S1043-2760(00)00306-4 |
| [6] |
Berger J, Moller D E. The mechanisms of action of PPARs[J]. Annu Rev Med, 2002, 53: 409-35. doi:10.1146/annurev.med.53.082901.104018 |
| [7] |
Willson T M, Lambert M H, Kliewer S A. Peroxisome proliferator-activated receptor γ and metabolic disease[J]. Annu Rev Biochem, 2001, 70: 341-67. doi:10.1146/annurev.biochem.70.1.341 |
| [8] |
Hamm J K, el Jack A K, Pilch P F, et al. Role of PPARγ in regulating adipocyte differentiation and insulin-responsive glucose uptake[J]. Ann NY Acad Sci, 1999, 892: 134-45. doi:10.1111/j.1749-6632.1999.tb07792.x |
| [9] |
Nugent C, Prins J B, Whitehead J P, et al. Arachidonic acid stimulates glucose uptake in 3T3-L1 adipocytes by increasing GLUT1 and GLUT4 levels at the plasma membrane. Evidence for involvement of lipoxygenase metabolites and peroxisome proliferator-activated receptor γ[J]. J Biol Chem, 2001, 276(12): 9149-57.
|
| [10] |
Ren D, Collingwood T N, Rebar E J, et al. PPARγ knockdown by engineered transcription factors: exogenous PPARγ2 but not PPARγ1 reactivates adipogenesis[J]. Genes Dev, 2002, 16(1): 27-32. doi:10.1101/gad.953802 |
| [11] |
Zhang W Y, Lee J J, Kim Y H, et al. Effect of eriodictyol on glucose uptake and insulin resistance in vitro[J]. J Agric Food Chem, 2012, 60(31): 7652-8. doi:10.1021/jf300601z |
| [12] |
Kamon J, Naitoh T, Kitahara M, et al. Prostaglandin F(2) alpha enhances glucose consumption through neither adipocyte differentiation nor GLUT1 expression in 3T3-L1 cells[J]. Cell Signal, 2001, 13(2): 105-9. |
| [13] |
许文, 罗奋熔, 赵万里, 等. 泽泻降糖活性提取物化学成分研究[J]. 中草药, 2014, 45(22): 3238-45. Xu W, Luo F R, Zhao W L, et al. Chemical constituents from Alisma orientalis extracts with hypoglycemic effect[J]. Chin Tradit Herb Drugs, 2014, 45(22): 3238-45. doi:10.7501/j.issn.0253-2670.2014.22.005 |
| [14] |
Choi W S, Lee J J, Kim Y, et al. Synergistic improvement in insulin resistance with a combination of fenofibrate and rosiglitazone in obese type 2 diabetic mice[J]. Arch Pharm Res, 2011, 34(4): 615-24. doi:10.1007/s12272-011-0412-9 |
| [15] |
张伟云, 陈全成, 王丽荣, 等. 泽泻降低2型糖尿病小鼠血糖的有效部位筛选[J]. 上海中医药杂志, 2016, 50(10): 81-5. Zhang W Y, Chen Q C, Wang L R, et al. Screening research on effective parts of Alisma orientalis (Samuel.) Juzep.associated with blood glucose decrease in type 2 diabetic mice[J]. Shanghai J Tradit Chin Med, 2016, 50(10): 81-5. |

