

2. 山西医科大学第二医院麻醉科, 山西 太原 030001
2. Dept of Anesthesiology, the Second Hospital of Shanxi Medical University,Shanxi Medical University, Taiyuan 030001, China
相关资料显示, 大约50%的糖尿病患者伴发明显的糖尿病周围神经病变(diabetic peripheral neuropathy, DPN), 出现症状早, 且病情隐匿不易发现。DPN易累及心脏感觉神经, 引起神经纤维的变性, 从而导致神经纤维进行性缺失和再生[1]。神经生长因子(nerve growth factor, NGF)是神经营养因子家族中重要的一员, 通过作用于高亲和力酪氨酸激酶A (tyrosine kinase A, TrkA)受体和低亲和力p75受体(75 kd neurotrophin receptor, p75NTR), 调控中枢及周围神经的生长、发育及再生[2]。糖尿病心脏感觉神经病变可引起NGF表达下调, 使受NGF调控的基因表达产物降钙素基因相关肽(calcitonin gene-related peptide, CGRP)大幅度减少, 从而导致心脏感觉神经病变、心肌细胞凋亡和心功能不全[3]。CGRP分布于心血管组织中, 具有舒血管作用, 保护心肌细胞和内皮细胞, 调节心功能[4]。重组腺相关病毒(recombinant adeno-associated virus, rAAV)具有安全性好、免疫源性低、转染时间长等特点, 其中rAAV9有较好的心脏亲和力, 能够稳定地转染到大鼠的心肌组织[5-6]。已有实验证明, 外源性补充NGF可以营养正常的神经纤维, 促进损伤神经纤维的修复再生, 改善糖尿病导致的心脏神经病变, 减少心肌细胞的凋亡, 提高心功能[7]。课题组前期研究表明, 糖尿病可使NGF表达减少。由此设想能否通过心肌转染技术, 使NGF在大鼠心肌组织中过表达, 本研究探讨能否通过心肌点注射的方法, 利用rAAV9-NGF基因转染糖尿病大鼠的心脏, 上调NGF的表达, 由此产生对糖尿病大鼠心脏损伤的保护作用。
1 材料与方法 1.1 实验动物健康♂SD大鼠32只, 体质量200~250 g, 7~8周龄, 由中国人民解放军军事医学科学院实验动物中心提供, 实验动物许可证:SCXK (京)2014-0013)。大鼠按随机数字表法分为4组(n=8):对照组(control组)、糖尿病手术组(D+P组)、糖尿病手术对照组(D+V组)、糖尿病转染组(D+NGF组)。实验操作程序经山西医科大学动物伦理委员会批准, 并按实验动物使用的3R原则给予人道关怀。
1.2 试剂与仪器rAAV9-NGF-GFP (滴度1.2×1015 vg·L-1)、rAAV9-GFP (滴度1.6×1015vg·L-1), 均购自上海汉恒生物科技有限公司; 链脲佐菌素(streptozotin, STZ, 美国Sigma公司); 大鼠NGF ELISA试剂盒、大鼠CGRP ELISA试剂盒(上海西唐生物科技有限公司); NGF抗体(美国Santa Cruz Biotechnology公司); 蛋白基因产物9.5(protein gene product 9.5, PGP9.5)抗体(美国Novus公司); CGRP抗体(美国Cell Signaling Technology公司); Alexa Fluor 594羊抗小鼠荧光二抗(美国Invitrogen公司)。小动物生命指标检测仪(四川仪器厂); Leica CM-1850恒冷切片机(德国Leica公司); BX-51型荧光显微镜(日本TKO光学仪器株式会社); Novapath酶标仪(美国Bio-Rad公司)。
1.3 方法 1.3.1 l型糖尿病模型的制备大鼠适应1周后, D+P组、D+V组、D+NGF组大鼠禁食24 h, 继以腹腔注射STZ (50 mg·kg-1)。连续测量之后7 d的空腹血糖, 以7次血糖值均>16.7 mmol·L-1为l型糖尿病造模成功。
1.3.2 测定大鼠甩尾反射潜伏期STZ注射前ld及以后每周, 使用小动物甩尾仪红外光源(光照强度40 mW·cm-2, 最大刺激时间30 s)对准大鼠尾尖端进行照射, 记录热痛刺激逃避性甩尾反射潜伏期。
1.3.3 病毒转染大鼠糖尿病成模后第4周, 以质量分数为7%的水合氯醛(300 mg·kg-1)腹腔注射麻醉后, 测血糖、体质量, 经口直视下气管插管, 连接呼吸机, 并控制呼吸(潮气量=10 ml·kg-1, 通气频率=70次每分钟, 吸呼比=1:2)。将大鼠仰卧位固定于手术台, 在胸骨体偏左侧1 cm处备皮消毒, 暴露上皮组织, 钝性分离胸壁组织直至肋骨, 用血管钳从心尖搏动最强处进入胸腔并扩张, 使心尖部暴露于视野。参考并已改良的实验方法[8], 选取心尖部为注射区域, 网格状选取5个注射点(点间隔约1 mm, 深度1~2 mm), 以前端针头被90°掰弯的胰岛素注射针, 注射磷酸缓冲盐浓液(phosphate buffer saline, PBS)或滴度为0.8×1015 vg·L-1的rAAV9-GFP、rAAV9-NGF-GFP各100 μL (每注射点20 μL), 逐层关胸。术后连续3 d肌肉注射庆大霉素1万单位以预防感染。
1.3.4 心功能指标的监测转染后第5周(糖尿病造模后9周), 大鼠以质量分数为25%的乌拉坦(5 ml·kg-1)腹腔麻醉, 测血糖、体质量。连接小动物生命指标检测仪, 监测大鼠心电图, 分离大鼠右侧颈动脉, 置动脉导管监测左心室收缩压(left ventricular systolic pressure, LVSP)、左心室舒张末压(left ventricular end-diastolic pressure, LVEDP)、心率(heart rate, HR)、左心室内压最大上升速率(+dp/dtmax)、左心室内压最大下降速率(-dp/dtmax)等指标。
1.3.5 心肌组织NGF、CGRP含量测定取左心室处心肌组织, 在液氮条件下研磨至粉末状, 按10 ml·g-1加入蛋白裂解液, 冰盒裂解1 h (每10 min混匀1次)后, 4℃、15 000×g离心30 min, 取上清, 严格按照说明书步骤, 采用ELISA试剂盒测定样本NGF、CGRP含量。
1.3.6 免疫荧光法测NGF、CGRP及神经纤维的表达造模后第7周和第9周, 取大鼠心脏, 质量分数为4%的多聚甲醛固定, 浓度梯度的蔗糖脱水, OCT包埋, 最后冰冻切片机切片(厚度10 μm)。切片室温平衡30min, 放入0.1%的Triton-100(用PBS 1:1 000稀释)中, 4℃冰箱内孵育10 min, 后以PBS洗5 min×3次; 滴加5%牛血清蛋白(BSA)封闭, 室温孵育2 h; 滴加以5% BSA稀释的一抗NGF (1:200)、PGP9.5(1:300)、CGRP (1:500), 4℃冰箱孵育过夜; 将切片从冰箱取出, 室温平衡10 min, 以PBS洗5 min×3次; 滴加5% BSA稀释的荧光标记的二抗(1:1 000), 室温避光孵育2 h, 以PBS洗5 min×3次; 甘油封片; 荧光显微镜下观察。
1.4 统计学分析采用SPSS 25.0统计软件分析数据, 正态分布的计量资料以x±s表示, 组间比较采用单因素方差分析, 两两比较采用LSD-t检验。
2 结果 2.1 大鼠生存状况D+P组、D+V组、D+NGF组均有1只大鼠死亡, 大鼠死亡率组间差异无统计学意义(P>0.05)。
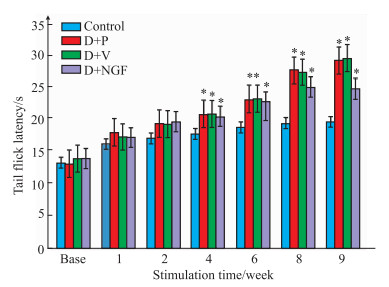
2.2 大鼠甩尾反射潜伏期如Fig 1所示, 与对照组相比, 第4周后, 其余3组的大鼠甩尾潜伏期均明显延长(P < 0.05)。
|
| Fig 1 Difference in tail-flick latency of rats between each group (x±s, n=6) *P < 0.05 vs control group |
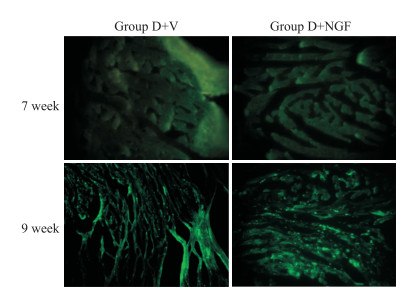
因rAAV9-NGF自身携带GFP标签, 故可借助免疫荧光技术验证外源基因NGF是否稳定转染入心脏组织中。如Fig 2所示, 第9周时, D+V组和D+NGF组有大量的GFP蛋白散在分布于细胞内, 表明病毒已稳定转染; 而第7周时却未见GFP蛋白的表达, rAAV9-NGF未稳定转染。
|
| Fig 2 Expression of GFP in group D+V and D+NGF (×20) At the ninth week, GFP could be seen clearly in group D+V and D+NGF. |
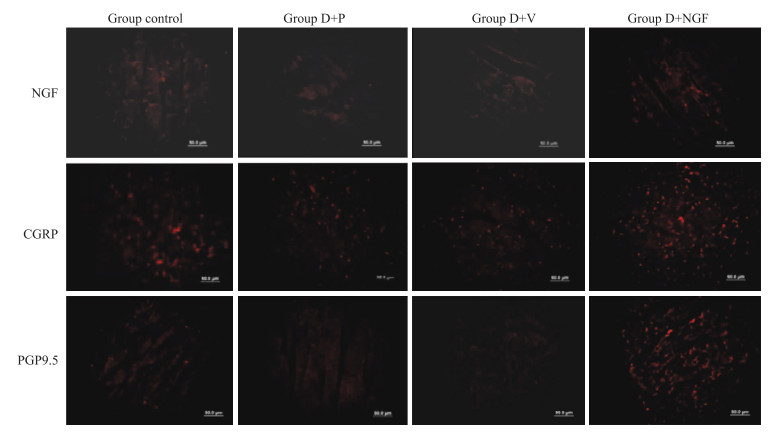
如Fig 3所示, 第7周时, 与对照组相比, D+P组、D+V组和D+NGF组大鼠心肌处的NGF、CGRP和神经纤维特异性标记物免疫荧光减弱, 但D+P组、D+V组和D+NGF组3组间无明显差异。如Fig 4所示, 第9周时, CGRP免疫反应阳性神经纤维多见于心外膜和心肌层, 尤其是血管周围和血管内皮处。D+P组和D+V组大鼠心肌处的NGF、CGRP和神经纤维特异性标记物PGP9.5比对照组和D+NGF组明显减少, 而对照组与D+NGF组无明显差异。

|
| Fig 3 Expression of NGF, CGRP and PGP9.5 in myocardium at 7th week (×40) Compared with group D+P, D+V and D+NGF, the red fluorescence could be seen clearly in group control. |
|
| Fig 4 Expression of NGF, CGRP and PGP9.5 in myocardium at 9th week (×40) Compared with group D+P and group D+V, the red fluorescence could be seen clearly in control group and group D+NGF. |
Tab 1结果显示, 对照组心肌组织中NGF、CGRP含量明显高于D+P组和D+V组(P < 0.05), 提示糖尿病会导致心肌组织的NGF、CGRP表达下降。但D+NGF组的NGF、CGRP的含量却明显高于D+P组与D+V组(P < 0.05)。对照组与D+NGF组差异无统计学意义。
| Group | NGF | CGRP |
| Control | 73.08±6.22 | 184.81±15.41 |
| D+P | 41.52±8.31* | 123.45±14.51* |
| D+V | 48.03±13.69* | 114.01±27.06* |
| D+NGF | 63.39±4.08#△ | 165.76±21.06#△ |
| *P < 0.05 vs control group; #P < 0.05 vs group D+P; △P < 0.05 vs group D+V | ||
Tab 2结果显示, 对照组的LVSP、LVEDP、HR、+dP/dtmax、-dP/dtmax明显高于D+P组和D+V组(P < 0.05), 提示糖尿病大鼠的心功能明显减弱。但D+NGF组的LVSP、LVEDP、HR、+dP/dtmax、-dP/dtmax却明显高于D+P组和D+V组(P < 0.05)。对照组与D+NGF组间无差异。
| Group | LVSP/mmHg | LVEDP/mmHg | HR/min-1 | +dP/dtmax/mmHg·s-1 | -dP/dtmax/mmHg·s-1 |
| Control | 140.53±5.05 | -3.76±1.61 | 296.83±40.05 | 9701.63±935.37 | -7460.72±1326.13 |
| D+P | 98.31±4.43* | 0.18±1.90* | 244.33±17.53* | 6712.42±550.87* | -5138.95±541.08* |
| D+V | 92.15±10.26* | 0.81±1.57* | 231.33±34.44* | 6128.54±911.69* | -4938.06±655.76* |
| D+NGF | 138.02±12.99#△ | -2.43±1.73#△ | 274.50±33.99#△ | 8856.27±1099.71#△ | -6261.74±867.28#△ |
| *P < 0.05 vs control group; #P < 0.05 vs group D+P; △P < 0.05 vs group D+V | |||||
DPN是一种由多病因引起的以血糖增高为特征的代谢性疾病, 由于胰岛素缺乏和血脂异常等因素相互作用, 影响感觉、运动和自主神经纤维, 尤其是极易影响心脏的感觉神经, 从而导致轴突萎缩、再生潜能减弱、发炎及纤维进行性丧失[9]。NGF广泛分布于周围组织、中枢及外周神经系统, 不仅能营养神经元, 而且能促进突触生长, 是介于神经系统和心血管系统之间的一种介质, 对大脑的发育、神经系统的生长、损伤神经的再生和功能恢复具有决定性的作用[2]。糖尿病心脏感觉神经病变发病机制包括缺血性微血管病变、NGF及其受体的缺乏、晚期糖基化终末产物的过度产生、氧化应激、线粒体功能紊乱、遗传易感性等, 其中NGF及其受体的缺乏是一个极其重要的因素[10]。NGF的表达下调后, 可使受其调节的神经肽CGRP减少, 使心脏感觉神经纤维进行性缺失和异常再生, 心肌细胞凋亡, 心功能恶化[3]。研究证明, 采用外源性的NGF治疗心脏感觉神经病变后, 糖尿病导致的心脏感觉神经变性得到改善[11]。
基因治疗为糖尿病心脏感觉神经病变开创了新的治疗途径。本研究采用腹腔注射STZ建立糖尿病模型, 利用心肌点注射转染rAAV9-NGF基因至心肌组织上。结果表明, 注射STZ后, 大鼠出现热痛阈值升高, 甩尾潜伏期延长, 并随着病程的进展而更加明显。由于构建的病毒需要至少3周, 才可稳定转染入心肌组织, 因此, NGF基因转染后第2周(注射STZ后第6周)时并未见明显的GFP的表达, 第5周(注射STZ后第9周)时可以看到明显的GFP表达, 表明rAAV9-NGF构建成功且感染心肌组织, 免疫荧光结果显示, 心肌组织中, 尤其是心外膜边界处和血管周围的NGF、CGRP和神经纤维分布增多。糖尿病大鼠心肌组织中NGF、CGRP蛋白的表达明显上调, 心功能得到改善。
已有研究证实, 心脏感觉神经元损伤时, NGF可与TrkA结合, 导致自身酪氨酸残基磷酸化, 逆转运至细胞质, 产生多种信号分子, 并将信号传递到细胞核, 调控细胞基因的表达, 如CGRP, 发挥生物效应, 从而维持受损神经元的存活和分化, 决定轴突生长方向, 促进受损神经修复, 诱导突触延伸[12]。CGRP具有广泛的生物学效应, 可以加强心肌收缩力, 增加心输出量, 提高灌注压, 加快心率, 降低血液黏稠度, 改善心肌血管血流性质[4]。因此, 本实验采用心肌点注射转染的方法, 将rAAV9-NGF原位导入心脏组织中, 使NGF过表达。前期研究表明, 过表达的NGF通过选择性地结合TrkA和p75NTR, 活化cAMP/Ras反应元件, 然后持续激活MAPK信号转导通路ERK, 进而上调CGRP的表达[13]。CGRP与其受体结合后, 激活鸟苷酸环化酶, 促进细胞内环磷酸腺苷和前列腺素的释放, 发挥强大的舒血管作用[4], 进而产生对心血管系统保护作用。
由此可以证实, rAAV9-NGF可以转染到糖尿病大鼠心肌组织中, 且稳定表达, 营养神经纤维, 促进神经纤维的再分布, 上调CGRP的表达, 部分改善心功能, 产生心脏保护作用。为临床有效地控制DPN, 尤其是心脏的感觉神经病变, 提供了新的治疗思路。
( 致谢: 本实验在山西医科大学第二医院麻醉实验室完成, 感谢各位老师和同学的对实验的指导和帮助! )
| [1] |
Fisher V L, Tahrani A A. Cardiac autonomic neuropathy in patients with diabetes mellitus:current perspectives[J]. Diabetes Metab Syndr Obes, 2017, 10: 419-34. doi:10.2147/DMSO |
| [2] |
Marlin M C, Li G. Biogenesis and function of the NGF/TrkA signaling endosome[J]. Int Rev Cell Mol Biol, 2015, 314(6): 239-57. |
| [3] |
Ieda M, Kanazawa H, Ieda Y, et al. Nerve growth factor is critical for cardiac sensory innervation and rescues neuropathy in diabetic hearts[J]. Circulation, 2006, 114(22): 2351-63. doi:10.1161/CIRCULATIONAHA.106.627588 |
| [4] |
Sheng Y, Zhu L. The crosstalk between autonomic nervous system and blood vessels[J]. Int J Physiol Pathophysiol Pharmacol, 2018, 10(1): 17. |
| [5] |
阙文忠, 陈君敏. 利用Gateway技术构建重组腺病毒pAd-NK4[J]. 中国药理学通报, 2011, 27(4): 462-7. Que W Z, Chen J M. Gateway technical supported construction of a recombinant adenovirus vector pAd-NK4[J]. Chin Pharmacol Bull, 2011, 27(4): 462-7. doi:10.3969/j.issn.1001-1978.2011.04.006 |
| [6] |
Pacak C A, Mah C S, Thattaliyath B D, et al. Recombinant adeno-associated virus serotype 9 leads to preferential cardiac transduction in vivo[J]. Circ Res, 2006, 99(4): 3-9. |
| [7] |
李琳, 刘振宅. 神经生长因子与糖尿病周围神经病变研究进展[J]. 国外医学(内分泌学分册), 2004, 24(z1): 30-3. Li L, Liu Z Z. Progress in the study of nerve growth factor and diabetic peripheral neuropathy[J]. Section Endocrinol Foreign Med Sci, 2004, 24(z1): 30-3. doi:10.3760/cma.j.issn.1673-4157.2004.z1.012 |
| [8] |
陈艳芳, 张銮坤, 王若伦. 腺病毒介导心脏特异性过表达RIP140对大鼠心脏功能及炎症通路的影响[J]. 中国药理学通报, 2017, 33(8): 1068-72. Chen Y F, Zhang L K, Wang R L, et al. Role of adenovirus-mediated cardiac-specific RIP140 overexpression in cardiac function and inflammation pathway[J]. Chin Pharmacol Bull, 2017, 33(8): 1068-72. doi:10.3969/j.issn.1001-1978.2017.08.007 |
| [9] |
Oakley I, Emond L. Diabetic cardiac autonomic neuropathy and anesthetic management: review of the literature[J]. AANA J, 2011, 79(6): 473-9. |
| [10] |
Landowski L M, Dyck P J, Engelstad J, et al. Axonopathy in peripheral neuropathies: mechanisms and therapeutic approaches for regeneration[J]. J Chem Neuroanat, 2016, 76. |
| [11] |
路丹, 刘艳霞, 李静. 鼠神经生长因子对糖尿病周围神经病变的疗效评估及药理分析[J]. 中国现代药物应用, 2016, 10(9): 16-7. Lu D, Liu Y X, Jing L, et al. Curative effect evaluation and pharmacological analysis of mouse nerve growth factor for diabetic peripheral neuropathy[J]. Chin J Mod Drug Appl, 2016, 10(9): 16-7. |
| [12] |
Hirose M, Kuroda Y, Murata E. NGF/TrkA signaling as a therapeutic target for pain[J]. Pain Pract, 2016, 16(2): 175-82. doi:10.1111/papr.2016.16.issue-2 |
| [13] |
岳维.急性心肌缺血早期降钙素基因相关肽和神经生长因子的表达[D].太原: 山西医科大学, 2011. Yue W. The expression of CGRP and NGF at stage of acute myocardial infarction[D].Taiyuan: Shanxi Medical University, 2011. |

