

2. 天津市新药非临床评价技术工程中心GLP实验室,天津 300301;
3. 山东省科学院生物研究所药物筛选技术重点实验室,山东 济南 250014
2. Tianjin Engineering Research Center of Drug Preclinical Assessment Technology, GLP Lab, Tianjin 300301, China;
3. Shandong Province Biology Institute of Shandong Academy of Sciences, Key Lab for Drug Screening Technology, Ji'nan 250014, China
斑马鱼作为一种公认的新型模式生物,目前被广泛应用于医药、环境等多个研究领域[1-2]。在斑马鱼实验中,检测终点和染毒频率不同,可能导致被检物的毒性表现发生明显差异,从而影响被检物毒性的准确判断。目前各领域对斑马鱼检测终点的选取未形成共识[1, 3-5],染毒频率的设定也参差不齐[2, 4]。本研究针对检测终点和染毒频率建立验证实验,阐明其对斑马鱼药物评价模型的影响,尝试摸索最佳实验方法,为更好地进行药物毒性的早期筛选提供参考。
1 材料与方法 1.1 仪器与试剂SZX16型体视荧光显微镜、DP2-BSW图像采集系统(Olympus公司); 斑马鱼养殖饲养系统(北京爱生科技有限公司)。全反式维甲酸(all-trans retinoic acid,ATRA,Sigma公司); 抗坏血酸(ascorbic acid,AA,天津市化学试剂供销公司); 二甲基亚砜(dimethyl sulfoxide,DMSO,生工生物工程上海股份有限公司); 三卡因(化学名3-氨基苯甲酸乙酯甲磺酸盐,Fluka公司); 钙黄绿素(Sigma公司)。DMSO配制成储备液,-20℃保存备用,使用前用斑马鱼胚胎培养用水(5 mmol·L-1 NaCl、0.17 mmol·L-1 KCl、0.4 mmol·L-1 CaCl2、0.16 mmol·L-1 MgSO4)稀释为70 mmol·L-1用于实验。
1.2 鱼卵制备健康性成熟的AB系斑马鱼所产受精卵,于受精2 h时经脱膜处理后,挑选受精6 h的健康脱膜斑马鱼胚胎用于实验。
1.3 实验方法实验共设9组,分别为空白对照组(胚胎培养用水)、溶剂对照组(DMSO,70 mmol·L-1)、阴性药物组(AA,10 mg·L-1)、阳性药物组(ATRA设置6个检测浓度:0.625、1.25、2.5、5.0、7.5、10 μg·L-1)。斑马鱼胚胎移入6孔培养板中,每孔30枚,每组3个重复孔。每24 h更换4/5的药液,连续染毒5 d。每天计数死亡受精卵和幼鱼数,计算累积死亡率,对照组累积死亡率应不高于10%。实验结束时,显微镜下观察存活幼鱼自主活动情况; 利用1 mmol·L-1三卡因麻醉幼鱼,固定焦距对侧面、背面照相,首先对每条存活幼鱼的形态发育进行镜下观察,随后每组选择6条幼鱼对体节、脊索、尾、鳍(胸鳍、背鳍、腹鳍、尾鳍)、脑、上面部结构(眼、耳囊、嗅区)、下面部结构(上下颚)、心脏、体形、肝、鳔的发育进行评分,并根据各组织器官评分情况,对每条斑马鱼进行总体评分[6]。将麻醉的幼鱼用3.2 mmol·L-1的钙黄绿素溶液染色,荧光显微镜下计数鱼体中具有荧光染色的脊椎骨(矿化椎骨)并拍照。
1.4 观察时间研究另取9组斑马鱼胚胎,在染毒5 d时去掉药液,加入胚胎培养用水,至d 7结束实验,观察斑马鱼幼鱼发育情况。其他实验方法同“1.3”项。
1.5 换液频率研究另取9组斑马鱼胚胎,在d 1时加入药液,实验期间不换液,在染毒5 d时结束实验,观察幼鱼发育情况。其他实验方法同“1.3”项。
1.6 统计学方法实验数据用x±s表示,使用SPSS 20.0软件进行统计分析。由于各组间方差不齐,因此进行非参数Kruskal-Wallis检验。
2 结果 2.1 对死亡率的影响如Tab 1所示,空白对照组、溶剂对照组和阴性药物组平均死亡率均 < 10%,但5 d不换液实验的死亡率较换液实验略有升高。ATRA各给药组,给药5 d每天换液和不换液实验各组的死亡率均≤10%,但不换液实验大部分组别的死亡率略低; 7 d换液实验,0.625、1.25、2.5、5.0 μg·L-1组死亡率较低,能保证有足够数量的胚胎用于发育评价,7.5、10 μg·L-1两组死亡率明显升高。
| Group | 5 d changing | 7 d changing | 5 d no-changing |
| Control | 2.22±1.92 | 6.67±5.77 | 10.00±10.00 |
| DMSO | 3.33±3.34 | 0.00±0.00 | 10.00±17.32 |
| AA | 3.33±5.77 | 6.67±5.77 | 6.67±11.55 |
| ATRA 0.625 μg·L-1 | 0.00±0.00 | 6.67±11.55 | 0.00±0.00 |
| ATRA 1.25 μg·L-1 | 6.67±5.77 | 3.33±5.77 | 0.00±0.00 |
| ATRA 2.5 μg·L-1 | 10.00±0.00 | 13.33±5.77 | 3.33±5.77 |
| ATRA 5.0 μg·L-1 | 6.67±5.77 | 6.67±5.77 | 10.00±17.32 |
| ATRA 7.5 μg·L-1 | 3.33±5.77 | 26.67±5.77 | 0.00±0.00 |
| ATRA 10 μg·L-1 | 3.33±5.77 | 73.33±15.28** | 0.00±0.00 |
| **P < 0.01 vs DMSO | |||
空白对照组、溶剂对照组和阴性药物组存活幼鱼均能自由游动; ATRA给药组存活幼鱼,低浓度下仅部分个体游动迟缓,随浓度增加,游动能力逐渐丧失至无法正常游动。观察时间和换液频率对存活幼鱼自主活动的影响不明显。
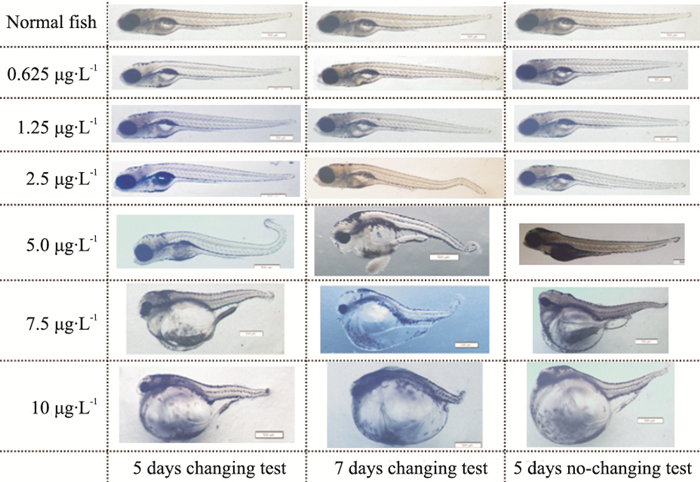
2.3 对形态发育的影响3种实验方法中,空白对照组、溶剂对照组和阴性药物组存活斑马鱼无明显畸形,仅见阴性药物组个别斑马鱼的体形、尾部、胸鳍、心出现发育延迟; ATRA经梯度浓度暴露后,呈现明显的正相关剂量-效应关系。如Fig 1所示,在给药5 d换液实验中,0.625、1.25、2.5 μg·L-1组斑马鱼仅鳍条有轻微的边缘不规则,尾部轻微弯曲,头部形态轻微异常,如脑部比例的微小变化; 5.0 μg·L-1组脊索和体节不规则,靠近尾部的体节发育受阻,尾部严重弯曲,鳍条发育不全,头部嗅区发育受阻,脑部发育尺寸异常,心脏、肝脏部位发育异常,鳔发育不全或不充气,个别个体出现水肿; 7.5、10 μg·L-1组严重畸形,水肿严重,脊索和体节不规则、不明晰,部分体节缺失,尾部扭曲,鳍条发育不全,两侧胸鳍严重异常、变小、不规则,眼睛小,上下颚、嗅区、耳蜗、脑部严重变形,各部位尺寸和比例失调,心脏、肝脏部位难以辨清,10 μg·L-1组比7.5 μg·L-1组畸形程度略严重。延长观察时间后,5.0、7.5、10 μg·L-1组部分个体腹部或尾部出现异常增生,7.5、10 μg·L-1组水肿程度略加重,总体评分可见2.5、5.0 μg·L-1组评分降低。不换液实验中,可见各组畸形程度略轻,5.0、7.5 μg·L-1组总体评分有所升高。评分结果见Tab 2。
|
| Fig 1 Development of zebrafish in ATRA treated groups |
| Group | 5 d changing | 7 d changing | 5 d no-changing |
| Control | 5.0±0.0 | 5.0±0.0 | 5.0±0.0 |
| DMSO | 5.0±0.0 | 5.0±0.0 | 5.0±0.0 |
| AA | 5.0±0.0 | 5.0±0.0 | 5.0±0.0 |
| ATRA 0.625 μg·L-1 | 3.0±0.0 | 3.0±0.0 | 3.0±0.0 |
| ATRA 1.25 μg·L-1 | 3.0±0.0 | 3.0±0.0 | 3.0±0.0 |
| ATRA 2.5 μg·L-1 | 3.0±0.0 | 1.7±0.8* | 3.0±0.0 |
| ATRA 5.0 μg·L-1 | 1.2±0.4** | 1.0±0.0** | 1.3±0.5** |
| ATRA 7.5 μg·L-1 | 1.0±0.0** | 1.0±0.0** | 1.2±0.4** |
| ATRA 10 μg·L-1 | 1.0±0.0** | 1.0±0.0** | 1.0±0.0** |
| *P < 0.05, **P < 0.01 vs control, DMSO and AA | |||
空白对照组、溶剂对照组、阴性药物组均有一定数量的椎骨发生钙化,7 d实验的空白对照和溶剂对照组斑马鱼矿化椎骨数较5 d实验有所增加。给药5 d换液与不换液实验中,ATRA各给药组的矿化椎骨数均为零,可见ATRA抑制斑马鱼的骨骼钙化,但未能体现剂量效应; 在7 d换液实验中,ATRA 0.625、1.25 μg·L-1给药组幼鱼出现少量矿化椎骨,呈现一定的剂量-效应关系。见Tab 3。
| Group | 5 d changing | 7 d changing | 5 d no-changing |
| Control | 1.2±1.5 | 2.7±0.5 | 0.7±1.2 |
| DMSO | 0.8±1.0 | 2.5±1.9 | 0.7±1.2 |
| AA | 2.0±0.9 | 1.7±1.0 | 1.8±0.8 |
| ATRA 0.625 μg·L-1 | 0.0±0.0## | 0.7±1.2 | 0.0±0.0## |
| ATRA 1.25 μg·L-1 | 0.0±0.0## | 0.7±0.8 | 0.0±0.0## |
| ATRA 2.5 μg·L-1 | 0.0±0.0## | 0.0±0.0** | 0.0±0.0## |
| ATRA 5.0 μg·L-1 | 0.0±0.0## | 0.0±0.0** | 0.0±0.0## |
| ATRA 7.5 μg·L-1 | 0.0±0.0## | 0.0±0.0** | 0.0±0.0## |
| ATRA 10 μg·L-1 | 0.0±0.0## | 0.0±0.0** | 0.0±0.0## |
| **P < 0.01 vs control; ##P < 0.01 vs AA | |||
斑马鱼作为新的模型动物,具有周期短、投入少等诸多优势,但较大鼠、小鼠、家兔等成熟动物模型,还有很多不确定因素需要摸索和探讨。斑马鱼受精卵48~72 h即可孵化成鱼,但刚孵出的幼鱼器官发育尚不完全成形、游动能力低,不利于发育评价和自主活动的观察。因此,本实验基础染毒周期和观察时间定为受精后1~5 d,覆盖胚胎早期发育和各器官形成期; 并在5 d染毒实验的基础上,对斑马鱼模型的观察终点和染毒频率进行探讨性研究。
在染毒5 d后延长观察2 d的实验中,斑马鱼死亡率较5 d实验升高、形态发育畸形程度加重,可见毒性作用的延迟表达。5.0 μg·L-1染毒浓度下,ATRA对斑马鱼的致畸程度已与5 d实验中7.5 μg·L-1基本一致,两组总体评分相同,可见适当延后观察终点会使评价物的毒性剂量降低、毒性等级升高,对被检物的安全性判定更加谨慎,同时也趋向保守。另外由骨骼发育结果可知,5 d染毒实验虽然可呈现ATRA对椎骨矿化的抑制,但由于对照组的矿化椎骨数即较少,并无剂量-效应关系,受骨骼发育阶段的影响较大; 将观察时间适当延长后,可显示不同给药量下的剂量-效应关系,能更好地呈现药物对骨骼发育的影响,因此在需要观察骨骼发育情况的评价研究中,观察终点的适当延后更加必要。
在染毒5 d不换液实验中,两个对照组的死亡率较换液实验略偏高,可见换液频率对斑马鱼的发育质量有一定的影响。同时各对照组的死亡率皆不超过10%,从一个侧面说明斑马鱼对培育环境要求较低,使斑马鱼模型的广泛推广应用成为可能。该实验ATRA染毒斑马鱼死亡率较换液实验偏低、形态发育畸形程度减弱、明显致畸剂量升高(10 μg·L-1),可见药物毒性作用表达不充分。同时,对照组死亡率偏高,又降低了毒性作用的检出概率,使被检物的毒性判定较实际偏低,增加了药物研发的风险。
综上所述,使用斑马模型进行药物毒性的早期筛选时,在染毒时间贯穿胚胎发育全程、规律重复染毒的基础上,适当增加观察时间有利于毒性作用的充分表达,尤其在需要进行骨骼发育评价时变得更加必要。但延长观察时间可能使毒性剂量/浓度降低、毒作用增强,使检测结果趋向保守,在药物研发过程中对预期前景的瞻望应考虑该因素的影响。
( 致谢: 本实验在山东省科学院生物研究所药物筛选技术重点实验室完成,感谢张云、何秋霞等老师的指导和帮助! )
| [1] |
许冰洁, 张立将, 李春启, 等. 斑马鱼胚胎评价5种药物的发育毒性与模型验证[J]. 中国药理学通报, 2016, 32(1): 74-9. Xu B J, Zhang L J, Li C Q, et al. Model validation and evaluation of developmental toxicity of five drugs using zebrafish embryos[J]. Chin Pharmacol Bull, 2016, 32(1): 74-9. doi:10.3969/j.issn.1001-1978.2016.01.016 |
| [2] |
吴玉琼, 陈莹, 胡永乐, 等. 四种新型农药对斑马鱼胚胎发育的毒性效应[J]. 生物技术通报, 2017, 33(6): 155-61. Wu Y Q, Chen Y, Hu Y L, et al. Toxic effects of four currently-used pesticides on zebrafish embryonic development[J]. Biotechnol Bull, 2017, 33(6): 155-61. |
| [3] |
Huang D, Li H, He Q, et al. Developmental toxicity of diethylnitrosamine in zebrafish embryos/ Juveniles related to excessive oxidative stress[J]. Water Air Soil Pollut, 2018, 229(3): 81-91. doi:10.1007/s11270-018-3739-8 |
| [4] |
陈颖, 王茉, 宋捷, 等. 补骨脂水煎液和醇提物对斑马鱼骨骼发育的影响及其毒性作用[J]. 中国药理学与毒理学杂志, 2017, 31(6): 661-9. Chen Y, Wang M, Song J, et al. Effect of extract ethanol and water decoction of Psoralea corylifolia L. on bone development and their toxicities in zebrafish[J]. Chin J Pharm Toxicol, 2017, 31(6): 661-9. doi:10.3867/j.issn.1000-3002.2017.06.024 |
| [5] |
陈锡强, 王荣春, 王希敏, 等. 斑马鱼皮肤损伤模型的建立及分子机制[J]. 中国药理学通报, 2018, 34(3): 433-7. Chen X Q, Wang R C, Wang X M, et al. Model establishment of skin damage and molecular mechanism on transgenic zebrafish embryos[J]. Chin Pharmacol Bull, 2018, 34(3): 433-7. doi:10.3969/j.issn.1001-1978.2018.03.026 |
| [6] |
Brannen K C, Panzica-Kelly J M, Danberry T L, et al. Development of a zebrafish embryo teratogenicity assay and quantitative prediction model[J]. Birth Defects Res B Dev Reprod Toxicol, 2010, 89(1): 66-77. doi:10.1002/bdrb.v89:1 |

