

慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)是以持续性气流受限为特征的,可以预防和治疗的疾病。COPD患者由于长期缺氧及CO2潴留,肺血管重构,右心室肥厚,甚至导致右心衰竭和死亡。因此,阐明COPD合并肺动脉高压(pulmonary arterial hypertension, PAH)的分子机制,实行尽快、尽早的干预,对减少呼吸衰竭、循环衰竭的发生,提高病人的生活质量具有现实的意义。近年来研究表明,缺氧诱导因子-1α(hypoxia inducible-factor-1α, HIF-1α)、内皮素-1(endothelin-1, ET-1)等生物活性物质与PAH的发生、发展密切相关[1-2]。研究发现,法舒地尔对PAH有保护作用,可以改善肺动脉重构,延缓疾病进展,具体机制尚不明确[3-5]。本研究主要观察法舒地尔对COPD合并PAH大鼠肺血管和血浆中HIF-1α、ET-1水平的影响,旨在探究其参与COPD合并PAH的作用机制。
1 材料与方法 1.1 材料 1.1.1 实验动物与分组清洁级健康SD成年♂大鼠50只,体质量(220±20)g,由安徽医科大学实验动物中心提供,许可证号:SCXK2011002。大鼠按照随机数字表法分为5组,即正常组、模型组、法舒地尔组(10、20、30 mg·kg-1),每组10只。
1.1.2 试剂脂多糖(批号L2880,美国Sigma公司); 法舒地尔(批号H20040356,2 mL,30 mg,天津红日药业有限公司); 红三环香烟(安徽中烟工业有限责任公司); Rho相关激酶1(Rho-associated kinase 1, ROCK1)单克隆抗体(批号ab45171,美国Abcam公司); 肌球蛋白磷酸酶靶蛋白1(myosine phosphatae targeting subunit 1, MYPT1)一抗(货号2634)、p-MYPT1一抗(货号4563),均购自美国CST公司; GAPDH一抗(北京博奥森生物有限公司); 大鼠HIF-1α及ET-1 ELISA检测试剂盒(武汉华美生物工程有限公司)。
1.1.3 仪器YCP-160D型常压低氧装置(长沙华曦电子科技有限公司); 自制烟熏箱(60 cm×80 cm×80 cm); PowerLab数据采集系统(澳大利亚AD公司)。
1.2 方法 1.2.1 动物模型的制备参照文献[6-7]制备COPD合并PAH大鼠模型。模型制备前,大鼠适应性饲养1周,模型组和法舒地尔组于d 1和d 15水合氯醛麻醉后,气管内滴注脂多糖200 μL(1 g·L-1),正常组注入等量的生理盐水之后,放回原饲养笼进食进水。模型组和法舒地尔组分别于d 2~14和d 16~42,每日上午将大鼠置于自制有机玻璃箱内香烟烟雾暴露2次,每次1 h,每次点燃10只卷烟。烟熏后,将大鼠放置在常压低氧装置中,保持室内氧浓度10%,每天7~8 h。4周后,法舒地尔组腹腔注射法舒地尔(10、20、30 mg·kg-1),正常组及模型组腹腔注射同等剂量的生理盐水。至6周末,处死大鼠。
1.2.2 一般情况的观察观察大鼠的饮食、毛发、体质量、活动量等变化。
1.2.3 右心室压力的检测和血浆的制备大鼠处死前,腹腔注射10%水合氯醛(3 mg·kg-1)麻醉,备皮,暴露颈外静脉,使用PE50管,通过右心导管法经颈外静脉测定右心室压力[8]。测量结束后,通过导管心脏取血,肝素抗凝,离心取上清液,分装于EP管中,-80 ℃超低温冰箱中保存,用于ELISA检测。
1.2.4 右心肥厚指数的测定放血处死大鼠,分离大鼠的心脏,生理盐水冲洗心脏。剪去左右心房及血管组织,然后沿室间隔剪下右心室,用滤纸吸干多余水分,使用电子天平分别称取右心室(right ventricle, RV)及左心室加室间隔重量(LV+S),以[RV/(LV+S)]作为右心肥厚指数。
1.2.5 肺组织病理标本的制备与分析解剖大鼠,剪取右外下肺叶,将组织置于4%多聚甲醛缓冲液固定、脱水、透明、石蜡包埋,制备肺组织标本。HE染色,显微镜下观察肺组织病理学改变。
1.2.6 大鼠血浆中HIF-1α、ET-1的检测按照说明书操作步骤进行,标本重复测定3次。
1.2.7 免疫组化法检测肺组织ROCK1的表达处死大鼠后,将大鼠左肺组织保存在4%多聚甲醛中,固定24 h,常规石蜡包埋,切片,脱蜡,加入ROCK1单克隆抗体4 ℃过夜,次日加二抗,37 ℃孵育20 min,显色、复染、脱水、透明、封片,高倍镜下观察,阳性颗粒呈棕黄色。
1.2.8 Western blot法测定肺组织ROCK1、MYPT1、p-MYPT1表达量提取肺组织总蛋白,加入上样缓冲液煮沸变性。SDS-PAGE电泳,转移到PVDF膜上,室温封闭2 h,TBST洗膜3次,加入一抗ROCK1(1 :5 000)、MYPT1(1 :1 000)、p-MYPT1(1 :1 000)、GAPDH(1 :2 000),4 ℃孵育过夜。次日加二抗(1 :2 000)室温孵育1 h,洗膜3次,ECL化学发光显影。在Tanon全自动凝胶成像系统中自动曝光,采集图像,采用Imaging J 1.38e图像分析软件进行条带光密度分析。以目的蛋白与GAPDH蛋白灰度值比值表示目的蛋白的相对表达量。
1.3 统计学分析采用SPSS 16.0统计学分析软件,正态分布的计量资料用x±s表示,组间比较采用单因素方差分析。
2 结果 2.1 大鼠的一般情况正常组大鼠活动敏捷,应激能力强,食欲良好,毛发光滑; 模型组大鼠活动量明显减少,行动缓慢,应激能力减弱,食欲明显减退,偶可闻及痰鸣音; 不同剂量组法舒地尔组大鼠较模型组食欲有所好转,活动耐量升高。
2.2 法舒地尔对COPD合并PAH大鼠体质量的影响Tab 1的结果显示,实验开始前,大鼠体质量差异无统计学意义(P>0.05);实验结束时,与正常组相比,模型组大鼠体质量明显减轻(P < 0.01);与模型组相比,法舒地尔组体质量均明显升高(P < 0.05),不同剂量法舒地尔组间体质量差异无统计学意义。
| Group | Dose /mg·kg-1 |
Weight baseline/g | Weight afterexperiment/g |
| Control | - | 229.00±14.00 | 364.70±21.20 |
| Model | - | 227.30±16.96 | 254.50±22.40** |
| Fasudil | 10 | 223.50±14.57 | 294.60±19.29# |
| 20 | 227.10±16.13 | 302.10±27.05# | |
| 30 | 224.40±15.46 | 308.10±25.90# | |
| **P <0.01 vs control group; #P < 0.05 vs model group | |||
Tab 2结果显示,与正常组相比,模型组右心室收缩压力、右心肥厚指数明显升高(P < 0.01);与模型组相比,法舒地尔组右心室收缩压、右心肥厚指数均明显降低(P < 0.05);不同剂量法舒地尔组间右心室收缩压力、右心肥厚指数差异无统计学意义。
| Group | Dose /mg·kg-1 |
RVSP /kPa |
RVHI |
| Control | - | 17.55±1.71 | 0.27±0.02 |
| Model | - | 32.88±5.19** | 0.48±0.07** |
| Fasudil | 10 | 27.88±4.03# | 0.39±0.07# |
| 20 | 25.49±4.36# | 0.36±0.07# | |
| 30 | 23.67±4.38# | 0.31±0.04# | |
| **P < 0.01 vs control group; #P < 0.05 vs model group | |||
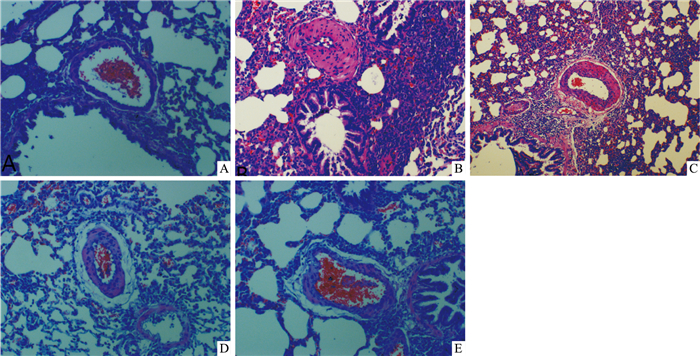
如Fig 1所示,正常组仅见少许炎性细胞浸润,气道结构正常,周围血管壁及肺泡壁结构正常。模型组可见肺气肿形成,大量炎性细胞浸润,内外弹力纤维层距离增宽,平滑肌细胞增殖明显,管腔近于闭塞,肺泡壁结构破坏。不同剂量组法舒地尔组肺结构破坏较模型组好转,炎症细胞减少,肺血管重构减轻。
|
| Fig 1 HE staining pulmonary arterioles(×200) A: Control; B: Model; C: Fasudil 10 mg·kg-1; D: Fasudil 20 mg·kg-1; E: Fasudil 30 mg·kg-1. |
Tab 3结果显示,与正常组相比,模型组HIF-1α、ET-1水平明显升高(P < 0.01);与模型组相比,法舒地尔组HIF-1α、ET-1水平明显降低(P < 0.05);不同剂量法舒地尔组间血浆HIF-1α、ET-1含量差异无统计学意义(P>0.05)。
| Group | Dose /mg·kg-1 |
HIF-1α /ng·L-1 |
ET-1 /ng·L-1 |
| Control | - | 4.015±1.013 | 45.657±6.960 |
| Model | - | 8.227±1.434** | 104.691±29.838** |
| Fasudil | 10 | 7.096±1.785 | 83.891±15.043# |
| 20 | 6.010±1.442# | 72.741±14.180# | |
| 30 | 5.536±1.091# | 67.527±13.139# | |
| **P < 0.01 vs control group; #P < 0.05 vs model group | |||
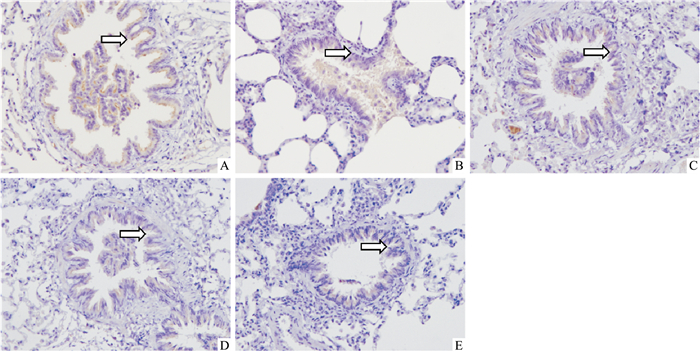
Fig 2肺组织切片免疫组化染色显示,棕褐色颗粒主要位于肺组织支气管肺泡上皮及肺动脉内皮细胞质膜上,正常组仅见少许阳性表达棕褐色颗粒,模型组大鼠肺组织可见大量棕褐色颗粒,法舒地尔组棕褐色颗粒明显减少。结果表明,与模型组相比,正常组和法舒地尔组ROCK1表达明显降低。
|
| Fig 2 Effects of fasudil on ROCK-1 expression determined by immunohistochemical staining (×200) A: Control; B: Model; C: Fasudil 10 mg·kg-1; D: Fasudil 20 mg·kg-1; E: Fasudil 30 mg·kg-1. |
Fig 3的Western blot结果显示,与正常组相比,模型组ROCK1、p-MYPT1表达增加(P < 0.01);与模型组相比,法舒地尔组ROCK1、p-MYPT1表达下降(P < 0.05);不同剂量法舒地尔组间ROCK1、p-MYPT1表达差异无统计学意义(P>0.05)。

|
| Fig 3 Effects of fasudil on ROCK1 and p-MYPT1 expression determined by Western blot(x±s, n=3) **P < 0.01 vs control group; #P < 0.05 vs model group |
目前,对于COPD合并PAH大鼠模型的建立缺乏统一的标准,宋一平等[6]采用烟熏联合脂多糖的方法,成功复制大鼠COPD模型,该复合方法是目前最常用的制备COPD模型的方法。本研究参照其造模方法,模型建成后,大鼠出现呼吸急促、反应迟钝、精神萎靡、毛发稀少、食量明显减少。肺组织病理提示大量炎性细胞浸润,肺大泡形成,肺组织结构明显破坏,肺血管重构。右心室心腔扩大,收缩压增大,提示模型复制成功。
研究发现,Rho激酶信号通路与肺血管收缩、肺血管重构有关。Rho蛋白是具有信息传导和分子开关功能的信号多肽,通过调节细胞内肌动蛋白骨架的聚合状态,参与多种生物行为,主要包括细胞黏附与迁移、平滑肌收缩、细胞增殖与凋亡等。Rho激酶信号通路的关键信号分子包括Rho蛋白、Rho激酶和肌球蛋白磷酸酶等。Rho激酶属于丝氨酸/苏氨酸蛋白激酶家族成员,以2种高度同源性的异构体形式存在(ROCK1、ROCK2)。ROCK是Rho下游的重要效应分子,活化的ROCK一方面磷酸化其底物肌球蛋白轻链磷酸酶(myosin light chain phosphatase,MLCP)的调节亚单位MYPT1,抑制MLCP的磷酸酶活性,减少MLC磷酸化基团的水解,因此p-MYPT1的表达水平是反映ROCK活性的重要标志; 另一方面,活化的ROCK可直接磷酸化MLC,增加MLC的磷酸化水平,从而促进肌动蛋白微丝骨架的聚合,影响细胞的收缩、黏附、增殖、凋亡、迁移等生物学行为和功能。Rho激酶抑制剂法舒地尔可渗透到血管平滑肌细胞,在正常或病理情况下,均与ATP竞争Rho激酶催化区的ATP结合位点,特异性阻断Rho激酶活性,剂量依赖性减弱以肌动蛋白为基础的平滑肌细胞收缩反应。临床上,法舒地尔用药方法主要是静脉滴注,但本研究中采用的方法是腹腔注射,主要是因为大鼠的顺从性差,静脉穿刺难度系数大,持续静脉滴注难以实现。另外,法舒地尔半衰期短,直接静脉注射作用持续时间短,需反复多次给药。本研究结果表明,与对照组大鼠相比,模型组大鼠肺小动脉内膜增厚,管腔明显狭窄甚至闭塞,右心室收缩压力升高,肺血管重构,肺组织ROCK1、p-MYPT1蛋白表达明显升高。法舒地尔组大鼠肺血管重构明显减轻,ROCK1、p-MYPT1蛋白表达较模型组明显下降,肺动脉压力降低,右心室肥厚减轻,提示Rho激酶信号通路与COPD合并PAH有关,与既往的研究结果一致。且随着法舒地尔用量的增加,表达均呈现下降的趋势,但无明显统计学意义,考虑可能与用药剂量间隔偏小、用药时间较短、实验误差等因素有关。
HIF是在缺氧诱导的细胞核抽提物中发现的一种DNA结合蛋白,是低氧情况下诱发的最直接的调控因子[9-10]。HIF-1α亚单位为HIF-1独有,为氧感应元件,在常氧状态下,其几乎不表达; 缺氧状态下,HIF-1α聚集并转移至细胞核,与核内HIF-1β形成聚合体,继而激活靶基因转录,从而组织细胞发生血管新生、重建、细胞增殖等一系列的耐氧适应性分子反应。ET-1主要由血管内皮产生, 具有强烈的缩血管作用,对维持血管内皮的平衡起重要的作用。ET-1主要通过下游的两个G蛋白偶联受体起作用,ETα和ETβ[11-12]。选择性的ET-α受体拮抗剂与非选择性的内皮素受体拮抗剂在PAH的治疗中均有效。既往研究发现,Rho激酶抑制剂法舒地尔可以降低野百合碱和低氧诱导PAH大鼠HIF-1α、ET-1的水平,但是在COPD合并低氧所致PAH大鼠中是否存在相同的作用,相关报道较少。本研究发现,模型组HIF-1α、ET-1明显升高,提示HIF-1α、ET-1参与了COPD合并低氧诱导的PAH的病理生理过程。可能是因为缺氧状态下HIF-1α表达升高,调节ET-1基因的表达,引起ET-1分泌增多,内皮舒张因子与收缩因子的平衡调节受到破坏,导致肺血管收缩,加重肺血管重构[13]。应用Rho激酶抑制剂法舒地尔后,肺组织炎症明显好转,肺动脉高压、心室肥厚明显降低,大鼠血浆HIF-1α、ET-1水平降低,且HIF-1α、ET-1水平随法舒地尔剂量的升高而呈逐渐下降的趋势,提示Rho激酶信号通路参与HIF-1α、ET-1所致的COPD合并PAH。因此,阻断Rho激酶信号有望阻断HIF-1α、ET-1作用通路,但其具体机制有待于进一步探究。
本实验通过大鼠COPD合并PAH模型的建立,检测各组大鼠RVSP、RV/(LV+S)、肺组织ROCK1、p-MYPT1以及血浆HIF-1α、ET-1水平的变化,验证了Rho激酶信号通路在PAH过程中表达的规律,同时发现法舒地尔可以降低血浆中HIF-1α、ET-1水平,为临床COPD合并PAH的诊治提供了理论基础。
( 致谢: 感谢安徽医科大学第二附属医院中心实验室为本课题研究提供仪器设备和技术支持。)
| [1] | 吕倩, 王昌明, 蒋明, 等. HIF-1α和VEGF在大鼠COPD中的表达及与肺血管重构的关系研究[J]. 中国药理学通报, 2012, 28(6): 772-7. Lyu Q, Wang C M, Jiang M, et al. Correlation between the expression of HIF-1α, VEGF and pulmonary remodeling in rat with COPD[J]. Chin Phamacol Bull, 2012, 28(6): 772-7. doi:10.3969/j.issn.1001-1978.2012.06.010 |
| [2] | 敖启林, 郝春荣, 熊密, 王迪浔. 低氧诱导因子-1α和内皮素-1基因在大鼠低氧性肺动脉高压中的表达[J]. 中国病理学杂志, 2002, 31(3): 140-2. Ao Q L, Hao C R, Xiong M, Wang D X. Expression of hypoxia-inducible factor-1α and endothelin-1 gene in hypoxic pulmonary hypertension[J]. Chin J Pathol, 2002, 31(3): 140-2. |
| [3] | Sun X Z, Tian X Y, Wang D W, Li J. Effects of fasudil on hypoxic pulmonary hypertension and pulmonary vascular remodeling in rats[J]. Eur Rev Med Pharmacol Sci, 2014, 18: 959-64. |
| [4] | 李明星, 王勇, 蒋德旗, 等. 参与肺动脉平滑肌细胞增殖信号转导机制及信号转导抑制剂的研究进展[J]. 中国药理学通报, 2015, 31(5): 605-10. Li M X, Wang Y, Jiang D Q, et al. Advances in research on signal transduction mechanisms and their inhibitors for the proliferation of pulmonary artery smooth muscle cells[J]. Chin Pharmacol Bull, 2015, 31(5): 605-10. doi:10.3969/j.issn.1001-1978.2015.05.004 |
| [5] | Liu P, Zhang H M, Tang Y J, et al. Influence of Rho kinase inhibitor fasudil on late endothelial progenitor cells in peripheral blood of COPD patients with pulmonary artery hypertension[J]. Bratisl Lek Listy, 2015, 116(3): 150-3. |
| [6] | 宋一平, 崔德健, 茅培英. 慢性阻塞性肺病大鼠模型的建立及药物干预的影响[J]. 中华内科杂志, 2000, 39(8): 556-7. Song Y P, Cui D J, Mao P Y. A new way of establishing a rat chronic obstructive pulmonary disease model and the effects of drugs on them[J]. Chin J Intern Med, 2000, 39(8): 556-7. doi:10.3760/j.issn:0578-1426.2000.08.019 |
| [7] | 王昌明, 蒋明, 谭宁, 等. NF-κB表达水平与大鼠慢性阻塞性肺疾病气道、肺血管重构的相关性[J]. 中国药理学通报, 2010, 26(11): 1495-500. Wang C M, Jiang M, Tan N, et al. The correlation between the expression of NF-κB and the airway remodeling, pulmonary vascular reconstruction in rats with chronic obstructive pulmonary disease[J]. Chin Pharmacol Bull, 2010, 26(11): 1495-500. |
| [8] | 陈传斯, 庞玉生, 马建法, 等. 右心导管法测大鼠肺动脉压力的改良[J]. 现代生物医学进展, 2014, 14(15): 2863-6. Chen C S, Pang Y S, Ma J F, et al. The improvement of right heart catheterization method to measure pulmonary artery pressure in rats[J]. Prog Mod Biomed, 2014, 14(15): 2863-6. |
| [9] | 邓鋆, 张旭, 喻珊珊. HIF-1α和HIF-2α在低氧性肺动脉高压中的不同作用研究进展[J]. 中国药理学通报, 2017, 33(1): 10-3. Deng J, Zhang X, Yu S S. Advances in differential roles of HIF-1α and HIF-2α in the pathogenesis of hypoxic pulmonary hypertension[J]. Chin Pharmacol Bull, 2017, 33(1): 10-3. doi:10.3969/j.issn.1001-1978.2017.01.002 |
| [10] | Semenza G L, Wang G L. A nuclear factor induced by hypoxia via de novo protein synthesis binds to the human erythropoietin gene enhancer at a site required for transcriptional activation[J]. Mol Cell Boil, 1992, 12(12): 5447-54. doi:10.1128/MCB.12.12.5447 |
| [11] | Galie N, Manes A, Branzi A. The endothelin system in pulmonary arterial hypertension[J]. Cardiovasc Res, 2004, 61: 227-37. doi:10.1016/j.cardiores.2003.11.026 |
| [12] | Homma N, Nagaoka T, Morio Y, et al. Endothelin-1 and serotonin are involved in activation of RhoA/Rho kinase signaling in the chronically hypoxic hypertensive rat pulmonary circulation[J]. J Cardiovasc Pharmacol, 2007, 50(6): 697-702. doi:10.1097/FJC.0b013e3181593774 |
| [13] | Wang L, Zhou Y, Li M X, et al. Expression of hypoxia-inducible factor-1α, endothelin-1 and adrenomedullin in newborn rats with hypoxia-induced pulmonary hypertension[J]. Exp Ther Med, 2014, 8(1): 335-9. doi:10.3892/etm.2014.1728 |

