


线粒体是细胞内能量代谢的枢纽,在细胞的生理过程中起着极其重要的作用,线粒体最主要的功能是进行氧化磷酸化合成腺嘌呤核苷三磷酸(adenosine triphosphate,ATP),为细胞生命活动提供能量[1]。线粒体与人体疾病、衰老和细胞凋亡有关。线粒体的生物合成及功能障碍会影响整个细胞的正常功能,从而导致病变[2-3]。
1-甲基-4-苯基-1, 2, 3, 6-四氢吡啶(1-methyl-4-phenyl-1, 2, 3, 6-tetrahydropyridine,MPTP)是一种能够影响细胞内能量消耗和自由基产生的神经毒素,常用于制备帕金森病动物模型。1-甲基-4-苯基吡啶离子(1-methyl-4-phenylpyridinum ion,MPP+)是MPTP在单胺氧化酶作用下产生的活性代谢产物。MPP+通过多巴胺转运体被选择性摄取到多巴胺神经元内,通过氧化应激和损伤线粒体两种方式导致细胞死亡[4-5]。
丹酚酸D(salvianolic acid D,SalD)是中药丹参中提取的水溶性成分,具有抗衰老、抗炎、抗氧化,以及神经保护等作用[6-7],其结构见Fig 1A。SalD是否能够调节神经细胞线粒体功能和生物合成尚未见报道。因此,本实验建立MPP+损伤SH-SY5Y细胞模型,探讨SalD对MPP+损伤SH-SY5Y细胞线粒体功能和生物合成的作用及机制。
|
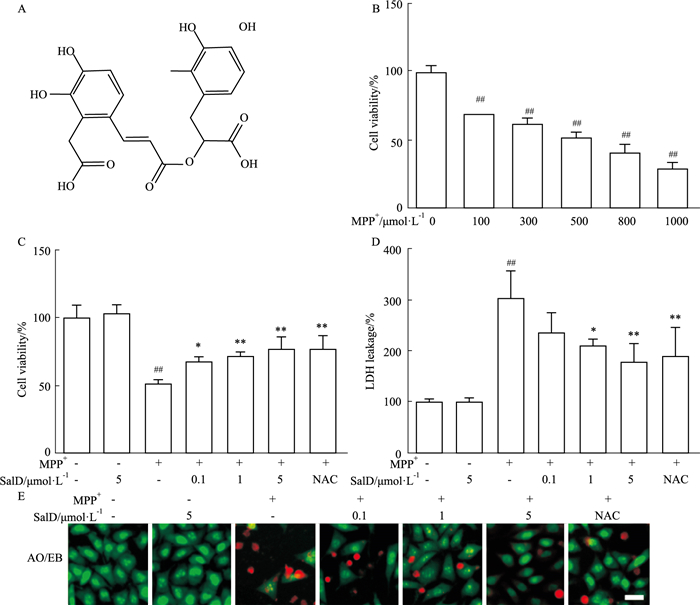
| Fig 1 Effect of SalD and MPP+ on SH-SY5Y cell viability (x±s, n=4) A: The chemical structure of SalD; B: The SH-SY5Y cell viability after treated with different concentrations of MPP+ for 24 h; C: The cell viability was determined using MTT assay; D: The LDH release was detected by the LDH cytotoxicity assay kit; E: The cell apoptosis was monitored using AO/EB staining (scale bar=20 μm). ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs MPP+ group. |
DMEM/F12培养基、胎牛血清、线粒体荧光探针MitoSOX、DCFH-DA、Alexa Fluor 488标记的二抗、TRIzol,均购自Thermo Scientific;N-乙酰半胱氨酸(N-acetyl-L-cysteine,NAC)、MPP+、Hoechst 33258和MTT均购自Sigma;乳酸脱氢酶(lactate dehydrogenase,LDH)细胞毒性检测试剂盒、ATP检测试剂盒、线粒体膜电位检测试剂盒(JC-1),均购自碧云天生物技术公司;Top Green qPCR SuperMix、全基因组DNA提取试剂盒,购自北京全式金生物公司;蛋白裂解液、β-actin抗体均购自Cell Signaling Technology;过氧化物酶体增殖物激活受体γ辅激因子1α(peroxisome proliferator activated receptor-γ coactivator-1α,PGC-1α)、核因子NF-E2相关因子1(nuclear factor erythroid-2-related factor 1,NRF1)、线粒体转录因子A(mitochondrial transcription factor A,TFAM)抗体,均购自Abcam;吖啶橙/溴化乙锭(acridine orange/ethidium bromide,AO/EB)双染试剂盒购自索莱宝。
1.2 仪器SpectraMax M5酶标仪(美国Molecular Devices);蛋白电泳仪、转膜仪、PCR扩增仪、Molecular Imager ChemiDoc XRS+System成像仪(美国Bio-Rad);ArrayScan Infinity高内涵分析仪(美国Thermo Scientific)。
1.3 细胞培养人神经母细胞瘤细胞SH-SY5Y购自中国医学科学院基础医学研究所。SH-SY5Y细胞用含10%胎牛血清的DMEM/F12培养液,37℃、5% CO2饱和湿度培养,细胞处于对数生长期时用于实验。
1.4 MPP+模型建立及分组细胞处于对数生长期时,以完全培养基接种于96孔板。分为正常对照组、MPP+损伤模型组、SalD低剂量组(MPP+ + 0.1 μmol·L-1 SalD)、SalD中剂量组(MPP+ + 1 μmol·L-1 SalD)、SalD高剂量组(MPP+ + 5 μmol·L-1 SalD)和阳性药组(MPP+ + 5 mmol·L-1 NAC)。
1.5 MTT法检测细胞存活率正常组始终使用完全培养基在常氧培养箱孵育24 h。加药组给予不同浓度的SalD或NAC预孵育2 h,之后损伤组加入500 μmol·L-1 MPP+,孵育24 h后,吸除原培养液,每孔加入100 μL 0.5 g·L-1 MTT溶液,37℃培养4 h,吸除MTT溶液,每孔加入100 μL二甲基亚砜振荡溶解结晶,用酶标仪在490 nm处测定吸光度。
1.6 LDH释放率考察细胞活力到达实验终点前1 h,在正常对照组中加入LDH释放试剂,吹打混匀,继续培养。1 h后,将细胞培养板400×g离心5 min。取各孔上清液120 μL,加入新的96孔板中,之后各孔分别加入60 μL LDH检测工作液,混匀,室温避光孵育30 min后,在490 nm处测定吸光度。
1.7 AO/EB染色检测细胞凋亡实验终点,吸弃细胞培养液,每孔加入100 μL磷酸缓冲盐溶液(phosphate buffer saline,PBS)洗涤2次,之后加入100 μL AO/EB染色工作液,室温静置2 min,于高内涵细胞分析系统进行检测。
1.8 活性氧(reactive oxygen species,ROS)的检测分别以MitoSOX和DCFH-DA检测SH-SY5Y线粒体超氧化物及细胞内ROS水平。实验终点,倾去细胞培养液,PBS洗涤细胞1次,每孔加入50 μL含有5 μmol·L-1 MitoSOX或10 μmol·L-1 DCFH-DA及10 mg·L-1 Hoechst 33258的培养基,37 ℃避光孵育30 min。PBS洗涤3次后进行检测。
1.9 线粒体膜电位JC-1的测定采用JC-1为荧光探针,检测线粒体膜电位的变化。在线粒体膜电位较高时,JC-1聚集在线粒体基质中,形成聚合物而产生红色荧光;线粒体膜电位较低时,JC-1以单体形式存在,发绿色荧光。通过JC-1从红色荧光到绿色荧光的转变反映线粒体膜电位的下降。具体方法如下:实验终点,倾去细胞培养液,用PBS溶液洗涤细胞1次,每孔加入50 μL含有1 × JC-1染色工作液及10 mg·L-1 Hoechst 33258的培养基,37 ℃孵育30 min。JC-1染色缓冲液洗涤2次。加入100 μL培养基,高内涵细胞分析系统检测。
1.10 细胞内ATP水平的测定实验终点,吸弃培养液,6孔板中每孔加入200 μL裂解液,裂解细胞后,4℃、12 000×g离心5 min,取上清。在新的96孔板中,每孔加入100 μL ATP检测工作液,室温放置5 min,之后加入20 μL样品混匀,用于检测ATP水平的变化。
1.11 qPCR检测蛋白转录水平将生长达90%的细胞置于冰上,弃培养基,PBS液洗3次,加入1 mL TRIzol试剂,反复吹打。将细胞裂解液转移至新的离心管中,室温放置5 min;加入0.2 mL氯仿,剧烈混匀15 s。室温放置3 min,4℃、12 000×g离心15 min。吸取上层水相,转至新的离心管中约0.5 mL,加入0.5 mL异丙醇混匀,室温放置10 min。4 ℃、12 000×g离心10 min,弃去液体,加入75%乙醇1 mL,剧烈混匀。4 ℃、9 000×g离心5 min,吸去液体,干燥,溶于DEPC处理水,得到总RNA。之后逆转录合成cDNA,real-time qPCR进行检测。引物序列见Tab 1。
| Target genes | Forward primers (5′-3′) | Reverse primers (5′-3′) |
| PGC-1α | TCCTCACAGAGACACTAGACA | CTGGTGCCAGTAAGAGCTTCT |
| NRF1 | CTTACAAGGTGGGGGACAGA | GGTGACTGCGCTGTCTGATA |
| TFAM | CCGAGGTGGTTTTCATCTGT | TCCGCCTATAAGCATCTTG |
| β-actin | AAACCCATCACCATCTTCCAG | AGGGGCCATCCACAGTCTTCT |
细胞实验终点时,弃上清,PBS洗涤3次,每皿加入蛋白裂解液100 μL,冰上裂解30 min后,4℃、12 000×g离心10 min,收集上清。依据BCA蛋白定量试剂盒测定各样品蛋白浓度,加入5×上样缓冲液和稀释液,将各组样品稀释至相同浓度,沸水中加热10 min,进行SDS-PAGE凝胶电泳,之后转印至PVDF膜上,5% BSA封闭2 h,稀释后的一抗共孵育,4 ℃过夜;TBST洗涤3次,每次10 min;再与对应的稀释二抗室温孵育2 h,TBST洗涤3次;BeyoECL Plus显色,通过凝胶成像系统捕获并分析图像。
1.13 细胞免疫荧光检测PGC-1α、NRF1和TFAM蛋白水平细胞实验终点,以0.01 mol·L-1的PBS洗3次,4%多聚甲醛固定15 min,0.3% Triton X-100作用10 min将细胞穿孔,再用5% BSA封闭1 h,弃BSA,加入一抗,4℃过夜;PBS洗3次,每次10 min,加入稀释后荧光二抗,37 ℃孵育2 h;弃二抗,PBS洗3次,每次10 min,加入核染料10 min,PBS洗3次,每次10 min,置高内涵细胞分析系统拍照。
1.14 统计学处理结果以x±s表示,对于统计学差异分析,使用GraphPad Prism version 6.0软件中One-way ANOVA(Tukey’s post hoc test)方法进行统计处理。
2 结果 2.1 SalD对MPP+损伤SH-SY5Y细胞活力的影响如Fig 1B所示,不同浓度MPP+处理SH-SY5Y细胞24 h后,细胞存活率随MPP+浓度升高而降低。其中500 μmol·L-1 MPP+作用SH-SY5Y细胞24 h后,模型组细胞活力为正常对照组的51.34%。选择500 μmol·L-1 MPP+作用SH-SY5Y细胞24 h作为后续实验条件。利用MTT及LDH方法考察0.1、1、5 μmol·L-1 SalD对SH-SY5Y细胞活力的影响。如Fig 1C所示,5 μmol·L-1 SalD作用SH-SY5Y细胞24 h,不影响细胞生长。500 μmol·L-1 MPP+明显降低SH-SY5Y细胞存活率,0.1、1、5 μmol·L-1 SalD和5 mmol·L-1 NAC能够减轻MPP+诱导的SH-SY5Y细胞损伤,其细胞存活率分别达到67.98%、71.79%、76.91%和77.55%。
如Fig 1D所示,5 μmol·L-1 SalD作用不影响SH-SY5Y细胞LDH的释放。MPP+能够明显提高LDH释放量,SalD(1、5 μmol·L-1)和阳性药NAC(5 mmol·L-1)能够明显降低MPP+诱导的LDH释放。
AO能够透过胞膜完整的细胞,嵌入细胞核DNA,从而发出绿色荧光。EB仅能透过受损的细胞,发出橘红色荧光。如Fig 1E所示,正常组细胞被染为绿色,MPP+损伤SH-SY5Y细胞处于凋亡状态,呈现橘色荧光。SalD能够减轻MPP+所引起的细胞凋亡。
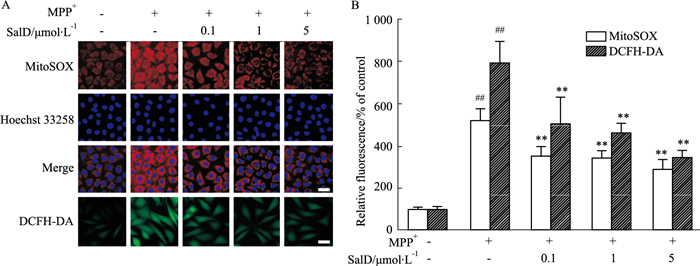
2.2 SalD抑制MPP+诱导的SH-SY5Y细胞ROS和线粒体超氧化物的产生应用MitoSOX和DCFH-DA荧光探针,分别检测MPP+损伤SH-SY5Y细胞后线粒体内超氧化物水平及细胞内ROS生成量。如Fig 2所示,模型组中MitoSOX和DCFH-DA的荧光强度明显高于正常对照组,而SalD(0.1、1、5 μmol·L-1)可以明显降低MitoSOX和DCFH-DA的荧光强度,降低线粒体中超氧化物水平及细胞内ROS的释放。
|
| Fig 2 Effects of SalD on MPP+ induced cellular ROS and mitochondrial superoxide production (x±s, n=4) A: Representative images of MitoSOX-loaded and DCFH-loaded SH-SY5Y cells (scale bar=20 μm); B: Quantitative analysis of the production of MitoSOX and DCFH-DA. ##P < 0.01 vs control group; **P < 0.01 vs MPP+ group. |
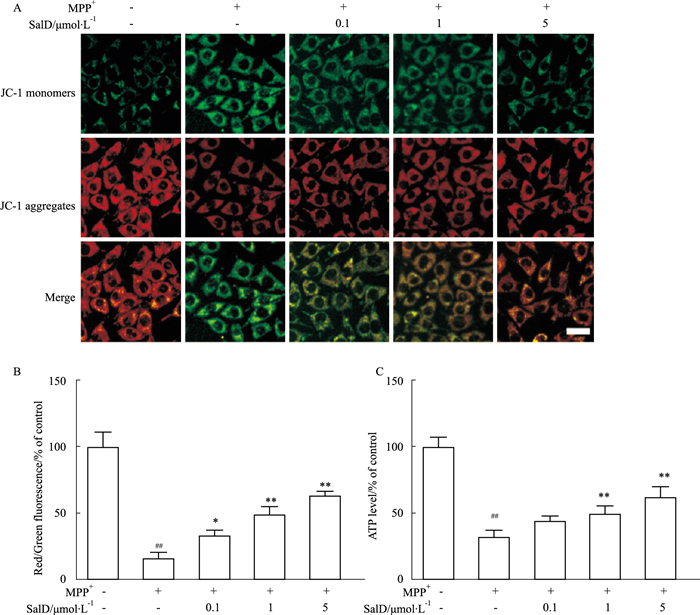
采用膜电位检测试剂JC-1测定SH-SY5Y细胞线粒体膜电位。如Fig 3A、3B所示,与正常对照组相比,MPP+损伤后,SH-SY5Y细胞线粒体由红色荧光转变为绿色荧光,膜电位明显下降。SalD(0.1、1、5 μmol·L-1)可以明显抑制MPP+损伤造成的细胞线粒体膜电位下降。
|
| Fig 3 Mitochondrial function protected by SalD in SH-SY5Y cells(x±s, n=4) A: Representative double immunofluorescent staining for JC-1 (scale bar=20 μm); B: The ratio of red and green fluorescence intensity; C: The ATP levels. ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs MPP+ group. |
ATP水平下降通常与线粒体膜电位下降同时发生,用来表明线粒体功能受损[8-9]。利用ATP检测试剂盒对MPP+诱导的SH-SY5Y细胞中ATP水平变化进行测定。如Fig 3C所示,SalD(1、5 μmol·L-1)能明显增加MPP+损伤下调的ATP水平。
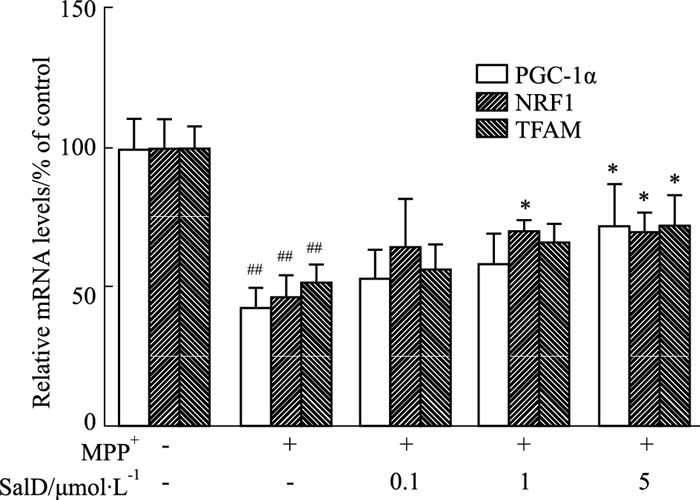
2.4 SalD调节MPP+损伤SH-SY5Y细胞线粒体生物合成相关基因转录利用RT-qPCR对PGC-1α及其下游调控基因的转录水平进行了检测。如Fig 4所示,MPP+处理SH-SY5Y细胞24 h后,PGC-1α及其下游调控基因NRF1、TFAM mRNA水平明显低于正常对照组。SalD具有明显增加PGC-1α、NRF1、TFAM mRNA的作用。
|
| Fig 4 The mRNA levels of mitobiogenesis-related genes enhanced by SalD in MPP+-treated SH-SY5Y cells (x±s, n=4) ##P < 0.01 vs control group; *P < 0.05 vs MPP+ group. |
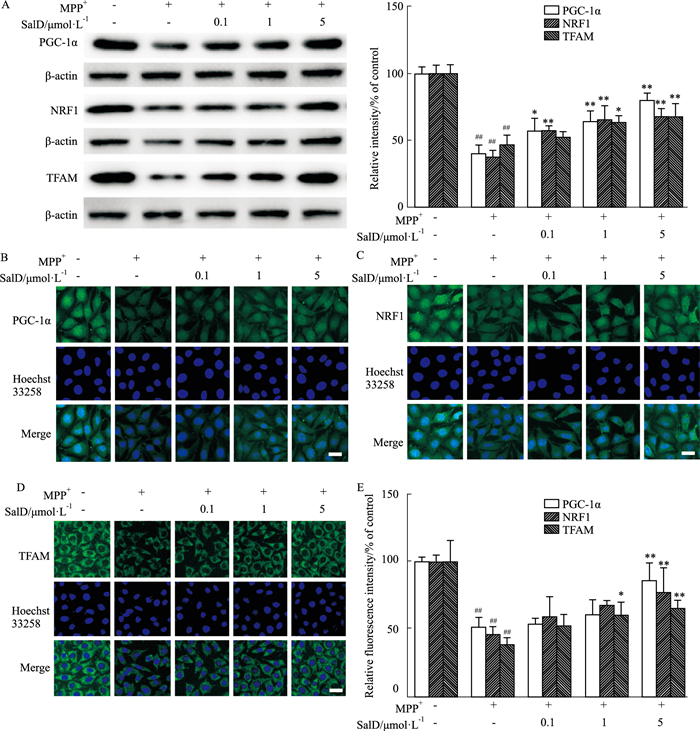
PGC-1α是介导线粒体生物合成的关键因子[10]。采用Western blot对SH-SY5Y细胞PGC-1α及参与线粒体生物合成的其他关键因子NRF1和TFAM蛋白表达进行检测。如Fig 5所示,500 μmol·L-1 MPP+作用24 h能明显降低细胞内PGC-1α、NRF1和TFAM的表达,SalD能够不同程度抑制MPP+导致的PGC-1α、NRF1和TFAM的降低。进一步采用免疫荧光方法对PGC-1α、NRF1和TFAM的表达进行检测,得到与Western blot实验一致的结果。
|
| Fig 5 Effects of SalD on mitochondrial biogenesis-related protein levels (x±s, n=4) A: PGC-1α, NRF1 and TFAM levels detected by Western blot; B: PGC-1α levels detected by immunofluorescence; C: NRF1 levels detected by immunofluorescence; D: TFAM levels detected by immunofluorescence; E: The quantitative analysis of the fluorescence. Scale bar=20 μm. ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs MPP+ group. |
线粒体是细胞凋亡的关键调节器,作为细胞的能量工厂,参与氧化磷酸化和ATP的生成,线粒体功能障碍将导致ATP合成受损。MPTP是一种脂溶性神经毒剂,可以通过血脑屏障,并且产生具有毒性作用的MPP+,MPP+进入多巴胺能神经元后,被线粒体摄取,特异性抑制复合物Ⅰ,进一步减少ATP生成而使能量耗竭,增强氧化应激,最终影响线粒体功能和生物合成[1, 4]。
本实验采用MPP+损伤SH-SY5Y细胞模型,探讨SalD对MPP+损伤SH-SY5Y细胞线粒体功能和生物合成的影响及机制。实验中,首先考察MPP+及SalD对SH-SY5Y细胞的毒性作用。通过建立MPP+诱导SH-SY5Y细胞损伤模型,评价SalD对MPP+损伤的细胞活力影响。实验结果表明,MPP+单独处理SH-SY5Y细胞时,其毒性作用具有明显浓度依赖性,选取500 μmol·L-1 MPP+损伤浓度用于后续实验,该条件下细胞存活率为51.34%。5 μmol·L-1 SalD单独作用SH-SY5Y细胞24 h,对细胞活力没有明显影响。在MPP+诱导的SH-SY5Y损伤细胞模型中,SalD(0.1、1、5 μmol·L-1)和5 mmol·L-1 NAC能够减轻MPP+诱导的SH-SY5Y细胞损伤,其细胞存活率分别达到67.98%、71.79%、76.91%和77.55%。同时,SalD能够明显降低MPP+诱导的LDH释放,改善MPP+引起的细胞核形态变化,抑制细胞凋亡。
ROS水平对细胞正常功能至关重要,线粒体是细胞内ROS的主要来源[11]。实验结果证实,MPP+损伤能够明显增加SH-SY5Y细胞ROS及线粒体超氧化物水平,而SalD可以明显降低MPP+诱导的细胞ROS和线粒体超氧化物升高。实验中,进一步考察了细胞线粒体膜电位以及ATP水平的变化,以明确SalD在改善线粒体功能中的作用。采用膜电位检测试剂JC-1测定线粒体膜电位,SalD能够明显抑制线粒体膜电位降低。ATP水平下降通常与线粒体膜电位下降同时发生,而SalD也能够抑制细胞中ATP水平的降低。以上结果表明,SalD能够有效改善MPP+损伤引起的线粒体功能障碍。
在正常生理情况下,线粒体功能处于正常状态,线粒体的生物合成不受影响,线粒体生物合成与线粒体功能处于动态平衡。然而在多种神经变性疾病中,线粒体功能受损,线粒体生物合成增强以补偿其功能下降。当线粒体生物合成不足时,可能诱导神经退行性疾病的发生[12-13]。研究发现,PGC-1α与机体的线粒体生物合成等生理活动密切相关。PGC-1α可通过激活其下游目标基因NRF1和TFAM的表达,参与调节线粒体功能[14-15]。在MPP+损伤SH-SY5Y细胞模型上,MPP+能够明显降低PGC-1α的蛋白表达,抑制线粒体生物合成。SalD孵育SH-SY5Y细胞后,能够明显增加PGC-1α、NRF1和TFAM的水平,改善受损的线粒体生物合成。同时,MPP+损伤后,细胞中PGC-1α及其下游调控基因NRF1、TFAM mRNA水平明显降低,而SalD孵育能够明显增加PGC-1α、NRF1、TFAM mRNA水平。以上结果表明,SalD能够改善受损线粒体的生物合成。
综上所述,MPP+损伤后,SH-SY5Y细胞线粒体生物合成受到明显抑制,损伤线粒体功能。SalD能够明显抑制MPP+诱导的SH-SY5Y细胞损伤,明显改善线粒体的功能,增加线粒体的生物合成,发挥线粒体和神经细胞的保护作用。
| [1] | Zhang S, Ding J H, Zhou F, et al. Iptakalim ameliorates MPP+-induced astrocyte mitochondrial dysfunction by increasing mitochondrial complex activity besides opening mitoK(ATP) channels[J]. J Neurosci Res, 2009, 87(5): 1230-9. doi:10.1002/jnr.v87:5 |
| [2] | Zhang X, Du L, Zhang W, et al. Therapeutic effects of baicalein on rotenone-induced Parkinson's disease through protecting mitochondrial function and biogenesis[J]. Sci Rep, 2017, 7(1): 9968. doi:10.1038/s41598-017-07442-y |
| [3] | 邓婕, 李怡芳, 栗原博, 等. 线粒体损伤与修复在帕金森病中的作用[J]. 中国药理学通报, 2015, 31(7): 906-10. Deng J, Li Y F, Li Y B, et al. Role of mitochondrial damage and repair in Parkinson's disease[J]. Chin Pharmacol Bull, 2015, 31(7): 906-10. doi:10.3969/j.issn.1001-1978.2015.07.004 |
| [4] | Schildknecht S, Di M D, Pape R, et al. Tipping points and endogenous determinants of nigrostriatal degeneration by MPTP[J]. Trends Pharmacol Sci, 2017, 38(6): 541-55. doi:10.1016/j.tips.2017.03.010 |
| [5] | Herraiz T. N-methyltetrahydropyridines and pyridinium cations as toxins and comparison with naturally-occurring alkaloids[J]. Food Chem Toxicol, 2016, 97: 23-39. doi:10.1016/j.fct.2016.08.009 |
| [6] | Jiang P, Guo Y, Dang R, et al. Salvianolic acid B protects against lipopolysaccharide-induced behavioral deficits and neuroinflammatory response: involvement of autophagy and NLRP3 inflammasome[J]. J Neuroinflammation, 2017, 14(1): 239-48. doi:10.1186/s12974-017-1013-4 |
| [7] | Zhou J, Qu X D, Li Z Y, et al. Salvianolic acid B attenuates toxin-induced neuronal damage via Nrf2-dependent glial cells-mediated protective activity in Parkinson disease models[J]. PLoS One, 2014, 9(7): e101668. doi:10.1371/journal.pone.0101668 |
| [8] | Yi F, He X, Wang D. Lycopene protects against MPP+-induced cytotoxicity by maintaining mitochondrial function in SH-SY5Y cells[J]. Neurochem Res, 2013, 38(8): 1747-57. doi:10.1007/s11064-013-1079-z |
| [9] | Zhang Y, Gong X G, Wang Z Z, et al. Protective effects of DJ-1 medicated Akt phosphorylation on mitochondrial function are promoted by Da-Bu-Yin-Wan in 1-methyl-4-phenylpyridinium-treated human neuroblastoma SH-SY5Y cells[J]. J Ethnopharmacol, 2016, 187: 83-93. doi:10.1016/j.jep.2016.04.029 |
| [10] | Ye Q, Chen C, Si E, et al. Mitochondrial effects of PGC-1alpha silencing in MPP+ treated human SH-SY5Y neuroblastoma cells[J]. Front Mol Neurosci, 2017, 10: 164. doi:10.3389/fnmol.2017.00164 |
| [11] | Teixeira J, Deus C M, Borges F, et al. Mitochondria: targeting mitochondrial reactive oxygen species with mitochondriotropic polyphenolic-based antioxidants[J]. Int J Biochem Cell Bio, 2018, 97: 98-103. doi:10.1016/j.biocel.2018.02.007 |
| [12] | Youle R J, Bliek A M. Mitochondrial fission, fusion, and stress[J]. Science, 2012, 337(6098): 1062-5. doi:10.1126/science.1219855 |
| [13] | Liu Y, Chong L, Li X, et al. Astragaloside Ⅳ rescues MPP+-induced mitochondrial dysfunction through upregulation of methionine sulfoxide reductase A[J]. Exp Ther Med, 2017, 14(3): 2650-6. doi:10.3892/etm.2017.4834 |
| [14] | 曹琼丹, 杨育红, 于胜男, 等. 黄芪甲苷对Ⅰ型糖尿病大鼠心肌细胞PGC-1α和NRF-1表达的影响[J]. 中国药理学通报, 2015, 31(8): 1096-101. Cao Q D, Yang Y H, Yu S N, et al. Effect of astragaloside Ⅳ on expression of PGC-1α and NRF-1 in myocardial cells of type Ⅰ diabetic rat[J]. Chin Pharmacol Bull, 2015, 31(8): 1096-101. doi:10.3969/j.issn.1001-1978.2015.08.014 |
| [15] | Ye Q, Huang W, Li D, et al. Overexpression of PGC-1α influences mitochondrial signal transduction of dopaminergic neurons[J]. Mol Neurobiol, 2016, 53(6): 3756-70. doi:10.1007/s12035-015-9299-7 |

