

2. 贵州省中国科学院天然产物化学 重点实验室药理与生物活性研究中心,贵州 贵阳 550014;
3. 贵州省人民医院干医科,贵州 贵阳 550002
2. Center for Pharmacology and Drug Screening, Key Laboratory of Chemistry for Natural Products, Guizhou Province and Chinese Academy of Science, Guiyang 550014, China;
3. General Ward, Guizhou Provincial People's Hospital, Guiyang 550002, China
淫羊藿是贵州特色民族药材中的传统补益中药,具有补肾阳、强筋骨、祛风湿等多种功效,淫羊藿苷(icariin,ICA)是一种黄酮类化合物,为淫羊藿的主要活性成分[1]。ICA的药理作用广泛,其在心脑血管系统、骨代谢、免疫系统、神经系统及肿瘤治疗等方面均表现出较好生理活性[2]。近年来,研究表明,ICA具有明显的抗炎作用,对骨关节炎、慢性阻塞型肺部炎症、哮喘性气道炎症等均有较好的改善作用[3-5]。急性肺损伤(acute lung injury,ALI)是以微血管内皮细胞急性炎症反应和损伤为早期病理学特征的综合征,其病因多样,发病机制复杂。在不同病因引发的ALI中均存在补体系统的激活,尤其是补体旁路途径激活造成的微血管内皮细胞的炎症反应和损伤在ALI发病过程中扮演重要角色[6]。本文基于挖掘ICA的药理药效作用,采用补体旁路激活诱导的ALI小鼠模型开展ICA对ALI的保护作用研究,以期为ICA的开发和ALI的防治提供参考。
1 材料 1.1 实验动物SPF级KM小鼠,32只,体质量(25±3)g,♂♀各半,由湖南斯莱克景达实验动物有限公司提供,生产许可证书:SCXK(湘)2013-0004,使用许可证号:SYXK(黔)2012-0001,实验操作和流程均遵守《实验动物管理条例》。
1.2 细胞株人微血管内皮细胞株(human microvascular endothelial cells,HMEC)为本实验室传代培养。
1.3 试剂眼镜蛇毒因子(cobra venom factor,CVF),为本课题组制备;RPMI 1640培养基(美国Gibco公司);胎牛血清(fetal bovine serum,FBS)购自天津灏洋生物科技有限公司;正常人血浆(normal human plasma,NHP)购自德国Siemens公司,经补体活性检测正常;灭活人血浆(inactivated normal human plasma,INHP)由NHP 56℃孵育30 min而得;ICA购自北京索莱宝有限公司;髓过氧化物酶(myeloperoxidase,MPO)试剂盒购自南京建成生物工程研究所;小鼠白介素6(interleukin 6,IL-6)、肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、P选择素(P-selectin)、细胞间黏附分子1(intercellular cell adhesion molecule 1,ICAM-1)ELISA试剂盒,均购自武汉博士德生物工程有限公司;p-NF-κB p65抗体购自Santa Cruz公司;双萤光素酶报告基因检测试剂盒、pRL-TK质粒、pGL4.32(luc2P/NF-κB-RE/Hygro)质粒,购自美国Promega公司;BCA蛋白定量试剂盒、核因子κB(nuclear factor κB,NF-κB)抑制剂吡咯烷二硫氨基甲酸(pyrrolidinedithinocarbamate,PDTC)、Lipofecter脂质体转染试剂、质粒抽提试剂盒,均购自江苏碧云天生物技术研究所。
1.4 仪器Forma 3111 CO2培养箱、Revco超低温冰箱(美国Thermo公司);Spectra MAX-190连续波长酶标仪(美国Molecular Devices公司);GloMax化学发光检测仪(美国Promega公司);Elix纯水系统和Milli Q超纯水系统(美国Millipore公司);5810R冷冻离心机(德国Eppendorf公司);Nikon TS100倒置显微镜(日本Nikon公司)。
2 方法 2.1 模型的制备与给药取材模型制备及取材方法参考文献[7]。SPF级KM小鼠32只,适应性喂养5 d后,称重后随机分为正常对照组、模型组、PDTC 100 mg·kg-1组、ICA 400 mg·kg-1组,每组8只。将PDTC和淫羊藿苷分别溶于0.2% CMCNa,预防给药1周,正常对照组和模型组灌胃给予等体积0.2% CMCNa,于d 7给药后1 h(PDTC组给药后30 min)尾静脉注射25 μg·kg-1的CVF(以灭菌PBS稀释,pH 7.4),正常对照组尾静脉注射等体积PBS。给予CVF后1 h摘眼球取血,静置3 h,4℃、3 000 r·min-1离心10 min制备血清;然后处死小鼠,开胸腔轻轻挑起右肺,以动脉夹夹住右肺,暴露气管,行气管插管,左肺用1.2 mL 4℃生理盐水分4次进行支气管肺泡灌洗,每次0.3 mL,来回灌洗3次,得支气管肺泡灌洗液(bronchoalveolar lavage fluid,BALF),行细胞计数,计数后BALF 4℃、3 000 r·min-1离心10 min,取上清液分装,-80℃冻存备用。将右肺上叶置于-80℃冻存,右肺中叶称湿重,右肺下叶置于4%多聚甲醛溶液中固定。
2.2 肺含水量及MPO测定称重后小鼠造模取材,右肺上叶取出后,马上置于-80℃冻存,用于MPO测定。右肺中叶称湿重,然后以70℃烘烤48 h至恒重,根据公式:(湿重-干重)/湿重×100%,计算肺含水量。
2.3 BALF细胞计数及蛋白浓度测定取BALF液,行细胞计数,计算血球计数板(25×16格)上5个大格的细胞总数n,按公式:细胞数(个·mL-1)=细胞总数n/80×400×104。取BALF上清液,采用BCA法检测,用酶标仪在562 nm测定吸光度值,并计算BALF中蛋白浓度。
2.4 炎症介质和黏附分子的测定取BALF上清液和血清,采用ELISA法检测,用酶标仪在450 nm分别测定吸光度值,并计算IL-6、TNF-α、P-selectin、ICAM-1的含量。
2.5 肺组织病理及免疫组化检测取右肺下叶用4%多聚甲醛溶液固定,常规石蜡包埋切片,HE染色,显微镜下观察肺组织病理变化。并作免疫组化染色,以胞核或胞质中呈现棕黄色或棕色颗粒为NF-κB p65磷酸化阳性反应,运用Image-Pro Plus软件分析计算平均光密度值(mean optical density,MOD),检测NF-κB p65磷酸化水平。MOD值=总积分光密度(IOD SUM)/面积(area)。
2.6 NF-κB核转录活性检测 2.6.1 HMEC培养HMEC在37℃、5% CO2饱和湿度条件下,用含10% FBS的RPMI 1640培养基培养,取对数生长期细胞进行实验。
2.6.2 补体旁路激活产物制备参照文献[8]方法,将CVF(6.5×104 U·L-1)与NHP等比例混合,37℃水浴孵育30 min,制备NHP的CVF激活产物(CVF-activated complement,CAC),现用现配。同时制备CVF与INHP的混合孵育物为对照。
2.6.3 质粒制备将1 μL重组质粒(1 ng)加入到100 μL感受态DH5α悬液中,混匀,冰浴30 min后, 42℃水浴90 s,转入冰水中放置3 min,然后加入LB培养基900 μL,置于37℃振荡45 min,取菌液100 μL,均匀涂布在筛选平板上,37℃培养12 h,挑用白色菌落扩增,然后按说明书抽提质粒。
2.6.4 双萤光素报告基因检测参照文献[9]方法,HMEC以每孔1×104个接种96孔板,培养24 h后弃上清,加入含血清无抗生素RPMI 1640培养基至90 μL,按Lipofecter脂质体转染试剂说明书加入10 μL转染混合液进行转染。转染步骤如下:取适量NF-κB表达质粒和内参质粒、脂质体试剂与无血清RPMI 1640培养基混匀,(20~25) ℃孵育20 min,取10 μL该转染混合液(含88 ng NF-κB表达质粒、45 ng内参质粒、0.2 μL脂质体试剂)加入每孔。转染6 h后去除上清,分别加入100 μL含PDTC(20 μmol·L-1)、淫羊藿苷(10-12 mol·L-1)的无血清培养基预处理2 h,后弃40 μL上清,加入40 μL CAC,同时设置CVF与INHP的混合孵育物作为对照。各孔培养体系总体积为100 μL,继续培养4 h后,根据双萤光素酶报告基因检测试剂盒说明书检测萤光强度,计算相对核转录活性。
2.7 统计学处理采用SPSS 18.0进行统计分析,实验结果以x±s表示,采用t检验进行组间比较,非正态分布的数据比较采用Mann-Whiney U法。
3 结果 3.1 ICA对ALI小鼠肺组织相关指标的影响Tab 1结果显示,与正常组比较,模型组小鼠蛋白含量、BALF细胞数目及MPO含量明显升高(P < 0.05,P < 0.01)。与模型组比较,PDTC、ICA均可以明显减少BALF中细胞数目、降低MPO含量(P < 0.01),同时,PDTC可以明显降低小鼠的蛋白含量(P < 0.05)。给药后小鼠肺含水量无明显变化(P > 0.05)。
| Group | Dose/mg·kg-1 | Lung water content/% | Protein content/mg·L-1 | BALF cells/107·L-1 | MPO/U·g-1 |
| Normal | - | 74.06±2.17 | 342.06±98.96 | 32.50±2.67 | 0.63±0.17 |
| Model | - | 72.60±2.99 | 503.95±188.78# | 86.88±5.30## | 3.05±1.91## |
| PDTC | 100 | 72.85±7.70 | 329.75±106.36* | 48.75±19.04**# | 0.69±0.30** |
| Icariin | 400 | 75.10±4.57 | 377.28±145.44 | 43.13±9.98**# | 0.48±0.15** |
| #P < 0.05,##P < 0.01 vs normal group; *P < 0.05,**P < 0.01 vs model group | |||||
如Tab 2所示,ICA可使小鼠BALF中炎症介质IL-6、TNF-α含量和黏附分子P-selectin含量明显降低,与模型组比较差异有统计学意义(P < 0.05,P < 0.01),ICAM-1含量降低但差异无统计学意义(P > 0.05);同时,与模型组比较,PDTC可以明显降低BALF中IL-6、TNF-α含量(P < 0.05,P < 0.01)。
| Group | Dose/mg·kg-1 | IL-6/ng·L-1 | TNF-α/ng·L-1 | P-selectin/ng·L-1 | ICAM-1/μg·L-1 |
| Normal | - | 14.95±11.02 | 17.22±4.92 | 283.43±47.69 | 9.13±4.63 |
| Model | - | 43.37±9.06## | 34.86±22.26# | 311.94±40.49 | 10.89±7.04 |
| PDTC | 100 | 21.65±18.41* | 16.24±8.10* | 277.37±39.12 | 10.49±5.36 |
| Icariin | 400 | 16.14±14.25** | 11.79±3.27**# | 267.46±32.11* | 8.34±4.07 |
| #P < 0.05,##P < 0.01 vs normal group; *P < 0.05,**P < 0.01 vs model group | |||||
如Tab 3所示,与正常组比较,模型组小鼠的炎症介质IL-6、TNF-α和黏附分子P-selectin、ICAM-1含量明显增加(P < 0.05,P < 0.01);与模型组比较,ICA可以明显降低小鼠血清中TNF-α及P-selectin、ICAM-1含量(P < 0.05);同时,与模型组比较,PDTC可以明显降低血清中TNF-α、ICAM-1含量(P < 0.05,P < 0.01)。
| Group | Dose/mg·kg-1 | IL-6/ng·L-1 | TNF-α/ng·L-1 | P-selectin/μg·L-1 | ICAM-1/μg·L-1 |
| Normal | - | 4.72±2.37 | 12.69±7.86 | 1.18±0.34 | 12.11±2.55 |
| Model | - | 34.36±17.52## | 40.61±27.08## | 2.67±0.58## | 19.69±5.85## |
| PDTC | 100 | 25.94±9.73## | 11.45±4.36** | 2.47±0.58## | 13.02±3.34* |
| Icariin | 400 | 24.36±7.82## | 12.55±3.17** | 2.11±0.27*## | 13.88±4.66* |
| #P < 0.05,##P < 0.01 vs normal group; *P < 0.05,**P < 0.01 vs model group | |||||
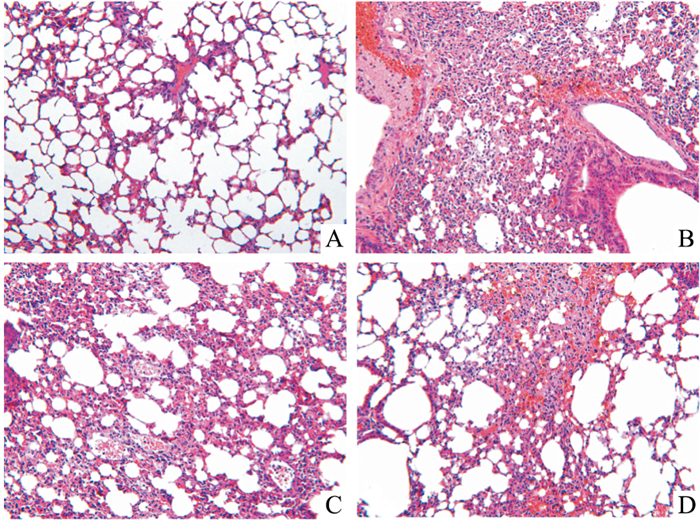
如Fig 1所示,正常组肺组织结构正常,少见炎性细胞浸润;模型组可见肺间质增宽,肺泡轻度扩张,普遍可见炎性细胞浸润;ICA组炎性细胞浸润程度减轻。
|
| Fig 1 Histological examination of lung tissue(×200) A: Normal group; B: Model group; C: PDTC group; D: ICA group. |
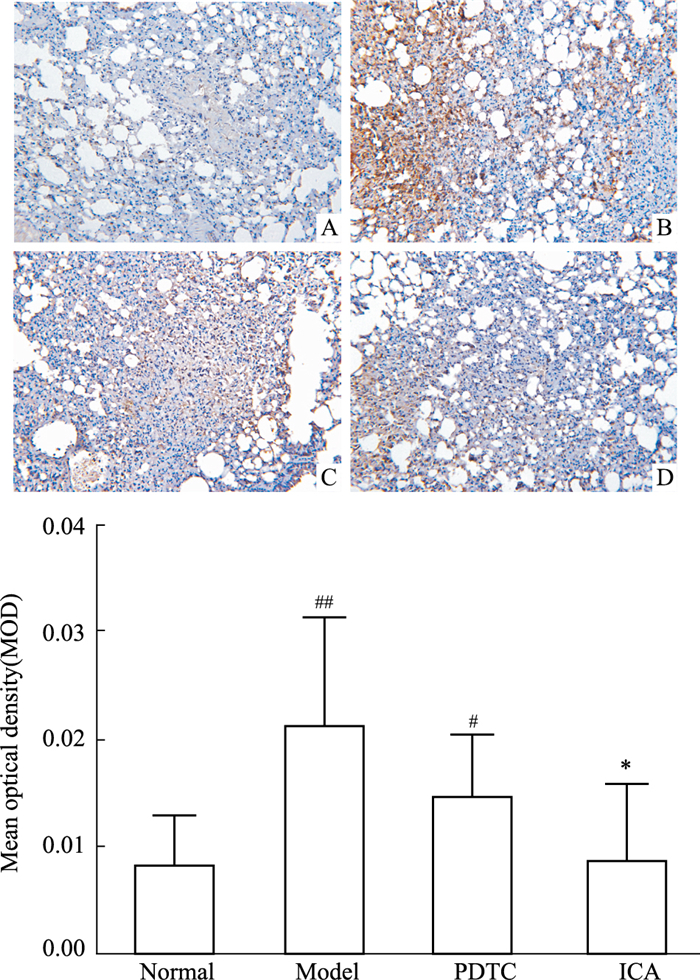
Fig 2免疫组化结果显示,与正常组比较,模型组小鼠肺组织中NF-κB p65的磷酸化水平明显升高(P < 0.01);与模型组比较,ICA可以明显下调NF-κB p65的磷酸化水平(P < 0.05)。
|
| Fig 2 The phosphorylation of NF-κB p65 in lung tissues(×200) A:Normal; B:Model; C:PDTC; D:ICA. #P < 0.05, ##P < 0.01 vs normal group; *P < 0.05 vs model group. |
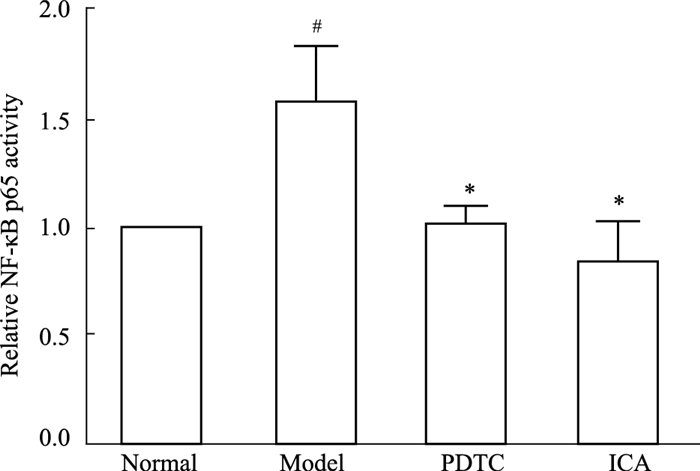
如Fig 3所示,补体旁路激活导致HMEC中NF-κB的核内转录活性明显增强(P < 0.05),而ICA能明显降低补体旁路激活所致的NF-κB核转录活性的上调(P < 0.05)。
|
| Fig 3 Effect of ICA on transcriptional activity of NF-κB after the complement alternative activation in endothelial cells (x±s, n=3) #P < 0.05 vs normal group; *P < 0.05 vs model group |
ALI是以肺部微血管急性炎症和内膜损伤为早期明显特征的临床常见急危重症。ALI发病早期,补体系统首先会被激活,而由其激活导致的微血管内皮细胞的炎症反应和损伤在ALI的发生发展中扮演着重要角色[6]。CVF是来源于眼镜蛇毒的一种高效补体激活蛋白,其激活补体旁路的方式与体内病理状态下的补体活化高度一致[7],鉴于此,我们前期采用CVF成功构建了小鼠ALI模型,在本研究中,我们采用该模型研究和评价ICA对补体旁路激活诱导的ALI的保护作用。
淫羊藿是具有温补肾阳的的一种传统补益中药,也是贵州民族药的特色药材,民间有记载将淫羊藿用于治疗风湿性关节炎、哮喘等疾病[10]。ICA是淫羊藿的主要活性成分,近年来,ICA被证实在心脑血管系统、骨代谢、抗肿瘤、抗炎等方面发挥着广泛的作用[2]。有研究表明,ICA可以通过降低肺组织MPO活性、抑制NF-κB p65激活等,减轻LPS诱导的小鼠肺部急性炎症反应[11]。然而,ICA对引发ALI的共性发病因素——补体激活的干预作用尚不明确。本研究表明,ICA可明显降低补体旁路诱导的ALI小鼠肺部炎症细胞浸润、抑制炎症介质(TNF-α、IL-6)和黏附分子(P-selectin、ICAM-1)的表达上调、抑制NF-κB p65的磷酸化,从而有效降低肺组织中的炎症反应水平。
基于肺微血管内皮细胞在ALI发病过程中的重要作用[6]及ICA可以有效抑制ALI小鼠肺部组织的NF-κB p65的磷酸化,我们进一步采用HMEC研究ICA对核内转录活性的影响。结果显示,ICA能明显下调补体旁路激活引起的HMEC中NF-κB核内转录活性的增强,提示ICA可通过抑制HMEC NF-κB p65的磷酸化,进而抑制转录活性的上调,从而抑制炎症反应,进一步明确了ICA对ALI的可能机制。
综上所述,ICA能明确抑制补体旁路激活导致的ALI早期炎症反应,下调炎症相关细胞因子,抑制NF-κB磷酸化及核内转录活性,提示其机制与抑制NF-κB相关信号通路的活化,调控炎症相关介质的转录表达有关。该工作也为进一步深入挖掘ICA的功效及其可能的开发提供实验依据和参考。
| [1] | 龚其海, 杨丹莉, 石京山, 等. 淫羊藿苷的神经药理作用及分子机制研究进展[J]. 中国新药与临床杂志, 2011, 30(7): 481-6. Gong Q H, Yang D L, Shi J S, et al. Advances in neuroharmacological effects and molecular mechanisms of icariin[J]. Chin J New Drugs Clin Rem, 2011, 30(7): 481-6. |
| [2] | 李梨, 周岐新, 石京山. 淫羊藿苷药理作用研究进展[J]. 中国药房, 2005, 16(12): 952-4. Li L, Zhou Q X, Shi J S. Progress of pharmacological research on icariin[J]. China Pharm, 2005, 16(12): 952-4. doi:10.3969/j.issn.1001-0408.2005.12.032 |
| [3] | Pan L H, Zhang Y H, Chen N, Yang L. Icariin regulates cellular functions and gene expression of osteoarthritis patient-derived human fibroblast-like synoviocytes[J]. Int J Mol Sci, 2017, 18(12): 2656. doi:10.3390/ijms18122656 |
| [4] | 孙玉姣, 李祎群, 李莉. 淫羊藿苷对慢性阻塞性肺疾病模型的抗炎和抗氧化作用[J]. 湖北中医药大学学报, 2015, 17(4): 4-7. Sun Y J, Li Y Q, Li L. Anti-inflammatory and antioxidant effects of icariin on chronic obstructive pulmonary disease model[J]. J Hubei Univ Chin Med, 2015, 17(4): 4-7. |
| [5] | Xu C Q, Le J J, Duan X H, et al. Molecular mechanism of icariin on rat asthmatic model[J]. Chin Med J, 2011, 124(18): 2899-906. |
| [6] | Bosmann M, Ward P A. Role of C3, C5 and anaphylatoxin receptors in acute lung injury and in sepsis[J]. Adv Exp Med Biol, 2012, 946: 147-59. doi:10.1007/978-1-4614-0106-3 |
| [7] | 郭静, 李敏, 杨付梅, 孙黔云. 补体旁路激活致小鼠急性肺损伤的炎症病理机制研究[J]. 中国药理学通报, 2016, 32(11): 1521-6. Guo J, Li M, Yang F M, Sun Q Y. Inflammatory mechanism of acute lung injury in mice induced by activation of complement alternative pathway[J]. Chin Pharmacol Bull, 2016, 32(11): 1521-6. doi:10.3969/j.issn.1001-1978.2016.11.009 |
| [8] | 孙黔云, 李敏, 叶巧玲, 李红玲. 补体旁路激活导致内皮细胞的活化和损伤[J]. 中国药理学通报, 2012, 28(7): 925-9. Sun Q Y, Li M, Ye Q L, Li H L. Endothelial cell activation and injury induced by complement alternative pathway[J]. Chin Pharmacol Bull, 2012, 28(7): 925-9. |
| [9] | 李敏, 孙玲, 李红玲, 孙黔云. 阿托伐他汀减轻氧化型低密度脂蛋白导致的人微血管内皮细胞活化和损伤[J]. 中国药理学通报, 2014, 30(5): 679-83. Li M, Sun L, Li H L, Sun Q Y. Atorvastatin attenuates activation and injury of human microvascular endothelial cells induced by oxidized low density lipoprotein[J]. Chin Pharmacol Bull, 2014, 30(5): 679-83. |
| [10] | 吴金峰, 董竞成, 徐长青, 等. 淫羊藿苷拮抗脂多糖炎症模型的体内和体外研究[J]. 中国中西医结合杂志, 2009, 29(4): 330-4. Wu J F, Dong J C, Xu C Q, et al. Effects of icariin on inflammation model stimulated by lipopolysaccharide in vitro and in vivo[J]. Chin J Integr Tradit West Med, 2009, 29(4): 330-4. |
| [11] | 徐长青. 淫羊藿苷对卵蛋白和内毒素诱导炎症反应的影响及机制研究[D]. 上海: 复旦大学, 2010. Xu C Q. The effects and mechanism of icariin on OVA and endotoxin-induced inflammation[D]. Shanghai: Fudan University, 2010. http://cdmd.cnki.com.cn/article/cdmd-10246-2010195073.htm |

