


2. 上海市生物物质成药性评价专业技术服务平台,上海 200437;
3. 上海医药工业研究院创新药物与制药工艺国家重点实验室,上海 200437
2. Shanghai Professional and Technical Service Center for Biological Material Drug Ability Evaluation, Shanghai 200437, China;
3. State Key Lab of New Drug and Pharmaceutical Process, Shanghai Institute of Pharmaceutical Industry, Shanghai 200437, China
在生活节奏日益加快的现代社会,疲劳对人类工作效率和生活质量的影响不可忽视,它是一种机体不能持续其机能在特定水平上或不能维持预定工作强度的状态,其主要表现为乏力、倦怠、烦躁、工作效率下降、身心状态不佳[1]。目前,临床抗疲劳促醒药物主要分为传统中枢兴奋性药物。如咖啡因、麻黄碱等,以及新型中枢兴奋性药物莫达非尼,但它们均存在严重不良反应[2],故开发新型抗疲劳促醒药物具有重要意义。
AMPA(α-amino-3-hydroxy-5-methyl-4-isoxazolepr-opionic acid)受体是中枢神经系统兴奋性神经递质谷氨酸的一类重要的离子型受体,参与介导兴奋性突触中的快速突触传递,在神经元发育、突触可塑性及神经元结构重构中都至关重要[3]。AMPA受体正向变构调节剂通过增强AMPA受体激动剂与AMPA受体的结合,从而减慢AMPA受体的失活或脱敏速度,可作为多种疾病治疗药物和中枢兴奋药进行开发。苯甲酰胺类是重点研究类别,已有多个化合物进入临床研究阶段。美国Cortex公司开发的一系列名为Ampakines的AMPA受体调节剂,如1-BCP、CX516、CX546、CX619等在抗疲劳方面表现出很好的疗效[4]。文献表明[5-7],苯甲酰胺基团与苯环上的甲氧基是必需基团,羰基氧原子通过二聚体GluR2亚基配体结合域与受体进行连接,甲氧基取代基与水分子形成的氢键连接其与亚基中的Ser729,这使得变构剂与受体的结合更加稳定。而对酰胺N原子连接基团进行修饰,可增加变构剂与其他亚区的连接,从而提高其减缓脱敏的作用。化合物酰胺N原子中引入苯基哌嗪可以提高化合物的脂溶性、药理活性。
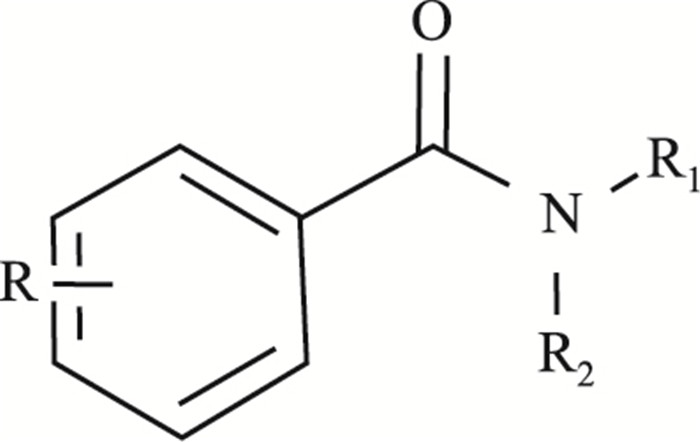
在保留苯甲酰胺基本结构(Fig 1)的基础上,我们通过对酰胺N原子上不同取代基团及苯甲酰胺环中不同位点甲氧基的取代,设计了3个系列43个化合物,并进行细胞毒性实验及抗疲劳活性筛选,最终得到1个候选化合物,进行后续进一步的研发。
|
| Fig 1 Structure of benzamides |
SPF级ICR小鼠,♂,体质量(20±2)g,由上海西普尔-必凯实验动物有限公司提供,生产许可证号:SCXK(沪)2013-0016,使用许可证号:SYXK(沪)2009-0068,饲养于SPF级实验动物房。动物饲料均使用标准SPF级全价鼠饲料。饲养条件:每笼10只,温度22~24 ℃,湿度:50%~70%,动物自由摄食饮水,12 h光亮/黑暗条件。所有动物进行实验前均适应性饲养1周。
1.2 细胞株人神经母细胞瘤细胞SH-SY5Y,由本实验室液氮保存和传代。
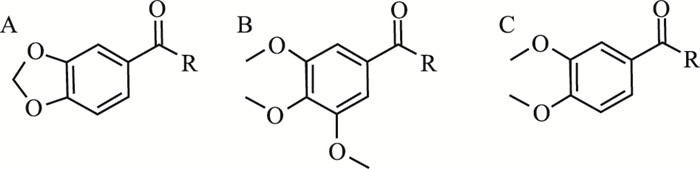
1.3 药品与试剂供筛选化合物由本实验室自主合成,化合物结构式见Fig 2与Tab 1~3。DMSO(Biosharp公司);MTT(Ameresco公司);DMEM培养基、胎牛血清(Gibco公司);青霉素、链霉素溶液(Corning公司);胰酶细胞消化液(Biological Industries公司);PEG-400、无水葡萄糖(国药集团化学试剂有限公司)。
|
| Fig 2 Structure of compounds A: 2a~2n; B: 3a~3o: C: 4a~4n |
| Number | R |
| 2a | 1-(3-fluorophenyl)piperazinyl |
| 2b | 1-(3-(trifluoromethyl)phenyl)piperazinyl |
| 2c | 1-(2, 3-dichlorophenyl)piperazinyl |
| 2d | 1-(2, 3-dimethylphenyl)piperazinyl |
| 2e | 1-(4-fluorophenyl)piperazinyl |
| 2f | 1-(3-methoxyphenyl)piperazinyl |
| 2g | 1-phenylpiperazinyl |
| 2h | 1-(m-tolyl)piperazine |
| 2i | morpholinyl |
| 2j | 1-(4-methoxyphenyl)piperazinyl |
| 2k | 1-(2-methoxyphenyl)piperazinyl |
| 2l | 1-(3-chlorophenyl)piperazinyl |
| 2m | 1-(4-chlorophenyl)piperazinyl |
| 2n | 1-(2-chlorophenyl)piperazinyl |
| Number | R |
| 3a | 1-(3-fluorophenyl)piperazinyl |
| 3b | 1-(4-methoxyphenyl)piperazinyl |
| 3c | 1-(4-fluorophenyl)piperazinyl |
| 3d | 1-(4-chlorophenyl)piperazinyl |
| 3e | 1-(2-chlorophenyl)piperazinyl |
| 3f | 1-(3-chlorophenyl)piperazinyl |
| 3g | 1-(m-tolyl)piperazine |
| 3h | 1-(2, 3-dimethylphenyl)piperazinyl |
| 3i | 1-(2, 3-dichlorophenyl)piperazinyl |
| 3j | 1-(3-(trifluoromethyl)phenyl)piperazinyl |
| 3k | 1-phenylpiperazinyl |
| 3l | 1-(3-methoxyphenyl)piperazinyl |
| 3m | 1-(2-methoxyphenyl)piperazinyl |
| 3n | piperidinyl |
| 3o | morpholinyl |
| Number | R |
| 4a | 1-(2, 3-dimethylphenyl)piperazinyl |
| 4b | 1-(3-methoxyphenyl)piperazinyl |
| 4c | 1-(4-methoxyphenyl)piperazinyl |
| 4d | 1-(2-methoxyphenyl)piperazinyl |
| 4e | 1-(2-chlorophenyl)piperazinyl |
| 4f | 1-(3-chlorophenyl)piperazinyl |
| 4g | 1-(4-chlorophenyl)piperazinyl |
| 4h | 1-(3-(trifluoromethyl)phenyl)piperazinyl |
| 4i | 1-(2, 3-dichlorophenyl)piperazinyl |
| 4j | 1-(4-fluorophenyl)piperazinyl |
| 4k | 1-(3-fluorophenyl)piperazinyl |
| 4l | 1-(m-tolyl)piperazine |
| 4m | 1-phenylpiperazinyl |
| 4n | piperidinyl |
370 Series CO2细胞培养箱(Thermo Scientific公司);SW-CJ-2FD型双人单面净化工作台(苏州净化设备有限公司);NIB-100倒置生物显微镜(宁波永新光学股份有限公司);电子天平(Mettler Toledo公司);全波长多功能酶标仪(Thermo Fisher Scientific公司);SCA210型Scout电子天平(奥豪斯国际贸易上海有限公司);自制游泳箱。
2 方法 2.1 化合物细胞毒性筛选 2.1.1 化合物配制由于每种化合物在DMSO中溶解性不同,导致所配各浓度不相同。将浓缩液用DMSO进行10倍梯度稀释,共8个浓度梯度,4℃保存备用。
2.1.2 MTT检测用含10% FBS、1%双抗的DMEM完全培养基培养SH-SY5Y细胞,待长到对数期后,对细胞进行消化、重悬,并铺于96孔板中,5×103个/孔,置37 ℃、5% CO2培养箱中培养24 h后,每孔分别加入不同浓度的药物,继续培养48 h后,加MTT,4 h后,加裂解液,至培养箱中过夜后测OD570。计算不同化合物对细胞生长的抑制率及IC50值,每组设3个复孔。细胞生长抑制率的计算公式如下:抑制率=(对照组OD值-受试组OD值)/对照组OD值×100%。
2.2 化合物中枢兴奋性筛选本动物实验经实验动物伦理委员会批准。将适应性饲养1周的ICR小鼠按照体质量随机分组,每组6只,分别为溶媒组、低剂量组(1.5 mg·kg-1)和高剂量组(5 mg·kg-1)。尾静脉分别给予对应剂量的溶媒及高、低剂量化合物,给药体积10 mL·kg-1,15 min后腹腔注射戊巴比妥钠(50 mg·kg-1,10 mL·kg-1),记下时间,以小鼠翻正反射消失为睡眠判断指标,记录小鼠睡眠时间。睡眠判断标准:将小鼠背卧放置,超过1 min不能翻正,即认为翻正反射消失,小鼠进入睡眠状态,记录下时间;当小鼠翻正反射恢复,认为小鼠觉醒,记录下时间。本实验的判断指标为睡眠时间和入睡潜伏期,公式如下:睡眠时间=翻正反射恢复时间-翻正反射消失时间;入睡潜伏期=翻正反射消失时间-注射戊巴比妥钠时间。
2.3 化合物抗疲劳活性筛选[8]将适应性饲养1周的ICR小鼠按照体质量随机分组,每组6只,分别为溶媒组、低剂量组(1.5 mg·kg-1)及高剂量组(5 mg·kg-1)。尾静脉分别给予对应剂量的溶媒及高、低剂量化合物,给药体积10 mL·kg-1,30 min后将尾部负重5%体重镍丝的小鼠放入游泳箱中游泳。水深不低于30 cm,水温保持在22~26℃。记录小鼠开始游泳到死亡的时间,即为小鼠负重游泳的时间。本实验的主要判断指标为小鼠负重游泳时间。
2.4 统计学方法采用GraphPad Prism 5软件进行统计分析,计数资料以x±s表示,用单因素方差分析检测差异性。
3 结果 3.1 MTT结果由Tab 4可以看出,大部分化合物IC50值大于40 mg·L-1,细胞毒性较小,可进行动物实验。
| Number | IC50/mg·L-1 | Number | IC50/mg·L-1 | Number | IC50/mg·L-1 |
| 2a | 22.42 | 3a | 47.11 | 4a | 11.97 |
| 2b | 15.85 | 3b | >100 | 4b | >100 |
| 2c | 18.34 | 3c | >100 | 4c | >100 |
| 2d | 13.81 | 3d | 69.40 | 4d | >100 |
| 2e | >100 | 3e | >100 | 4e | 86.82 |
| 2f | >100 | 3f | 25.43 | 4f | 29.46 |
| 2g | 84.23 | 3g | 64.15 | 4g | 64.47 |
| 2h | 29.14 | 3h | 22.44 | 4h | - |
| 2i | >100 | 3i | >100 | 4i | 13.81 |
| 2j | >100 | 3j | 40.62 | 4j | >100 |
| 2k | >100 | 3k | >100 | 4k | >100 |
| 2l | 20.24 | 3l | >100 | 4l | 76.61 |
| 2m | 51.47 | 3m | >100 | 4m | >100 |
| 2n | 20.78 | 3n | >100 | 4n | - |
| 3o | >100 |
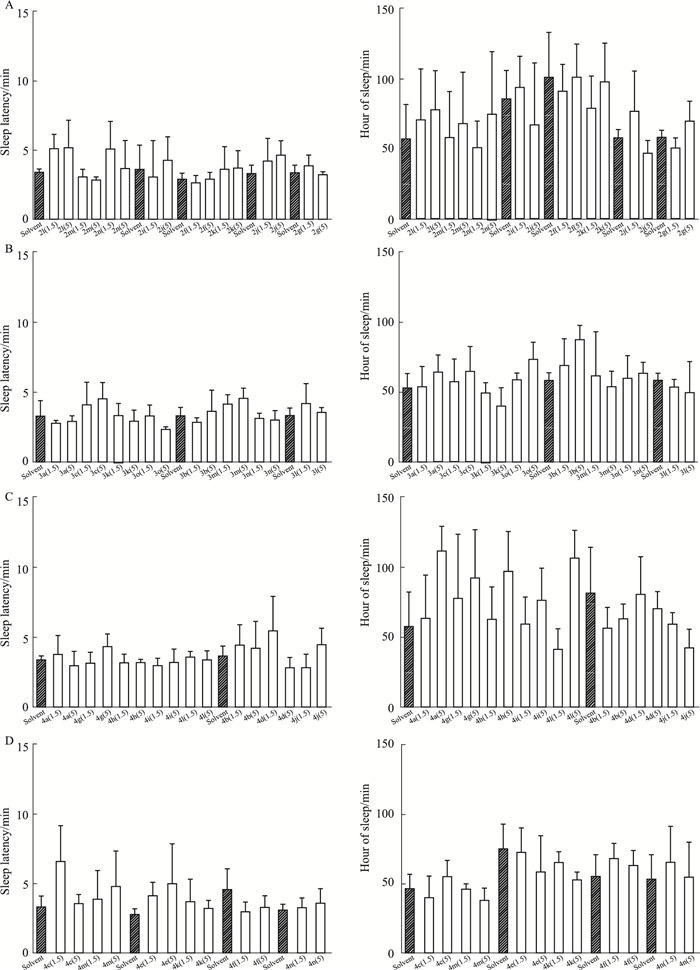
Fig 3A结果表明,系列2的化合物2f、2g、2i、2j、2k、2l、2m、2n中,与溶媒对照相比,化合物2i、2j (1.5、5 mg·kg-1)呈现出抑制戊巴比妥钠所致小鼠睡眠的趋势,但是差异无统计学意义(P>0.05);同时睡眠潜伏期结果显示,化合物2i、2j与溶媒对照相比,差异无显著性(P>0.05)。Fig 3B结果表明,系列3的化合物3a、3b、3c、3k、3l、3m、3n、3o中,与溶媒对照相比,化合物3k、3l (1.5、5 mg·kg-1)有抑制戊巴比妥钠所致小鼠睡眠的趋势,但是差异无统计学意义(P>0.05);睡眠潜伏期结果显示,化合物3l (1.5、5 mg·kg-1)呈现出延长入睡潜伏期的趋势,但是与溶媒对照组相比,差异无显著性(P>0.05),而化合物3k对入睡潜伏期没有影响。Fig 3C、3D结果表明,在系列4的化合物4a~4n中,与溶媒对照相比,化合物4j、4k、4m (1.5、5 mg·kg-1)有抑制戊巴比妥钠所致的小鼠睡眠的趋势,但是差异无统计学意义(P>0.05);睡眠潜伏期结果显示,化合物4m (1.5、5 mg·kg-1)有延长入睡潜伏期的趋势,但是差异无统计学意义(P>0.05),而化合物4k及4j对睡眠潜伏期没有影响。综上,化合物2i、2j、3k、3l、4j、4m、4k有一定的中枢兴奋作用,可进行抗疲劳活性筛选。
|
| Fig 3 Effects of compounds on sleep latency and time of sleep (x±s, n=6) A: Compound 2l, 2m, 2n, 2i, 2f, 2k, 2j, 2g; B: Compound 3a, 3c, 3k, 3o, 3b, 3m, 3n, 3l; C: Compound 4a, 4g, 4h, 4i, 4l, 4b, 4d, 4j; D: Compound 4c, 4m, 4e, 4k, 4f, 4n. |
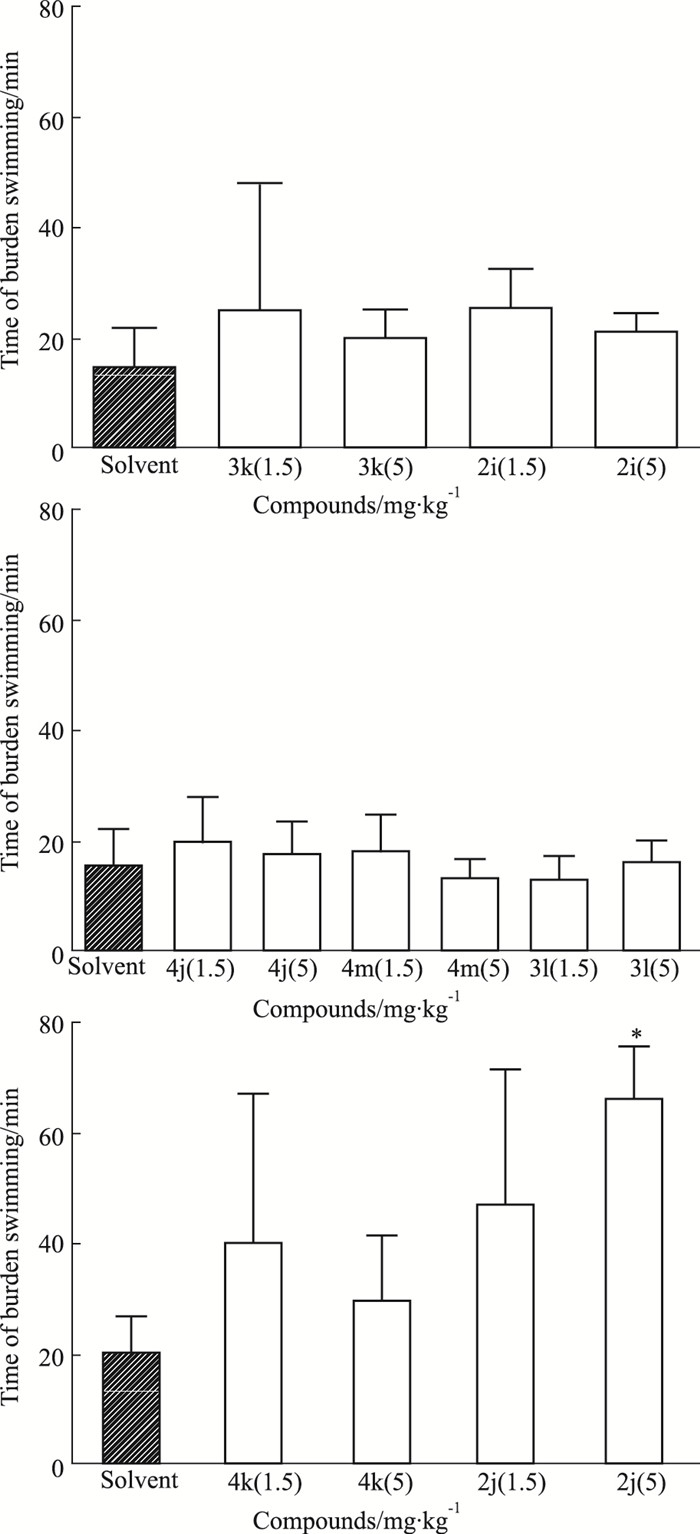
如Fig 4所示,与溶媒对照相比,化合物2i、3k、3l、4j、4m、4k对小鼠的负重游泳时间无明显影响(P>0.05);而化合物2j 5 mg·kg-1与溶媒对照相比,能够明显延长小鼠负重游泳的时间(P < 0.05)。综上,化合物2j具有一定的抗疲劳活性,有进一步开发的潜力。
|
| Fig 4 Effects of compound on burden swimming of mice(x±s, n=6) |
谷氨酸是哺乳动物中枢神经系统中最主要的兴奋性神经递质,AMPA受体属于谷氨酸离子型的受体,参与快速兴奋性突触传递,调节突触的传递效率、递质的释放,对神经元的整合功能及突触可塑性均有重要作用。AMPA受体的这些作用决定了AMPA受体与很多中枢系统疾病有关,如阿尔茨海默病、抑郁症、注意力缺陷多动症等。而AMPA受体正向变构调节剂通过增强AMPA受体激动剂与受体的结合,减慢AMPA受体脱敏和失活的速度,进而增强AMPA受体的功能[9]。
本文在对苯甲酰胺类AMPA受体正向变构调节剂进行构效分析的基础上,选择胡椒酸、3, 4, 5-三甲氧基苯甲酸、3, 4-二甲氧基苯甲酸作为母体化合物,设计了3个系列43个化合物进行合成。合成得到的43个化合物进行了IC50值的测定和活性筛选。选择人神经母细胞瘤SH-SY5Y这一具有谷氨酸能活性的细胞株,采用MTT法进行IC50值的测定,结合结构发现,当所选胺类化合物为环状脂肪胺类或苯基哌嗪衍生物中苯基的3或4位有卤原子或甲氧基时,IC50值较大,化合物对细胞几乎无毒性作用。
根据化合物的溶解性和化合物对细胞的抑制作用,对3个系列的30个化合物进行中枢兴奋性活性筛选,选择戊巴比妥钠镇静催眠实验进行筛选。结果显示,与溶媒对照组相比,化合物2i、2j、3k、3l、4j、4k、4m随着剂量的增加,有缩短戊巴比妥钠所致的睡眠时间的趋势(P>0.05),并且化合物3l、4m随着剂量的增加,还有延长入睡潜伏期的趋势(P>0.05)。结合结构分析发现,当胺类化合物为3, 4位卤原子或者甲氧基取代时,中枢兴奋作用增强,而对甲氧基苯甲酰胺系列几乎没有中枢兴奋的作用。
经过中枢兴奋性活性筛选,发现有潜在中枢兴奋作用的7个化合物,进行进一步抗疲劳活性筛选,选择小鼠负重游泳模型进行筛选。结果显示,与溶媒对照组相比,随着剂量的增加,化合物2j有延长小鼠负重游泳时间的趋势,而且高剂量组与溶媒对照之间差异有显著性(P < 0.05)。说明化合物2j既有一定的中枢兴奋作用,也有较好的抗疲劳活性,结合结构分析发现,胡椒酸系列化合物抗疲劳活性效果较好,与其他系列化合物相比,中枢兴奋作用较强,且当与酰胺氮原子相连的基团为苯基哌嗪类时,苯基4位为卤原子或者甲氧基取代时效果明显,尤其是甲氧基取代时效果最好。
本文通过对苯甲酰胺类AMPA受体正向变构调节剂进行设计、合成及活性筛选,筛选出1个具有抗疲劳活性的化合物,并且该化合物可以作为中枢兴奋活性的候选药物进行开发。该化合物也可以作为先导化合物进行进一步结构修饰。
( 致谢: 本文实验是在上海医药工业研究院药理中心完成,感谢中心全体人员对本研究的支持和帮助 )
| [1] | Nakanishi S. Molecular diversity of glutamate receptors and implications for brain function[J]. Science, 1992, 258(5082): 597-603. doi:10.1126/science.1329206 |
| [2] | Fiorillo C D, Williams J T. Glutamate mediates an inhibitory postsynaptic potential in dopamine neurons[J]. Nature, 1998, 394(6688): 78-82. doi:10.1038/27919 |
| [3] | Gou Z H, Wang X, Wang W. Evolution of neurotransmitter gamma-aminobutyric acid, glutamate and their receptors[J]. Zoolog Res, 2012, 33(e5): 75-81. |
| [4] | Lynch G. Glutamate-based therapeutic approaches: ampakines[J]. Curr Opin Pharmacol, 2006, 6(1): 82-8. doi:10.1016/j.coph.2005.09.005 |
| [5] | Harms J E, Benveniste M, Maclean J K F, et al. Functional analysis of a novel positive allosteric modulator of AMPA receptors derived from a structure-based drug design strategy[J]. Neuropharmacology, 2013, 64(1): 45-52. |
| [6] | Weeks A M, Harms J E, Partin K M, et al. Functional insight into development of positive allosteric modulators of AMPA receptors[J]. Neuropharmacology, 2014, 85(10): 57-66. |
| [7] | Krintel C, Harpsøe K, Zachariassen L G, et al. Structural analysis of the positive AMPA receptor modulators CX516 and Me-CX516 in complex with the GluA2 ligand-binding domain[J]. Acta Crystallogr D Biol Crystallogr, 2013, 69(9): 1645-52. doi:10.1107/S0907444913011839 |
| [8] | 李吉萍, 孙婷婷, 胡天骄, 等. 板蓝根活性组分对小鼠耐缺氧及抗疲劳作用的实验研究[J]. 中国药理学通报, 2016, 32(5): 712-5. Li J P, Sun T T, Hu T J, et al. Effects of active component of Radix Isatidis on anti-anoxia and anti-fatigue in mice[J]. Chin Pharmacol Bull, 2016, 32(5): 712-5. |
| [9] | 范於菟, 徐金林, 王琦瓅, 等. AMPA受体正向变构调节剂的研究进展[J]. 化学试剂, 2016, 38(2): 129-36. Fan W T, Xu J L, Wang Q L, et al. Progress of AMPA receptor positive allosteric modulators[J]. Chem Reagent, 2016, 38(2): 129-36. |

