


2. 广西医科大学 第一附属医院药学部, 广西 南宁 530021;
3. 广西医科大学 第一附属医院结直肠肛门外科, 广西 南宁 530021
 ,
LI Qing1,
GAN Jia-liang3,
LI Wan-ting1,
PAN Xiao-hang3,
JIANG Wei-zhe1
,
LI Qing1,
GAN Jia-liang3,
LI Wan-ting1,
PAN Xiao-hang3,
JIANG Wei-zhe1
 ,
TANG Shuang-yi2
,
TANG Shuang-yi2

2. Dept of Pharmacy, the First Affiliated Hospital, Guangxi Medical University, Nanning 530021, China;
3. Dept of Colorectal and Anal Surgery, the First Affiliated Hospital, Guangxi Medical University, Nanning 530021, China
胃癌是最为常见的癌症死亡原因之一, 2017年美国估计新增胃癌病例约28 000例, 新死亡病例约有10 960例[1]。胃癌发病率和死亡率极高, 对公众的健康有重大影响, 预计胃癌相关的死亡率将持续增加[2]。化疗是一种全身性治疗手段, 对恶性肿瘤的原发灶、转移灶和亚临床转移灶均有治疗作用, 但是化疗药物的选择性差, 在产生治疗效果的同时, 常出现不同程度的毒副作用[3]。因此, 寻找具有低毒、高效的抗肿瘤药物成为广大科研人员的重要任务。面对现有化疗药物的特异性不足、疗效不强、毒副作用较大的缺点, 中药给恶性肿瘤的临床治疗带来新的希望。利用现代生化方法深入研究中药的抗肿瘤作用机制, 对发现新的抗肿瘤药物是很有意义的。迷迭香酸是一种天然来源的多酚羟基化合物, 是迷迭香、紫苏、夏枯草、滇丹参等中药的有效成分, 广泛应用于食品、医药品等领域, 具有抗菌、抗氧化、抗炎、抗肿瘤等多种生物活性[4]。郭峰等[5]报道, 迷迭香酸能拮抗H2O2诱导血管平滑肌细胞凋亡。还有研究报道, 迷迭香酸可体外抑制人胃癌细胞MKN45的Warburg效应和生长[6]。为了优化迷迭香酸的抗肿瘤活性, 本课题组前期合成了几种迷迭香酸衍生物, 通过初筛发现迷迭香酸衍生物RAD-9具有明显的抗肿瘤活性, 本研究进一步从细胞水平初步探讨其诱导MGC-803细胞凋亡可能机制, 为后续开发利用奠定坚实的理论基础。
1 材料 1.1 细胞与试剂人胃癌MGC-803细胞由广西医科大学第一附属医院胃肠外科肖强课题组赠予; RPMI 1640培养基购于美国Gibco公司; 噻唑蓝(MTT)购于中国索莱宝生物科技有限公司; 荧光染料Hoechst 33258购于中国万类生物科技有限公司; Akt、p-Akt、p38、p-p38、GAPDH、Bax、Bcl-2、caspase-3兔抗人单克隆抗体, 购自美国Cell Signaling Technology公司; 0.25%胰蛋白酶、RIPA裂解液(强)、SDS-PAGE凝胶配制试剂盒、BCA蛋白定量试剂盒, 均购自中国碧云天生物技术有限公司。
1.2 仪器Series 8000 WJ型CO2培养箱(美国Thermo Fisher Scientific公司), DMILLED DFC425C型倒置荧光显微镜(德国Leica公司), VersaMAXTM型多功能酶标仪(美国Molecular Dvices公司), 电泳仪及半干转印槽(美国Bio-Rad公司)。
2 方法 2.1 细胞培养及药品储存液的配制人胃癌细胞MGC-803用含10%胎牛血清的RPMI 1640培养基, 于37℃、5% CO2饱和湿度下常规培养, 每2~3 d传代1次。迷迭香酸衍生物RAD-9(纯度大于90%)由本课题组合成, RAD-9溶于DMSO配制成100 mmol·L-1储存液, 避光-20℃保存, 实验时用含10%胎牛血清的RPMI 1640培养基稀释成相应浓度(DMSO终体积分数不超过0.1%)。
2.2 MTT法检测细胞增殖将对数生长期的MGC-803细胞, 以4 000个/孔接种于96孔板中, 培养12 h待细胞贴壁后, 弃去孔内培养基, 加入用培养基配制好的终浓度为0、12.5、25、50、100、150 μmol·L-1的RAD-9药液, 每孔200 μL, 每个浓度设5个复孔, 培养24、48、72 h。终止培养后, 每孔加入20 μL 5 g·L-1的MTT, 于培养箱中避光孵育4 h, 弃掉孔里的液体, 加入100 μL DMSO, 于震荡器上避光震荡10 min使结晶充分溶解, 在492 nm处用酶标仪测定各孔的吸光值(A值)。细胞存活抑制率=(正常对照组A492 nm-给药组A492 nm)/正常对照组A492 nm×100%。
2.3 流式细胞术检测细胞的凋亡率将对数生长期的MGC-803细胞接种于6孔板中, 待细胞长至80%汇合时, 弃去培养基, 加入含有不同浓度RAD-9(0、12.5、25、50 μmol·L-1)的培养基, 置于37℃、5% CO2培养箱继续培养36 h, 收集细胞上清液, 用冰PBS洗3遍(收集PBS洗液), 用不含EDTA的胰蛋白酶将细胞消化下来, 收集所有细胞, 用冰PBS洗3遍, 弃掉PBS, 加入100 μL Binding Buffer重悬细胞, 再加入5 μL PI和5 μL Annexin V, 避光室温孵育15 min, 再加入400 μL Binding Buffer, 于1 h内上机检测。
2.4 Hoechst 33258染色法观察细胞核的凋亡形态将对数期的MGC-803细胞接种到内嵌有经过无菌处理的盖玻片的6孔板中, 待细胞长至80%汇合时, 吸出孔内培养基, 加入用培养基配好的含有不同浓度RAD-9(0、12.5、25、50 μmol·L-1)的药液, 置于37℃、5% CO2培养箱中培养36 h, 吸出孔内液体, 用PBS轻轻漂洗3遍, 加入4%多聚甲醛固定20 min, 吸出4%多聚甲醛后, 用PBS轻轻漂洗3遍, 再用Hoechst 33258工作液室温避光染色20 min, 吸出工作液, 用PBS轻轻漂洗3遍, 再用抗荧光淬灭封片液(甘油:PBS=1 :9)封片, 于荧光显微镜下观察拍照。
2.5 Western blot检测相关蛋白表达将对数期的MGC-803细胞接种于25 cm2的培养瓶中, 待细胞长至80%汇合时, 吸出培养基, 加入用培养基配好的含有不同浓度RAD-9(0、12.5、25、50 μmol·L-1)的药液, 置于37℃、5% CO2培养箱中培养36 h, 吸出并收集瓶内液体, 用PBS轻轻漂洗3遍, 再加入细胞裂解液冰上裂解30 min, 12 000 r·min-1离心30 min, 用BCA法检测蛋白浓度。加入适量上样蛋白缓存液, 于沸水浴中高温变性8 min, 取50 μg的蛋白, 经10% SDS-PAGE电泳分离后, 使蛋白转移至PVDF膜上, 用5% BSA室温封闭40 min, 再将PVDF膜置于配好的一抗中冰上孵育过夜, 二抗室温孵育60 min, 用TBST室温避光洗膜3遍, 最后利用双色红外荧光扫描成像系统扫膜并采集图像。每组实验重复3次。
2.6 统计学分析数据以x±s表示, 经SPSS 21.0软件进行统计分析, 组间均数比较采用单因素方差分析, 用SNK法进行两两比较。
3 结果 3.1 RAD-9对胃癌MGC-803细胞增殖的影响如Tab 1所示, 与空白组比较, RAD-9干预胃癌MGC-803细胞24、48、72 h后, MGC-803细胞的存活率明显受到抑制(P < 0.01)。抑制效果呈时间、浓度依赖, 细胞的存活率随着药物浓度的升高而降低, 说明RAD-9可以有效抑制胃癌MGC-803细胞的增殖。
| RAD-9 /μmol·L-1 | Viability rate/% | ||
| 24 h | 48 h | 72 h | |
| 0 | 100.00±0.00 | 100.00±0.00 | 100.00±0.00 |
| 12.5 | 91.66±3.05* | 86.00±4.58** | 77.06±3.60** |
| 25 | 82.66±3.21** | 79.54±0.80** | 68.98±3.00** |
| 50 | 70.33±3.05** | 40.69±2.04** | 36.66±4.50** |
| 100 | 47.33±6.02** | 29.25±1.62** | 28.33±3.05** |
| 150 | 36.66±4.16** | 16.08±2.57** | 10.02±1.00** |
| *P<0.05, **P<0.01 vs control(0 μmol·L-1) | |||
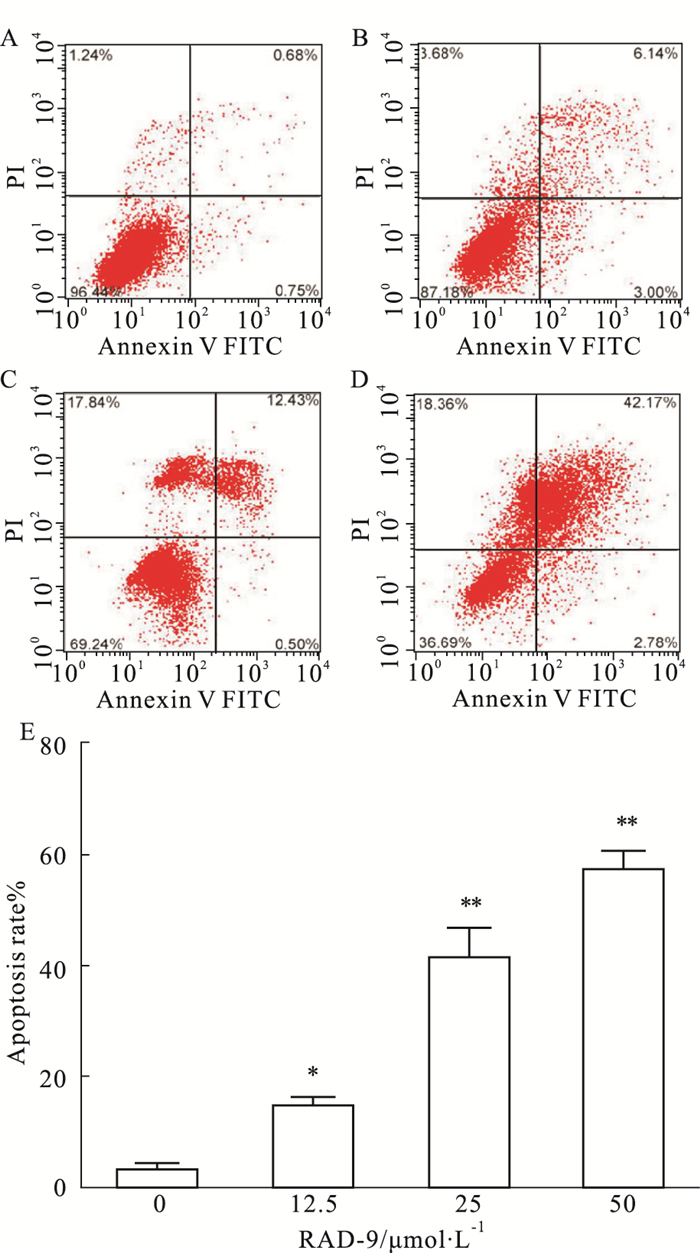
如Fig 1所示, 与空白组比较, 12.5、25、50 μmol·L-1的RAD-9干预胃癌MGC-803细胞36 h后, MGC-803细胞出现明显凋亡(P < 0.01), 活细胞数随着药物浓度的升高而下降, 晚期凋亡细胞随着药物浓度升高而增多, 说明RAD-9可以促进胃癌MGC-803细胞的凋亡。
|
| Fig 1 Effect of different concentrations of RAD-9 on apoptosis of MGC-803 cells(x±s, n=3) A:Control group; B:12.5 μmol·L-1 RAD-9;C:25 μmol·L-1 RAD-9;D:50 μmol·L-1 RAD-9;E:Bar graph of apoptosis rate.*P<0.05, **P<0.01 vs control(0 μmol·L-1) |
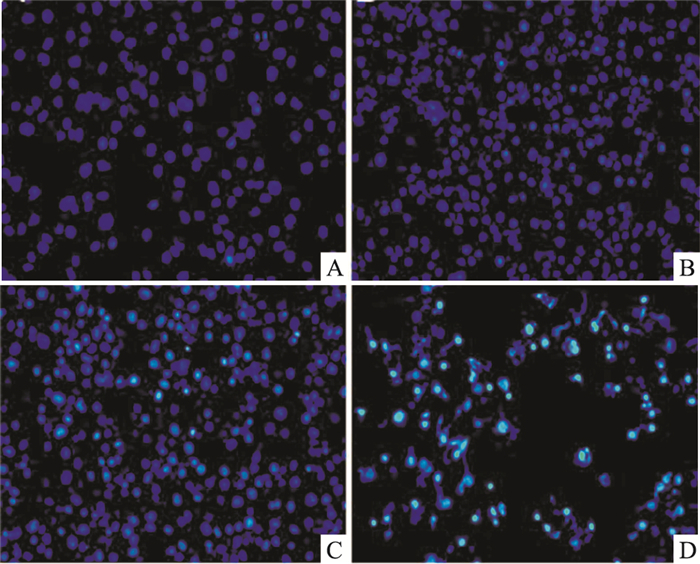
Fig 2的Hoechst 33258染色结果显示, 与空白组比较, 12.5、25、50 μmol·L-1的RAD-9干预胃癌MGC-803细胞36 h后, 空白组中的细胞核形态呈圆形, 淡蓝色; 而经RAD-9处理后的细胞, 细胞出现明显的凋亡特征, 可见凋亡的细胞由于细胞核固缩, 细胞核染色质凝聚、固缩呈明亮的月牙状、不规则圆形、椭圆形亮蓝白色亮光。表明RAD-9对MGC-803细胞有一定的促凋亡作用。
|
| Fig 2 Effect of RAD-9 on morphology of MGC-803 cells(×200) A:Control group; B:12.5 μmol·L-1 RAD-9;C:25 μmol·L-1 RAD-9;D:50 μmol·L-1 RAD-9 |
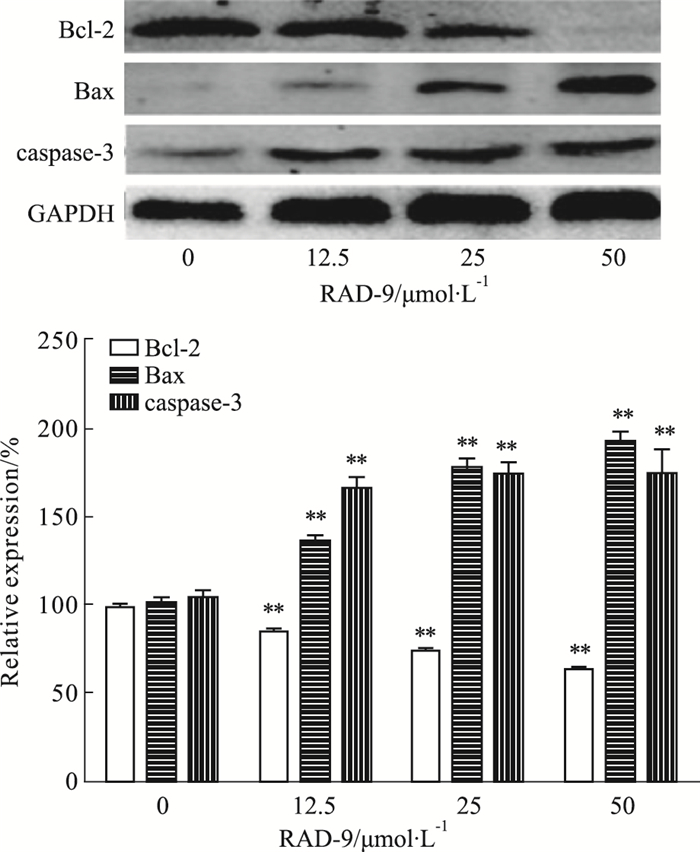
如Fig 3所示, 与空白组相比, RAD-9作用36 h后, 给药组Bcl-2蛋白表达明显下调(P < 0.01), Bax、caspase-3蛋白表达明显上调(P < 0.01), 提示RAD-9对促凋亡蛋白具有明显的诱导作用。
|
| Fig 3 Effect of RAD-9 on expression of apoptosis-related proteins in MGC-803 cells (x±s, n=3) **P<0.01 vs control(0 μmol·L-1) |
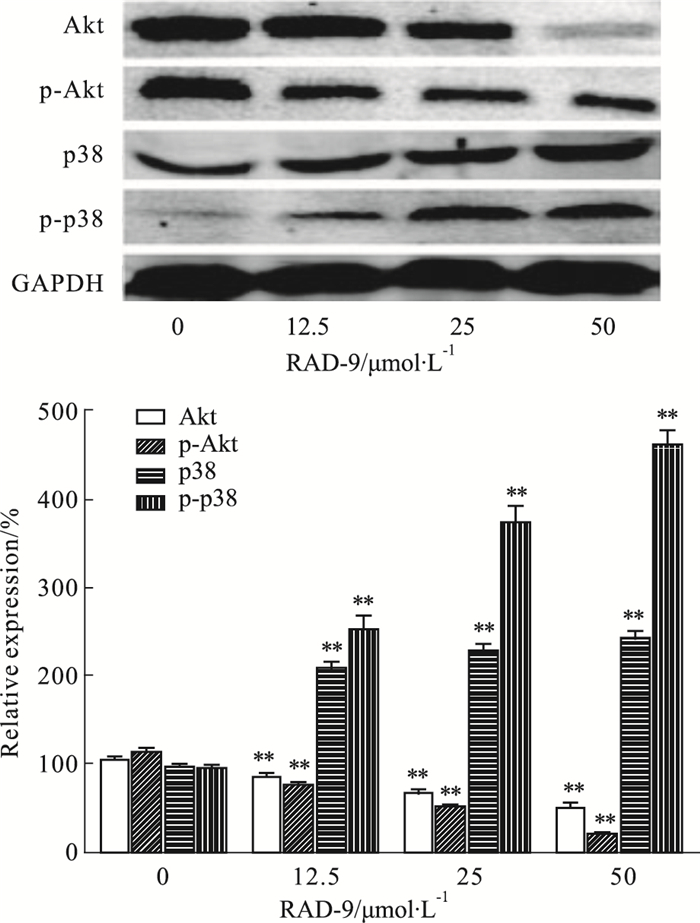
如Fig 4所示, 与空白组相比, RAD-9作用36 h后, Akt、p-Akt蛋白表达下调(P < 0.01), p38 MAPK通路蛋白p38、p-p38上调(P < 0.01)。提示RAD-9可能是通过抑制PI3K/Akt、激活p38 MAPK信号通路, 诱导胃癌MGC-803凋亡。
|
| Fig 4 Effect of RAD-9 on expression of Akt, p-Akt, p38, p-p38 proteins in MGC-803 cells (x±s, n=3) **P < 0.01 vs control(0 μmol ·L-1) |
最新统计数据显示, 2015年中国有67.9万例新发胃癌患者, 有49.8万人死于胃癌[7]。可见, 胃癌仍然是临床上威胁国人健康最常见的消化系统恶性肿瘤之一。尽管有外科手术和化疗等有效的治疗手段, 但我国胃癌总体预后仍不太乐观[8]。中药在胃癌等肿瘤治疗中具有一定优势[9], 因此, 如何挖掘和开发更多疗效好、毒性低的抗肿瘤中药, 对改善胃癌预后具有很重要的现实意义。
细胞凋亡是组织稳态的关键调节因子, 受通路激活和抑制相互作用的调控, 细胞凋亡的调控异常与神经退行性疾病、慢性炎症性疾病、自身免疫性疾病等明显相关[10], 这种主动诱导细胞死亡是中药抗肿瘤治疗的重要机制之一[9]。本研究结果显示, RAD-9能明显抑制人胃癌MGC-803细胞的增殖, 并随着浓度的递增, 出现更多核固缩等凋亡形态学特征的肿瘤细胞, 流式细胞术定量检测结果也显示, 凋亡细胞数随着药物浓度增大而增多。进一步的Western blot检测结果显示, 抑制凋亡的Bcl-2蛋白表达明显减少, 而促进凋亡的Bax蛋白水平明显提高, 凋亡启动标志蛋白caspase-3表达明显增强。这些结果提示RAD-9具有明显的凋亡诱导作用。
PI3K/Akt信号通路是细胞的重要调节通路, 参与调节细胞生长、代谢、凋亡、转移、化疗耐药等, 在大多数人类肿瘤中存在表达失调, 越来越多的研究表明, PI3K/Akt与许多类型癌症(包括胃癌)的发生发展密切相关[11]。PI3K/Akt可以调控凋亡相关蛋白Bcl-2家族成员, Akt的激活能使Bcl-2从聚合体中释放出来, 从而发挥抗凋亡作用[12], 因此, 抑制PI3K/Akt通路可以抑制肿瘤的生长或发展。在本研究中, 迷迭香酸衍生物RAD-9可以明显抑制Akt、p-Akt蛋白表达水平, 提示RAD-9可以明显抑制PI3K/Akt通路的信号传导。
丝裂原活化蛋白激酶(MAPK)包括JNK、p38和ERK, 其中p38受紫外线、渗透压、热休克和多种细胞因子等刺激而产生相应效应, 参与调节细胞的增殖、分化、迁移、侵袭和死亡等, 其功能异常与肿瘤的发生、进展和患者的生存期明显相关[13]。活化的p38可诱导Bax转位, 介导caspases家族蛋白的活化[14]。p38 MAPK信号转导通路主要与促进肿瘤细胞凋亡密切相关, p-p38对肿瘤的形成有负向调控作用, 能抑制恶性肿瘤的形成和肿瘤细胞的增殖。p38 MAPK促进细胞凋亡的机制主要有:增强c-myc基因表达, 促进p53、c-jun磷酸化, 参与介导Fas/FasL凋亡途径, 使Bax转位以诱导线粒体凋亡途径等, 最终诱导细胞凋亡[15]。我们的研究显示, RAD-9干预MGC-803细胞后, p38、p-p38明显上调, 提示RAD-9可能通过激活p38 MAPK通路, 诱导细胞凋亡。
综上所述, 迷迭香酸衍生物RAD-9可以抑制胃癌MGC-803细胞增殖, 并能诱导其凋亡, 其机制可能与抑制PI3K/Akt、激活p38 MAPK信号通路有关, 本研究为开发和改造迷迭香酸衍生物提供了理论参考。
( 致谢: 本实验于广西医科大学医学科学实验中心完成, 感谢实验室老师和同学的指导和帮助!)
| [1] | Siegel R L, Miller K D, Jemal A. Cancer statistics, 2017[J]. CA Cancer J Clin, 2017, 67(1): 7-30. doi:10.3322/caac.21387 |
| [2] | Yuan L W, Yamashita H, Seto Y. Glucose metabolism in gastric cancer:the cutting-edge[J]. World J Gastroenterol, 2016, 22(6): 2046-59. doi:10.3748/wjg.v22.i6.2046 |
| [3] | Hu Q, Sun W, Wang C, et al. Recent advances of cocktail chemotherapy by combination drug delivery systems[J]. Adv Drug Deliv Rev, 2016, 98: 19. doi:10.1016/j.addr.2015.10.022 |
| [4] | 牟宜双, 邓文龙, 周黎明. 迷迭香酸抗肿瘤作用研究进展[J]. 中药药理与临床, 2015, 31(1): 266-9. Mou Y S, Deng W L, Zhou L M. Research progress of antitumor effect of rosmarinic acid[J]. Pharmacol Clin Chin Mater Med, 2015, 31(1): 266-9. |
| [5] | 郭峰, 朱炳阳, 迟秀玲, 等. 迷迭香酸抗过氧化氢诱导血管平滑肌细胞凋亡作用的研究[J]. 中国药理学通报, 2007, 23(3): 365-70. Guo F, Zhu B Y, Chi X L, et al. Inhibition of rosmarinic acid on the apoptosis of vascular smooth muscle cells induced by hydrogen peroxide[J]. Chin Pharmacol Bull, 2007, 23(3): 365-70. |
| [6] | Zhou L, Zhang P, Zhai C, et al. Anti-Warburg effect of rosmarinic acid via miR-155 in gastric cancer cells[J]. Drug Des Devel Ther, 2015, 9: 2695-703. |
| [7] | Chen W, Zheng R, Baade P D, et al. Cancer statistics in China, 2015[J]. CA Cancer J Clin, 2016, 66(2): 115. doi:10.3322/caac.21338 |
| [8] | 陈凛, 张珂诚. 转移性胃癌的外科治疗[J]. 中华胃肠外科杂志, 2017, 20(7): 731-4. Chen L, Zhang K C. Surgical treatment for metastatic gastric cancer[J]. Chin J Gastrointest Surg, 2017, 20(7): 731-4. |
| [9] | Gao L, Hao J, Niu Y Y, et al. Network pharmacology dissection of multiscale mechanisms of herbal medicines in stage Ⅳ gastric adenocarcinoma treatment[J]. Medicine, 2016, 95(35): e4389. doi:10.1097/MD.0000000000004389 |
| [10] | Peng Y T, Chen P, Ouyang R Y, et al. Multifaceted role of prohibitin in cell survival and apoptosis[J]. Apoptosis, 2015, 20(9): 1135-49. doi:10.1007/s10495-015-1143-z |
| [11] | Li B, Li J, Xu W W, et al. Suppression of esophageal tumor growth and chemoresistance by directly targeting the PI3K/AKT pathway[J]. Oncotarget, 2014, 5(22): 11576-87. |
| [12] | Siddiqui W A, Ahad A, Ahsan H. The mystery of BCL2 family:Bcl-2 proteins and apoptosis:an update[J]. Arch Toxicol, 2015, 89(3): 289-317. doi:10.1007/s00204-014-1448-7 |
| [13] | 陈前昭, 曾于桦, 邵英, 等. 白藜芦醇抑制人结肠癌细胞增殖与p38 MAPK的关系研究[J]. 中国药理学通报, 2016, 32(8): 1110-4. Chen Q Z, Zeng Y Y, Shao Y, et al. Anti-proliferation effect of resveratrol and p38 MAPK in human colon cancer cells[J]. Chin Pharmacol Bull, 2016, 32(8): 1110-4. |
| [14] | Ghatan S, Larner S, Kinoshita Y, et al. p38 MAP kinase mediates Bax translocation in nitric oxide-induced apoptosis in neurons[J]. J Cell Biol, 2000, 150(2): 335-47. doi:10.1083/jcb.150.2.335 |
| [15] | 梁先敏, 杨克敌. Caspase和JNK/SAPK、p38 MAPK与细胞凋亡[J]. 国外医学卫生学分册, 2008, 35(1): 5-10. Liang X M, Yang K D. Caspase and JNK/SAPK, p38 MAPK and apoptosis[J]. Foreign Med Sci(Sect Hyg), 2008, 35(1): 5-10. |