


心肌缺血是指心脏的血液灌注减少,导致心脏的供氧减少,心肌能量代谢不正常,不能支持心脏正常工作的一种病理状态。近年来,心血管疾病呈逐年上升的趋势。人参是传统中药之一,人参皂苷Re(ginsenoside, Re)为人参的主要活性成分之一。研究表明,人参皂苷Re可增加心肌供氧量,使心率明显降慢[1-2],抑制caspase-3表达[3],诱导心肌细胞凋亡。由于心肌缺血过程中心肌损伤的发生是多因素、多途径的,所以心肌损伤级联反应中的信号通路是探讨防治心肌损伤和细胞凋亡的有效方法。本课题组前期发现,人参皂苷对大鼠急性心肌缺血的心肌具有一定的保护作用[4-5],但其机制有待于进一步研究。有研究表明,在心肌细胞发生缺血/再灌注时,Janus激酶2(Janus kinase 2,JAK2)信号转导因子和转录活化因子3(signal transducer and activator of transcription 3,STAT3)信号通路激活与心肌细胞凋亡的发生密切相关[6]。因此, 本研究通过复制大鼠急性心肌缺血损伤模型, 探讨人参皂苷Re预处理对急性心肌缺血大鼠心肌凋亡蛋白Bax、Bcl-2与JAK2/STAT3通路的影响,进一步探讨心肌缺血的发生机制。
1 材料与方法 1.1 药品与试剂人参皂苷Re、葛根素(puerarin, PUE)(成都普菲德生物技术有限公司);异丙肾上腺素(isoprenaline,ISO)(Sigma公司);乳酸脱氢酶(lactate dehydrogenase,LDH)、肌酸激酶(creatine kinase,CK)、谷胱甘肽合成酶(glutathione, GSH)、超氧化物歧化酶(superoxide dismutas, SOD)、丙二醛(malondialdehyd, MDA)测定试剂盒、SABC试剂盒,均购自基尔顿生物科技(上海)有限公司;Bax、Bcl-2、JAK2、p-JAK2、STAT3、p-STAT3、生物素化山羊抗小鼠IgG(北京博奥森生物技术公司)。
1.2 动物模型的建立及分组给药清洁级SD大鼠,♂,体质量(180±20)g,由辽宁省本溪实验动物中心提供,许可证号:SCXK(辽)2013-0009。SD大鼠75只,♀♂不限,随机分为5组(n=15),分别为空白对照组(control)、模型组(model)、葛根素组(PUE 30 mg·kg-1)、人参皂苷Re高剂量(20 mg·kg-1)组(Re-H)、人参皂苷Re低剂量(10 mg·kg-1)组(Re-L)。各组均腹腔注射给药(10 mL·kg-1),空白对照组、模型组分别给予等量的生理盐水。连续给药6 d,每天1次。开始给药后的d 5和d 6,除空白对照组外,其余各组连续2次皮下多点注射给予ISO(30 mg·kg-1),空白对照组给予等量生理盐水,给药体积均为10 mL·kg-1。
1.3 检测指标 1.3.1 心肌表面血流量检测每组末次给药10 min后,随机取5只,10%水合氯醛3 mL·kg-1腹腔注射麻醉,仰卧位固定,麻醉后5 min,除空白对照组皮下给予等量生理盐水外,其余各组均皮下多点注射ISO,用FLPI2-MOOR激光散斑实时成像系统(英国Moor公司)进行心脏表面微循环扫描,记录注射3 min后心脏表面30 s内的心脏血流情况。
1.3.2 心肌指标LDH、CK、SOD、MDA、GSH含量检测取各组其余的10只大鼠,给药15 min后,生理盐水将心肌组织匀浆,制备10%心肌匀浆液,然后按照ELISA试剂盒说明书,分别设计标准孔及对照孔,利用标准曲线算出结果。
1.3.3 心肌Bax、Bcl-2免疫组化检测常规心肌脱蜡入水后,3%过氧化氢除去内源性酶20 min, 微波修复10 min, 冷却后按照SABC试剂盒进行操作,加5% BSA封闭液, 室温10 min。加1 : 500大鼠抗Bcl-2、Bax抗体, 4℃过夜; 加生物素化山羊抗小鼠IgG, 25℃ 20 min, 加SABC, 25℃ 20 min。以上每步后均以0.5 mol·L-1 PBS冲洗3~4次,DAB显色, 苏木精复染后脱水、透明、封片。
1.3.4 JAK2、p-JAK2、STAT3、p-STAT3蛋白表达的测定实验结束后,取各组大鼠心肌组织,称取100 mg放入玻璃匀浆器中,加入1 mL裂解液,冰上充分研磨;12 000 r·min-1、4℃离心10 min,取上清;BCA试剂盒测定蛋白浓度,每孔上样20 μL,电泳后转膜3 h,一抗孵育1 h后,4℃过夜,次日二抗孵育1 h后,暗室中加入ECL发光液后,曝光30 min,扫描图像后分析结果,计算目的蛋白与内参β-actin条带的光密度比值,再各组比较。
1.3.5 统计学处理用SPSS 19.0统计软件进行分析。数据均采用x±s表示,多组间比较采用单因素方差分析(ANOVA)。
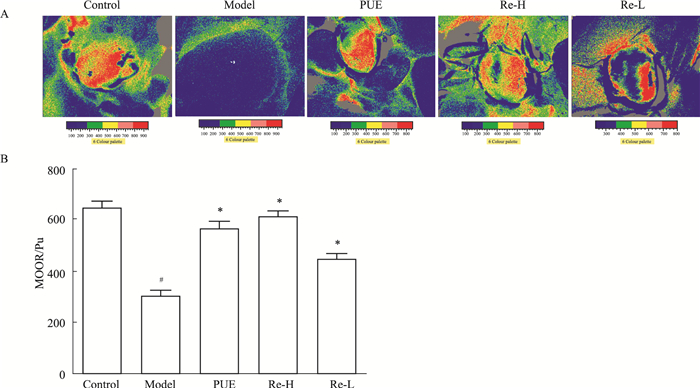
2 结果 2.1 各组大鼠心肌平均血流灌注量(pu)如Fig 1所示,与对照组相比,模型组大鼠心肌平均血流量明显降低(P<0.05);与模型组比较,PUE组和Re-H可明显提高心肌平均血流量(P<0.05),Re-L组也有增高趋势,但小于PUE和Re-H组(P<0.05)。
|
| Fig 1 Effects on microcirculation blood flow in myocardium of ISO-induced acute myocardial ischemia rats A: The microcirculation of heart surface of each group; B:The statistics microcirculation of heart surface of each group. #P < 0.05 νs control; *P < 0.05 vs model |
Tab 1结果显示,与对照组相比,模型组大鼠CK、LDH、MDA含量均增多(P<0.05),SOD、GSH含量降低(P<0.05);与模型组比较,PUE组、Re-H组可明显降低CK、LDH的含量(P<0.05);Re-H组和Re-L组MDA含量明显降低(P<0.05),PUE组和Re-H组GSH-Px含量明显升高(P<0.05);SOD含量的差异无统计学意义,但其变化趋势与GSH含量的变化一致。
| Group | Dose/mg·kg-1 | LDH/kU·L-1 | CK/kU·L-1 | MDA/μmol·g-1 | SOD/kU·L-1 | GSH/kU·g-1 |
| Control | - | 157.48±10.11 | 120.63±9.05 | 233.31±23.75 | 388.77±43.52 | 141.98±23.46 |
| Model | - | 214.37±20.51# | 262.92±29.83# | 535.39±34.92# | 188.91±6.32# | 102.22±6.63# |
| PUE | 15 | 151.90±3.43* | 113.61±5.37* | 400.58±25.94 | 250.88±17.11 | 141.07±15.05* |
| Re-H | 20 | 170.29±4.68* | 109.87±8.11* | 255.34±50.29* | 244.56±22.55 | 160.39±9.32* |
| Re-L | 10 | 191.45±23.39 | 120.44±23.08* | 221.69±11.65* | 270.02±15.36 | 129.68±23.46 |
| #P < 0.05 vs control; *P < 0.05 vs model | ||||||
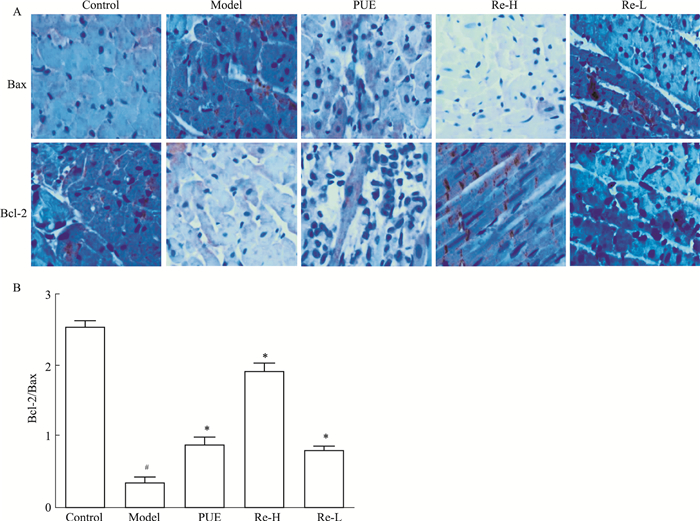
如Fig 2所示,与对照组相比,模型组Bax蛋白表达增强,Bcl-2蛋白表达降低;Bax蛋白阳性胞质多位于心肌缺血区周围的心肌细胞,Bcl-2/Bax比值明显降低(P<0.05)。与模型组相比,PUE、Re-H、Re-L三组Bax蛋白阳性胞质数减少,蛋白表达降低,Re-H组表达降低更明显;三组Bcl-2蛋白阳性胞质数增强,蛋白表达增强,Re-H组表达明显增强,Bcl-2/Bax比值明显升高(P<0.05)。
|
| Fig 2 Expression of Bax and Bcl-2 protein(A) and Bcl-2/Bax ratio(B) in myocardium of ISO-induced acute myocardial ischemia rats (×400) #P < 0.05 vs control; *P < 0.05 vs model |
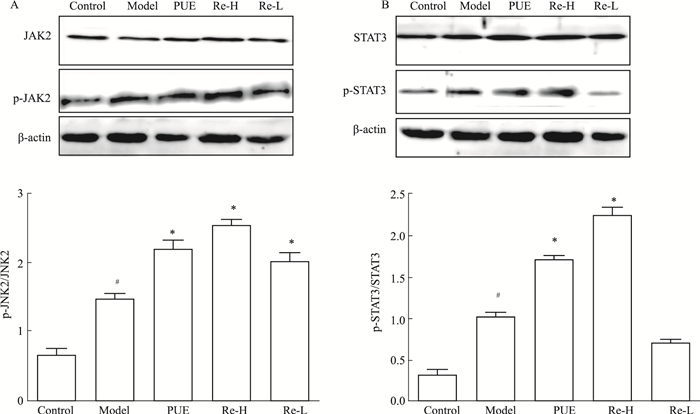
如Fig 3所示,与对照组相比,模型组大鼠心肌组织JAK2、STAT3蛋白磷酸化水平明显增加(P<0.05);与模型组比较,PUE、Re-H组可以明显增强心肌组织JAK2、STAT3蛋白磷酸化水平(P<0.05)。
|
| Fig 3 3 Effect on expression of JAK2, p-JAK2(A), STAT3 and p-STAT3 (B) protein in myocardium of ISO-induced acute myocardial ischemia rats #P < 0.05 vs control; *P < 0.05 vs model |
ISO导致心肌缺血、缺氧的主要原因是儿茶酚胺类物质的氧化产物[7]。本研究采用这种无创的操作制备急性心肌缺血模型,通过给予人参皂苷Re,研究了其对心肌缺血损伤心肌JAK/STAT信号通路的作用。
氧化应激常发生于心肌缺血中,急性缺血时,心肌产生大量氧自由基,容易引起细胞坏死或者凋亡[8]。SOD、GSH是抗氧化系统中的重要组成部分,组织中的相关抗氧化物质的动态变化可以体现机体的抗氧化能力[9]。本实验发现,大鼠急性心肌缺血后LDH、CK含量有所提高,说明急性心肌缺血大鼠出现了心肌损伤,同时PUE、Re-H、Re-L组都能同时改善以上情况,说明人参皂苷Re对急性心肌缺血大鼠起到保护作用。MDA含量明显增加,SOD、GSH活性降低,给予高剂量人参皂苷Re处理后,SOD活性有所增加,提示人参皂苷Re可抑制氧化应激,同时人参皂苷Re可增加心肌的血流量,实现对心肌缺血大鼠心肌的保护作用。
JAK-STAT信号通路是涉及免疫、细胞凋亡、炎症、肿瘤等多种生理、病理过程的重要细胞内信号转导通路。哺乳动物JAK/STAT信号通路共有4个JAK家族成员和7个STAT家族成员组成,4个JAK家族成员分别为JAK1、JAK2、JAK3、Tyk2; STAT家族成员分别为SATA1、2、3、4、5a、5b、6。许多细胞外信号能够激活JAK-STAT通路,这些细胞外信号与靶细胞上相应的受体结合后活化JAK,进一步磷酸化STAT,2个磷酸化的STAT分子形成二聚体并转位到细胞核,与靶基因DNA结合,调节靶基因的表达,从而发挥多种生物学效应[10]。Bcl-2家族按其功能可分为抗凋亡的Bcl-2亚族和促凋亡的Bax亚族,心肌损伤会导致Bax蛋白表达增多。在细胞凋亡信号转导途径中,Bcl-2家族成员的构成比例是凋亡调控的关键因素,Bcl-2/Bax在细胞凋亡过程中具有重要意义。有研究显示,STAT1、STAT3的过度活化有促进神经元凋亡的作用,能降低抗凋亡基因Bcl-2、Bcl-x的表达[11]。有研究证明[12-13],JAK2-STAT3通路在缺血预处理,特别是预处理的晚期心肌保护机制中具有核心地位,它通过上调抗凋亡蛋白比例以及NOS、COX-2等保护蛋白,发挥心肌保护作用。
本研究显示,人参皂苷Re可以明显改善ISO诱导的心肌缺血小鼠心肌血流量变化,减少血清中心肌损伤酶的含量,增加Bcl-2/Bax比值,并上调JAK2/STAT3的磷酸化水平。提示人参皂苷Re作为人参的重要活性成分,具有明显的抗心肌缺血作用,其机制可能与增加心肌血流量,稳定机体抗氧化系统,调节凋亡蛋白表达及JAK2/STAT3信号通路有关。
| [1] | Peng L, Sun S, Xie L H, et al. Ginsenoside Re: pharmacologicaleffects on cardiovascular system[J]. Cardiovasc Therap, 2012, 30(4): 183-8. doi:10.1111/cdr.2012.30.issue-4 |
| [2] | Xie J T, Shao Z H, Vanden Hoek T L, et al. Antioxidant effects of ginsenoside Re in cardiomyocytes[J]. Eur J Pharmacol, 2006, 532(3): 201-7. doi:10.1016/j.ejphar.2006.01.001 |
| [3] | 高莹, 杨积武, 王艳春, 等. 人参皂苷Re对大鼠心肌缺血再灌注细胞凋亡及Caspase-3的影响[J]. 辽宁中医药大学学报, 2011, 13(2): 123-4. Gao Y, Yang J W, Wang Y C, et al. Effects of ginsenoside Re on apoptosis and caspase-3 expression in myocardial ischemia reperfusion rats[J]. J Liaoning Univ Tradit Chin Med, 2011, 13(2): 123-4. |
| [4] | 冷雪, 臧安缘, 李其芳. 人参皂苷Rg1通过PI3K /Akt /eNOS信号通路调控异丙肾上腺素致急性心肌缺血大鼠心肌的抗氧化作用[J]. 中国实验方剂学杂志, 2017, 23(11): 145-50. Leng X, Zang A Y, Li Q F, et al. Ginsenoside Rg1 through PI3K/Akt/eNOS signal pathway regulation of isoproterenol induced acute myocardial ischemia rat myocardial antioxidant[J]. Chin J Exp Tradit Chin Med, 2017, 23(11): 145-50. |
| [5] | 冷雪, 张立德, 贾连群, 等. 人参皂苷Rb1对异丙肾上腺素诱导大鼠急性心肌缺血影响的作用机制[J]. 中国实验方剂学杂志, 2015, 21(24): 104-8. Leng X, Zang A Y, Li Q F, et al. Effects of ginsenoside Rb1 on isoprenaline-induced acute myocardial ischemia in rats[J]. J Exp Tradit Chin Med, 2015, 21(24): 104-8. |
| [6] | Zhang M, Wang X, Wang X, et al. Oxymatrine protects against myocardial injury via inhibition of JAK2/STAT3 signal in rat septic shock[J]. Mol Med Rep, 2013, 7(4): 1293-9. doi:10.3892/mmr.2013.1315 |
| [7] | 牛子冉, 徐晓娜, 陈俞材, 等. 丹酚酸A对异丙肾上腺素致小鼠心肌缺血的保护作用及其机制[J]. 中国药理学通报, 2015, 31(12): 1667-74. Niu Z R, Xu X N, Chen Y C, et al. Effect of salvianolic acid A on isoproterenol-induced myocardial ischemia in mice and its mechanism[J]. Chin Pharmacol Bull, 2015, 31(12): 1667-74. doi:10.3969/j.issn.1001-1978.2015.12.009 |
| [8] | Giordano F J. Oxygen, oxidative stress, hypoxia, and hearu failure[J]. J Clin Invest, 2005, 115(3): 500-8. doi:10.1172/JCI200524408 |
| [9] | Khatua T N, Padiya R, Karnewar S, et al. Garlic provides protection to mice heart against isoproterenol induced oxidative damage:role of nitric oxide[J]. Nitric Oxide, 2012, 27(1): 9-17. doi:10.1016/j.niox.2012.03.004 |
| [10] | 黄文林, 朱孝峰. 信号转导[M]. 北京: 人民卫生出版社, 2005: 182-91. Hang W L, Zhu X F. Signal transduction[M]. Beijing: People's Health Publishing House, 2005: 182-91. |
| [11] | 杨志宏, 胡亚, 孙晓波. JAK/STAT信号转导通路及中药干预在缺血性脑卒中的研究进展[J]. 中国药理学通报, 2016, 32(7): 889-94. Yang Z H, Hu Y, Sun X B. JAK/STAT signal transduction pathway and traditional Chinese intervention in ischemic stroke[J]. Chin Pharmacol Bull, 2016, 32(7): 889-94. |
| [12] | Gross E R, Hsu A K, Gross G J. The JAK-STAT pathwayis essential for opioid-induced cardioproteetion: JAK2 as amediator of STAT3, Akt, and GSK-3 beta[J]. Am J Physiol Heart Cite Physiol, 2006, 291(2): H827-34. doi:10.1152/ajpheart.00003.2006 |
| [13] | 颜丽晖, 江晓菁. JAK2-STAT3通路对七氟烷后处理在体大鼠缺血/再灌注心肌的影响[J]. 中国药理学通报, 2011, 27(10): 1368-73. Yan L H, Jiang X Q. JAK2-STAT3 pathway on ischemic/reperfusion myocardium in rats after pretreatment of sevoflurane[J]. Chin Pharmacol Bull, 2011, 27(10): 1368-73. doi:10.3969/j.issn.1001-1978.2011.10.009 |

