


缺血性脑卒中(ischemic stroke,IS)是由于脑血流的突然中断导致脑细胞死亡和神经缺陷的一类疾病,是全世界主要的健康危机[1]。脑缺血/再灌注损伤(cerebral ischemia/reperfusion injury,CIRI)是导致IS进一步恶化的重要原因。课题组前期研究表明,天麻乙酸乙酯提取物具有明显的抗CIRI的作用,其作用机制与抗神经细胞的凋亡有关[2]。对羟基苯甲醛(4-hydroxybenzaldehyde,4-HBd,结构式见Fig 1)是天麻主要活性成分之一[3],前期课题组已证实,4-HBd具有抗炎[4]、抗血小板聚集作用[5],同时有明显的血管平滑肌松弛[6]等作用。本研究采用线栓法复制大鼠脑缺血/再灌注(middle cerebral artery occlusion/reperfusion,MCAO/R)损伤模型,Longa 5分法对模型大鼠神经功能缺损症状进行神经病学评分、TTC染色法检测脑梗死体积,以评价4-HBd对CIRI的保护作用;培养大鼠原代皮层神经元,复制缺糖缺氧/复糖复氧(oxygen glucose deprivation/reoxygenation,OGD/Rep)损伤模型,检测细胞存活率、超氧化物歧化酶(superoxide dismutase,SOD)活性、丙二醛(malondialdehyde,MDA)含量、一氧化氮(nitric oxide,NO)释放量,以及Bax、Bcl-2、caspase-3蛋白的表达水平,以探讨4-HBd对CIRI的保护作用机制是否与抗神经细胞的凋亡有关。
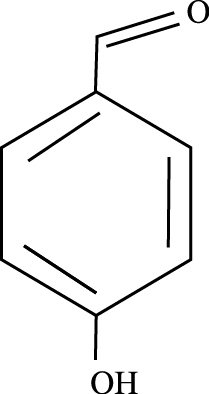
|
| Fig 1 Chemical structure of 4-hydroxybenzaldehyde |
成年健康Sprague-Dawley(SD)大鼠,体质量250~300 g,SPF级,四川省医学科学院实验动物研究所提供,生产许可证号:SCXK(川)2008-24,合格证号:0002777。
1.2 试剂Na2S2O4(汕头市西陇化工有限公司,批号:110902);SOD试剂盒(批号:20131204)、MDA试剂盒(批号:20131126)、NO试剂盒(批号:20131119),均购自南京建成生物工程研究所;Bax抗体(货号:50599-2-lg)、caspase-3抗体(货号:19677-1-AP),均购自Proteintech;辣根过氧化物酶标记山羊抗大鼠IgG(H+L) (Beyotime公司,批号:AO192);β-actin抗体(北京博奥森生物科技有限公司,批号:bs-0061R);细胞裂解液(北京索莱宝科技有限公司,批号:20130307);SABC(兔IgG)-POD Kit(Solarbio公司,批号:SA0021);神经元特异性烯醇酶(2-phospho-D-glycerate hydrolase,NSE),购自武汉博士德公司,批号:BA0535。
1.3 仪器酶标仪(Infinite M200 PRO),瑞士Tecan;生物安全柜(BSC-1300ⅡA2),苏净集团苏州安泰空气技术有限公司;CO2细胞培养箱(3111),美国Thermo Scientific公司;超纯水系统(ZMQS 50F01),美国Millipore公司;真空安全吸液系统(VACUSAFE),瑞士Integra-biosciences公司。
2 方法 2.1 实验分组及药物处理将SD大鼠随机分为假手术组、模型组、4-HBd高剂量组(20 mg·kg-1)、4-HBd低剂量组(10 mg·kg-1)。高、低剂量组在复制模型前用4-HBd预处理5 d;假手术组与模型组给予同体积溶媒。
采用线栓法复制大鼠(MCAO/R)模型[7-9]:大鼠10%水合氯醛(3 mL·kg-1)腹腔注射麻醉,翻正反射消失后仰卧固定于手术台,手术过程中用智能恒温控制仪维持大鼠肛温37℃,颈部剃毛并进行常规消毒,在颈正中偏左0.5 cm处纵切口长约1.5 cm,分离右侧颈总动脉,栓线经颈总动脉、颈内动脉插入大脑中动脉,微遇阻力时停止,栓线插入深度约为18~20 mm,记录大鼠脑缺血开始时间,缺血2 h后,将栓线缓慢拔出以恢复缺血区供血造成再灌注,在缺血及再灌注期间保持室温在(25~30)℃。
各组大鼠缺血2 h,再灌注24 h时,检测神经病学评分[10-11]:无明显神经功能障碍者为0分;提尾悬空不能伸展左侧前爪、有运动障碍者为1分;行动不协调,行走时向左侧倾斜、划圈为2分;行走困难,并向左侧倾倒为3分;不能自发行走,意识水平下降为4分。纳入标准:考虑实验为预防性给药,故将中途死亡的动物排除,其余动物全部纳入实验。
各组大鼠用10%水合氯醛腹腔注射麻醉后,断头取脑并沿脑桥上界面切断,去除嗅球后称全脑重,放入-20℃冰箱5 min后取出。由前向后连续做冠状切片5片,再将脑切片置入0.2% TTC溶液中,放入恒温振荡器37℃避光染色10 min。取出脑切片放入4%中性多聚甲醛中固定24 h后用数码相机拍摄脑片,梗死面积用Image J显微图像分析系统计算。
2.2 原代皮层神经元的培养及鉴定取妊娠19 d大鼠的胚胎,放入含75%乙醇的烧杯中浸泡3 min,再将胎鼠放入装有预冷D-Hank’s的培养皿中解剖,分离胎鼠脑皮层并用剪刀剪碎,用0.125%胰酶消化,过滤,离心,计数,加入神经元培养基,调整浓度,接种于提前包被好的培养板中,置于5% CO2培养箱中培养。
NSE染色方法:取出培养7 d的神经细胞,吸出培养基,PBS洗2遍,用4%的多聚甲醛室温固定1 h;PBS漂洗,滴加0.1% TitonX-100室温孵育20 min,使细胞的通透性增加;PBS漂洗,滴加3%的H2O2,室温孵育20 min,PBS漂洗,滴加5% BSA封闭液,室温条件下孵育30 min,吸去多余液体;滴加一抗NSE,用稀释液按1 :100稀释,37℃孵育1 h;PBS漂洗,滴加二抗(Bio-羊抗兔IgG,1 :100稀释),室温条件下孵育30 min;PBS漂洗,滴加SABC(兔IgG)-POD Kit (1 :100稀释),37℃避光孵育30 min,PBS漂洗,滴加显色液,蒸馏水漂洗终止显色,苏木精轻度复染1~3 min,蒸馏水洗,染核成蓝色,显微镜下观察NSE表达:取上、下、中、左、右5个视野,计算NSE表达阳性细胞数占总细胞数的比例。
微管相关蛋白(microtubule-associated protein-2,MAP-2)染色方法:取出培养7 d的神经细胞,吸走培养基,PBS漂洗,4%多聚甲醛室温固定细胞1 h,PBS洗后,每孔加入200 μL 0.5% TritonX-100,室温通透30 min,PBS漂洗,10%山羊血清室温封闭1 h,除阴性对照外,每孔加入MAP-2多克隆抗体稀释液,室温孵育1 h后4℃冰箱过夜,PBS漂洗。避光环境下,加FITC标记山羊抗小鼠IgG抗体稀释液,室温孵育3 h,PBS洗3次,每次5 min。加入DAPI稀释液,室温静置10 min,PBS漂洗,将细胞置于荧光显微镜下观察,拍照。
将皮层神经细胞按3×102·L-1的密度接种于96孔板,置于CO2培养箱内培养7 d,培养条件为37℃、5% CO2、95%空气、饱和湿度,分为6组复制模型,Na2S2O4的浓度依次为40、20、10、5、2.5、0 mmol·L-1,用Na2S2O4无糖Earle’s液继续培养,置于37℃、5% CO2、95%空气及饱和湿度条件的培养箱中缺糖缺氧损伤2 h后,替换为神经元培养基培养1 h。采用MTT法检测细胞存活率,酶标仪测定各孔吸光度(OD),计算细胞相对存活率。
2.3 细胞MDA含量、SOD的活性及NO释放量检测原代皮层神经元按1×103·L-1接种于明胶包被的6孔板中培养7 d,分为正常组、模型组、给药组(0.82、4.09、8.18、25.6 mol·L-1),正常组和模型组每孔加入等量的神经培养液,给药组设3个平行孔,置于CO2培养箱内培养24 h后复制OGD/Rep损伤模型。造模结束后收集培养液,按照试剂盒说明书以硝酸还原酶法检测计算NO释放量;每孔加1 mL双蒸水,反复冻融裂解细胞,观察有无完整细胞,收集细胞裂解液,按照试剂盒说明书检测计算细胞内MDA及SOD的含量。
2.4 Western blot检测Bax、Bcl-2、caspase-3蛋白表达造模结束后,弃上清液,加入100 μL细胞裂解液,收集细胞,冰浴裂解5 min,收集细胞裂解液,4℃ 14 000 r·min-1离心5 min,取上清液,BSA方法测定蛋白浓度。于沸水中煮5~10 min使蛋白变性后,以含30~60 μg蛋白的溶液体积为上样量进行SDS-聚丙烯酰胺凝胶电泳,以半干转法将蛋白质转移到硝酸纤维素膜,将膜用含5%脱脂牛奶的TBST封闭液封闭1 h后,一抗Bax(1 :1 000)、Bcl-2(1 :1 000)、caspase-3(1 :1 000)室温孵育2 h,二抗辣根过氧化物酶标记抗小鼠IgG(H+L) (1 :2000)及驴抗山羊IgG(H+L) (1 :2000)室温孵育1 h,化学发光试剂显色后,UVP凝胶成像系统成像记录,利用Image J进行图像灰度值处理。
2.5 统计学分析数据符合正态分布,方差齐者用one-factor ANOVA分析,组间比较用LSD检验;数据符合正态,方差不齐者用Tamhane’ T2检验。
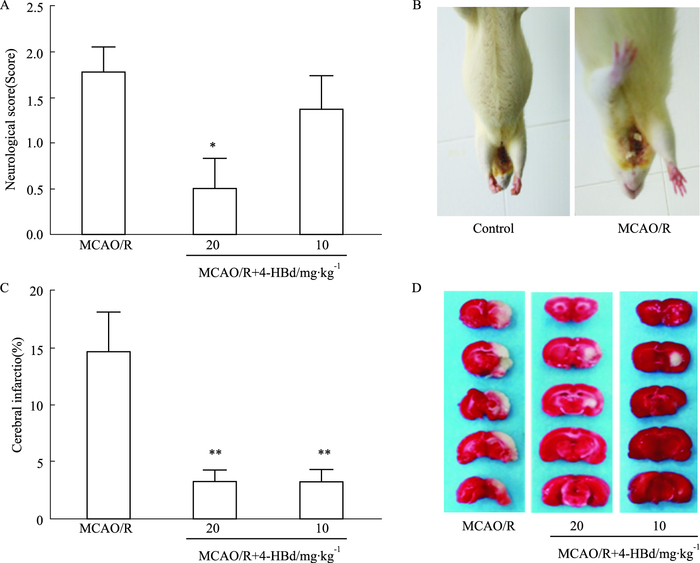
3 结果 3.1 4-HBd对MCAO/R模型大鼠神经病学评分的影响如Fig 2所示,与模型组比较,天麻成分4-HBd 20 mg·kg-1剂量组可明显降低模型大鼠的神经病学评分,差异有统计学意义(P<0.05);天麻成分4-HBd(20、10 mg·kg-1)剂量组均能明显降低模型大鼠的脑梗死体积,差异具有统计学意义(P<0.01)。
|
| Fig 2 Effects of 4-hydroxybenzaldehyde on neurological score and infarct volume in brain tissues of MCAO/R rats (x±s, n=6) Effects of 4-hydroxybenzaldehyde treatment on neurological score (A), neurological changes (B), cerebral infarction rate (C) and infarct size (D) in MCAO/R rats. *P < 0.05, **P < 0.01 vs MCAO/R group |
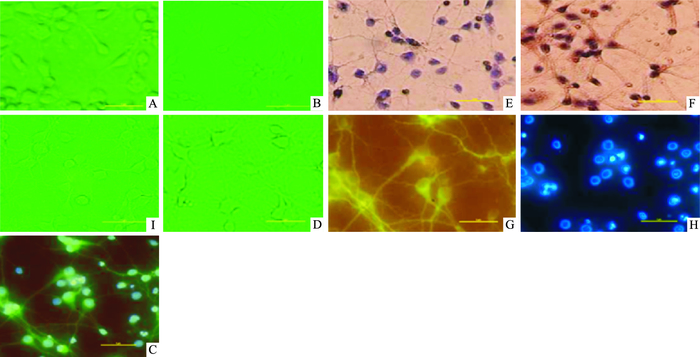
于倒置显微镜下观察原代皮层神经元培养d 2 (Fig 3A)、d 3 (Fig 3B)、d 5 (Fig 3C)、d 7 (Fig 3D)形态,并通过NSE鉴定。培养7 d的神经元的细胞质、轴突和树突呈棕黄色(Fig 3E),表明该细胞为神经元,经过计数神经元的纯度能够达到90%以上(Fig 3F);通过MAP-2鉴定,FITC和DAPI免疫荧光染色,在一定波长的荧光下胞质会发绿色荧光(Fig 3G),DAPI染色的所有细胞核发蓝色荧光(Fig 3I),合并图见Fig 3H,用图像分析软件分析,其纯度达90%以上,可用于实验研究。
|
| Fig 3 Morphology observation and identification of rat primary cortical neurons Primary cortical neuron morphology, rats cultured for 2 d (A), 3 d (B), 5 d (C), 7d (D); primary cortical neurons morphology, rats stained with NSE for negative control (E), normal control (F); analysis of MAP-2 protein expression and DAPI in primary cortical neuron morphology, rat immunofluorescence for MAP-2 (G), DAPI (H), Merge (I). |
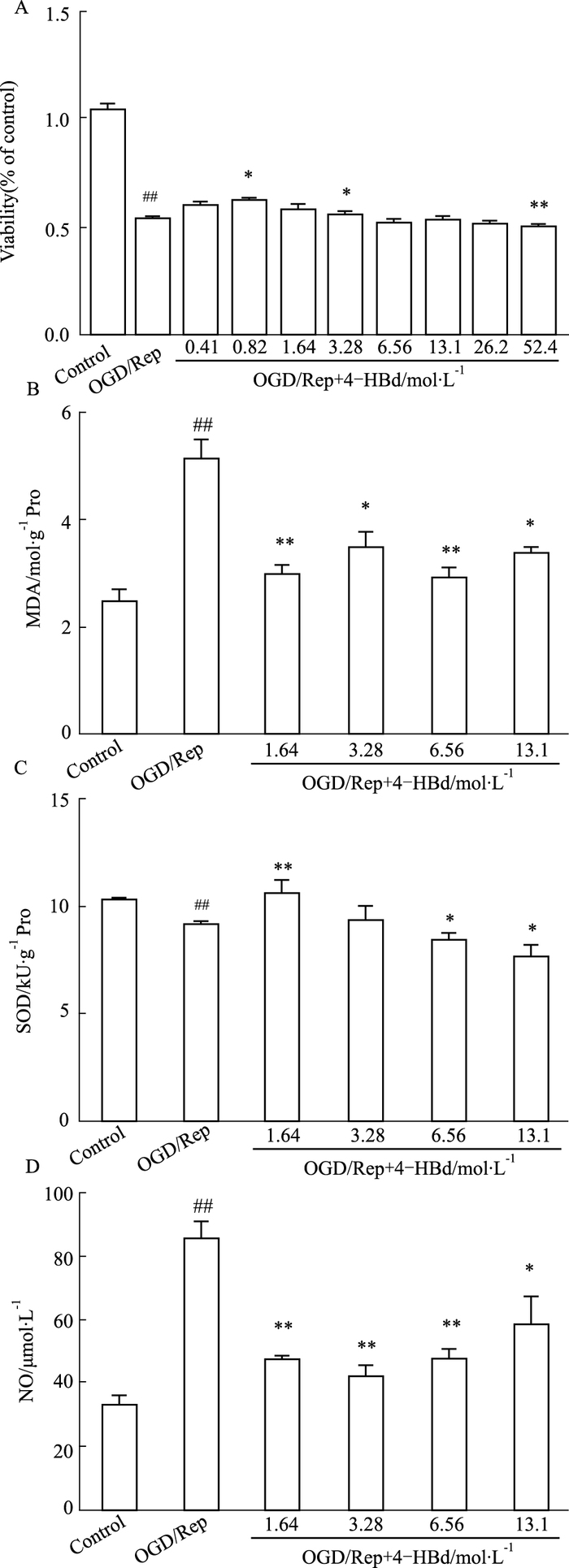
与模型组比较,天麻成分4-HBd(0.41、0.82、1.64、3.28、6.56、13.1 mol·L-1)组可提高OGD/Rep损伤的原代皮层神经元的存活率,差异有统计学意义(P<0.01或P<0.05),见Fig 4A;与模型组(OGD/Rep)比较,4-HBd(1.64、3.28、6.56、13.1 mol·L-1)组均能减少MDA的含量,与模型组比较,差异有统计学意义(P<0.01或P<0.05),见Fig 4B;4-HBd各组均能提高SOD活性,与模型组比较,差异有统计学意义(P<0.01或P<0.05),见Fig 4C;4-HBd各组均能减少NO的释放,与模型组比较,差异有统计学意义(P<0.01或P<0.05),见Fig 4D。
|
| Fig 4 Effects of 4-hydroxybenzaldehyde on primary cortex neuron rate (A) and MDA (B), SOD (C), NO (D) to OGD/Rep injury (x±s, n=6) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs OGD/Rep group |
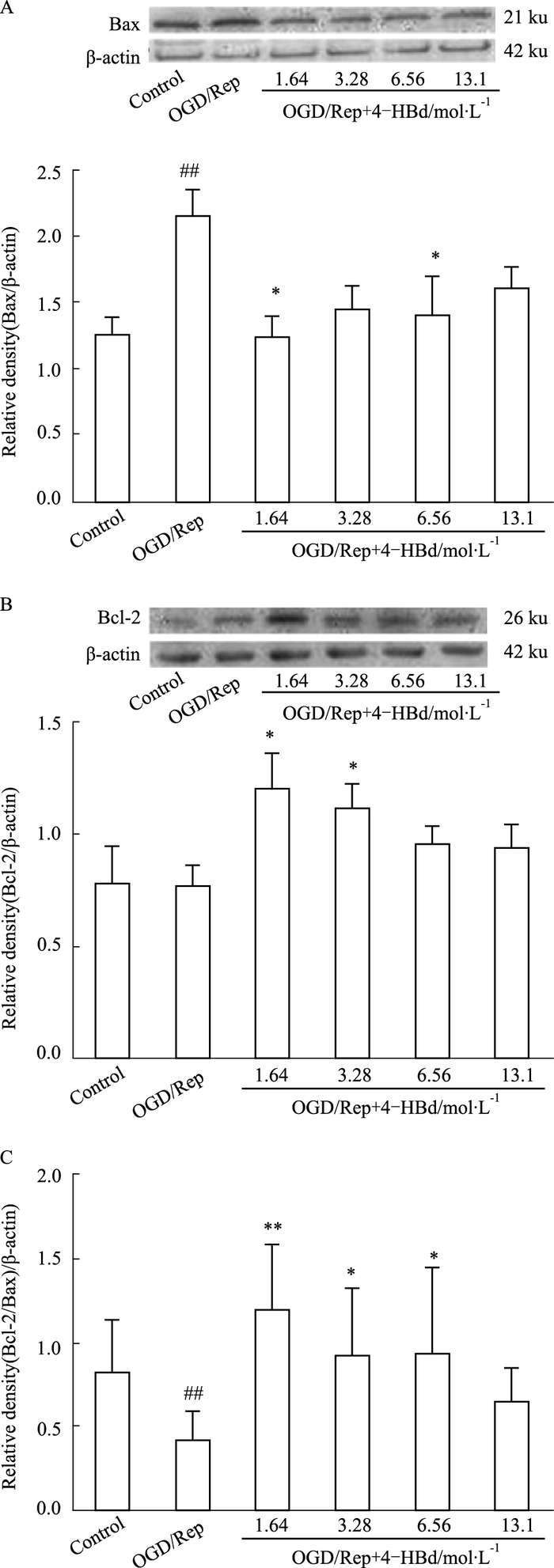
与模型组(OGD/Rep)比较,天麻成分4-HBd(1.64、6.56 mol·L-1)组下调Bax蛋白的表达,差异有统计学意义(P<0.05),见Fig 5A;4-HBd(1.64、3.28 mol·L-1)组上调Bcl-2蛋白的表达,差异有统计学意义(P<0.05),见Fig 5B;4-HBd(1.64、3.28、6.56 mol·L-1)组Bcl-2/Bax蛋白的比例上升,差异有统计学意义(P<0.01或P<0.05),见Fig 5C。
|
| Fig 5 Effects of 4-hydroxybenzaldehyde on cortical neurons Bax (A), Bcl-2 (B) protein and Bcl-2/Bax (C)(x±s, n=6) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs OGD/Rep group |
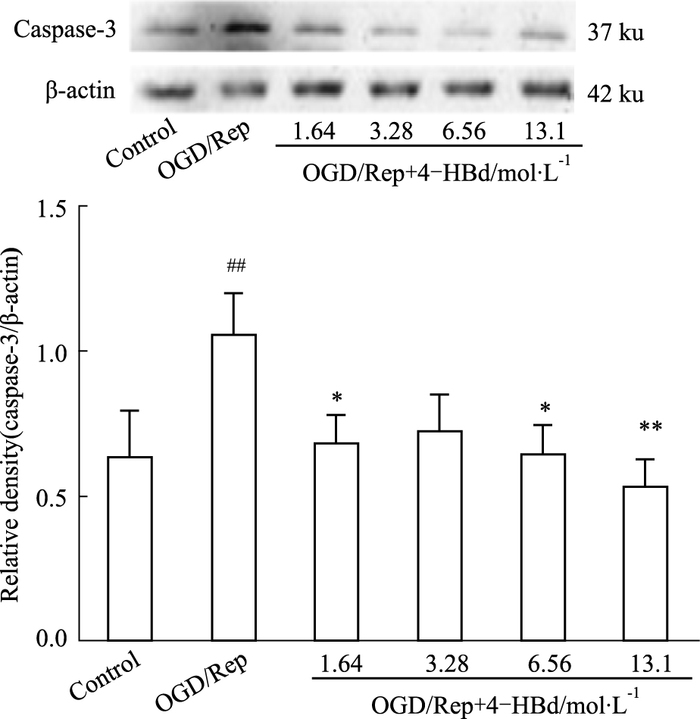
如Fig 6所示,与模型组(OGD/Rep)比较,天麻成分4-HBd(1.64、6.56、13.1 mol·L-1)组下调caspase-3蛋白的表达,差异有统计学意义(P<0.01或P<0.05)。
|
| Fig 6 Effect of 4-hydroxybenzaldehyde on cortical neurons caspase-3 protein (x±s, n=6) ##P < 0.01 vs control group; *P < 0.05, **P < 0.01 vs OGD/Rep group |
在脑缺血发生过程中,溶栓药物的超时间窗使用、血栓脱落、血栓自溶以及缺血区侧支循环的建立等都会造成CIRI。CIRI发生后,缺血中心区神经细胞发生坏死,而缺血半暗带神经细胞则以凋亡为主要死亡方式[12],若药物能够阻止缺血半暗带神经细胞的凋亡,将对CIRI的修复产生积极的意义。
神经病学评分通过模型大鼠体征异常变化判断神经功能缺损的程度,TTC染色能够直观地显示模型大鼠脑梗死的区域,并可通过测定脑梗死体积的大小,反映脑损伤程度。天麻成分4-HBd能降低MCAO/R模型大鼠的神经病学评分和脑组织梗死体积,提示其对CIRI有保护作用。
NSE表达于神经元胞质和突起,在突起及胞质内有棕黄色颗粒状沉积物,在非神经细胞均没有表达。MAP-2表达于树突轴心,是神经元特异性的细胞骨架蛋白,可作为神经细胞标记物。本实验采用MAP-2和NSE免疫荧光法鉴定神经元,经鉴定神经细胞的纯度达到90%以上,可满足实验用细胞的需求。
脑组织缺血缺氧时,SOD活性下调,再灌注时可产生大量氧自由基(reactive oxygen species,ROS),并使缺血期因氧耗竭而停止的烷自由基向脂质过氧化自由基的转化得以延续,从而产生一些脂类过氧化中间产物,如MDA含量增加。此外,大量增加的ROS超出了SOD等酶的防御清除能力,导致脂质过氧化,进一步破坏线粒体膜的完整性,细胞功能遭破坏,引发脑损伤。同时,在脑缺血/再灌注损伤情况下,神经元型NOS(neuronal NOS,nNOS)介导早期神经元损伤,nNOS被催化产生NO,NO在高浓度时可抑制线粒体电荷传递系统的酶,从而抑制细胞呼吸和能量代谢,NO还可与自由基反应形成一系列高反应性的有毒基团,通过脂质过氧化作用、酶灭活以及DNA硝化作用,导致神经元的死亡[13]。研究结果显示,4-HBd能明显提高OGD/Rep损伤模型细胞的存活率、SOD的活性,减少模型细胞MDA的含量、NO的释放量,提示其有保护OGD/Rep损伤神经细胞的作用。
CIRI损伤过程中,缺血半暗带神经细胞以凋亡为主要死亡方式,主要由线粒体凋亡通路介导。在线粒体凋亡通路中Bax与Bcl-2是重要的一对互相拮抗的凋亡相关蛋白,Bcl-2/Bax的比值决定凋亡启动与否,进而激活细胞凋亡下游的caspase-3、caspase-6等细胞凋亡。Caspase家族是一类凋亡调控蛋白,caspase-3是凋亡过程中最重要的蛋白酶,是caspase级联“瀑布”下游最关键的执行者。Caspase-3通常于正常细胞中以酶原形式存在,凋亡因素诱导其活化后细胞骨架蛋白及DNA修复酶等,细胞形态发生变化后最终导致细胞凋亡[14]。本研究结果显示,4-HBd能下调OGD/Rep损伤模型细胞Bax蛋白、上调模型细胞Bcl-2蛋白的表达、上调Bcl-2/Bax的比例,并最终下调模型细胞caspase-3蛋白的表达,提示其有抑制神经细胞凋亡的作用。
综上所述,天麻成分4-HBd对MCAO/R模型大鼠的CIRI有保护作用,其保护机制可能与提高神经细胞SOD的活性、减少MDA的含量、降低NO的释放、下调Bax蛋白表达、上调Bcl-2蛋白表达、下调caspase-3蛋白表达,进而对抗神经细胞凋亡有关。
( 致谢: 本研究所有实验均在云南中医学院药理学教研室进行,感谢教研室老师们的倾力协助!)
| [1] | 杨志宏, 胡亚, 孙晓波. JAK/STAT信号转导通路及中药干预在缺血性脑卒中的研究进展[J]. 中国药理学通报, 2016, 32(7): 889-94. Yang Z H, Hu Y, Sun X B. A review on JAK/STAT signaling pathway in cell apoptosis of ischemic stroke and intervention of TCM medicine[J]. Chin Pharmacol Bull, 2016, 32(7): 889-94. |
| [2] | Duan X, Wang W, Liu X, et al. Neuroprotective effect of ethyl acetate extract from gastrodia elata against transient focal cerebral ischemia in rats induced by middle cerebral artery occlusion[J]. J Tradit Chin Med, 2015, 35(6): 671-8. doi:10.1016/S0254-6272(15)30158-8 |
| [3] | 段小花, 李资磊, 杨大松, 等. 昭通产天麻化学成分研究[J]. 中药材, 2013, 36(10): 1608-11. Duan X H, Li Z L, Yang D S, et al. Study on the chemical constituents of Gastrodia elata[J]. J Chin Med Mater, 2013, 36(10): 1608-11. |
| [4] | 刘珊珊, 向彬, 郭营营, 等. 天麻成分对羟基苯甲醛抗炎作用及机制研究[J]. 中国民族民间医药, 2016, 25(9): 16-9. Liu S S, Xiang B, Guo Y Y, et al. Study of anti-inflammation of p-hydroxybenzaldehyde from Gastrodia elata Blume[J]. Chin J Ethnomed Ethnopharm, 2016, 25(9): 16-9. |
| [5] | 李秀芳, 代蓉, 李国花, 等. 天麻成分对羟基苯甲醛抗血小板聚集作用及急性毒性研究[J]. 天然产物研究与开发, 2013, 25(3): 317-20. Li X F, Dai R, Li G H, et al. Anti-platelet aggregation function and acute toxicity of 4-hydroxybenzylaldehyde (4-HBAL) extracted from Gastrodia elata Blume[J]. Nat Prod Res Dev, 2013, 25(3): 317-20. |
| [6] | Dai R, Wang T, Si X, et al. Vasodilatory effects and underlying mechanisms of the ethyl acetate extracts from Gastrodia elata[J]. Can J Physiol Pharmacol, 2017, 95(5): 564-71. doi:10.1139/cjpp-2016-0407 |
| [7] | Longa E Z, Weinstein P R, Carlson S, et al. Reversible middle cerebral artery occlusion without craniectomy in rats[J]. Stroke, 1989, 20(1): 84-91. doi:10.1161/01.STR.20.1.84 |
| [8] | 何芳雁, 韩春妮, 李艳, 等. 制作线栓法大鼠脑缺血再灌注模型的要点及体会[J]. 实验动物科学, 2013, 30(4): 46-8. He F Y, Han C N, Li Y, et al. Research and experience on making rat model of middle cerebral artery occlusion/reperfusion by the thread occlusion method[J]. Lab Anim Sci, 2013, 30(4): 46-8. |
| [9] | 赖文芳, 张小琴, 洪海棉, 等. 红景天苷对大鼠局灶性脑缺血/再灌注损伤的神经保护作用[J]. 中国药理学通报, 2015, 31(6): 775-80. Lai W F, Zhang X Q, Hong H M, et al. Experimental studies on the effects of salidroside in rats with focal cerebral ischemia-reperfusion injury[J]. Chin Pharmacol Bull, 2015, 31(6): 775-80. |
| [10] | Bederson J B, Pitts L H, Tsuji M, et al. Rat middle cerebral artery occlusion: evaluation of the model and development of a neurologic examination[J]. Stroke, 1986, 17(3): 472-6. doi:10.1161/01.STR.17.3.472 |
| [11] | Choi B I, Park D, Lee S H, et al. Neurobehavioural deficits correlate with the cerebral infarction volume of stroke animals: a comparative study on ischaemia-reperfusion and photothrombosis models[J]. Environ Toxicol Pharmacol, 2012, 33(1): 60-9. doi:10.1016/j.etap.2011.11.001 |
| [12] | Matsumori Y, Hong S M, Fan Y, et al. Enriched environment and spatial learning enhance hippocampal neurogenesis and salvages ischemic penumbra after focal cerebral ischemia[J]. Neurobiol Dis, 2006, 22(1): 187-98. doi:10.1016/j.nbd.2005.10.015 |
| [13] | Tahir A, Ashfaq M, Aqeel A K, et al. Imbalance of serum trace elements in acute leukemia contributes to pro and anti-oxidative stress via ROS and SOD regulation: a population based study[J]. Trace Elements Electrolytes, 2014, 32(1): 22-7. |
| [14] | Lari P, Abnous K, Imenshahidi M, et al. Evaluation of diazinon-induced hepatotoxicity and protective effects of crocin[J]. Toxicol Ind Health, 2015, 31(4): 367-76. doi:10.1177/0748233713475519 |

