


2. 山西医科大学,山西 太原 030001
2. School of Public Health, Shanxi Medical University, Taiyuan 030001, China
糖尿病可以引起心血管系统发生相应的结构和功能改变,其中对冠状动脉(coronary artery, CA)的损伤会引起糖尿病冠心病(coronary heart disease, CHD)。有研究报道,糖尿病病人患CHD的风险会比其他疾病明显增加[1],而且高血糖能够损伤CA血管平滑肌细胞(vascular smooth muscle cell, VSMC)电压依赖性钾通道(voltage-gated K+ channels, Kv)[2]。在VSMC上主要表达的钾通道中,Kv是表达量最高的[3-4],而且最新研究发现,Kv1.5对调节CA供血是必需的[5]。
槲皮素(quercetin, quer)作用广泛,可对抗氧化反应[6-7]、抑制炎症[8]等。研究发现,如果在膳食中摄入比较多的槲皮素,能够大幅度降低心血管疾病的风险[9]。而且我们课题组前期离体实验发现,槲皮素可舒张大鼠CA,与其增大Kv电流有关[10]。有研究报道,饮食中较多摄入黄酮可降低糖尿病及相关心血管疾病发生风险[11-12],然而,关于槲皮素是否会对糖尿病引起的大鼠CA损伤产生影响,尚未见相关研究。
综上所述,糖尿病能够通过抑制CA VSMC Kv引起CA损伤,而槲皮素舒张大鼠CA与增大CA VSMC Kv电流有关,并且Kv1.5对调节CA供血至关重要。所以,我们提出实验假设,槲皮素是否能够通过增大Kv1.5,改善糖尿病大鼠CA损伤。因此在本课题中,我们综合应用离体心脏灌流、CA张力测定、膜片钳电生理和PCR实验,从Kv1.5角度研究槲皮素在保护糖尿病引起大鼠CA损伤中的作用。
1 材料 1.1 药品与试剂槲皮素购自Sigma公司,美国;其余试剂为分析纯,国产。
1.2 实验动物30只SD大鼠,♂,7~8周龄,体质量(220±20) g,购自山西医科大学动物中心。
1.3 仪器血管张力测定仪:澳大利亚DMT公司;膜片钳放大器:美国AXON公司;离体心脏灌流装置:泰盟科技有限公司;PCR仪:美国Bio-Rad C1000 TM and CFX96TM Real-time system。
2 方法 2.1 糖尿病大鼠模型的制备与分组将大鼠(30只)随机分组,空白对照组(10只):生理盐水,i.p.;糖尿病组(20只):链脲佐菌素,i.p.,每日100 mg·kg-1,连续2 d给药。2周后,如果血糖>0.0167 mol·L-1,认为糖尿病模型制备成功,成功造模20只。然后,将这部分大鼠继续分组:糖尿病组(10只,生理盐水,i.g.,8周)和槲皮素干预组(10只,每日槲皮素50 mg·kg-1,i.g.,连续8周)。
2.2 离体心脏灌流大鼠麻醉后处死,开胸并快速将大鼠心脏连同主动脉根部剪下,利用主动脉根部将心脏固定于灌流装置上,记录每分钟的CA流量(coronary flow,CF)。
2.3 CA张力测定参照本课题组前期方法[10, 13],把大鼠CA固定到张力测定仪上,正式实验前需要验证血管的活性,用KCl(60 mmol·L-1)收缩CA,当收缩幅度能达到3 mN以上,且坪台能够稳定时,可以继续实验。分别向浴槽内加入不同的药物:KCl(60 mmol·L-1)、Kv阻断剂4-氨基吡啶(4-aminopyridine, 4-AP, 10-4 mol·L-1)、KCa阻断剂蝎毒素(iberiotoxin, Iber, 10-3 mol·L-1)、KATP阻断剂格列本脲(glibenclamide, Glib, 10-4 mol·L-1)和KIR阻断剂氯化钡(barium chloride, BaCl2, 10-3 mol·L-1),观察CA的收缩反应并记录其张力数值。
2.4 Kv电流记录方法采用分开两步进行酶解的方法得到CA VSMC,对细胞进行序列电压刺激(-80 mV~ +60 mV,间隔为10 mV),或单一给予+60 mV刺激),记录Kv电流。不论是序列电压刺激还是单一电压刺激,均选择最后50 ms的电流值,并且取其平均值,CA VSMC分离方法及Kv记录方法参照文献[10]。
2.5 RT-PCR检测大鼠CA Kv1.5 mRNA表达大鼠处死后,显微镜下急性分离3组大鼠CA,并快速将CA放入液氮中保存,观察3组大鼠CA Kv1.5 mRNA变化,内参为β-actin,具体方法参照文献[14]。Kv1.5引物,正向: 5′-ATGCAGGGTCACTCCATC-3′,反向:5′-GGCTTCTCCTCTTCCTTG-3′;β-actin引物,正向:5′-AAGATCCTGACCGAGCGTGG-3′,反向:5′-CAGCACTGTGTTGGCATAGAGG-3′。
2.6 统计学方法所有数据用x±s表示,Graphpad prism6作图,应用两因素重复测量方差分析。
3 结果 3.1 槲皮素对糖尿病大鼠CF的影响正常对照组CF为(7.81±0.62) mL·min-1,糖尿病组CF明显下降,其值为(6.13±0.45) mL·min-1,给糖尿病大鼠膳食补充槲皮素8周后,其CF有所增加,其值为(7.14±0.52) mL·min-1,见Tab 1。
| Group | CF/ mL·min-1 |
| Control | 7.81±0.62 |
| Diabetes | 6.13±0.45* |
| Diabetes+quer | 7.14±0.52*# |
| *P<0.05 vs control; #P<0.05 vs diabetes | |
KCl对空白组大鼠CA的最大收缩张力为(3.64±0.27) mN;糖尿病组大鼠的收缩幅度明显增强,达到(5.12±0.44) mN;膳食补充槲皮素可减弱糖尿病大鼠CA对KCl的收缩反应,其收缩幅度为(4.35±0.16) mN。与糖尿病组相比,“糖尿病+槲皮素”组CA对Kv通道阻断剂4-AP的收缩幅度明显低于单纯糖尿病组,证实槲皮素减轻糖尿病所致CA损伤的作用与激活Kv有关,见Tab 2。
| Vasoconstrictor | KCl | 4-AP | Iber | BaCl2 | Glib |
| Control | 3.64±0.27 | 3.01±0.45 | 3.17±0.36 | 3.78±0.42 | 3.46±0.52 |
| Diabetes | 5.12±0.44* | 4.21±0.51* | 4.37±0.27* | 4.64±0.39* | 4.76±0.47* |
| Diabetes+quer | 4.35± 0.16*# | 3.24±0.40# | 4.16±0.27* | 4.30±0.32* | 4.36±0.17* |
| *P<0.05 vs control; #P<0.0.5 vs diabetes | |||||
如Fig 1所示,空白对照组、糖尿病组、“糖尿病+槲皮素”组大鼠CA VSMC Kv最大电流密度分别为(54.52±4.15) pA·pF-1、(22.62±3.24) pA·pF-1和(41.40±2.45) pA·pF-1。与空白组相比,糖尿病组CA VSMC Kv电流明显减小,差异有统计学意义;糖尿病组补充槲皮素后,其CA VSMC Kv电流降低幅度有所减弱。
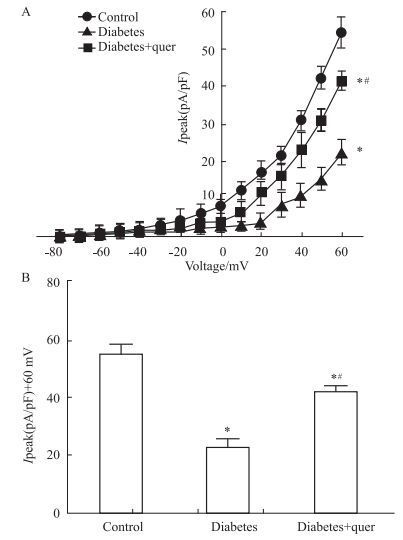
|
| Fig 1 The Kv currents on isolated rat CA VSMC (n=6) A: The I-V relationship curve of Kv currents when the currents were evoked by a series of depolarizing pulses (from -80 mV to +60 mV); B: The Kv currents were recorded when the currents were evoked by +60 mV depolarizing pulses. *P < 0.05 vs control; #P < 0.0.5 vs diabetes. |
如Fig 2所示,Kv1.5 mRNA在3组大鼠CA的相对表达量(与β-actin表达的比值)依次为:空白对照组表达量最多,“糖尿病+槲皮素”组次之,糖尿病组表达量最少。
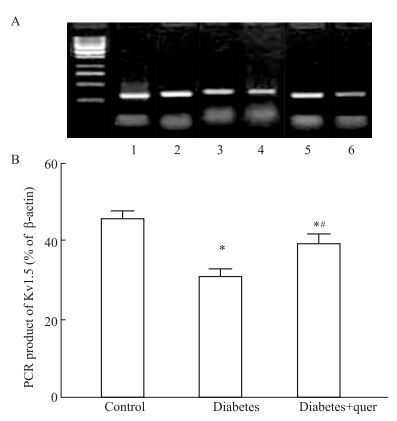
|
| Fig 2 The mRNA expression of Kv 1.5 on rat CA (n=6) A: The photograph of electrophoresis of RT-PCR amplification of Kv1.5 mRNA on rat CA; B: The mRNA expression of Kv1.5 normalized to the amount of β-actin. 1: β-actin of control, 2: Kv1.5 of control, 3: β-actin of diabetes+quer, 4: Kv1.5 of diabetes+quer, 5:β-actin of diabetes, 6: Kv1.5 of diabetes.*P < 0.05 vs control; #P < 0.05 vs diabetes. |
CA给心肌细胞提供养分,其管壁主要是VSMC。在本实验中我们发现,糖尿病组的CF明显低于正常组,在糖尿病大鼠的饮食中补充8周槲皮素后,其CF有所回升,说明糖尿病削弱了大鼠CA的舒张能力。而且该结论在离体CA张力测定中也得到了进一步证实,糖尿病组大鼠CA对KCl的收缩反应更敏感,而补充槲皮素后得到了好转。此外我们发现,糖尿病补充槲皮素组CA对Kv通道阻断剂4-AP的收缩反应明显低于糖尿病组,而对其他几种阻断剂没有明显差异,这提示槲皮素减轻糖尿病所致CA损伤与激活Kv有关。
课题组前期研究发现,槲皮素可舒张正常SD大鼠CA,该作用与激活大鼠CA VSMC Kv有关[10]。因此,为了进一步证实槲皮素对糖尿病所引起CA损伤的改善作用是否也与Kv相关,我们记录了3组大鼠CA VSMC Kv电流,其最大电流密度分别为:空白对照组(54.52±4.15) pA·pF-1,糖尿病组(22.62±3.24) pA·pF-1,糖尿病+槲皮素组(41.40±2.45) pA·pF-1。有研究报道,高浓度葡萄糖可损伤CA VSMC Kv[2],在本实验中我们也发现了与之相一致的现象,糖尿病组Kv电流较空白对照组明显降低,膳食补充槲皮素可以得到改善。
在目前已经明确的钾离子通道中,VSMC上表达最多的是Kv,Kv在调节CA张力方面起着关键性的作用[15],而且最新研究发现Kv1.5对调节CA供血是必需的[5]。在本实验中,我们进一步通过RT-PCR实验测定CA VSMC Kv1.5 mRNA表达变化,得出了与前述实验相吻合的结论,同时也证明槲皮素是通过激活Kv1.5起到了对糖尿病所导致的大鼠CA损伤的保护作用。本课题的实验结果将为临床使用槲皮素预防和治疗糖尿病CA损伤提供基础依据。
| [1] | Wang R X, Shi H F, Chai Q, et al. Molecular mechanisms of diabetic coronary dysfunction due to large conductance Ca2+-activated K+ channel impairment[J]. Chin Med J, 2012, 125(14): 2548-55. |
| [2] | Liu Y, Terata K, Rusch N J, et al. High glucose impairs voltage-gated K(+) channel current in rat small coronary arteries[J]. Circ Res, 2001, 89(2): 146-52. doi:10.1161/hh1401.093294 |
| [3] | Ko E A, Han J, Jung I D, et al. Physiological roles of K+ channels in vascular smooth muscle cells[J]. J Smooth Muscle Res, 2008, 44(2): 65-81. doi:10.1540/jsmr.44.65 |
| [4] | Cox R H. Molecular determinants of voltage-gated potassium currents in vascular smooth muscle[J]. Cell Biochem Biophys, 2005, 42(2): 167-95. doi:10.1385/CBB:42:2:167 |
| [5] | Ohanyan V, Yin L, Bardakjian R, et al. Requisite role of Kv1.5 channels in coronary metabolic dilation[J]. Circ Res, 2015, 117(7): 612-21. doi:10.1161/CIRCRESAHA.115.306642 |
| [6] | 卢宁, 韩吉春, 任博雪, 等. 二氢槲皮素预处理对心肌缺血/再灌注损伤抗氧化作用的影响[J]. 中国药理学通报, 2017, 33(4): 487-92. Lu N, Han J C, Ren B X, et al. Antioxidation effect of dihydroquercetin pretreatment in isolated rat hearts during myocardial ischemia reperfusion injury[J]. Chin Pharmacol Bull, 2017, 33(4): 487-92. |
| [7] | 刘红亮, 胡磊, 王靖凯, 等. 槲皮素对H2O2损伤PCI2细胞的保护效果与机制[J]. 中国药理学通报, 2014, 30(3): 373-7. Liu H L, Hu L, Wang J K, et al. Protective effects of quercetin on PCI2 cells with H2O2-induced oxidative damage[J]. Chin Pharmacol Bull, 2014, 30(3): 373-7. |
| [8] | Mahmoud M F, Hassan N A, El Bassossy H M, et al. Quercetin protects against diabetes-induced exaggerated vasoconstriction in rats: effect on low grade inflammation[J]. PLoS One, 2013, 8(5): e63784. doi:10.1371/journal.pone.0063784 |
| [9] | Zamora-Ros R, Jimenez C, Cleries R, et al. Dietary flavonoid and lignan intake and mortality in a Spanish cohort[J]. Epidemiology, 2013, 24(5): 726-33. doi:10.1097/EDE.0b013e31829d5902 |
| [10] | Hou X, Liu Y, Niu L, et al. Enhancement of voltage-gated K+ channels and depression of voltage-gated Ca2+ channels are involved in quercetin-induced vasorelaxation in rat coronary artery[J]. Planta Med, 2014, 80(6): 465-72. doi:10.1055/s-00000058 |
| [11] | Jacques P F, Cassidy A, Rogers G, et al. Higher dietary flavonol intake is associated with lower incidence of type 2 diabetes[J]. J Nutr, 2013, 143(9): 1474-80. doi:10.3945/jn.113.177212 |
| [12] | Kim J H, Kang M J, Choi H N, et al. Quercetin attenuates fasting and postprandial hyperglycemia in animal models of diabetes mellitus[J]. Nutr Res Pract, 2011, 5(2): 107-11. doi:10.4162/nrp.2011.5.2.107 |
| [13] | 房龙梅, 侯晓敏, 杨蓉, 等. 阿魏酸对离体大鼠冠状动脉的舒张作用及机制探讨[J]. 中国药理学通报, 2016, 32(4): 554-8. Fang L M, Hou X M, Yang R, et al. Vasodilatory effect of Ferulic acid on in vitro rat coronary arter[J]. Chin Pharmacol Bull, 2016, 32(4): 554-8. |
| [14] | Chai Q, Xu X, Jia Q, et al. Molecular basis of dysfunctional Kv channels in small coronary artery smooth muscle cells of streptozotocin-induced diabetic rats[J]. Chin J Physiol, 2007, 50(4): 171-7. |
| [15] | Dick G M, Tune J D. Role of potassium channels in coronary vasodilation[J]. Exp Biol Med, 2010, 235(1): 10-22. doi:10.1258/ebm.2009.009201 |

