


2. 沈阳医学院 病原生物学教研室,辽宁省环境污染与微生态重点实验室,辽宁 沈阳 110034
2. Dept of Pathogen Biology, Key Lab of Environmental Pollution and Microecology of Liaoning Province, Shenyang Medical College, Shenyang 110034, China
乳腺癌是乳腺上皮组织细胞发生癌变所形成的,近年来其发病率逐年上升,并有年轻化的趋势[1]。乳腺癌的发生和发展与雌激素受体(estrogen receptor, ER)表达密切相关。雌激素信号经ER介导,刺激癌基因的表达,抑制抑癌基因的功能,引起癌变。临床上大多数乳腺癌患者为ER阳性,约占总发病率的70%以上。但是ER在乳腺癌中的作用机制还不是很明确,通过对ER的研究,阐明其在乳腺癌中的发病机制,并探究其在预防及治疗乳腺癌中的意义都十分重要[2-3]。
p21WAF1/CIP1属于细胞周期蛋白依赖性激酶抑制因子(cyclin dependent kinase inhibitor,CKI)家族,定位于6p21.2染色体,基因全长8.6 kb,编码164个氨基酸残基组成的蛋白质。p21WAF1/CIP1可以促使细胞周期停滞、促进细胞凋亡并抑制癌细胞的转移和侵袭[4]。
大量研究表明,组蛋白去乙酰化酶(histone deacetylase,HDAC)的异常可引发乳腺癌。而通过抑制HDAC的功能可以起到治疗肿瘤的目的[5-6]。辛二酰苯胺异羟肟酸(suberoylanilide hydroxamic acid,SAHA)为一种广谱HDAC抑制剂,近年来的研究证明其可抑制乳腺癌细胞增殖并引起细胞凋亡[7]。本文以乳腺癌ER阳性细胞系MCF-7为研究对象,探讨SAHA对ER阳性乳腺癌细胞增殖的分子机制。
1 材料与方法 1.1 材料人乳腺癌细胞株MCF-7由本实验室冻存;RPMI 1640培养液、胎牛血清、青霉素以及链霉素,购自美国Thermo公司;SAHA、人重组Leptin蛋白,购自美国Sigma-Aldrich公司;EZ ChIP试剂盒购自美国Thermo Fisher公司;HRP偶联多克隆抗体、抗β-actin抗体,购自美国Abcam公司;抗HDAC1单克隆抗体、抗乙酰化组蛋白H4多克隆抗体、抗组蛋白H4多克隆抗体、抗乙酰化组蛋白H3多克隆抗体、抗组蛋白H3多克隆抗体等购自美国Millipore公司;其他化学试剂购自美国Sigma-Aldrich公司。
1.2 方法 1.2.1 细胞培养人乳腺癌MCF-7细胞培养于含10%胎牛血清、100 kU·L-1青霉素、100 mg·L-1链霉素的RPMI 1640培养基中。
1.2.2 全细胞RNA提取和实时定量PCR将5×108·L-1乳腺癌MCF-7细胞接种于6孔板各孔中,细胞无血清同步化处理后,加入0.625 nmol·L-1 Leptin和10 μmol·L-1 SAHA与MCF-7细胞孵育24 h。Rneasy mini kit提取全细胞RNA,第一条链cDNA合成后,应用SYBR Green方法,以GAPDH为内参进行实时定量PCR反应。25 μL反应体系中包含1×SYBR Green Supermix试剂12.5 μL, 0.1 μmol·L-1上、下游引物各0.5 μL,2 μL cDNA(10 ng)和9.5 μL双蒸水。实时定量PCR扩增参数为:50℃ 2 min,95℃预变性2 min;95℃变性15 s,60℃延伸1 min,延伸后检测荧光信号,共40个循环。每个样品设置3个复孔,mRNA相对表达量按照2-△△Ct法计算。引物序列见Tab 1。
| Gene | Prime sequence |
| Cyclin D1 | Upstream 5′-GCAAGGCCTGAACCTGAGGA-3′ |
| Downstream 5′-GCCTTGGGGTCCATGTTCTG-3′ | |
| p21WAF1/CIP1 | Upstream 5′-ATGAAATTCACCCCCTTTCC-3′ |
| Downstream 5′-CCCTAGGCTGTGCTCACTTC-3′ | |
| Cyclin E1 | Upstream 5′-AGCGGTAAGAAGCAGAGCAG-3 |
| Downstream 5′-TTTGATGCCATCCACAGAAA-3′ | |
| CDK4 | Upstream 5′-GAAACTCTGAAGCCGACCAG-3′ |
| Downstream 5′-AGGCAGAGATTCGCTTGTGT-3′ | |
| CDK2 | Upstream 5′-CATTCCTCTTCCCCTCATCA-3′ |
| Downstream 5′-CAGGGACTCCAAAAGCTCTG-3′ | |
| HDAC1 | Upstream 5′-GGAAATCTATCGCCCTCACA-3′ |
| Downstream 5′-AACAGGCCATCGAATACTGG-3′ | |
| GAPDH | Upstream 5′-GAGTCAACGGATTTGGTCGT-3′ |
| Downstream 5′-GACAAGCTTCCCGTTCTCAG-3′ |
上述Leptin和SAHA处理后的MCF-7细胞经胰蛋白酶消化、离心后,取细胞团块经M-PER裂解液裂解,应用BCA法检测蛋白浓度。取20 μg各样品组蛋白进行SDS-PAGE电泳,PVDF转膜后,加入1:1 000稀释的羊抗HDAC1单克隆抗体、羊抗乙酰化组蛋白H3多克隆抗体、羊抗组蛋白H3多克隆抗体、羊抗乙酰化组蛋白H4多克隆抗体、羊抗组蛋白H4多克隆抗体和羊抗p21WAF1/CIP1多克隆抗体,4 ℃孵育过夜,以羊抗β-actin多克隆抗体作对照。加入1:5 000包被HRP的兔抗羊多克隆抗体,室温孵育1 h后,化学发光法测定蛋白含量。
1.2.4 DNA-ChIP将6×109·L-1的乳腺癌MCF-7细胞接种于100 mm培养皿中,血清饥饿同步化处理后,加入0.625 nmol·L-1 Leptin和10 μmol·L-1 SAHA共同培养24 h(培养方法与孵育时间同“1.2.2”)。经预冷PBS冲洗2次后,1 %戊二醛室温振荡固定10 min。1×甘氨酸室温中和5 min后,预冷PBS冲洗2次。用细胞铲刮掉培养皿中细胞,700×g离心5 min后,用含Micrococcal nuclease (10 unit·μL-1)的细胞裂解液溶解细胞。离心后,取上清液,分别与羊抗乙酰化组蛋白H3多克隆抗体和羊抗乙酰化组蛋白H4多克隆抗体4℃孵育过夜。加入Protein G Agarose和细胞IP孵育液4℃振荡作用1 h,5 000×g离心1 min,取Protein G Agarose细胞IP复合物,依次经低盐、高盐、LiCl、TE溶液冲洗后,经Elution Buffer洗脱、5 mol·L-1 NaCl 65℃去交联、DNA柱纯化后,所得沉淀即为ChIP产物。加入2.5 μL ChIP产物进行实时定量PCR分析,以GAPDH基因启动子片段为内参。
1.3 统计学处理应用SPSS 17.0软件完成Student’s t-test分析,进行统计学处理,结果以x±s表示,采用单因素方差分析方法。
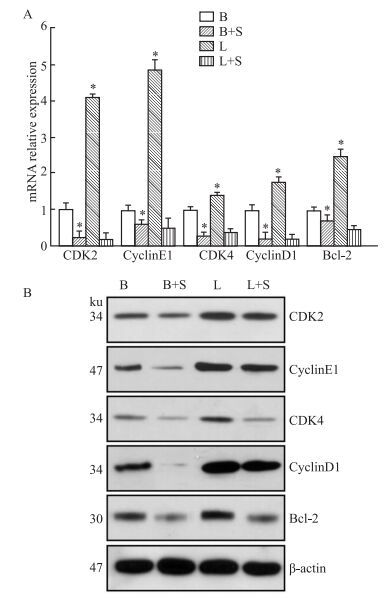
2 结果 2.1 SAHA通过调控乳腺癌细胞周期调控系统因子的表达而影响乳腺癌细胞生长Fig 1结果显示,将SAHA与乳腺癌MCF-7细胞作用后发现,SAHA明显抑制了乳腺癌细胞CDK2、CyclinE1、CDK4、CyclinD1 mRNA和蛋白的表达。经SAHA作用后,CDK2、CyclinE1、CDK4、CyclinD1都有不同程度的下降,而Leptin处理后,这些因子的表达都明显上升。另外,我们发现,凋亡调控因子Bcl-2的表达也发生了变化,SAHA抑制了其mRNA和蛋白的表达,而Leptin则诱导了其表达。
|
| Fig 1 Effects of SAHA on expressions of cell cycle regulators in MCF-7 breast cancer cells A: Quantitative real-time PCR; B: Western blot. B: Basal; B+S: Basal+SAHA; L: Leptin; L+S: Leptin+SAHA. *P < 0.05 vs basal |
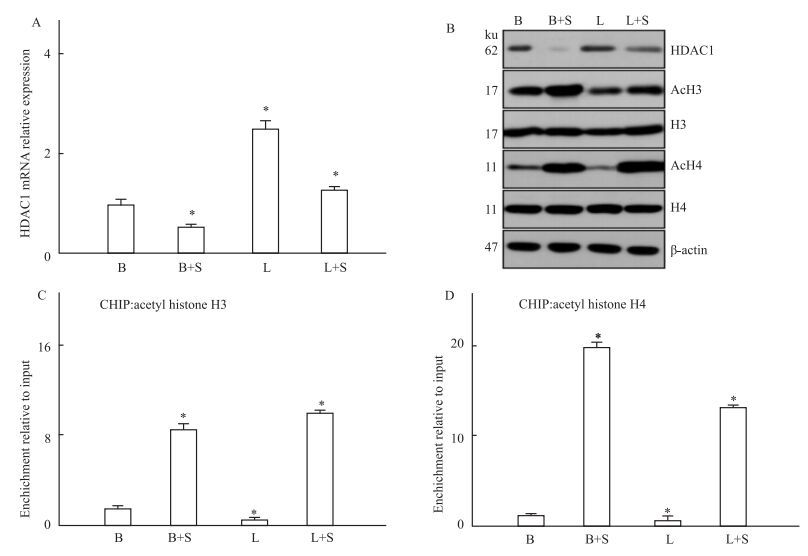
SAHA作用MCF-7细胞后对乙酰化水平的影响,结果见Fig 2,SAHA可抑制HDAC1 mRNA和蛋白的表达。而乙酰化组蛋白H3和H4的蛋白表达量在SAHA的作用下大幅上升,而作为细胞生长因子的Leptin则有相反的作用效果。DNA-CIhP实验证实了SAHA作用后,MCF-7细胞内与乙酰化H3和H4抗体结合的DNA物质大幅升高,而Leptin作用后,与乙酰化H3和H4抗体结合的DNA量明显减少。
|
| Fig 2 Effects of SAHA on acetylated levels in MCF-7 breast cancer cells A:Determination of HDAC1 by quantitative real-time PCR; B: Western blot; C: Determination of acetylated histone H3 by ChIP; D: Determination of acetylated histone H4 by ChIP. B: Basal; B+S: Basal+SAHA; L: Leptin; L+S: Leptin+SAHA. *P < 0.05 vs basal |
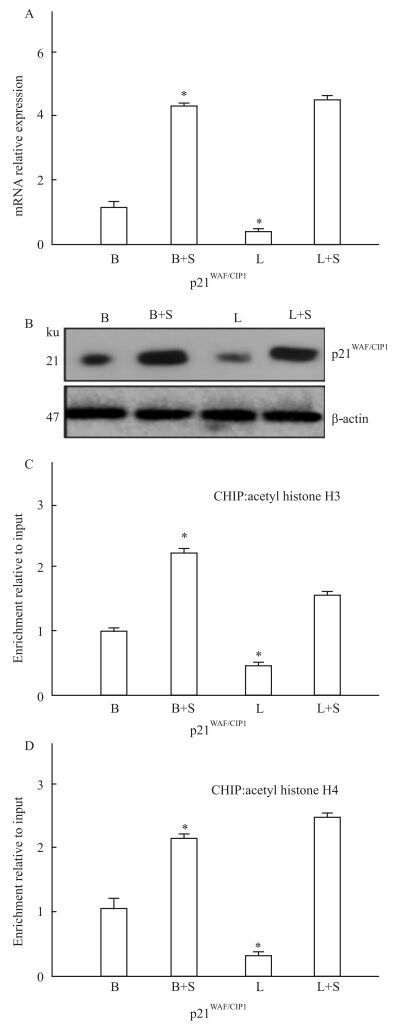
Fig 3结果表明,SAHA处理的乳腺癌MCF-7细胞中p21WAF/CIP1 mRNA及蛋白表达水平明显高于对照组细胞,而Leptin则抑制了p21WAF/CIP1的功能(Fig 2A、2B)。DNA-ChIP结果显示,SAHA作用MCF-7细胞后,p21WAF/CIP1启动子区域与乙酰化组蛋白H3、H4结合的染色质物质明显多于未处理细胞组,而同样Leptin处理后p21WAF/CIP1启动子区域结合的DNA量明显减少(Fig 2C、2D)。
|
| Fig 3 SAHA functions on specific regions of p21WAF/CIP1 to inhibit HDAC1 expressions A: Quantitative real-time PCR; B: Western blot; C: ChIP for AcH3;D: ChIP for AcH4. B: Basal; B+S: Basal+SAHA; L: Leptin; L+S: Leptin+SAHA. *P < 0.05 vs basal |
乳腺癌是女性最常见的恶性肿瘤之一,其发病率上升趋势明显。p21WAF1/CIP1是具有广泛激酶抑制活性的细胞周期抑制蛋白,与肿瘤的分化、浸润深度、增生和转移有关。HDAC的过度表达可使核心组蛋白高度去乙酰化,进而染色体发生凝聚,使相关基因转录受到抑制,引起癌变的发生[8-9]。HDAC抑制剂因此被视为一类有广阔应用前景的抗癌药物[10-12]。SAHA作为组蛋白去乙酰化酶抑制剂,具有良好的抗肿瘤作用。在本研究中,我们应用SAHA与乳腺癌MCF-7细胞作用,发现SAHA明显抑制了乳腺癌细胞周期相关调控因子的表达,其主要对G1-S期进程进行调控,因此SAHA可能通过抑制细胞周期S期进程而发挥调控作用。另外,针对p21WAF1/CIP1基因功能的筛查中发现,SAHA可明显诱导p21WAF1/CIP1 mRNA和蛋白的表达,并且可调节p21WAF1/CIP1启动子的功能。综上所述,本文明确了SAHA通过调控p21WAF1/CIP1启动子乙酰化水平,影响乳腺癌MCF-7细胞周期。
( 致谢: 衷心感谢沈阳医学院辽宁省环境污染与微生态重点实验室为本实验提供的实验设备,感谢实验室全体工作人员对本实验的大力协助。)
| [1] | Parbin S, Shilpi A, Kar S, et al. Insights into the molecular interactions of thymoquinone with histone deacetylase: evaluation of the therapeutic intervention potential against breast cancer[J]. Mol Biosyst, 2016, 12(1): 48-58. doi:10.1039/C5MB00412H |
| [2] | Mawatari T, Ninomiya I, Inokuchi M, et al. Valproic acid inhibits proliferation of HER2-expressing Breast cancer cells by inducing cell cycle arrest and apoptosis through Hsp70 acetylation[J]. Int J Oncol, 2015, 47(6): 2073-81. doi:10.3892/ijo.2015.3213 |
| [3] | Clocchiatti A, Di Giorgio E, Viviani G, et al. The MEF2-HDAC axis controls proliferation of mammary epithelial cells and acini formation in vitro[J]. J Cell Sci, 2015, 128(21): 3961-76. doi:10.1242/jcs.170357 |
| [4] | 邹丹, 周伟强. 乳腺癌MCF-7细胞p21WAF1/CIP1启动子区HDAC1高功能结合位点的研究[J]. 中国药理学通报, 2017, 33(3): 317-21. Zou D, Zhou W Q. A study on high function binding site of HDAC1 in p21WAF1/CIP1 promoter region in breast cancer MCF-7 cells[J]. Chin Pharmacol Bull, 2017, 33(3): 317-21. |
| [5] | Raha P, Thomas S, Thurn K T, et al. Combined histone deacetylase inhibition and tamoxifen induces apoptosis in tamoxifen-resistantbreast cancer models, by reversing Bcl-2 overexpression[J]. Breast Cancer Res, 2015, 17(1): 26-42. doi:10.1186/s13058-015-0533-z |
| [6] | Wang L, Chen G, Chen K, et al. Dual targeting of retinoid X receptor and histone deacetylase with DW22 as a novel antitumor approach[J]. Oncotarget, 2015, 6(12): 9740-55. doi:10.18632/oncotarget.v6i12 |
| [7] | Ma J, Guo X, Zhang S, et al. Trichostatin A, a histone deacetylase inhibitor, suppresses proliferation and promotes apoptosis of esophageal squamous cell lines[J]. Mol Med Rep, 2015, 11(6): 4525-31. doi:10.3892/mmr.2015.3268 |
| [8] | Ji Z, Su J, Liu C, et al. Integrating genomics and proteomics data to predict drug effects using binary linear programming[J]. PLoS One, 2014, 9(7): e102798. doi:10.1371/journal.pone.0102798 |
| [9] | Speirs V, Adams I P, Walton D S, et al. Identification of wild-type and exon 5 deletion variants of estrogen receptor beta in normal human mammary gland[J]. J Clin Endocrinol Metab, 2000, 85(4): 1601-5. |
| [10] | Speirs V, Carder P J, Lane S, et al. Estrogen receptor β what is means for patients with breast cancer[J]. Lancet Oncol, 2004, 5(3): 174-81. doi:10.1016/S1470-2045(04)01413-5 |
| [11] | Murphy L C, Watson P H. Is estrogen receptor-beta a predictor of endocrine therapy responsiveness in human breast cancer[J]. Endocr Relat Cancer, 2006, 13(2): 327-34. doi:10.1677/erc.1.01141 |
| [12] | 龚爱华, 熊二梦, 张严, 等. SAHA诱导的p21表达致U251MG细胞抗凋亡效应[J]. 中国药理学通报, 2013, 29(12): 1743-7. Gong A H, Xiong E M, Zhang Y, et al. SAHA-induced p21 expression results in anti-apoptotic effects in U251MG cells[J]. Chin Pharmacol Bull, 2013, 29(12): 1743-7. doi:10.3969/j.issn.1001-1978.2013.12.027 |

