


2. 中国科学院深圳先进技术研究院,广东 深圳 518000
2. Shenzhen Institutes of Advanced Technology, Chinese Academy of Sciences, Shenzhen 518000, China
非酒精性脂肪肝 (nonalcoholic fatty liver disease,NAFLD) 是一种常见的慢性肝脏疾病,与代谢综合征密切相关[1]。研究表明乳清酸能够通过扰乱脂质代谢诱导大鼠形成脂肪肝[2]。胰岛素抵抗 (insulin resistance,IR) 是指机体胰岛素作用的靶器官 (肝脏、骨骼肌、脂肪组织等) 对胰岛素作用的敏感性下降,即正常剂量的胰岛素产生低于其正常生物学效应的一种状态。IR在NAFLD发展过程中有着关键作用,几乎所有的NAFLD患者都存在胰岛素抑制内源性葡萄糖生成能力降低,全身葡萄糖利用减少45%~50%等现象[3]。绝大多数IR是胰岛素和胰岛素受体结合后信号传导过程发生障碍的结果[4]。骨骼肌是利用血糖的重要外周组织,是IR发生的主要部位,在维持体内葡萄糖动态平衡中具有重要作用。肌肉组织中胰岛素信号传导通路任一位点的异常都可能阻碍葡萄糖的转运,从而引起IR。海星皂苷是一种甾体皂苷,具有广泛生理和药理活性。本实验通过长期喂食乳清酸诱导大鼠形成NAFLD,研究海星皂苷对NAFLD大鼠肌肉胰岛素信号通路的影响,并对其机制进行初步探究。
1 材料与方法 1.1 动物♂清洁级Wistar大鼠,体质量 (180±10) g,购自北京维通利华实验动物公司。
1.2 主要试剂乳清酸 (日本和光纯药工业株式会社);AB-8型大孔树脂 (南开大学化工厂);甘油三酯 (triglyceride,TG) 测定试剂盒、葡萄糖测定试剂盒 (北京中生北控生物科技股份有限公司);胰岛素测定试剂盒 (德国BD公司);谷丙转氨酶 (alanine aminotransferase,ALT) 测定试剂盒、谷氨酰转移酶 (gamma-glutamyl transferase,GGT) 测定试剂盒、天门冬氨酸氨基转移酶 (aspartate transaminase,AST) 测定试剂盒、糖原测定试剂盒 (南京建成生物工程研究所);RIPA蛋白裂解液 (碧云天研究所);ECL发光试剂 (普利莱基因技术有限公司);IRS1多克隆抗体、p-IRS1(Ser307) 多克隆抗体、PI3K多克隆抗体、AKT多克隆抗体、p-AKT单克隆抗体、GLUT4单克隆抗体、GSK3单克隆抗体、p-GSK3单克隆抗体、β-actin单克隆抗体、Na, K-ATPase单克隆抗体 (Cell signaling technology公司);辣根过氧化物酶标记山羊抗兔二抗 (北京康为世纪生物科技有限公司);其他试剂为国产分析纯。
1.3 仪器与设备Model680型酶标仪 (美国Bio Rad公司);UV-2550型分光光度计 (日本岛津公司);ST-Ⅱ型半干转移电泳槽 (大连竞迈生物科技有限公司);CP100MX型离心机 (日本日立公司)。
1.4 实验方法 1.4.1 海星皂苷的制备参照张铮[5]的方法制备海星皂苷。具体步骤如下:称取一定量的新鲜海星,加入体积分数为0.95的乙醇浸提过夜得上清液,再加入体积分数为0.60的乙醇溶液反复浸提2次,收集每次抽提所得上清液,减压回收乙醇,得水溶液,然后过AB-8型大孔树脂,依次用水和体积分数为0.80的乙醇洗脱,收集体积分数为0.80的乙醇洗脱液减压浓缩,经真空冷冻干燥后得海星皂苷。以海星皂苷纯品作为标准对照,采用香草醛-硫酸法[6]测定所得海星皂苷的纯度为80%。
1.4.2 实验动物分组与喂养适应性喂养1周后将Wistar大鼠按体重分为2组:正常对照组 (Con,n=8) 和乳清酸组 (n=16),分别喂食标准饲料和1%乳清酸饲料。6周后将乳清酸组随机分为模型组 (Model,n=8) 和海星皂苷组 (Sfs,n=8),分别喂食1%乳清酸饲料和含有0.04%海星皂苷的1%乳清酸饲料,饲养8周。具体饲料配方见Tab 1。大鼠自由摄食及饮水,在室温 (23±2)℃、12 h/12 h明暗交替条件下喂养。饲料每日换新,并测定大鼠每日摄食量。于实验结束前禁食12 h,自由饮水,经乙醚麻醉后腹主动脉取血,取肝脏、肌肉等脏器组织称重后于-80℃保存备用。
| Group | Sucrose | Casein | Corn Starch |
Corn Oil |
Cellullose | Mineral Mix |
Vitamin Mix |
DL- Methionine |
Choline | Orotic acid |
Starfish Saponins |
| Con | 500 | 200 | 150 | 50 | 50 | 35 | 10 | 3 | 2 | 0 | 0 |
| Model | 490 | 200 | 150 | 50 | 50 | 35 | 10 | 3 | 2 | 10 | 0 |
| Sfs | 489.6 | 200 | 150 | 50 | 50 | 35 | 10 | 3 | 2 | 10 | 0.4 |
参照Folch等[7]的方法,准确称取一定质量肝脏,制成肝脏匀浆,按照试剂盒说明书测定肝脏TG含量。血液在室温静置30 min后,4℃下7 500 r·min-1离心15 min后取上层血清,按照试剂盒说明书测定AST、GGT和ALT。
1.4.4 葡萄糖耐受实验13周时,大鼠禁食不禁水10h后进行葡萄糖耐受实验,腹腔注射葡萄糖溶液 (2 g·kg-1·bw) 后0、0.5、1和2 h时进行尾静脉取血。血液于室温静置30 min后,4℃下7 500 r·min-1离心15min后取上清,按照试剂盒说明书测定血清葡萄糖水平。
1.4.5 空腹葡萄糖、胰岛素、ISI测定大鼠于实验结束前禁食12h,自由饮水,经乙醚麻醉后腹主动脉取血。血液在室温静置30 min后,4℃下7 500 r·min-1离心15min后取上层血清,按照试剂盒说明书测定葡萄糖和胰岛素水平。并根据李光伟等[8]的方法,计算胰岛素敏感指数 (insulin sensitivity index,ISI),分析时取其自然对数值。
1.4.6 肌糖原测定实验前根据组织重量计算碱液加入量,沸水浴30 min冷却,加入蒸馏水制备成5%糖原检测液。按照糖原试剂盒说明书操作。
1.4.7 蛋白表达量测定取适量肌肉组织加入RIPA裂解液提取蛋白。蛋白浓度用BCA试剂盒测定。利用SDS-PAGE电泳对不同分子量蛋白进行分离后通过半干转膜的方法将蛋白样品转移至PVDF膜上,并用BSA溶液进行封闭。利用TBST对封闭后的PVDF膜进行洗涤以去除多余封闭液。此后根据抗体说明书进行一抗和经HRP标记的二抗孵育。最后,加入ECL化学发光试剂进行显色,利用化学发光成像系统进行拍照和灰度统计。
1.5 数据分析采用SPSS18.0统计软件进行t检验分析,结果用x±s表示。
2 结果 2.1 大鼠摄食量、体重、脏器质量变化由Tab 2可知,各组大鼠在摄食期间的摄食量与体质量增加量无明显差异。模型组大鼠肝脏质量明显增加 (P < 0.01)。海星皂苷对大鼠肝脏质量无明显影响。
| Group | Food intake /g·d-1 |
Body weight gain/g |
Liver weight/g |
| Con | 19.29±0.59 | 56.25±3.17 | 13.48±0.58 |
| Model | 21.23±0.46 | 60.50±4.66 | 22.04±1.17## |
| Sfs | 22.97±0.32 | 61.00±6.01 | 23.61±1.15 |
| ##P < 0.01 vs control | |||
如Tab 3所示,模型组大鼠肝脏甘油三酯 (TG) 水平明显升高 (P < 0.01)。与模型组相比,海星皂苷组大鼠肝脏TG水平降低41.20%(P < 0.01)。模型组大鼠血清ALT、GGT、AST活性分别是对照组的2.92倍 (P < 0.01)、1.24倍 (P < 0.01) 和4.13倍 (P < 0.05),这表明模型组大鼠肝功能严重受损,实验造模成功。海星皂苷明显下调了血清ALT和GGT活性 (P < 0.05),对AST活性无明显调节作用。
| Group | Liver TG content /mg·g-1 |
Serum ALT activity/IU·g-1 |
Serum GGT activity/IU·g-1 |
Serum AST activity/IU·g-1 |
| Con | 10.04±1.95 | 10.07±1.20 | 57.66±1.47 | 3.68±0.94 |
| Model | 124.49±5.28## | 29.38±4.74## | 71.26±3.86## | 15.20±4.08# |
| Sfs | 73.20±15.66** | 17.72±0.92* | 62.00±1.81* | 18.74±2.78 |
| #P < 0.05,##P < 0.01 vs control;*P < 0.05,**P < 0.01 vs model | ||||
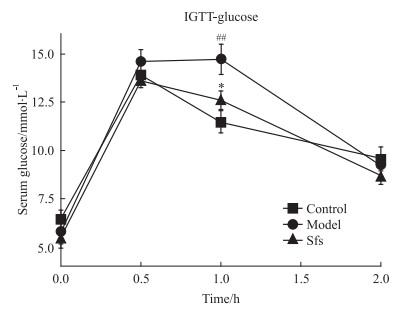
海星皂苷干预7周 (喂食乳清酸13周) 后,进行葡萄糖耐受实验。如Fig 1所示,腹腔注射葡萄糖1 h时,模型组大鼠血清葡萄糖水平明显高于对照组 (P < 0.01),表明了胰岛素抵抗的存在。海星皂苷干预后,血清葡萄糖水平明显下降 (P < 0.05),与对照组大鼠的血清葡萄糖水平接近。
|
| Fig 1 Chronic effects of starfish saponins on IGTT in rats (n=8) ##P < 0.01 vs control; *P < 0.05 vs model |
如Tab 4所示,模型组大鼠的空腹血糖水平和空腹胰岛素水平明显高于正常组大鼠 (P < 0.05,P < 0.01),胰岛素敏感指数明显降低 (P < 0.01),这进一步表明模型组大鼠出现胰岛素抵抗。海星皂苷干预后,胰岛素敏感指数明显上调 (P < 0.01)。
| Group | FPG/ mmol·L-1 |
FINS/ μg·L-1 |
ISI |
| Con | 5.45±0.08 | 0.09±0.007 | -2.37±0.08 |
| Model | 6.59±0.53* | 0.22±0.013** | -3.45±0.05** |
| Sfs | 5.23±0.24# | 0.13±0.009## | -2.68±0.06## |
| #P < 0.05,##P < 0.01 vs control;*P < 0.05,**P < 0.01 vs model | |||
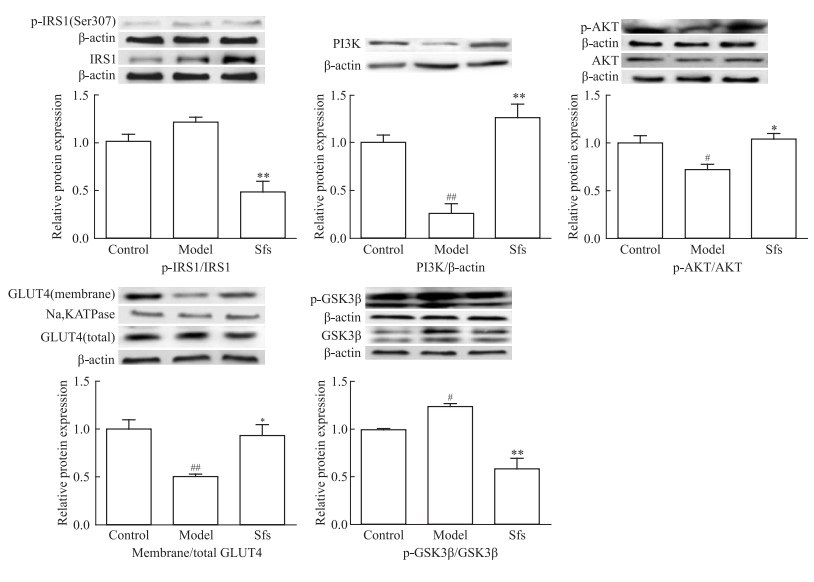
胰岛素受体底物 (IRS1) 是肌肉胰岛素信号中关键转导者。IRS1在Ser307的磷酸化程度增加会导致IRS1酪氨酸磷酸化和AKT磷酸化水平降低[9]。活化后的IRS激活其下游的磷脂酰肌醇3激酶 (PI3K)-蛋白激酶B (PKB / AKT),使葡萄糖转运蛋白4(GLUT4) 转位到细胞膜上,增加葡萄糖的摄取。如Fig 2所示,模型组大鼠肌肉组织中PI3K和p-AKT蛋白表达量明显减少 (P < 0.01;P < 0.05),GLUT4转位到细胞膜上的比例明显降低 (P < 0.01),这表明了模型组大鼠肌肉组织胰岛素信号通路受损以及对葡萄糖的摄取减少。海星皂苷明显下调p-IRS1(Ser307) 的蛋白表达水平 (P < 0.01),上调PI3K和p-AKT的蛋白表达水平 (P < 0.01;P < 0.05),并明显增加GLUT4在细胞膜上的比例 (P < 0.05)。
|
| Fig 2 Chronic effects of starfish saponins on muscle relevant protein expression and muscle glycogen content in rats (n=8) #P < 0.05, ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model |
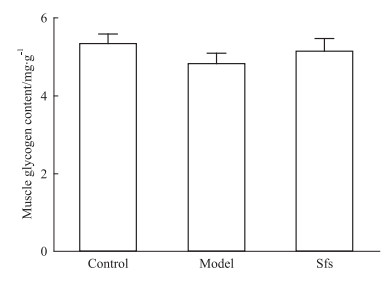
GSK-3β是胰岛素作用的关键负性调节因子,它能够磷酸化糖原合成酶进而使其失活,使得血糖水平升高[10]。实验结果表明喂食乳清酸14周后模型组大鼠GSK-3β磷酸化水平明显增加 (P < 0.05),海星皂苷的干预明显下调GSK-3β的磷酸化水平 (P < 0.01)。但是如Fig 3所示,模型组与海星皂苷组的肌糖原含量无明显变化。
|
| Fig 3 Chronic effects of starfish saponins onmuscle glycogen content in rats (n=8) |
IR是引起许多代谢疾病如2型糖尿病、脂肪肝、动脉粥样硬化的共同生理病理基础[11]。IR在NAFLD的“二次打击”学说中处于重要环节--机体发生IR时会使得肝脏中的脂肪过度蓄积,进而发生脂肪肝[12]。肌肉组织通过对葡萄糖的摄取和糖原的分解来维持机体的糖代谢[13],是外周胰岛素抵抗发生的主要靶位。研究表明[14-15],肌肉胰岛素抵抗发生在代谢异常的早期阶段,并对NAFLD的发展有重要作用。本实验探究了海星皂苷对乳清酸诱导NAFLD大鼠肌肉胰岛素信号通路的影响。实验结果表明:海星皂苷可通过增强胰岛素信号通路来改善肌肉组织的胰岛素抵抗,同时降低NAFLD大鼠肝脏脂质水平,改善肝功能。
由糖耐实验结果可知,摄食乳清酸后,模型组大鼠血清中葡萄糖水平明显升高。空腹血糖和空腹胰岛素的测定结果以及胰岛素敏感指数进一步表明模型组大鼠出现胰岛素抵抗。胰岛素信号通路受阻是发生胰岛素抵抗的主要原因。胰岛素受体与胰岛素结合后引起胰岛素受体底物 (IRS) 发生磷酸化,从而激活PI3K/AKT这一主要胰岛素信号传递通路。GLUT4是肌肉组织中糖代谢最重要的葡萄糖转运载体[16],主要存在于细胞内,在运动刺激或胰岛素刺激下会转位到细胞膜上,以增加对葡萄糖的摄取。从实验结果可知,海星皂苷能够改变IRS-1/PI3K/Akt信号通路中主要蛋白的表达来改善胰岛素信号通路,并上调GLUT4的蛋白水平,增加葡萄糖的摄取。糖原合成是胰岛素刺激葡萄糖代谢的重要途径。GSK3β的磷酸化会使得糖原合成酶 (GS) 活性降低,糖原合成减少。从实验结果可知,海星皂苷的干预下调肌肉中p-GSK3β蛋白水平,但是对于肌糖原含量没有明显的调控作用。这可能是因为调节肌糖原合成的关键酶--GS--的活性还受到变构作用的调节[17]。
海星皂苷具有抗病毒、抗肿瘤、抗炎症、降血压等多种生物活性[5, 18],但是有关海星皂苷对NAFLD和IR影响方面的报道较少。本实验探究了海星皂苷对乳清酸诱导的NAFLD大鼠肌肉组织中IR的改善作用。综上所述,海星皂苷通过激活肌肉组织中IRS-1/PI3K/Akt信号通路以及上调GLUT4的表达改善了乳清酸诱导的NAFLD大鼠肌肉胰岛素抵抗现象,为海星皂苷的开发利用提供了理论依据。
( 致谢: 本实验于中国海洋大学食品学院人类健康实验室完成,感谢实验室所提供的帮助与支持。 )
| [1] | 韩雪晶, 荆雪, 高普均. 非酒精性脂肪性肝病与代谢综合征相关性的临床研究[J]. 临床肝胆病杂志, 2009, 25 (4): 269-71. Han X J, Jing X, Gao P J. Nonalcoholic fatty liver disease and metabolic syndrome[J]. Chin J Clin Hepatol, 2009, 25 (4): 269-71. |
| [2] | 刘春花. 乳清酸诱导大鼠糖、脂代谢异常的机理以及海参皂苷与结构修饰物对其的影响研究[D]. 青岛: 中国海洋大学, 2013. Liu C H. Studies of the mechanism by which orotic acid induce glucose and lipid metabolic disorders, and effects of sea cucumber saponin and its modifications in rats[D]. Qingdao: Ocean University of China, 2013. |
| [3] | Marchesini G, Brizi M, Bianchi G, et al. Nonalcoholic fatty liver disease: a feature of the metabolic syndrome[J]. Diabetes, 2001, 50 (8): 1844-50. doi:10.2337/diabetes.50.8.1844 |
| [4] | 窦梅, 马爱国. 胰岛素抵抗主要原因及机制的研究进展[J]. 国外医学 (卫生学分册), 2009, 36 (3): 174-9. Dou M, Ma A G. Research progress of main reasons and mechanism of insulin resistance[J]. Foreign Med Sci (Section Hygiene), 2009, 36 (3): 174-9. |
| [5] | 张铮. 罗氏海盘车 (Asterias rollestoni) 水溶性海星皂苷的分离纯化及其部分生物学活性研究[D]. 青岛: 中国海洋大学, 2008. Zhang Z. Studies on preparation and purification of water-soluble starfish glycosides from asterias rollestoni and some biological activity examination[D]. Qingdao:Ocean University of China, 2008. |
| [6] | 张立新, 薛峰, 赵爱云, 等. 海星中皂苷总含量测定方法的研究[J]. 食品科学, 2007, 28 (1): 243-6. Zhang L X, Xue F, Zhao A Y, et al. Study on determination methods of total asterosaponins content from starfish[J]. Food Sci, 2007, 28 (1): 243-6. |
| [7] | Folch J, Lees M, Sloane Stanley G H. A simple method for the isolation and purification of total lipides from animal tissues[J]. J Biol Chem, 1957, 226 (1): 497-509. |
| [8] | 李光伟, 潘孝仁, StephenLillioja, 等. 检测人群胰岛素敏感性的一项新指数[J]. 中华内科杂志, 1993, 32 (10): 656-60. Li G W, Pan X R, Stephen Lillioja, et al. A new insulin-sensitivity index for the population-based study[J]. Chin J Intern Med, 1993, 32 (10): 656-60. |
| [9] | Ueki K, Yamamoto-Honda R, Kaburagi Y, et al. Potential role of protein kinase B in insulin-induced glucose transport, glycogen synthesis, and protein synthesis[J]. J Biol Chem, 1998, 273 (9): 5315-22. doi:10.1074/jbc.273.9.5315 |
| [10] | Eldar-Finkelman H. Glycogen synthase kinase 3: an emerging therapeutic target[J]. Trends Mol Med, 2002, 8 (3): 126-32. doi:10.1016/S1471-4914(01)02266-3 |
| [11] | 金鑫, 张彦芬, 秘尧, 等. 津力达对高脂诱导的胰岛素抵抗ApoE-/-小鼠骨骼肌胆固醇相关基因的影响[J]. 中国药理学通报, 2014, 30 (11): 1600-4. Jing J, Zhang Y F, Mi R, et al. Effect of Jinlida on cholesterol-related genes in skeletal muscle in fat-induced insulin resistance ApoE-/- mice[J]. Chin Pharmacol Bull, 2014, 30 (11): 1600-4. doi:10.3969/j.issn.1001-1978.2014.11.024 |
| [12] | Day C P, James O F. Steatohepatitis: A tale of two "hits"?[J]. Gastroenterology, 1998, 114 (4): 842-5. doi:10.1016/S0016-5085(98)70599-2 |
| [13] | Hei Y J. Recent progress in insulin signal transduction[J]. J Pharmacol Toxicol Methods, 1998, 40 (3): 123-35. doi:10.1016/S1056-8719(98)00051-3 |
| [14] | Rab∅l R, Petersen K F, Dufour S, et al. Reversal of muscle insulin resistance with exercise reduces postprandial hepatic de novo lipogenesis in insulin resistant individuals[J]. Proc Natl Acad Sci USA, 2011, 108 (33): 13705-9. doi:10.1073/pnas.1110105108 |
| [15] | Petersen K F, Dufour S, Savage D B, et al. The role of skeletal muscle insulin resistance in the pathogenesis of the metabolic syndrome[J]. Proc Natl Acad Sci USA, 2007, 104 (31): 12587-94. doi:10.1073/pnas.0705408104 |
| [16] | James D E, Brown R, Navarro J, et al. Insulin-regulatable tissues express a unique insulin-sensitive glucose transport protein[J]. Nature, 1988, 333 (6169): 183-5. doi:10.1038/333183a0 |
| [17] | Bouskila M, Hunter R W, Ibrahim A F, et al. Allosteric regulation of glycogen synthase controls glycogen synthesis in muscle[J]. Cell Metab, 2010, 12 (5): 456-66. doi:10.1016/j.cmet.2010.10.006 |
| [18] | 周鹏, 顾谦群, 王长云. 海星皂甙及其他活性成分研究概况[J]. 海洋科学, 2000, 24 (2): 35-7. Zhou P, Gu Q Q, Wang C Y. Survey of studies on starfish saponins and the other bioactive substances[J]. Mar Sci, 2000, 24 (2): 35-7. |

