


2. 南京中医药大学药学院,江苏 南京 210023;
3. 江苏省中药药效与安全性评价重点实验室,江苏 南京 210023;
4. 浙江中医药大学药学院,浙江 杭州 310053
2. College of Pharmacy, Nanjing University of Chinese Medicine, Nanjing 210023, China;
3. Jiangsu Key Laboratory for Pharmacology and Safety Evaluation of Chinese Materia Medica, Nanjing University of Chinese Medicine, Nanjing 210023, China;
4. Zhejiang Chinese Medical University, Hangzhou 310053, China
肝脏是人体内最大、最重要的消化及代谢器官,肝病则是世界范围内的一种重要且难治的疾病。全世界约有3亿多人感染乙型肝炎病毒,1.7亿多人感染丙型肝炎病毒,以及众多因酒精、化学物质、遗传及代谢性疾病等原因导致的其他类型肝脏疾病的人群[1-2]。持续性的肝脏损伤,可导致肝纤维化、肝硬化甚至肝癌的产生[2]。中国是一个肝病大国,各种慢性肝病严重危害人类的健康和生命,深入阐明各类肝病发病机制,并寻求有效治疗策略已刻不容缓。
现代医学认为通过减少胶原纤维的生成和增强其降解,肝纤维化是可以逆转的,肝硬化的逆转也是可能的[3]。然而,目前疗效确切、副作用少的抗纤维化西药、化学药物很少,大多还处在实验研究阶段。由于西药抗肝纤维化治疗的种种限制,国内发挥中医药整体调节优势,遵循“方从法立,以法统方”的原则,进行抗肝纤维化研究,发现中医药在抗肝纤维化治疗中具有独特的优势,如丹参、三七、姜黄、桃仁及其提取物、衍生物和一些在中医理论指导下组成的复方制剂,如复方861、复方鳖甲软肝方等在实验研究中证实具有明显抗肝纤维化作用[4-7]。纵观近十年来运用中药复方抗肝纤维化的治法,研究已从过去单纯活血化瘀法发展到扶正化痕、健脾软肝、清热利湿、滋养肝肾等多种治法的研究,从而发挥了中医的辨证论治特色,研究水平不断深人[7-8]。由于肝纤维化的形成和发展是一个复杂的过程,其病理因素呈现多元化,且相兼为患,其治疗也非一法一方一药能解决。因此,发扬中医辨证论治的优势所在,拟定各个阶段的基本治则,治疗上采取多种治法,并有所兼顾,才能提高临床疗效。我们在前期研究中发现川芎嗪(ligustrazine, TMP)具有确切的预防和治疗纤维化的作用,川芎嗪能够抑制肝星状细胞(hepatic stellate cell, HSC)增殖活化、迁移、运动,分子机制研究发现川芎嗪能够下调HSC中PDGF/MAPK、PI3K/Akt通路的蛋白与基因表达[9-10]。同时,研究发现其可以改善CCl4所致的大鼠纤维化的病理学改变;明显降低纤维化时异常升高的ALT、AST、HA、LN、Ⅲ型前胶原(PC-Ⅲ);降低血清细胞因子NO、TGF-β1、MMP-2和TNF-α水平[11]。临床研究发现,川芎嗪联合促肝细胞生长素能够明显降低血清肝纤维化指标(P < 0.01),有较好的抗肝纤维化和改善肝功能作用[12]。我们在研究丹皮酚(paeonol)抗肝纤维化效应的实验中发现,丹皮酚同样能够改善CCl4所致的大鼠纤维化的病理学改变,减少细胞外基质成分的形成,抑制炎症指标NF-κB、TNF-α等的表达,降低肝内炎症水平[13]。
综合考虑到肝纤维化形成与发展的复杂性,以及中药有效成分所表现出的良好的抗肝纤维化活性,再加上临床有效化学药物的缺失,我们提出联合应用中药活性成分进行抗肝纤维化治疗的方案。本研究应用前期证实有确切抗肝纤维化效应的川芎嗪与丹皮酚进行相关实验研究。重点阐释二者联合应用是否在抑制肝内胶原生成与降低炎症水平等方面具有协同抗肝纤维化的效应。
1 材料与方法 1.1 动物与试剂清洁级♂SD大鼠,体质量200 g~300 g,南京中医药大学实验动物中心提供。HSC-T6细胞(中科院上海细胞库),川芎嗪(分子质量:136.20,无色针状结晶)、丹皮酚(分子质量:166.18,白色针状结晶)购自南京泽朗医药有限责任公司,ALT、AST、ALP及羟脯氨酸测定试剂盒(南京建成生物工程研究所),蛋白抽提试剂盒(碧云天生物技术研究所),α-SMA、Fibronectin、Procollagen、TNF-α、NF-κB p65、caspase-3、Bcl-2、Bax和β-actin抗体(均购自Abcam公司),逆转录试剂盒、Real time-PCR用试剂(Bio-Rad公司)。
1.2 分组及造模动物随机分为5组,每组10只,空白对照组、模型组、川芎嗪组(100 mg·kg-1)、丹皮酚组(100 mg·kg-1)以及联合用药组(川芎嗪100 mg·kg-1+丹皮酚100 mg·kg-1)。除空白对照组外,其余各组采用CCl4油溶液造模,按体质量给药,5 mL·kg-1,腹腔注射,3次/周。实验期间动物均饲养于同一环境下,保持室温,环境安静,动物自由进食、进水。造模2周后,从第3周开始灌胃给予相应药物,空白对照组和模型组给予等体积生理盐水。8周后取血制备血清做生化检查,取肝脏制备病理切片和10%组织匀浆备用。
细胞实验:取对数生长期HSC-T6细胞,分为模型组(HSC-T6培养后自动活化)、川芎嗪组(20 μmol·L-1)、丹皮酚组(25 μmol·L-1)、联合用药组(川芎嗪20 μmol·L-1+丹皮酚25 μmol·L-1),干预处理24 h。
1.3 组织病理学观察肝脏组织经10%中性甲醛溶液固定后,常规石蜡包埋,切片厚4~5 μm,常规HE染色后,于光学显微镜下观察肝组织病理学改变,Masson染色及天狼星红(Sirius red)染色后,观察各组肝组织中胶原纤维沉积情况,采用国际通用的ISHAK肝脏组织活检病理学评分和纤维化分期标准,对所有标本进行炎症反应评分和纤维化分期的病理学诊断。
1.4 血清ALT、AST、ALP、羟脯氨酸含量测定全自动生化分析仪测定各组血清中ALT、AST、ALP、羟脯氨酸含量。
1.5 Western blot检测肝组织中纤维化标志蛋白及HSC中炎症及凋亡相关通路蛋白的表达称取肝脏50 mg,按质量/体积比1 :5加入预冷RIPA裂解液,立即加入PMSF和磷酸酶抑制剂,冰上孵育30 min,移入离心管4℃、15 000 r·min-1离心15 min,取上清液为细胞裂解液。HSC用冰冷的RIPA裂解缓冲液裂解,收集细胞裂解物,-20 ℃储藏过夜。BCA法测定蛋白浓度,其余加等体积的6×电泳加样缓冲液,沸水浴10 min。实验前4 500 r·min-1离心10min,配制SDS-PAGE凝胶进行上样(上样量50 μg),电泳40 mA 1.5 h,转膜100 V/1.5 h。脱脂奶粉封闭,一抗及二抗孵育,化学发光剂ECL显色,用图像分析系统进行半定量分析。
1.6 Real-time PCR检测HSC中炎症及凋亡相关通路的基因表达按TRIzol Reagent说明书提取HSC总RNA,酶标仪测定RNA含量。将mRNA反转录成cDNA,取反转录产物进行实时定量PCR反应。PCR以GAPDH为内参,所用特异性引物如下,基于比较CT (threshold cycle)值法实时荧光定量PCR法检测mRNA相对表达,每个样本的mRNA含量用各内参GAPDH含量进行标准化。GAPDH (F): 5′-GGCCCCTCTGGAAAGCTGTG-3′,GAPDH (R):5′-CCGCCTGCTTCACCACCTTCT-3′,caspase-3(F):5′-GGAACGAACGGACCTGTGG-3′,caspase-3(R):5′-CGGGTGCGGTAGAGTAAGC-3′,NF-κB (F):5′-AGGAATGTTCCCATGCCTTCAC-3′, NF-κB (R):5′-GCAACTCTCATTCTTGGTTAATTC-3′。
1.7 统计学分析采用SPSS17.0统计软件进行方差分析,计量资料用x±s表示,组间比较用单因素方差分析。
2 结果 2.1 动物一般情况空白对照组大鼠实验期间皮毛光滑,活动正常。模型组和各给药组造模后见皮毛蓬乱,精神萎靡,行动迟缓,易激惹,个别具有攻击性。给药组较模型组毛发光泽度较好,活动增加明显,体重均高于模型组。
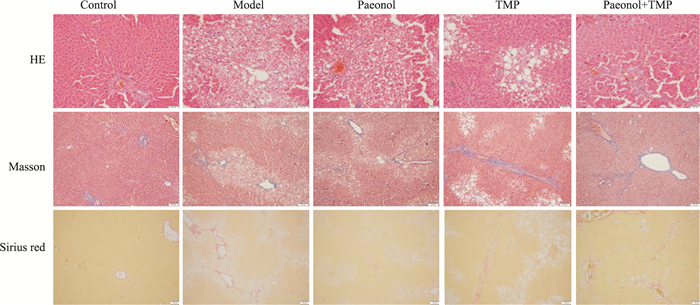
2.2 肝脏组织病理学改变Fig 1结果显示,正常组肝脏肝细胞索排列较整齐, 未见纤维结缔组织增生及假小叶形成,无变性、坏死,无炎细胞浸润,汇管区未见纤维组织增生。模型组大鼠肝小叶结构被破坏,肝细胞索排列紊乱, 有炎症细胞浸润,肝细胞水肿,大量纤维组织增生,部分可见假小叶形成。川芎嗪组与丹皮酚组大鼠肝细胞变性坏死明显减轻,结缔组织明显减少,偶见假小叶形成,可见炎症细胞浸润,肝细胞水肿减轻。联合用药组大鼠肝小叶结构基本正常,肝细胞排列尚整齐,中央静脉周围可见部分肝细胞变性,纤维组织异常增生不明显。
|
| Fig 1 HE (×200), Masson (×100) and Sirius red (×100) staining of liver tissue in control, model, paeonol or/and TMP treatment group |
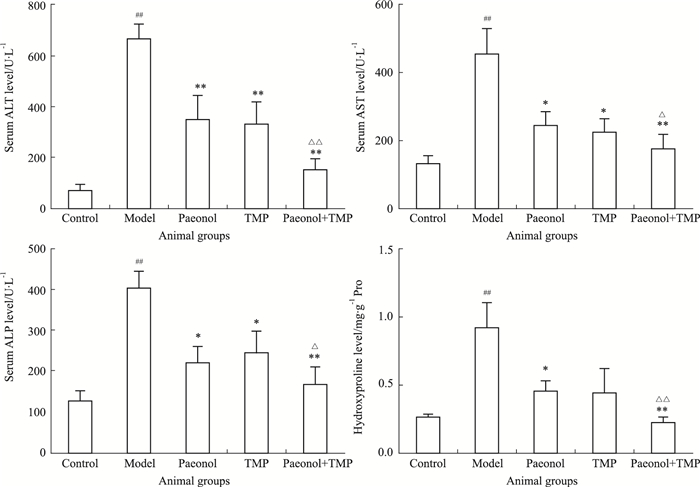
如Fig 2所示,造模后大鼠血清ALT、AST、ALP和羟脯氨酸水平明显高于正常对照组(P < 0.01)。与模型组比较,川芎嗪和丹皮酚组ALT、AST、ALP和羟脯氨酸水平明显降低(P < 0.05),联合用药组的效果更加明显(P < 0.01),联合用药组与川芎嗪或丹皮酚组比较差异有统计学意义(P < 0.05)。
|
| Fig 2 Effects of paeonol or/and TMP on serum ALT, AST, ALP and hydroxyproline activities Supplement with paeonol or/and TMP for 32 d significantly inhibited the enhancement of serum ALT, AST, ALP and hydroxyproline activities, respectively. ##P < 0.01 vs control; *P < 0.05, **P < 0.01 vs model; △P < 0.05, △△P < 0.01 vs paeonol or TMP. |
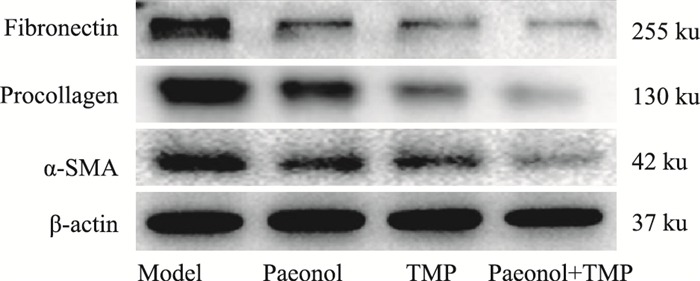
Western blot检测结果显示(Fig 3),模型组大鼠肝组织内高表达HSC活化标志物α-SMA以及ECM主要成分Fibronectin、Procollagen;丹皮酚、川芎嗪干预组的肝组织内这3种成分的表达明显降低;而两者联合用药组3种成分的表达量要明显低于单独干预组,联合用药组与丹皮酚或川芎嗪干预组比较,差异有统计学意义(P < 0.05)。
|
| Fig 3 Paeonol or/and TMP inhibits expression of ECM related protein in liver tissue Western blot analyses of α-SMA, fibronectin and procollagen. β-actin was used as an invariant control for equal loading. |
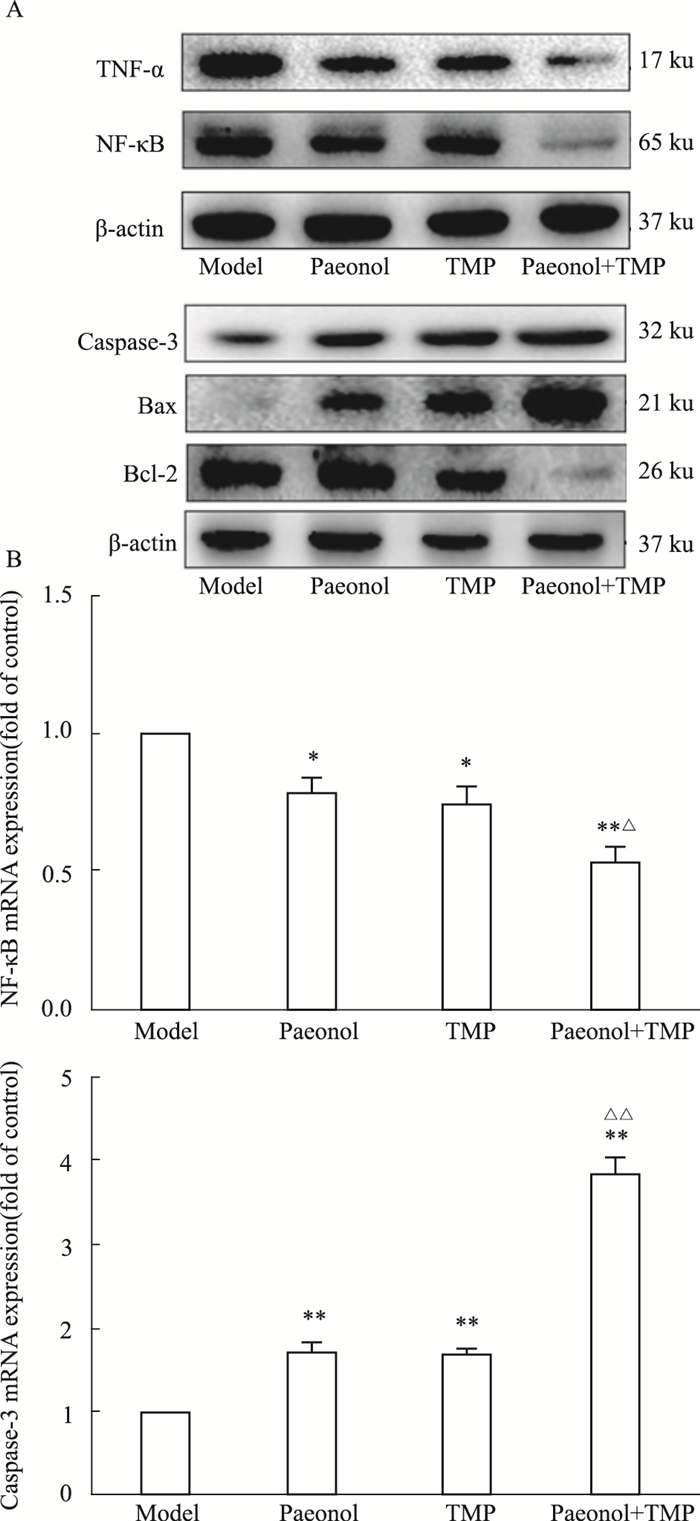
模型组TNF-α、NF-κB p65有较强的表达,各治疗组TNF-α、NF-κB p65表达较模型组有所降低,各组水平依次为:模型组>丹皮酚组或川芎嗪组>联合用药组,各组间差异均有统计学意义。研究发现,HSC中Bax与caspase-3蛋白表达在模型组、丹皮酚治疗组或川芎嗪治疗组、联合用药组依次升高,Bcl-2蛋白表达则呈现出相反的趋势。在基因水平,各组NF-κB p65与caspase-3的mRNA表达与蛋白表达情况相同(Fig 4)。
|
| Fig 4 Interference with inflammation and apoptosis signaling was associated with paeonol or/and TMP inhibition of activation of HSC A:Western blot analyses of TNF-α, NF-κB p65, Bax, caspase-3, Bcl-2. β-actin was used as an invariant control for equal loading. B: Real time-PCR analyses of NF-κB and caspase-3, GAPDH was used as an invariant control for equal loading. *P < 0.05, **P < 0.01 vs model; △P < 0.05, △△P < 0.01 vs paeonol or TMP. |
肝纤维化是指由于肝损伤诱因的持续存在,导致肝细胞持续坏死,继发肝脏炎症或损伤修复过程中持续的炎症反应,导致肝脏内纤维性结缔组织异常增生,细胞外基质在肝内过量沉积为特征的病理变化[1-2]。因此,理论上如果能通过各种途径消除致病因素和刺激因子,抑制各种炎症反应和肝细胞外基质沉积,促进其降解则有望逆转或阻止肝纤维化的发生和进展,最终阻止肝硬化的发生。
本研究发现,川芎嗪、丹皮酚均具有明显抗肝纤维化作用,抑制细胞外基质的生成与沉积,两者联合应用效果更加明显,与两者单独应用相比具有统计学意义(P < 0.05),为临床抗肝纤维化提供了新的治疗策略。近年来研究发现,TNF-α/NF-κB在肝损伤发病机制中起重要作用,它在肝脏中高表达与继发引起的下游调控基因激活共同参与了肝损伤的发生和发展。本实验对川芎嗪联合丹皮酚抗肝纤维化的机制进行了观察,川芎嗪、丹皮酚可改善肝功能、肝组织纤维化及炎症坏死程度,具有延缓或阻止肝纤维化的作用。川芎嗪联合丹皮酚较单用两药的大鼠肝纤维化程度轻,效果明显,其机制可能与这些药物从基因和蛋白水平抑制了TNF-α/NF-κB通路的活性,进而促进了HSC中Bax与caspase-3蛋白表达,抑制了Bcl-2的表达,恢复了Bcl-2与Bax的比例,从而促进了HSC的凋亡,减轻了肝纤维化程度。
本研究仍存在诸多不足,将在后续研究中进一步解决:① 项目的机制研究还有待于进一步深入,川芎嗪、丹皮酚具体作用靶点在哪里,两者是如何协同等;② 需要筛选出合适的川芎嗪和丹皮酚的配伍方案,有必要进一步进行相关配比处方优化的研究,以进一步提高药物组合的抗肝纤维化效应。
( 致谢: 本文实验在南京中医药大学“江苏省中药药效与安全性评价重点实验室”完成,感谢实验室对本项目实验的鼎力支持! )
| [1] | Koyama Y, Xu J, Liu X, Brenner D A. New developments on the treatment of liver fibrosis[J]. Dig Dis, 2016, 34 (5): 589-96. doi:10.1159/000445269 |
| [2] | Anthony B, Allen J T, Li Y S, et al. Hepatic stellate cells and parasite-induced liver fibrosis[J]. Parasi Vectors, 2010, 3 (1): 60. |
| [3] | Marrone G, Shah V H, Gracia-Sancho J. Sinusoidal communication in liver fibrosis and regeneration[J]. J Hepatol, 2016, 65 (3): 608-17. doi:10.1016/j.jhep.2016.04.018 |
| [4] | 高衍义, 薛敬东. 中医药治疗肝纤维化的概述[J]. 中医药导报, 2015, 21 (23) : 112-4. Gao Y Y, Xue J D. An overview of Chinese medicine treatment of liver fibrosis[J]. Guid J Tradit Chin Med Pharm, 2015, 21 (23): 112-4. |
| [5] | 黄小华, 孙永, 沈能, 等. 双亲姜黄素衍生物减轻大鼠肝纤维化与抗炎抗氧化作用的研究[J]. 中国药理学通报, 2015, 31 (4) : 470-5. Huang X H, Sun Y, Shen N, et al. The amphiphilic curcumin derivative attenuates liver fibrosis by anti-inflammatory and antioxidant effect[J]. Chin Pharmacol Bull, 2015, 31 (4): 470-5. |
| [6] | 章圣朋, 何勇, 徐涛, 等. 夏枯草总三萜调控ERK、TGF-β1 /Smad通路对肝纤维化大鼠的保护作用研究[J]. 中国药理学通报, 2015, 31 (2) : 261-6. Zhang S P, He Y, Xu T, et al. Regulatory effects of total triterpenoid of Prunella vulgarisL. on activities of ERK and TGF-β1/Smad signaling pathway in protecting hepatic fibrosis in rats[J]. Chin Pharmacol Bull, 2015, 31 (2): 261-6. |
| [7] | 刘平. 肝纤维化肝硬化的中西医结合诊疗发展问题[J]. 中国中西医结合杂志, 2015, 35 (3) : 268-71. Liu P. Development of liver fibrosis, cirrhosis diagnosis and treatment combining traditional Chinese and western medicine[J]. Chin J Integr Tradit West Med, 2015, 35 (3): 268-71. |
| [8] | 王保芹. 中医药治疗肝纤维化研究进展[J]. 中国民族民间医药, 2015, 24 (13) : 18-9. Wang B Q. Progress of Chinese medicine in treating liver fibrosis[J]. Chin J Ethnomed Ethnopharm, 2015, 24 (13): 18-9. |
| [9] | Zhang X P, Zhang F, Kong D S, et al. Tetramethylpyrazine inhibits angiotensin II-induced activation of hepatic stellate cells associated with interference of platelet-derived growth factor-β receptor pathways[J]. FEBS J, 2014, 281 (12): 2754-68. doi:10.1111/febs.12818 |
| [10] | Zhang F, Kong D, Lei N, et al. Tetramethylpyrazine induces G0/G1 cell cycle arrest and stimulates mitochondrial-mediated and caspase-dependent apoptosis through modulating ERK/p53 signaling in hepatic stellate cells in vitro[J]. Apoptosis, 2013, 18 (2): 135-49. doi:10.1007/s10495-012-0791-5 |
| [11] | 陈玮, 陈维维, 陆允敏, 等. 川芎嗪干预大鼠实验性肝纤维化的研究[J]. 世界临床药物, 2007, 28 (9) : 522-5. Chen W, Chen W W, Lu Y M, et al. Experiment studies on the therapeutic effects of ligustrazine on liver fibrosis in rats[J]. Wold Clin Drugs, 2007, 28 (9): 522-5. |
| [12] | 郭屏, 王淑平, 刘丹萍. 川芎嗪联合促肝细胞生长素治疗慢性乙型病毒性肝炎肝纤维化疗效观察[J]. 中国药房, 2007, 8 (18) : 601-2. Guo P, Wang S P, Liu D P. Observation of therapeutic effects of ligustrazine combined with PHGF in the treatment of chronic type B hepatitis with hepatic fibrosis[J]. China Pharm, 2007, 8 (18): 601-2. |
| [13] | Kong D, Zhang F, Wei D, et al. Paeonol inhibits hepatic brogenesis via disrupting nuclear factor-κB pathway in activated stellate cells: in vivoand in vitrostudies[J]. J Gastroenterol Hepatol, 2013, 28 (7): 1223-33. doi:10.1111/jgh.2013.28.issue-7 |

