


2. 中国航天科工集团七三一医院药剂科,北京 100074;
3. 生物医学检测技术与仪器北京实验室,北京 100069
2. Dept of Pharmacy, Aerospace731 Hospital, Beijing 100074, China ;
3. Beijing Laboratory for Biomedical Detection Technology and Instrument, Beijing 100069, China
低氧(hypoxia)是影响生命活动和疾病发展的重要因素之一,在低氧环境下,机体组织器官的代谢功能会发生异常变化[1-2],结果会影响药物在体内的吸收、分布、代谢和排泄等药代动力学过程,进而影响药物的疗效和毒性[3-4]。因此,随着药代动力学研究的深入和临床个体化给药的需求,尤其是高原低氧环境影响和急进高原人群的增加,人们越来越关注低氧对药物药代动力学的影响及其后果[5]。在高原低氧条件容易引起呼吸系统感染,而罗红霉素(roxithromycin)是临床治疗肺部感染的常用抗生素之一,罗红霉素配合头孢类等抗生素广泛用于高原呼吸系统的感染治疗[6-9]。同时,罗红霉素对支原体肺炎和解脲脲原体引起的泌尿系统感染等也有良好疗效[10]。在药代动力学方面,罗红霉素耐酸而不易被胃酸破坏,在胃肠道吸收好,维持血药浓度较高水平,其峰值为所有大环内酯类最高,组织分布广泛[11-12]。基于罗红霉素的抗感染疗效与其体内血药浓度水平和药代动力学特征密切相关,因此,本文应用我们建立的UPLC-MS/MS方法研究比较了低氧和常氧状态下大鼠体内药代动力学特征,结果为临床合理用药提供重要的实验依据。
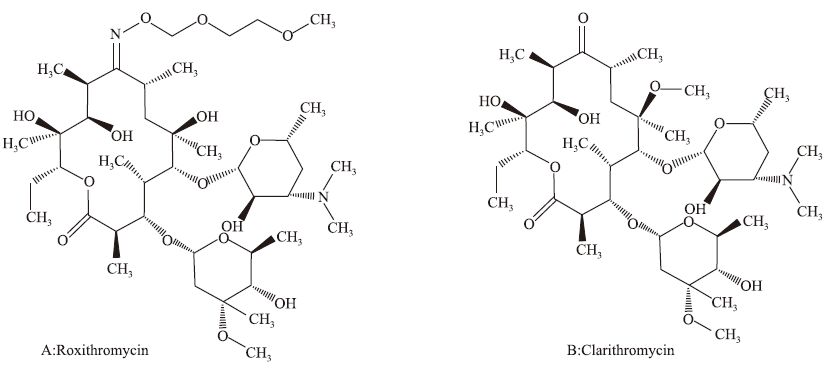
1 材料与方法 1.1 药物与试剂罗红霉素(批号:130557-201103)和克拉霉素(批号: 130558-201303)标准品均购自中国食品药品检定研究院,纯度≥99%,结构见Fig 1。乙腈、甲醇购自Thermo Fisher 公司 (Waltham,Australia)。实验所用水为双蒸水,甲酸购自Dikma Reagent 公司 (Beijing,China)。实验所用其他试剂纯度均为色谱级别。
|
| Fig 1 Chemical structures of roxithromycin (A) and clarithromycin (B) |
Sprague-Dawley (SD) 大鼠,体质量220 g~260 g,♂,购自北京维通利华实验动物技术有限公司,动物合格证编号:SCXK (京) 2012-0001。颈静脉插管大鼠,体质量为220 g~260 g,♂,购自思科诺思生物科技有限公司,实验动物合格证号:SCXK (京) 2016-0001。动物实验部分经过首都医科大学动物伦理委员会批准,动物伦理编号AEEI-2016-016。
1.3 仪器Agilent 1290超高效液相色谱仪联用Agilent 6490三重四级杆质谱;2D5-2A型低速离心机(北京医用离心机厂产品);高速离心机(美国Sigma公司);万分之一电子天平(北京赛多利斯科学仪器有限公司);Vortex-Genie 2旋涡混合器(美国SI公司);ZORBAX Eclipse Plus-C18色谱柱(100 mm×2.1 mm i.d,3.5 μm,美国Agilent公司);pH测试计(德国赛多利斯公司);一次性针头式尼龙滤膜(0.22 μm,北京鼎国昌盛生物技术有限责任公司);1~10 μL,1~200 μL及1~1 000 μL移液器(德国Brand公司)。
1.4 色谱与质谱条件液相色谱 (liquid chromatography,LC):流动相为乙腈 ∶水(35 ∶65,V/V)(水相中加入15 mmol·L-1乙酸),流速0.4 mL·min-1;柱温40 ℃;进样量5 μL。质谱部分:电喷雾离子化离子源(electro spray ionization,ESI),正离子检测模式;干燥气温度为200 ℃;干燥气体流速为16 L·min-1;喷雾器压力为35 Psi;鞘气温度为250 ℃;鞘气 (N2)流速为12 L·min-1;毛细管电压为3 500 V;喷嘴电压为1 500 V。质谱扫描方式为多重反应监测模式(multiple reaction monitoring,MRM),定量分析的离子(m/z) 分别为837.5→679.5(罗红霉素,20 ev)和748.5.→158.1(内标为克拉霉素,30 ev)。
1.5 血浆样品处理取1.5 mL离心管,加入大鼠血浆样品100 μL,加入浓度为200 μg·L-1的内标克拉霉素溶液10 μL,涡旋混匀。之后加入300 μL甲醇进行蛋白沉淀,每个样品均涡旋2 min,使其充分混匀,于13 000 r·min-1高速离心10 min。用一次性针头吸取上清液,过0.22 μm的有机膜,转移到样品瓶内插管中。进样体积均为5 μL。
1.6 标准溶液配置分别精密称取罗红霉素和克拉霉素5 mg,溶解于5 mL容量瓶中,以色谱级甲醇定容,分别配制成1 g·L-1的克拉霉素和罗红霉素标准储备液。再用流动相将罗红霉素储备液稀释成梯度工作液:10 000、5 000、1 000、500、100、50、10 μg·L-1,同时将内标克拉霉素储备液稀释成200 μg·L-1的工作液。将储备液和工作液均保存在4 ℃冰箱中备用。
1.7 罗红霉素在大鼠体内的药代动力学比较 1.7.1 常氧状态下的药代动力学将6只♂ SD插管大鼠分别编号并称重,按照10 mg·kg-1的给药剂量,灌胃给药。给药前禁食12 h,自由饮水。分别于给药前和给药后5、10、20、30 min及1、2、4、6、8、16、24、36 h经颈静脉取血约0.4 mL,置于含肝素的EP管中,13 000 r·min-1离心10 min,分离得到上层血浆。之后按“1.5”项下操作处理。
1.7.2 低氧状态下的药代动力学将6只♂ SD插管大鼠分别编号,每次取1只大鼠放入特制低氧箱 (含9 % 的氧气) 内,使大鼠持续低氧72 h,并且给药前禁食12 h,自由饮水。称重,按照常氧每公斤体质量给药量换算进行灌胃给药。分别于给药后5、10、20、30 min及1、2、4、6、8、16、24、36 h经颈静脉取血约0.4 mL,置于含肝素的EP管中,13 000 r·min-1离心10 min,分离血浆。按“1.5”项下操作处理。
1.8 统计学分析通过DAS2.0软件计算主要药代动力学参数,包括AUC(药时曲线下面积)、T1/2(血浆半衰期)、Cmax(达峰浓度)、tmax(达峰时间)、MRT(平均驻留时间)、CL(清除率) 和 V(分布容积)。所有数据用x±s表示。采用SPSS13.0 统计学软件进行t检验。
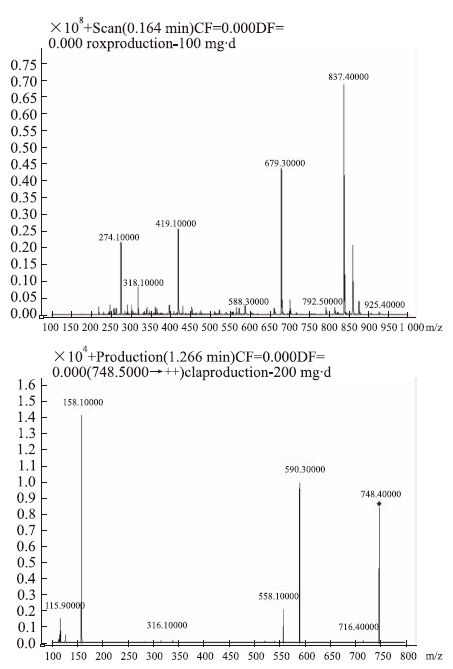
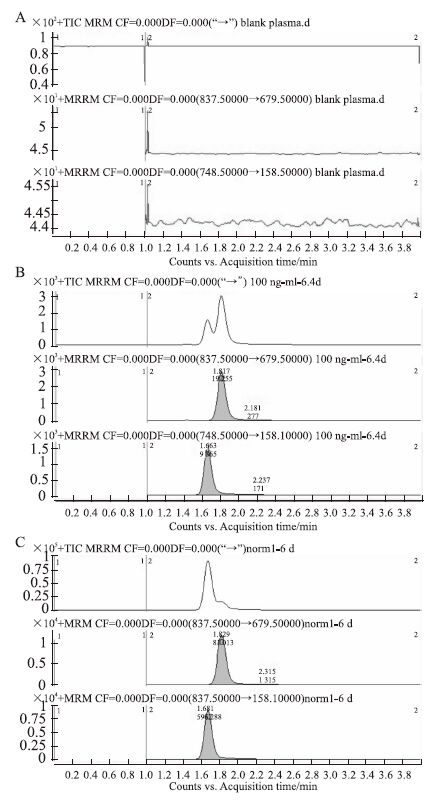
2 结果 2.1 方法学考察与验证 2.1.1 方法的专属性按照“1.4”的质谱条件,分别对罗红霉素和内标克拉霉素进行质谱全扫,测得罗红霉素的核质比为:m/z 837.5→679.5(Fig 2)、克拉霉素为:m/z 748.5→158.1(Fig 2)。大鼠空白血浆、空白血浆外加药物、大鼠给药后血浆样品经处理后的MRM模式色谱图见Fig 3,由图可见,罗红霉素与内标克拉霉素在血浆中无内源性干扰。罗红霉素的出峰时间为1.8 min,内标的出峰时间为1.6 min。
|
| Fig 2 Product ions of roxithromycin and clarithromycin (IS) |
|
| Fig 3 Chromatograms of rat plasma withroxithromycin and internal standard A:Blank rat plasma; B: Blank rat plasma spiked with roxithromycin (200 μg·L-1) and internal standard (200 μg·L-1); C: Rat plasma sample obtained 8 h after p.o. administration with a dose of 10 mg·kg-1 of roxithromycin. |
取1.5 mL离心管数支,分别加入梯度浓度的罗红霉素溶液10 μL和内标溶液 (200 μg·L-1) 10 μL,再分别加入大鼠空白血浆100 μL,涡旋混匀,配制成罗红霉素浓度分别为1、5、10、50、100、500、1 000 μg·L-1的含药血浆。按“1.5”项下操作,进行LC-MS/MS分析。以罗红霉素质量浓度X (μg·L-1)为横坐标,罗红霉素与内标峰面积之比Y为纵坐标,采用加权 (1/X2) 最小二乘法进行线性回归,制作标准曲线,得到回归方程为Y=0.028+0.016X,r2=0.991。多次测量最低定量下限(S/N>10),其值为1 μg·L-1。
2.1.3 准确度与精密度测定配制罗红霉素浓度分别为1、2、200、800 μg·L-1的含药血浆作为质控样品,在1 d内每个浓度各配制5份样品,计算样品和内标峰面积的比值,代入随行的标准曲线,得出样品的浓度,计算日内准确度与精密度。连续测定3 d共3批样品,计算日间准确度与精密度,结果见Tab 1。从表中看出,大鼠血浆质控样品的日内、日间精密度均小于9%,准确度均在±11.2%以内,符合生物样品分析要求。
| Concentration//μg·L-1 | Intra-day | Inter-day | ||
| Accuracy/% | Precision/% | |||
| Accuracy/% | Precision/% | |||
| 1 | 95.1±17.2 | 5.4 | 101±18.7 | 4.9 |
| 2 | 92.3±1.7 | 4.1 | 92.8±4.0 | 4.7 |
| 200 | 108.0±1.9 | 6.8 | 107.0±2.1 | 6.3 |
| 800 | 88.8±4.9 | 8.9 | 90.9±10.0 | 5.8 |
配制罗红霉素浓度分别为1、2、200、800 μg·L-1的含药血浆,每个浓度平行5份,测定所得罗红霉素的峰面积与空白血浆经样品处理后加入对应浓度的标准溶液的峰面积之比,计算提取回收率;空白血浆经过样品处理后加入最低定量下限、低、中、高4个浓度的标准溶液得到的峰面积与对应浓度的标准溶液的峰面积之比,计算基质效应,结果见Tab 2。结果表明,罗红霉素在该方法下回收率在76.8%以上,基质效应控制在±15.3%之内。
| Concentration/μg·L-1 | Recovery/% | Matrix effect/% |
| 1 | 76.8±4.9 | 87.9±8.8 |
| 2 | 104.0±2.4 | 115.0±2.7 |
| 200 | 102.0±1.0 | 90.1±0.5 |
| 800 | 93.8±1.4 | 89.2±1.2 |
配制罗红霉素浓度分别为1、2、200、800 μg·L-1的含药血浆,每个浓度平行5份,分别考察其室温放置4 h、3次冻融循环和-80℃冻存30 d稳定性。结果表明,与0时刻含药血浆相比较,变异均在1%范围内(Tab 3)。表明含药血浆在上述条件下稳定。
| Concentration/μg·L-1 | Measured/% | ||
| Room temperature for 4 h | Freeze thaw for three times | -80℃ for 30 d | |
| 1 | 99.5±6.5 | 100.1±12.7 | 99.7±2.9 |
| 2 | 99.6±3.0 | 99.9±3.7 | 100.9±1.8 |
| 200 | 100.2±0.4 | 100.1±0.8 | 100.3±0.5 |
| 800 | 100.1±1.2 | 101.3±1.3 | 100.1±0.8 |
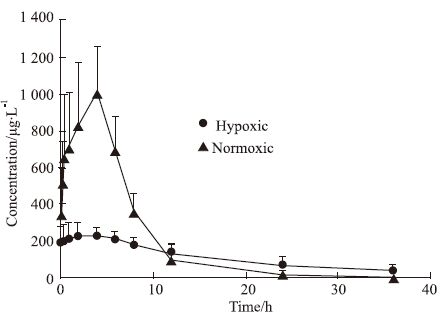
对常氧状态和低氧状态下的大鼠,分别给药后测定其对应时间点的血浆中罗红霉素的峰面积,并根据回归方程计算血药浓度。常氧与低氧状态下,相同剂量组的罗红霉素在大鼠体内对应的药物浓度-时间曲线见Fig 4。
|
| Fig 4 Mean plasma concentration-timecurves of roxithromycin in normoxic andhypoxic rats following intragastric administration to rats (n=6) |
将得到的罗红霉素血药浓度数据用药动学处理软件(DAS)处理后,得到常氧与低氧状态下大鼠的体内药物代谢动力学参数,见Tab 4。
| Parameters | Normoxic group | Hypoxic group |
| AUC(0-t)/μg·h·L-1 | 7 576±1 765 | 3 761±1 202** |
| AUC(0-∞)/μg·h·L-1 | 7 586±1 769 | 3 777±1 219** |
| MRT(0-t)/h | 5.6±0.7 | 7.7±0.9* |
| MRT(0-∞)/h | 5.6±0.8 | 7.9±0.9* |
| T1/2/h | 3.4±0.8 | 3.9±0.9 |
| tmax /h | 3.1±1.5 | 3.4±2.3 |
| V/L·kg-1 | 6.5±0.9 | 16.5±4.7** |
| CL /L·h-1·kg-2 | 1.5±0.5 | 3.0±0.8* |
| Cmax /μg·L-1 | 1 116±293 | 372±102** |
| *P<0.05,**P<0.01 vs normoxic group | ||
我们用特制的低氧操作装置维持环境9%的氧分压,将大鼠置于9%的氧气环境中72 h,建立了常压大鼠急性低氧模型[13-14]。该低氧装置的优点在于可设定不同程度的低氧环境,并且能保持氧浓度的恒定,在气体环境条件改变后可以迅速恢复,模拟低氧环境的重现性高。
超高效液相质谱联用的采用,提高了液相的分离测定效率[15-17]。经测定,常氧条件下罗红霉素在大鼠体内的主要药动学参数为:AUC(0-t)7 576 μg·h·L-1,MRT(0-t)5.6 h,T1/2 3.4 h,CL 1.5 L·h-1·kg-2,tmax 3.1 h,Cmax 1 116.2 μg·L-1。罗红霉素在低氧条件下的主要药动学参数为:AUC(0-t)3 761 μg· h·L-1,MRT(0-t)7.7h,T1/2 3.9 h,CL 3.0 L·h-1·kg-2,tmax 3.4 h,Cmax 372.1 μg·L-1 。比较低氧与常氧状态下,罗红霉素在大鼠体内的药代动力学参数可见,低氧状态下,Cmax与AUC的值明显降低,提示罗红霉素在低氧状态大鼠体内的吸收降低,体内暴露量明显减低。低氧状态下,罗红霉素的清除率CL明显增加,提示单位时间内每毫升血浆中罗红霉素被机体清除的量增大,这也可能是低氧状态AUC与体存量降低的原因。低氧状态下的T1/2和tmax与常氧的参数差异没有统计学意义,提示罗红霉素在低氧大鼠体内的消除半衰期和体内平均贮留时间没有明显变化。
罗红霉素脂溶性很强,容易透过生物膜,一般通过一级动力学被动扩散方式进行体内转运。而低氧状态下,药物的吸收和体存量减少,可能一方面源于外排蛋白,另一方面也可能是缺氧造成肠胃排空变慢,pH变化影响药物电离性,或者造成胃肠局部微环境改变,进而影响药物吸收[3, 4, 18]。低氧影响罗红霉素在动物体内代谢转运和药代动力学过程的分子机制尚待进一步研究。我们的研究结果表明,低氧可以明显降低罗红霉素在大鼠体内的达峰浓度和体存量,降低血浆药物浓度水平,进而影响药物治疗,结果为罗红霉素在低氧状态下的给药方案优化和调整提供了重要的实验依据。与常氧状态相比,缺氧状态下,罗红霉素的体内消除半衰期没有发生明显变化,但体内吸收和暴露量明显降低。因此,在缺氧状态下临床使用罗红霉素时,给药次数和时间间隔不变,但给药剂量至少需要增大1倍。
| [1] | West J B. High-altitude medicine[J]. Am J Respir Crit Care Med, 2012, 186 (12): 1229-37. doi:10.1164/rccm.201207-1323CI |
| [2] | Zafren K. Prevention of high altitude illness[J]. Travel Med Infect Dis,, 2014, 12 (1): 29-39. doi:10.1016/j.tmaid.2013.12.002 |
| [3] | 张娟玲, 李向阳. 高原低氧影响药物代谢的研究进展[J]. 药学学报, 2015, 50 (9) : 1073-9. Zhang J L, Li X Y. A review of drug metabolism under hypoxia environment at high altitude[J]. Acta Pharm Sin, 2015, 50 (9): 1073-9. |
| [4] | Ribeiro A L, Ribeiro V. Drug metabolism and transport under hypoxia[J]. Curr Drug Metab, , 2013, 14 (9): 969-75. doi:10.2174/1389200211314090003 |
| [5] | 郑悦, 嵇扬. 抗缺氧研究常用动物模型及抗缺氧药物[J]. 解放军药学学报, 2010, 26 (2) : 170-3. Zheng Y, Ji Y. The animal model and drugs for anti-hypoxia[J]. Pharm J Chin PLA, 2010, 26 (2): 170-3. |
| [6] | 吕雄文, 李俊, 徐元宏, 等. 单剂量与多剂量口服罗红霉素缓释片与普通片的犬体药物动力学研究[J]. 中国药理学通报, 2004, 20 (7) : 811-4. Lyu X W, Li J, Xu Y H, et al. Pharmacokinetics of orally administered sustained release cupsles and conventional tablets of roxithromycin in dogs[J]. Chin Pharmacol Bull, 2004, 20 (7): 811-4. |
| [7] | Janvier E A, Luo Z, Liu R J, et al. Study of pharmacokinetic interaction of paroxetine and roxithromycin on bencycloquidium bromide in healthy subjects[J]. Eur J Pharm Sci, 2015, 69 : 37-43. doi:10.1016/j.ejps.2014.12.019 |
| [8] | 夏晓东, 吴立琴, 徐慧罗, 等. 红霉素通过诱导型一氧化氮合酶/一氧化氮途径抑制哮喘大鼠气道炎症[J]. 中国药理学通报, 2009, 25 (9) : 1223-7. Xia X D, Wu L Q, Xu H L, et al. Roxithromycin inhibited airway inflammation through pathway of inducible nitricoxide synthase and nitric oxide in rat asthmatic model[J]. Chin Pharmacol Bull, 2009, 25 (9): 1223-7. |
| [9] | 徐慧, 戴元荣, 李凤琴, 等. 罗红霉素对哮喘平滑肌细胞增殖以及微囊蛋白-1及PI3K/Akt的影响[J]. 中国药理学通报, 2015, 31 (3) : 407-11. Xu H, Dai Y R, Li F Q, et al. Effect of roxithromycin on asthma smooth muscle cells proliferation,caveolin-1 and PI3K/Akt pathway[J]. Chin Pharmacol Bull, 2015, 31 (3): 407-11. |
| [10] | 郭文琪. 罗红霉素治疗泌尿生殖道衣原体与支原体感染65例[J]. 中国新药杂志, 1999, 8 (10) : 697-8. Guo W Q. Treatment with roxithromycin in 65 patients with chlamydia and mycoplasma infections in genitourinary tracts[J]. Chin J New Drug, 1999, 8 (10): 697-8. |
| [11] | Franciszek K G, Marta K L. Determination of roxithromycin in human plasma by HPLC with fluorescence and UV absorbance detection: application to a pharmacokinetic study[J]. J Chromatogra B, 2007, 852 (1): 669-73. |
| [12] | Wang P, Qi M, Jin X. Determination of roxithromycin in rat lung tissue by liquid chromatography-mass spectrometry[J]. J Pharm Biomed Anal, 2005, 39 (3): 618-23. |
| [13] | 徐唯哲, 赵妍, 秦一, 等. 低氧与常氧状态下芍药苷在大鼠体内的药代动力学比较[J]. 国际药学研究杂志, 2016, 43 (2) : 336-40. Xu W Z, Zhao Y, Qin Y, et al. Pharmacokinetic comparison of paeoniflorin in rats under normoxic and hypoxic conditions[J]. J Int Pharm Res, 2016, 43 (2): 336-40. |
| [14] | Gong W, Liu S, Xu P, et al. Simultaneous quantification of diazepam and dexamethasone in plasma by high-performance liquid chromatography with tandem mass spectrometry and its application to a pharmacokinetic comparison between normoxic and hypoxic rats[J]. Molecules,, 2015, 20 (4): 6901-12. doi:10.3390/molecules20046901 |
| [15] | 刘泽娟, 赵萍, 陈娟, 等. LC-MS/MS法测定人血浆中甲磺酸雷沙吉兰的浓度及其体内药动学研究[J]. 中国药理学通报, 2016, 32 (7) : 1017-22. Liu Z J, Zhao P, Chen J, et al. Determination of rasagiline mesylate in plasma by LC-MS/MS and its pharmacokinetics study[J]. Chin Pharmacol Bull, 2016, 32 (7): 1017-22. |
| [16] | 黄勇, 胡杰, 陆苑, 等. UPLC-MS法测定大鼠血浆中荭草花的3个指标成分及其药动学研究[J]. 中国药理学通报, 2015, 31 (9) : 1314-8. Huang Y, Hu J, Lu Y, et al. Pharmacokinetics of three index components in flower of Polygonumorientale L. in rat plasma by UPLC-MS[J]. Chin Pharmacol Bull, 2015, 31 (9): 1314-8. |
| [17] | 张璠璠, 王宇光, 梁乾德, 等. 基于UPLC-TOF-MS 研究冰片对丹参酮ⅡA在大鼠体内药代动力学的影响[J]. 中国药理学通报, 2014, 30 (6) : 862-6. Zhang F F, Wang Y G, Liang Q D, et al. UPLC-TOF-MS based profiling approach in evaluation of effect of borneol on pharmacokinetics of Tanshinone IIA in mice[J]. Chin Pharmacol Bull, 2014, 30 (6): 862-6. |
| [18] | Souic P D, Fradett C. The effect and clinical consequences of hypoxia on cytochrome P450, membrane carrier proteins activity and expression[J]. Expert Opin Drug Metab Toxicol,, 2011, 7 (9): 1083-100. doi:10.1517/17425255.2011.586630 |

