


2. 中国人民解放军总医院临床药理研究室,北京 100853;
3. 总参第六十一研究所门诊部,北京 100041;
4. 中国人民解放军总医院肿瘤内一科,北京 100853
 ,
DONG Xian-zhe2,
FENG Xia3,
HU Yuan2,
ZHENG Xiao-li2,
GE Xiao-yue2,
WANG Jin-liang4,
LIU Ping2
,
DONG Xian-zhe2,
FENG Xia3,
HU Yuan2,
ZHENG Xiao-li2,
GE Xiao-yue2,
WANG Jin-liang4,
LIU Ping2

2. Dept of Clinical Pharmacology,General Hospital of PLA, Beijing 100853,China ;
3. Outpatient Department of the 61st Research Institute of the PLA General Staff Headquarters, Beijing 100041 ;
4. Dept of Medical Oncology, General Hospital of PLA, Beijing 100853
血根碱(Sanguinaria canadensis,SAN)是一种苯并菲啶类生物碱,主要来源于血根草的根或者罂粟紫堇植物,分布于我国的长江流域、华南、华东地区。天然的SAN是罂粟科植物受到外界环境的有害刺激时产生的用于对抗真菌和细菌病原体等的抗毒素类物质,其本身可以被烟酰胺腺嘌呤二核苷酸磷酸还原为低毒的二氢还原体,使植物本身不受影响。由于其具有抗菌消炎的作用,最初作为牙膏添加剂来降低牙菌斑和牙龈炎的发生,或者用于空腔消毒清洗,它的独特作用已受到国内外的高度重视。
近年来,国内外的很多研究表明SAN具有抑制肿瘤细胞增殖和诱导细胞凋亡的作用,如结肠癌、口腔鳞状细胞癌、前列腺癌、人骨肉瘤以及胃癌等[1-6]。本课题组前期的研究也证明,SAN能够抑制人乳腺癌细胞MCF-7增殖,并诱导其凋亡[7]。本研究以氧化应激和caspase家族为切入点,探索其抑制MCF-7增殖的机制。
1 材料 1.1 细胞株人乳腺癌细胞MCF-7购自中国医学科学院肿瘤医院细胞库,由本实验室传代冻存。
1.2 主要试剂RPMI 1640培养基、胎牛血清(FBS),美国Gibco公司;MTT(四氮甲基四唑蓝),美国Sigma公司产品;活性氧检测试剂盒,碧云天生物技术研究所;caspase-Glo 3检测试剂盒、caspase- Glo 8检测试剂盒、caspase-Glo 9检测试剂盒,美国Promega公司;NAC,美国Sigma公司; caspase-3抑制剂(Ac-DEVD-CHO),美国Promega公司;caspase-8抑制剂(Z-IETD-FMK),美国BioVision公司;caspase-9 抑制剂(Z-LEHD-FMK·TFA),美国Sigma公司。
2 方法 2.1 MTT法检测SAN对MCF-7的增殖抑制作用取对数生长期MCF-7细胞,以7×107·L-1的密度接种于96孔培养板中,每孔100 μL,37 ℃、5% CO2、饱和湿度条件下培养24 h,然后加入不同浓度的SAN,使其终浓度分别为2.5、5、10、20、40 μmol·L-1,正常对照组加入不完全RPMI 1640。考察NAC及caspase抑制剂对细胞存活率的影响时,在加入5、10 μmol·L-1 SAN的同时再分别加入5或10 μmol·L-1的NAC,caspase-3抑制剂 (Ac-DEVD-CHO)、caspase-8抑制剂(Z-IETD-FMK)和caspase-9 抑制剂(Z-LEHD-FMK·TFA)组在加入10 μmol·L-1的SAN的同时分别加入上述抑制剂,终浓度分别为1、2、20 μmol·L-1[8]。细胞继续培养48 h,然后加入终浓度为0.5 mg·L-1的MTT,4 h后弃去培养液,每孔加入150 μL的DMSO,振荡溶解10 min后,在570 nm处检测OD值[9]。
2.2 SAN对MCF-7细胞内ROS的影响取对数生长期MCF-7细胞,以2×108·L-1的密度接种于Petri皿,每个皿200 μL。CO2孵箱中培养24 h。然后分别加入终浓度为5、10 μmol·L-1的SAN,正常对照组加入不完全RPMI 1640,NAC组及Ac-DEVD-CHO、Z-IETD-FMK和Z-LEHD-FMK·TFA组的处理方法同前。继续培养48 h后吸去培养液,PBS洗3次。各组分别加入200 μL终浓度为10 μmol·L-1的ROS特异性荧光探针DCFH-DA。37℃避光孵育35 min。其间每隔3~5 min轻摇混匀一下,使探针和细胞充分接触。孵育结束后用无血清培养基洗涤细胞3次,以除去未进入细胞内的DCFH-DA。将Petri皿置于活细胞激光扫描共聚焦显微镜(UltraView-Vox,美国 PinkerElmer公司)物镜下方的细胞培养小室内,设置温度为37 ℃,CO2浓度为5%。在明场光源下调整焦距,在汞灯下观察细胞内荧光探针标记情况,并进一步调整焦距。然后将光路转换至左光路,关闭明场光源,打开激光,设置激发波长为488 nm。每组选择10个视野,检测细胞内荧光强度,由Volocity软件计算各组荧光强度。
2.3 SAN对MCF-7细胞内caspase-3、caspase-8、caspase-9活性的影响取对数生长期细胞,调整细胞密度至7×107·L-1,接种于96孔板,每孔100 μL,37 ℃、5% CO2饱和湿度条件下培养24 h。然后分别加入终浓度为5、10 μmol·L-1的SAN,正常对照组加入不完全RPMI 1640,NAC组同时加入5、10 μmol·L-1的NAC,NAC组及Ac-DEVD-CHO、Z-IETD-FMK和Z-LEHD-FMK·TFA组的处理方法同前,继续培养48 h。按照caspase-3、-8、-9说明书,先将caspase-Glo底物溶于caspase-Glo缓冲液中,并加入蛋白酶体抑制剂,配制成caspase-Glo试剂,将caspase-Glo试剂加入93孔板中,室温避光孵育相应时间,然后将上清液转移至不透光的96孔白板中,多标记微孔板检测仪(Victor 1420,美国 PinkerElmer公司)选择luminescence模式,检测各孔化学发光强度,读数即代表各组细胞内caspase-3、-8、-9的相对活性。
2.4 统计学分析结果用x±s表示。用Sigmaplot 10.0绘图软件做图,采用SPSS 16.0统计软件进行统计学数据处理,组间均数比较均采用单因素方差分析(one-way ANOVA)。
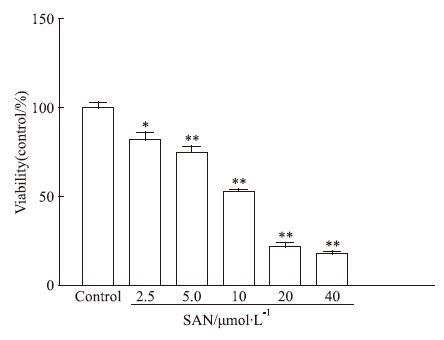
3 结果 3.1 SAN对MCF-7细胞的增殖抑制作用MTT法检测不同浓度的SAN作用48 h对MCF-7细胞增殖情况的影响。如Fig 1所示,SAN在2.5~40 μmol·L-1浓度范围内对MCF-7细胞的增殖有明显的抑制作用,并且呈现浓度依赖性。10 μmol·L-1的SAN作用48 h对MCF-7细胞的抑制率即接近50%。
|
| Fig 1 Antiproliferation effects of various concentrations of SAN on MCF-7 cells(n=5) *P<0.05,**P<0.01 vs control |
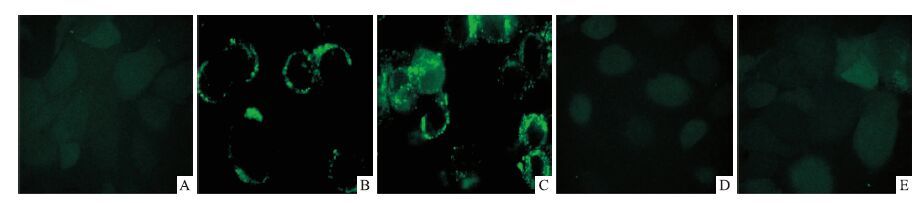
如Fig 2所示,以终浓度为5、10 μmol·L-1的SAN作用于MCF-7细胞48 h后,活细胞激光扫描共聚焦显微镜下采集图片并分析荧光强度(FI),SAN干预组细胞内荧光强度较正常对照组明显升高;而在10 μmol·L-1SAN干预的同时,给予5、10 μmol·L-1的NAC,细胞内的荧光强度明显降低,低于10 μmol·L-1 SAN单独干预组(P<0.01)。
|
| Fig 2 Effects of SAN and NAC on ROS content in MCF-7 cells(n=3) A: Control; B:SAN 5 μmol·L-1; C: SAN 10 μmol·L-1; D: SAN 10 μmol·L-1+NAC 5 μmol·L-1; E: SAN 10 μmol·L-1+NAC 10 μmol·L-1; F: A semiquantitative assay of fluorescence intensity. *P<0.05,**P<0.01 vs control; ##P<0.01 vs SAN 10 μmol·L-1 |
如Fig 3所示,终浓度为5、10 μmol·L-1的SAN可明显降低细胞存活率(P<0.01),5、10 μmol·L-1的NAC单独使用对细胞增殖没有影响;5、10 μmol·L-1的NAC可逆转10 μmol·L-1的SAN对MCF-7细胞增殖的抑制作用(P<0.05,P<0.01)。
|
| Fig 3 Effects of SAN and NAC on cell proliferation in MCF-7 cells(n=5) **P<0.01 vs control; #P<0.05,##P<0.01 vs SAN 10 μmol·L-1 |
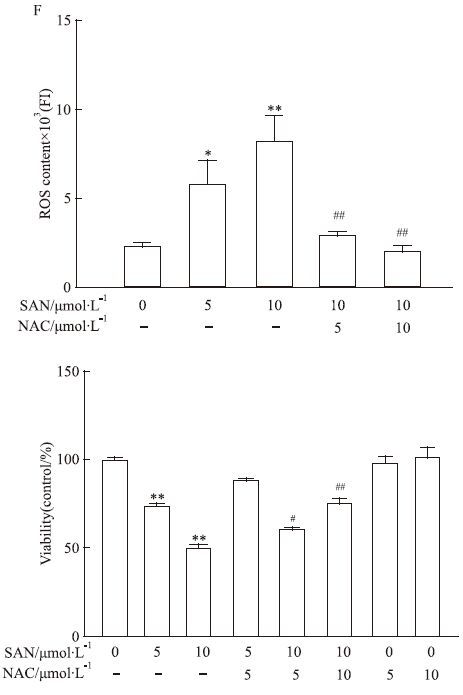
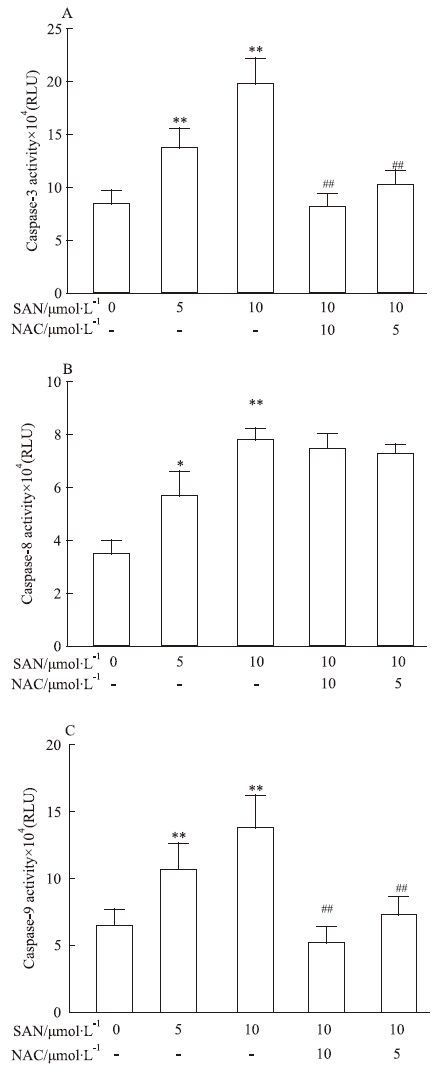
化学发光法检测发现,终浓度为5、10 μmol·L-1的SAN作用于MCF-7细胞后,MCF-7细胞内caspase-3、caspase-8和caspase-9的活性与正常对照组相比都有明显升高(P<0.01),呈明显的浓度依赖关系;5、10 μmol·L-1的NAC可抑制SAN对caspase-3和caspase-9活性的升高作用(P<0.01),对caspase-8活性未见明显影响(Fig 4)。
|
| Fig 4 Effects of SAN on caspase-3 (A),caspase-8 (B) and caspase-9 (C) activities in MCF-7 cell(n=5) *P<0.05,**P<0.01 vs control;##P<0.01 vs SAN 10 μmol·L-1 |
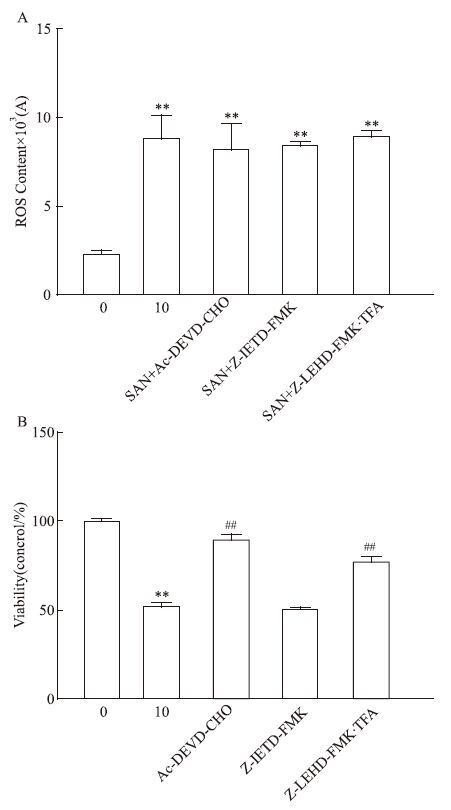
鉴于NAC对caspase-3和caspase-9活性的抑制作用,观 察了caspase-3、caspase-8和caspase-9的抑制剂对细胞内ROS及细胞增殖的影响。由Fig 5A可见,单用10 μmol·L-1的SAN作用后,MCF-7细胞内ROS含量较正常对照组明显升高,细胞活力明显下降;caspase-3、caspase-8、caspase-9抑制剂与10 μmol·L-1的SAN同时使用后,MCF-7细胞内ROS含量较单用SAN没有明显的变化;然而,caspase-3和caspase-9的抑制剂虽不能降低细胞内ROS水平,却能明显逆转SAN导致的MCF-7细胞存活率的下降(Fig 5B)。
|
| Fig 5 Effects of inhibitors of caspase-3,caspase-8 and caspase-9 on ROS content (A) and cell proliferation (B) in MCF-7 cells(n=5) **P<0.01 vs control;##P<0.01 vs SAN 10 μmol·L-1 |
活性氧(reactive oxygen species,ROS)是呼吸链底物端和氧端漏出的电子,没有参加ATP合成,而在体内被氧化产生的一类氧的单电子还原产物[10],包括氧的一电子还原产物超氧阴离子、二电子还原产物过氧化氢、三电子还原产物羟基自由基以及一氧化氮等[11]。在生物体内,氧化与抗氧化处于一种动态平衡状态。ROS是细胞代谢不可避免的产物,正常情况下,细胞代谢并释放低浓度的ROS以促进细胞增殖,同时生物体内有多种清除ROS的酶,如超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GSH-Px)等。它们可以清除代谢过程中不断产生的ROS,使得细胞内ROS处于一个相对稳定的水平[12]。当这种平衡一旦被某些因素打破,使细胞内ROS产生增多,就可以通过激活相关的细胞凋亡信号转导途径,诱导细胞凋亡,甚至死亡[13]。
caspases是近年来发现的一组存在于胞质溶胶中的结构上相关的半胱氨酸蛋白酶,它们是细胞凋亡信号转导通路中最重要的一类酶。由于caspase可自我活化并能相互激活,因此凋亡过程一旦触发,即呈级联放大效应[14]。caspases依赖的细胞凋亡信号转导途径包括线粒体途径和死亡受体途径。线粒体途径中caspase-9最为重要,又称为caspase-9途径;死亡受体途径中caspase-8尤其关键,所以又称为caspase-8途径[15],这两条途径最终都激活caspase-3。caspase-3是效应型半胱天冬蛋白酶 ,可以进一步裂解与凋亡相关的靶蛋白和酶类,进而导致细胞凋亡。
本研究发现,SAN能够明显抑制人乳腺癌细胞MCF-7增殖。采用活细胞激光扫描共聚焦显微镜观察发现,SAN可以升高细胞内ROS的水平;化学发光实验结果显示,SAN能升高MCF-7细胞内caspase-3、capase-8、caspase-9活性。由此提示SAN抑制MCF-7细胞增殖与升高细胞内ROS、激活caspases级联反应密切相关,但二者何为因果尚不明确。因此,本文又进一步分别研究了ROS抑制剂对caspase-3、capase-8、caspase-9活性和细胞增殖的影响,以及caspase-3、capase-8、caspase-9的抑制剂对细胞内ROS含量和细胞增殖情况的影响。结果显示,ROS抑制剂NAC能明显抑制caspase-3和caspase-9的活性,升高细胞存活率;caspase-3、caspase-9的抑制剂也能明显升高细胞的存活率,却不能降低SAN作用后MCF-7细胞内ROS水平。由此可初步确定,SAN通过升高细胞内ROS的水平,进而激活caspase级联反应,升高caspase-3活性,抑制MCF-7细胞增殖。
( 致谢: 本实验在中国人民解放军总医院临床药理研究室肿瘤实验室完成,感谢刘屏老师、董宪喆老师对本实验整体设计的把握和指导,感谢胡园老师在数据统计分析方面给予的帮助;感谢汪进良教授对本研究的资助,感谢郑小丽、葛晓悦在细胞培养、激光共聚焦检测等实验技术上给予的帮助 )
| [1] | Choi W Y, Jin C Y, Han M H, et al. Sanguinarine sensitizes human gastric adenocarcinoma AGS cells to TRAIL-mediated apoptosis via down-regulation of AKT and activation of caspase-3[J]. Anticancer Res, 2009, 29 (11) : 4457-65 . |
| [2] | Park H, Bergeron E, Senta H, et al. Sanguinarine induces apoptosis of human osteosarcoma cells through the extrinsic and intrinsic pathways[J]. Biochem Biophys Res Commun, 2010, 399 (3) : 446-51 . |
| [3] | Sun M, Lou W, Chun J Y, et al. Sanguinarine suppresses prostate tumor growth and inhibits survivin expression[J]. Genes Cancer, 2010, 1 (3) : 283-92 . |
| [4] | Sun M, Liu C, Nadiminty N, et al. Inhibition of Stat3 activation by sanguinarine suppresses prostate cancer cell growth and invasion[J]. Prostate, 2012, 72 (1) : 82-9 . |
| [5] | Tsukamoto H, Kondo S, Mukudai Y, et al.Evaluation of anticancer activities of benzo[c] phenanthridine alkaloid sanguinarine in oral squamous cell carcinoma cell line[J].Anticancer Res,2011,31(9): 2841-6. |
| [6] | Lee J S, Jung W K, Jeong M H, et al. Sanguinarine induces apoptosis of HT-29 human colon cancer cells via the regulation of Bax/Bcl-2 ratio and caspase-9-dependent pathway[J]. Int J Toxicol, 2012, 31 (1) : 70-7 . |
| [7] | Dong X Z, Zhang M, Wang K, et al. Sanguinarine inhibits vascular endothelial growth factor release by generation of reactive oxygen species in MCF-7 human mammary adenocarcinoma cells[J]. Biomed Res Int 2013, 2013 : 517698 . |
| [8] | He X L, Zhang P, Dong X Z, et al. JR6, a new compound isolated from Justicia procumbens, induces apoptosis in human bladder cancer EJ cells through caspase-dependent pathway[J]. J Ethnopharmacol, 2012, 144 (2) : 284-92 . |
| [9] | Dong X Z, Xie T T, Zhou X J, et al. AG4, a compound isolated from Radix Ardisiae Gigantifoliae, induces apoptosis in human nasopharyngeal cancer CNE cells through intrinsic and extrinsic apoptosis pathways[J]. Anticancer Drugs, 2015, 26 (3) : 331-42 . |
| [10] | 董宪喆, 毕明刚. 活性氧对P-糖蛋白调节作用的研究进展[J]. 中国药理学通报, 2010, 26 (10) : 1386-90 . Dong X Z, Bi M G. Research progress on regulation of P-glycoprotein by reactive oxygen species[J]. Chin Pharmacol Bull, 2010, 26 (10) : 1386-90 . |
| [11] | Gores G J, Miyoshi H, Bolta R, et al. Induction of mitochondrial permeability transition as a mechanism of liver injury during cholestasis: a potential role for mitochondrial protease[J]. Biochim Biophys Acta, 1998, 1366 (1-2) : 167-75 . |
| [12] | Jin Y, Dai J, Chamlmer S, et al. Arsenic trioxide selectively induces acute promyelocytic leukemia cell apoptosis via hydrogen peroxide dependent[J]. Blood, 1999, 94 (8) : 2102-11 . |
| [13] | 马永成, 苏楠, 秦玉花, 等. 新天然化合物Jaridonin通过诱导氧化应激选择性杀伤肿瘤细胞[J]. 中国药理学通报, 2015, 31 (2) : 198-203 . Ma Y C, Su N, Qin Y H, et al. Jaridonin : selective killing of cancer cells through oxidative stress[J]. Chin Pharmacol Bull, 2015, 31 (2) : 198-203 . |
| [14] | Mi S L, An C C, Wang Y, et al. Trichomislin, a novel ribosome-inactivating protein, induces apoptosis that involves mitochondria and caspase-3[J]. Arch Biochem Biophys, 2005, 434 (2) : 258-65 . |
| [15] | Senthil V, Ramadevi S, Venkatakrishnan V, et al. Withanolide induces apoptosis in HL-60 leukemia cells via mitochondria mediated cytochrome c release and caspase activation[J]. Chem Biol Interact, 2007, 167 (1) : 19-30 . |