


2. 青岛大学附属医院乳腺外科,山东 青岛 266000;
3. 即墨市妇幼保健院检验科,山东 即墨 266012;
4. 青岛大学医学院生物化学与分子生物学教研室,山东 青岛 266000
2. Dept of Breast Surgery, the Affiliated Hospital of Qingdao University, Qingdao Shandong 266000, China ;
3. Dept of Laboratory,Women and Children´s Care Center of Jimo, Jimo Shandong 266012, China ;
4. Dept of Biochemistry, Medical College, Qingdao University, Qingdao Shandong 266021,China
随着长春碱、长春新碱等新型抗肿瘤药物在临床上的应用,天然吲哚类化合物的抗肿瘤作用日益引起人们的关注,因其毒性低而迅速成为抗癌药物研究的热点。isatin,又名靛红,系天然存在于自然界的吲哚类化合物[1],是我国独创I类天然抗癌新药靛玉红的单体结构,存在于人体及多种生物体中,也存在于大青叶及清热解毒抗癌中药青黛中,具有广泛的生物学活性[2]和生物学效应[3]。1999年,Yue等[4]首次报告了isatin有抗氧自由基作用,能够保护正常神经细胞,并可减轻H2O2导致的多巴胺能细胞损伤。在之后的研究中,Cane等[5]报道用isatin和5-羟基吲哚处理N1E-115神经母瘤细胞系,可抑制ERK-2的磷酸化,从而抑制细胞增殖、促进细胞凋亡。isatin的这种既能抗肿瘤,又可通过抗氧自由基保护正常细胞的特性是目前大多数抗肿瘤药所不具有的重要特征。isatin分子量小(Mr147),能口服给药,具有靶向抑制肿瘤细胞增殖并避免损伤正常细胞的优点,毒副作用低(已完成急性毒性实验和6个月的长期毒性实验,未发现isatin有明显毒性),故认为isatin是很有开发价值的天然的小分子化合物类药物。
研究表明,isatin及其衍生物具有抗肿瘤活性,但这些研究大多限于现象描述,对抗肿瘤活性机制的研究报道较少,如isatin能明显抑制人类急性骨髓性白血病(HL60)肿瘤细胞系的增殖。进一步对isatin进行研究评估,认为isatin既可以预防氧自由基诱发肿瘤,又可以直接诱导肿瘤细胞凋亡[6];在体外用isatin处理中国仓鼠卵巢细胞(CHO-K1)和人宫颈癌细胞(HeLa)24 h后,能够抑制细胞增殖、促进细胞凋亡[7];课题组前期发表的文章也证实isatin对神经母细胞瘤细胞SH-SY5Y有明显的抑制作用[8]。迄今为止,有关isatin抗乳腺癌的研究较少,刘娜等[9]的研究认为isatin 对DMBA 诱发的大鼠乳腺癌有预防作用。我们前期实验结果显示:isatin能明显诱导乳腺癌细胞MCF-7凋亡,并抑制其增殖;同时使Bcl-2蛋白表达下降,Bax蛋白表达增加[10]。因此,本实验的目的是在前期研究的基础上,进一步证实isatin对MCF-7细胞的促凋亡作用,探究其可能的调控机制。
1 材料与方法 1.1 主要试剂isatin购自上海元吉化工有限公司,使用少量DMSO将其溶解,母液浓度配制为5 mmol·L-1,于4 ℃保存,备用。实验时用无血清培养基稀释至实验浓度(0、50、100、200 μmol·L-1)(DMSO浓度控制在<1 %); p53、Bcl-2、Bax和β-actin的抗体购自New England Biolabs公司; TRIzol RNA isolation kit购自Life Technologies公司;ECL发光试剂购于Amersham Biosciences公司; Hoechst33258、碘化丙啶(PI)染料购自美国Sigma公司。
1.2 细胞株及其培养乳腺癌细胞系MCF-7来自北京协和医学院基础学院细胞中心。细胞用H-DMEM 培养基(Gibco公司产品),含15%胎牛血清(杭州四季青生物公司),5% CO2、37 ℃饱和湿度条件下培养。
1.3 Hoechst 33258 荧光染色检测细胞凋亡的形态学改变对数生长期的细胞,调节细胞密度为每毫升5×104,接种于6孔板,并放入包被了多聚赖氨酸的盖玻片。37 ℃、5% CO2条件下孵育24 h后更换新培养液,同时加入不同浓度isatin,继续培养48 h后弃培养液,用甲醇 ∶冰醋酸(3 ∶1)于4 ℃固定5 min,PBS漂洗2遍,终浓度为5 mg·L-1 Hoechst 33258避光染色10 min,PBS清洗后封片,在荧光显微镜下观察,实验重复3次。
1.4 RT-PCR测定p53 mRNA、Bcl-2 mRNA、Bax mRNA的相对表达水平各实验组的细胞收集于1.5 mL的Eppendorf管中,PBS洗涤3次后,利用TRIzol RNA isolation kit提取RNA,按试剂盒说明进行RT-PCR。p53的引物序列为:5´-CTGAGGTTGGCTCTGACTGTACCACCATCC-3´,5´-CTCATTCAGCT CTCGGAACATCTCGAAGCG-3´,370 bp;内参照GAPDH的引物序列为:5´-CGTGGAAGGACTCATGACCA-3´,5´-TCCAGGGGTCTTACTCCTTG-3´,512 bp。Bcl-2的引物序列为:5´-GGAGGATTGTGGCCTTCTTTG-3´,5´-GGTGCCGGTTCAGGTACTCA-3´,120 bp;Bax的引物序列为:5´-TCCACCAAGAAGCTGAGCGAG-3´,5´-GTCCAGCCCATGATGGTTCT-3´,257 bp;内参照GAPDH的引物序列为:5´-ACCACAGTCCATGCCATCAC-3´,5´-TCCACCACCCTGTTGCTGTA-3´,452 bp。取PCR反应产物5 μL,1.5%的琼脂糖凝胶电泳分析,对照标准分子量检测扩增结果。上海培清凝胶紫外摄像分析系统照相后对条带进行光密度(A)扫描,分别检测各组PCR产物与其对应的内参A值,实验重复3次。
1.5 Western blot检测Bcl-2、Bax、p53 蛋白表达4 ℃条件下收集不同处理组细胞,PBS 洗涤2次后,每管加入150 μL蛋白裂解液,冰上裂解30 min,4 ℃ 12 000 r·min-1离心5 min后,收集上清液,考马斯亮蓝法确定蛋白质浓度。蛋白质样品与样品Buffer按4 ∶1的比例混匀,煮沸3 min。每孔加样40 μg,12% SDS-PAGE凝胶电泳分离样品。室温恒流(40 mA)1.5 h将蛋白转至PVDF膜,封闭液(5%脱脂奶粉,溶于TBS)室温封闭2 h后,将膜与含一抗稀释液(1%脱脂奶粉,溶于TBS中)的一抗(兔抗人β-actin 抗体1 ∶ 1 000,兔抗人p53抗体1 ∶ 1 000,兔抗人Bcl-2 抗体1 ∶1 000,兔抗人Bax 抗体1 ∶ 1 000)封于塑胶袋中,4 ℃过夜,再室温孵育2 h,TBS洗15 min×3次,将膜与含有第二抗体的稀释液(1%脱脂奶粉,溶于TBS中) 室温孵育3 h,TBST洗15 min×3次,将膜包在保鲜膜中,加入ECL发光试剂,在暗室曝光,显影,定影。X光底片经扫描后,永久保存并对结果进行光密度分析。实验重复3次。
1.6 流式细胞仪检测细胞膜电位收集对照组及不同浓度isatin处理组细胞,PBS洗涤2次后,与含5 μmol·L-1 Rhodamine 123的PBS室温避光孵育30 min,PBS清洗2次,离心弃PBS,PBS 重悬,用流式细胞仪进行检测(CantoⅡ,Becton Dickinson,USA)。实验重复3 次。
1.7 Western blot分别检测胞质和线粒体Cyto-chrome C蛋白表达收集对照组及不同浓度isatin处理组细胞,冰冷的PBS洗两次,将细胞重悬于Buffer A(250 mmol·L-1 sucrose,1 mmol·L-1 EDTA,50 mmol·L-1 Tris-HCl,1 mmol·L-1 DTT,1 mmol·L-1 PMSF,1 mmol·L-1 Benzamidine,280 u·L-1 apotinin,50 mg·L-1 leupeptin,and 7 mg·L-1 pepstainA,pH 7.4)中,转移至1 mL玻璃匀浆器,放至冰浴中,上下抽拉30次后离心(1 000 g×10 min,4 ℃),弃沉淀,将上清移至一新EP管中,再离心(10 000 g×20 min,4 ℃),所得上清和沉淀分别为胞质、线粒体粗品。为排除溶酶体和过氧化物体污染,需做进一步处理,将胞质部分转移至超离管中,离心(100 000×g,1 h,4 ℃),所得上清为纯化的胞质蛋白;将线粒体沉淀部分重悬于Buffer B(250 mmol·L-1 sucrose,1 mmol·L-1 EGTA,10 mmol·L-1 Tris-HCl,1 mmol·L-1 DTT,1 mmol·L-1 PMSF,1 mmol·L-1 Benzamidine,280 u·L-1 apotinin,50 mg·L-1 leupeptin,and 7 mg·L-1 pepstain A,pH 7.4)中,离心(10 000×g,10 min,4℃),重复3次,所得线粒体沉淀于细胞裂解液中裂解(10 mmol·L-1 Tris-HCl,pH 7.5;150 mmol·L-1 NaCl;5 mmol·L-1 EDTA;1% Triton X-100;1%去氧胆酸钠;1% SDS;1 mmol·L-1 PMSF;280 u·L-1 Aprotinin;50 mg·L-1 leupeptin;7 mg·L-1 Pepstatin A),分装以上蛋白溶液备用。Western blot步骤同“1.5”中所述。
1.8 流式细胞仪检测caspase-9的活化收集对照组及不同浓度isatin处理组细胞,PBS清洗2次后,与FITC-LEHD-FMK(a specific inhibitor of caspase-9)(eBioscience,1 ∶300)室温避光孵育30 min,PBS清洗2次,离心弃PBS,再用PBS 重悬,流式细胞仪进行检测(CantoⅡ,Becton Dickinson,USA)。实验重复3次。
1.9 统计学处理计量资料以x±s表示,利用SPSS 11.5统计软件进行单因素方差分析。
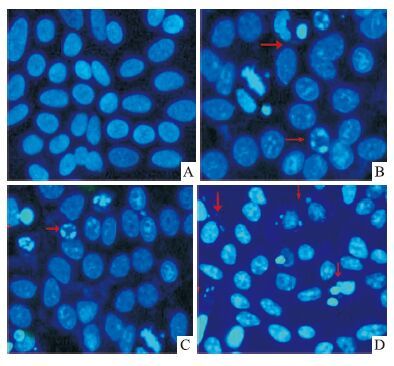
2 结果 2.1 isatin处理后细胞形态学变化如Fig 1所示,MCF-7细胞与不同浓度isatin共同孵育48 h后,在荧光显微镜下观察到细胞胞体缩小、胞质发生浓缩、核染色质聚集,并有凋亡小体等典型的凋亡形态学改变。而对照组细胞核呈现均匀的蓝色荧光。
|
| Fig 1 Apoptosis induction after 48 h treatment with isatin in MCF-7 cells Morphology of MCF-7 cells observed under fluorescence microscope(Hoechst33258×400). DNA fragment and chromatin condensation were observed in isatin-treated cells(B: 50 μmol·L-1 isatin,C: 100 μmol·L-1 isatin,D: 200 μmol·L-1 isatin),but few in untreated cells(A: Control). |
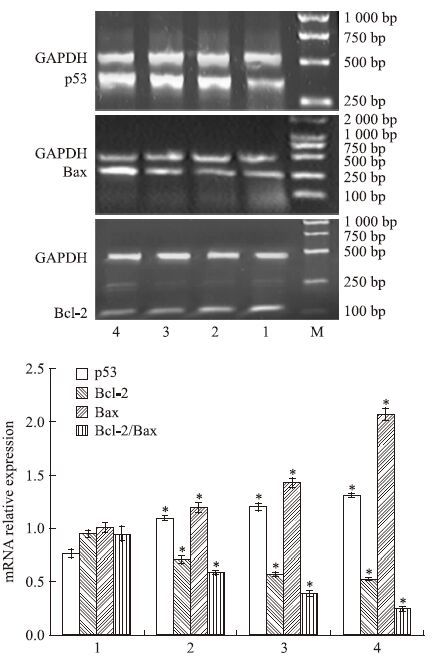
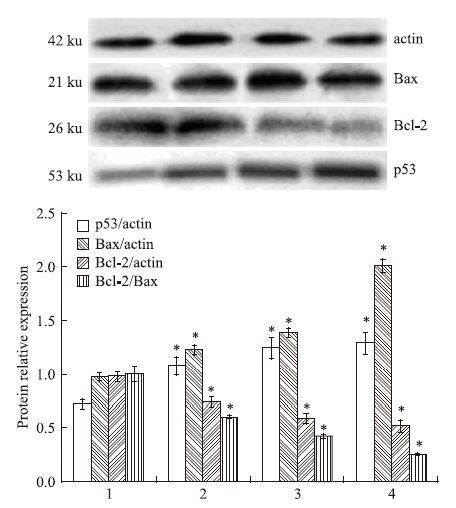
与对照组细胞相比,经50、 100、 200 μmol·L-1 isatin处理的各组MCF-7细胞,随着isatin浓度的不断增加,p53 mRNA、蛋白表达量相应增加,差异具有显著性(P<0.05);对照组细胞表达一定量的Bcl-2 mRNA、蛋白,不同浓度isatin处理组细胞Bcl-2 mRNA、蛋白表达量均出现不同程度下降(P<0.05),而Bax mRNA、蛋白在各组之间的差异没有明显改变,Bcl-2/Bax 逐渐下降(P<0.05),见Fig 2、3。
|
| Fig 2 RT-PCR of p53(Ap53/AGAPDH),Bcl-2(ABcl-2/AGAPDH) and Bax(ABax/AGAPDH) mRNA relative expression in MCF-7 cells after 48 h of culture with isatin Total RNA was extracted from the cultured cells using a Trizol RNA isolation kit and detected by RT-PCR. The densitometric quantification was normalized to GAPDH. Data are shown as the x±s. for three independent experiments.*P<0.05 vs Control. The Gel electrophoresis is representative of three independent experiments. Lane 1: Control cells; lanes 2~4: MCF-7 cells treated with 50,100 and 200 μmol·L-1 isatin,respectively. |
|
| Fig 3 Expression of p53,Bcl-2 and Bax proteins in MCF-7 cells after 48 h of treatment with isatin detected by Western blot Total protein from whole-cell extracts were separated by SDS-PAGE. Western blot analysis was performed with specific antibodies against cytochrome C. The densitometric quantification was normalized to β-actin. Data are shown as the x±s. for three independent experiments.*P<0.05 vs Control. The immunoblot is representative of three independent experiments. Lane 1: Control cells; lanes 2~4: MCF-7 cells treated with 50,100 and 200 μmol·L-1 isatin,respectively. |
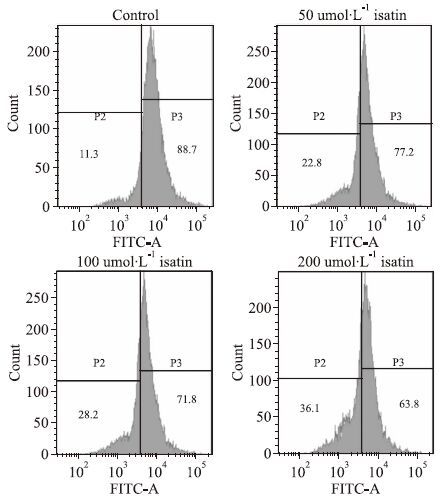
细胞膜电位下降是细胞凋亡的早期形态学特征,利用特征性探针Rhodamine 123与各组细胞孵育,细胞结合荧光染料的强度与线粒体膜的极化状态直接相关。流式细胞仪检测的结果是不同浓度(50、100、200 μmol·L-1)isatin处理组细胞线粒体膜电位分别为(77.00±2.27)%、(71.47±2.12)%、 (63.67±4.40)%,明显低于对照组细胞的电位(88.40±6.15)%(P<0.05),见Fig 4。
|
| Fig 4 Isatin-induced Dym depolarization in MCF-7 cells(representative experiment). Cells treated with isatin for 48 h were stained with rhodamine 123 for 30 min and then measured by flow cytometry (representative experiment). |
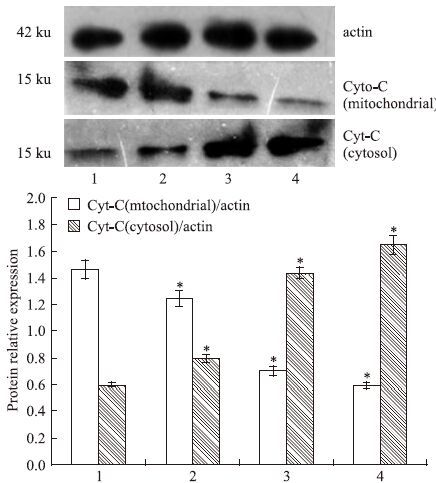
Cytochrome C的释放是凋亡级联反应中关键的一步,因为它可以激活下游的caspase,如Fig 5结果所示与对照组细胞相比,经不同浓度(50、100、200 μmol·L-1)isatin处理的MCF-7细胞胞质Cytochrome C含量明显增加,相反线粒体Cytochrome C表达明显下降(P<0.05)。
|
| Fig 5 Expression of cytochrome C proteins in MCF-7 cells after 48 h of treatment with isatin detected by western blot Total protein from whole-cell extracts were separated by SDS-PAGE. Western blot analysis was performed with specific antibodies against cytochrome C. The densitometric quantification was normalized to β-actin. Data are shown as the x±s. for three independent experiments.*P<0.05 vs control. The immunoblot is representative of three independent experiments.Lane 1: Control cells; lanes 2~4: MCF-7 cells treated with 50,100 and 200 μmol·L-1 isatin,respectively. |
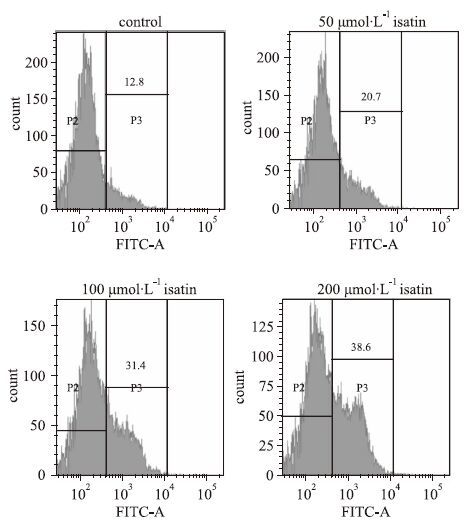
众所周知像Cytochrome C这类的促凋亡蛋白释放后,会激活caspase级联反应,本实验用流式细胞仪检测与不同浓度isatin(50、100、200 μmol·L-1) 孵育48 h后的MCF-7细胞中caspase-9的活化情况,如Fig 6所示,相比较对照组细胞的(13.07±2.81)%,isatin处理的各组细胞活化caspase-9蛋白水平均有不同程度的增加[(21.17±2.63)%、(31.77±3.56)%、(38.73±4.30%)],差异具有显著性(P<0.05)。
|
| Fig 6 Effect of isatin on caspase-9 activity in MCF-7 Cells(representative experiment) Cells treated with isatin for 48 h were incubated with FITC-LEHD-FMK for 30 min and then measured by flow cytometry (representative experiment). |
乳腺癌是目前女性发病率最高的恶性肿瘤,是导致女性死亡的主要原因之一[11]。到目前为止,尽管系统的化疗方案已常规用于临床治疗,但化疗耐药及化疗所带来的副作用仍是困扰乳腺癌治疗的严峻问题[12]。而天然化合物毒副作用小,具有靶向杀伤肿瘤细胞的特点,是目前抗肿瘤研究的热点。isatin作为一种天然活性物质,已经被证实具有明显的抗肿瘤作用。课题组前期的研究认为isatin能明显诱导乳腺癌细胞MCF-7凋亡,同时明显降低Bcl-2/Bax比值[10],但对具体的调控机制未做进一步研究。isatin是如何调控Bcl-2/Bax的,Bcl-2/Bax又是通过什么样的途径诱发凋亡的?肿瘤的生成是细胞增殖和凋亡调控失衡的结果,通过诱导肿瘤细胞凋亡来杀死肿瘤细胞已成为一种有效的肿瘤治疗途径。因此抑制肿瘤细胞生长,可以通过诱导肿瘤细胞凋亡来完成。本研究通过细胞荧光染色进一步证实不同浓度的isatin能明显诱导MCF-7细胞凋亡,荧光显微镜下观察到isatin处理组细胞发生典型的凋亡形态学改变:胞体缩小、胞质浓缩、核染色质聚集,并有DNA碎片。而对照组细胞无变化。
作为肿瘤抑制基因,p53主要通过激活其下游靶基因进一步控制细胞的生长与死亡[13],其次是在细胞周期的G期监视DNA的完整性。在依赖p53蛋白的凋亡中,p53蛋白能特异地抑制Bcl-2蛋白的表达,但对Bax蛋白的表达有明显促进作用,在这类细胞中p53蛋白的积累和活化引起了线粒体膜的去极化,进而引发细胞凋亡。有研究表明,人乳腺癌细胞MCF-7表达wild-p53蛋白,且通过一些抗肿瘤药物的诱导,能明显增强其表达量,进而诱导细胞凋亡[14, 15]。课题组前期的研究认为,Bcl-2家族蛋白中Bcl-2、Bax蛋白在isatin的抗肿瘤作用中不可或缺。isatin作用后可以导致Bcl-2蛋白表达降低,Bax蛋白表达增加。因此推测p53可能是isatin作用Bcl-2的上游靶分子之一。实验结果表明isatin作用后,p53mRNA及蛋白表达均明显增加。
众所周知,Bcl-2家族蛋白存在于线粒体膜上,与细胞凋亡密切相关。该家族蛋白的表达情况可能会影响到细胞膜电位的变化。本研究利用流式细胞仪检测不同浓度isatin处理组细胞膜电位,结果显示除对照组细胞外,其他各组细胞膜电位均出现不同程度下降。线粒体膜电位改变是细胞凋亡发生的早期特征,在膜电位发生改变后通常会释放一些促凋亡蛋白,像Cytochrome C,smac等。Western blot的结果显示isatin作用后线粒体Cytochrome C表达下降,而胞质中浓度增加。Cytochrome C等促凋亡蛋白会进一步作用,激活下游的caspase家族,引发凋亡。依照上述的结果,我们推测caspase家族中的caspase-9会被顺序激活,因此我们利用流式细胞仪检测了不同组别细胞caspase-9的活化情况,结果与预想的一致,经isatin作用后,活化的caspase-9表达增加。综上所述,有充分的理由认为isatin诱导乳腺癌MCF-7细胞凋亡可能是通过p53介导的线粒体凋亡途径。
( 致谢: 本实验是在青岛市妇女儿童医院检验科及青岛大学生物化学与分子生物学教研室完成。感谢马中良、迟晓伟及陈艳萍在实验过程中的协助 )
| [1] | Ray D, Paul B K, Guchhait N. Differential binding modes of anti-cancer, anti-HIV drugs belonging to isatin family with a model transport protein: a joint refinement from spectroscopic and molecular modeling approaches[J]. J Photochem Photobiol B, 2013, 127 : 18-27 . |
| [2] | Pakravan P, Kashanian S, Khodaei M M, Harding F J. Biochemical and pharmacological characterization of isatin and its derivatives: from structure to activity[J]. Pharmacol Rep, 2013, 65 (2) : 313-35 . |
| [3] | 洪锐, 孙圆圆, 金景, 等. 2,3-吲哚醌对大鼠离体胸主动脉舒缩功能的影响[J]. 中国药理学通报, 2014, 30 (8) : 1179-80 . Hong R, Sun Y Y, Jin J, et al. Effect of isatin on contraction and relaxation function of isolated rat thoracic aorta[J]. Chin Pharmacol Bull, 2014, 30 (8) : 1179-80 . |
| [4] | Yue W, Abe Y. Isatin, an endogenous MAO-B inhibitor, antagonizes the neurotoxic action of MPTP on central dopaminergic system in C57BL/6J mice[J]. Jpn J Pharmacol, 1999, 79 : 252 . |
| [5] | Cane A, Tournaire M C, Barritault D, Crumeyrolle-Arias M. The endogenous oxindoles 5-hydroxyoxindole and isatin are antiproliferative and proapoptotic[J]. Biochem Biophys Res Commun, 2000, 276 (1) : 379-84 . |
| [6] | Premanathan M, Radhakrishnan S, Kulangiappar K, et al. Antioxidant and anticancer activities of isatin(1H-indole-2,3-dione), isolated from the flowers of Couroupita guianensis Aubl[J]. Indian J Med Res, 2012, 136 (5) : 822-6 . |
| [7] | Cãndido-Bacani Pde M, Mori M P, Calvo T R, et al. In vitro assessment of the cytotoxic, apoptotic, and mutagenic potentials of isatin[J]. J Toxicol Environ Health A, 2013, 76 (6) : 354-62 . |
| [8] | Song J, Hou L, Ju C, et al. Isatin inhibits proliferation and induces apoptosis of SH-SY5Y neuroblastoma cells in vitro and in vivo[J]. Eur J Pharmacol, 2013, 702 (1-3) : 235-41 . |
| [9] | 刘娜, 鞠传霞, 岳旺. 2, 3-吲哚醌对二甲基苯蒽诱导的大鼠乳腺癌的预防作用[J]. 中国药理学通报, 2010, 26 (10) : 1353-6 . Liu N, JU C X, Yue W. Chemopreventive effect of isatin against DMBA-induced mammary carcinoma in rats[J]. Chin Pharmacol Bull, 2010, 26 (10) : 1353-6 . |
| [10] | 王艳丽, 侯琳, 宋金莲, 等. 2,3-吲哚醌对MCF-7和HT-29细胞株的增殖抑制和凋亡诱导[J]. 现代生物医学进展, 2009, 9 (5) : 824-8 . Wang Y L, Hou L, Song J L, et al. Effects of 2, 3-dioxoindolineon anti-proliferation and apoptosis on MCF-7 and HT-29 cell lines[J]. Prog Mod Biomed, 2009, 9 (5) : 824-8 . |
| [11] | Siegel R, Naishadham D, Jemal A. Cancer statistics[J]. CA Cancer J Clin, 2012, 62 (1) : 10-29 . |
| [12] | Smith N Z. Treating metastatic breast cancer with systemic chemotherapies: current trends and future perspectives[J]. Clin J Oncol Nurs, 2012, 16 (E33-43) : 1-22 . |
| [13] | Vousden K H, Lane D P. p53 in health and disease[J]. Nat Rev Mol Cell Biol, 2007, 8 (4) : 275-83 . |
| [14] | Suganyadevi P, Saravanakumar K M, Mohandas S. The antiproliferative activity of 3-deoxyanthocyanins extracted from red sorghum 53(Sorghum bicolor) bran through P-dependent and Bcl-2 gene expression in breast cancer cell line[J]. Life Sci, 2013, 92 (6-7) : 379-82 . |
| [15] | Cui Q, Yu J H, Wu J N, et al. P53-mediated cell cycle arrest and apoptosis through a caspase-3-independent, but caspase-9-dependent pathway in oridonin-treated MCF-7 human breast cancer cells[J]. Acta Pharmacol Sin, 2007, 28 (7) : 1057-66 . |

