


人参自古被称为益智良药,其主要药理活性成分为人参皂苷[1],其中人参皂苷Rg1为一种原人参三醇型皂苷[2]。大量研究表明,人参皂苷Rg1与改善胆碱能神经系统病变[3]、促进神经再生[4, 5]、激活学习记忆转导途径[6, 7, 8]和提高神经可塑性[9, 10]等关系密切,由于其主要作用部位为脑,因此考察其在学习记忆相关脑区的吸收程度尤为重要。目前较常用的考察脑内药物浓度的方法为微透析方法[11],然而检测到的微透析液中药物浓度不等同于脑内真实药物浓度,因此需进行探针回收率校正。考察探针回收率一般分为体内和体外两种方法[12],本文即通过建立LC-MS/MS法测定大鼠脑脊液中人参皂苷Rg1的浓度,进而考察探针体外与体内回收率,并比较两者之间的差异,为今后进一步研究其在各脑区中的分布奠定基础。
1 材料 1.1 药品与试剂复方氯化钠注射液(Ringer’s,北京双鹤药业股份有限公司),人参皂苷Rg1对照品(中国食品药品检定研究院,含量93.4%,批号110703-201128),紫杉醇(中国食品药品检定研究院,含量99.6%,批号100382-201102),甲醇(美国Fisher公司),超纯水(法国Millipore公司Milli-QA10 Synthesis制备)。
1.2 仪器AB API 5000型三重四极杆串联质谱仪,配备电喷雾电离源(ESI)(美国AB SCIEX公司);SHIMADZU 20AD 高效液相色谱仪,含LC-30AD型二元液相泵(日本岛津公司)。
1.3 动物清洁级Sprague Dawley大鼠(北京,维通利华公司),♂,250~300 g。实验动物生产许可证号:SCXK(京)2012-0001。
2 方法 2.1 LC-MS/MS法检测透析液中Rg1浓度 2.1.1 溶液配制人参皂苷Rg1对照品溶液的配制:精密称取人参皂苷Rg1标准品10.72 mg,用甲醇 ∶水=1 ∶1(V ∶V)溶解并定容至50 mL,制成200 mg·L-1的Rg1储备溶液。
紫杉醇(内标)溶液的配制:精密称取紫杉醇标准品10.35 mg,用甲醇 ∶水=1 ∶1(V ∶V)溶解并定容至50 mL,制成200 mg·L-1的紫杉醇储备溶液。
2.1.2 生物样品预处理精密量取10 μL微透析样品置于1.5 mL PCR离心管中,加入10 μL甲醇混匀后,再加入100 μL紫杉醇(内标)溶液,混匀,加入进样小瓶中进样。
2.1.3 色谱条件色谱柱:ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μm,Waters);流动相:A相:水,B相:甲醇;流速:0.4 mL·min-1;洗脱程序:0~0.5 min 10%~90%甲醇,0.5~2.5 min 90%甲醇,2.5~2.7 min 90%~10%甲醇,2.7~3.5 min 10%甲醇,总分析时间为3.5 min,梯度流速恒定为0.4 mL·min-1,柱温:40 ℃;自动进样器:4 ℃;进样量为10 μL。
2.1.4 质谱条件电喷雾电离源(ESI),离子源电压:5500 V,离子源温度:500 ℃;离子源气体1(N2)压力:50 psi(1 psi≈6.9 kPa);离子源气体2(N2)压力:60 psi;气帘气(N2)压力:20 psi;碰撞气压(CAD)压力:7 psi;去簇电压(DP)均为200 V;碰撞电压(EP)均为20 V;射入电压(2CE):47 V(Rg1),32 V(内标紫杉醇);碰撞室射出电压(CXP):20 V(Rg1),14 V(内标紫杉醇);正离子模式检测;扫描方式为多反应监测(MRM);待测物离子反应分别为:m/z 823.5→m/z 643.7(Rg1),m/z 876.9→m/z 308.5(内标紫杉醇)。
2.2 人参皂苷Rg1的探针回收率考察 2.2.1 体外探针回收率考察用Ringer’s溶液配制成浓度为25 μg·L-1人参皂苷Rg1标准溶液,将探针置于其中,平衡2 h后,每30 min收集1次样品,共收集3个样品。以同样的方法采集探针外液浓度(CECF)分别为50、100 μg·L-1的人参皂苷Rg1标准溶液的透析样品,并测定对应透析液中Rg1浓度(Cdialysate),计算公式为:R(in vitro)=Cdialysate/CECF×100%。
2.2.2 大鼠体内探针回收率考察♂ SD大鼠随机分为3组,每组5只,每组灌流液浓度(Cperfusate)分别为1、10、50 μg·L-1,定位脑区均为脑室(LV)及海马(HIP)。将大鼠麻醉,定位侧脑室(前卤后0.8 mm,旁开2.4 mm,硬膜下3.4 mm)以及海马(前卤后5.6 mm,旁右开5.0 mm,硬膜下5.2 mm)后,在脑区内埋置探针引导管,将接受以上手术的大鼠正常饲养3 d后,依次将两个探针植入导管抵达两目标脑区,再将探针连入由Ringer’s溶液配制的对应浓度的人参皂苷Rg1灌流系统,灌流液流速调至1.5 μL·min-1,平衡2 h后开始微透析液的收集工作,每0.5 h收集1次样品,共收集9 h。 其计算公式为:R(in vivo)=[(Cperfusate-Cdialysate)/Cperfusate]×100%。
2.3 统计学方法本文中所有实验结果以±s表示。比较不同浓度及各采样时间点的探针回收率时采用SPSS 17.0分析软件单因素方差分析(one-way ANOVA) 。两种探针回收率的比较采用SPSS 17.0分析软件两独立样本t检验(independent-samples t test)。
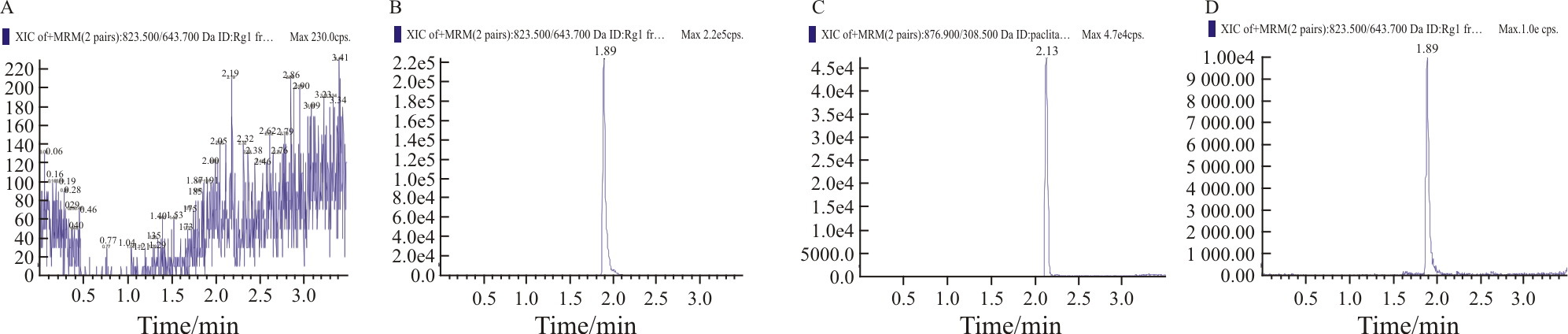
3 结果 3.1 方法学验证 3.1.1 特异性按“2.1.2”样品预处理方法处理空白Ringer′s溶液、空白Ringer′s溶液加人参皂苷Rg1标准品、空白Ringer′s溶液加内标标准品、大鼠脑微透析样品。采用“2.1.3”及“2.1.4”中色谱、质谱方法检测并比较。结果表明,在选定的条件下,基线噪音小,人参皂苷Rg1与脑内内源性物质得到良好的分离,峰形良好,且与内标互不干扰。保留时间为1.91 min,见Fig1。
|
| Fig.1 Chromatography of several samples of rats A: Blank Ring′s solution;B: Ringer′s with ginsenoside Rg1 standard;C: Ringer′s with internal standard; D: Microdialysis samples |
精密量取Rg1储备液适量,用甲醇 ∶水=1 ∶1(V ∶V)溶液依次稀释成50、20、10、5、2、1、0.5、0.2、0.1、0.05 μg·L-1的标准溶液,混匀后分别取20 μL,并加入100 μL内标,混匀后进样测定。以待测物峰面积Y 为纵坐标,待测物浓度X为横坐标,用加权(1/X2 ) 最小二乘法进行回归运算,得标准曲线回归方程即为标准曲线。由结果可知,人参皂苷Rg1的线性范围是0.05~50 μg·L-1。典型标准曲线为:=0.265X+4.65e-007(R2=0.9991)。
3.1.3 精密度与准确度取LLOQ、低、中、高4个浓度 (人参皂苷Rg1浓度分别为0.05、 0.1、2、40 μg·L-1) 的QC样品,按“2.1.2”项下操作,每个浓度进行5 样本分析,分别在3 日内测试,根据当日标准曲线计算QC 样品的测得浓度,同时得出本法的日内、日间精密度与准确度。结果见Tab1,人参皂苷Rg1各浓度QC样品日内、日间相对标准差小于15%,且每个浓度的QC样品(n=5)至少有3个准确度在85%~115%之间,且平均值也在该浓度之间。由此可见,该测试结果符合生物样品有关测定要求。
| Concentration/μg·L-1 | RSD/% | Accuracy/% | |
| Intra-day | Inter-day | ||
| 0.05 | 11.12 | 9.83 | 98.26±11.12 |
| 0.1 | 9.46 | 10.05 | 86.25±9.46 |
| 2 | 1.75 | 3.16 | 97.38±1.75 |
| 40 | 7.50 | 4.60 | 98.87±7.50 |
从-80 ℃取出配制浓度为200 mg·L-1人参皂苷Rg1储备液分装液,室温放置10 h后,与新取出的Rg1储备液各稀释5份,分别按照“2.1.2”项下样品预处理方法进行处理,并进样测定。结果显示,Rg1放置10 h后与新配制样品峰面积的RSD(n=5)分别为1.8%及6.3%,比值为0.99,表明Rg1储备液在室温放置10 h内稳定。
3.1.4.2 样品处理后进样器放置稳定性按“3.1.2”项下方法配制浓度为0.1、2、40 μg·L-1 3个浓度质控溶液,按“2.1.2”项下方法处理后测定,并代入新配制的标准曲线,计算各浓度,12 h后重新进样,并将其代入标准曲线计算浓度。结果显示,4 ℃进样器的放置12 h的处理后的透析液样品准确度均在85%~115%之间,表明人参皂苷Rg1处理后在4 ℃进样器中至少能稳定放置12 h。
3.1.4.3 样品短期室温放置稳定性考察用甲醇 ∶Ringer’s溶液=1 ∶1(V ∶V)配制Rg1 10、200、 4 000 μg·L-1 3个浓度的样品各5份,再分别吸取10 μL至990 μL的Ringer’s溶液中,得到Rg1浓度为0.1、2、40 μg·L-1的3个浓度的质控样品各5份,置于室温,于2 h后按“2.1.2”项下方法处理并进样测定,代入新配制的标准曲线计算浓度,结果显示各质控点准确度均在85%~115%之间,表明Rg1样品在室温至少能稳定放置2 h。
3.2 人参皂苷Rg1的探针回收率 3.2.1 Rg1体外探针回收率按照“2.2.1”项下方法操作,Rg1体外探针回收率结果见Tab2,结果表明,Rg1在3种浓度标准外液中探针回收率相对稳定。
| CECF/μg·L-1 | Cdialysate/μg·L-1 | R(in vitro)/% | |||
| 1 | 2 | 3 | 4 | ||
| 25 | 1.072 | 0.976 | 0.879 | 0.967 | 3.91±0.31 |
| 50 | 2.033 | 2.219 | 1.977 | 2.067 | 4.10±0.20 |
| 100 | 3.865 | 3.899 | 4.125 | 4.357 | 4.04±0.23 |
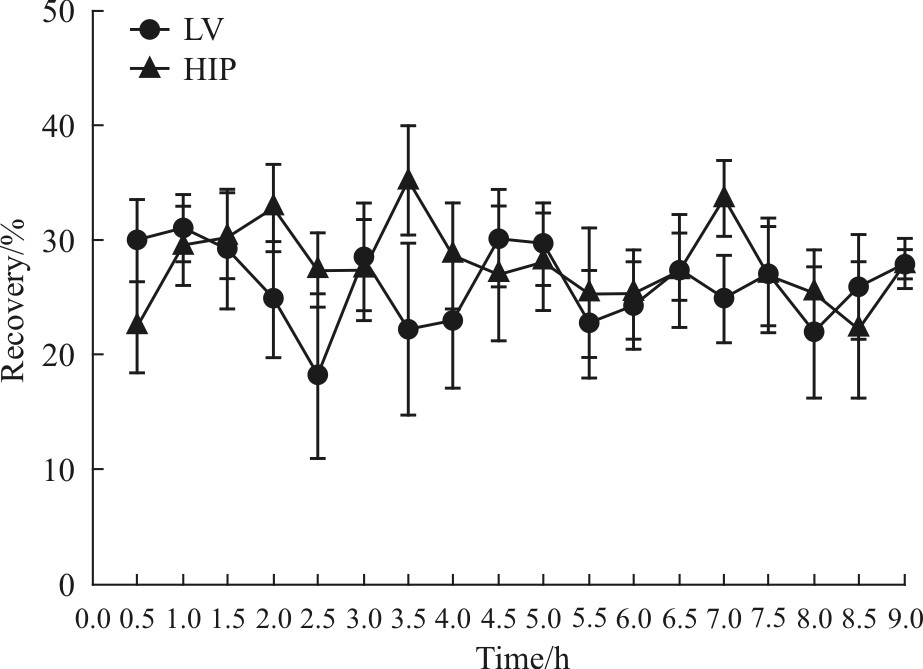
按照“2.2.2”项下方法操作,Rg1在3种灌流液浓度下体内探针回收率在9 h内的均值见Tab3,9 h内各采样点的侧脑室及海马内回收率见Fig2,由结果可见,Rg1在脑室及海马以3个浓度的灌流液得到的回收率差异均无显著性(P>0.05),且在9 h内回收率较稳定。
| Cperfusate/μg·L-1 | R(in vivo)/% | |
| LV | HIP | |
| 1 | 25.94±9.04 | 23.62±10.7 |
| 10 | 26.93±5.41 | 25.89±6.91 |
| 50 | 23.68±5.27 | 23.72±5.83 |
|
| Fig.2 Relationship between probe recovery of Rg1 in rats and time(x±s,n=5) |
本实验采用质谱方法进行检测,灵敏度高,且线性范围宽。此外,采用的液相方法中,流动相为甲醇、水,配制简单且对色谱柱损伤小,且该法分析时间短,同时该方法具有样品处理方法简单、所需样品量小、可行性高的优点。
在采用HPLC-MS/MS方法检测时,各组分响应在使用正离子模式比使用负离子模式时强,灵敏度高,且人参皂苷Rg1及内标的加钠母离子[M+Na]+比其各自的加氢母离子[M+H]+响应更高。对MS/MS方法优化后,采用多反应离子监控模式对各组分进行检测。
此外,在实验中发现配制人参皂苷Rg1标准溶液时直接用Ringer’s溶液稀释准确度差,不能达到实验要求,而增加稀释液中有机相比例,有明显改善。因此推测为Rg1在Ringer’s溶液中溶解度低的原因所致,为方便配制,本实验最终选择用甲醇 ∶Ringer’s溶液=1 ∶1(V ∶V)溶液逐级稀释的方法对样品进行处理。然而由于基质不同,标准溶液稳定性有很大差异,因此,本文在考察样品室温放置稳定性时,采取先用甲醇 ∶Ringer’s溶液=1 ∶1(V ∶V)溶液逐级稀释到目标浓度的100倍,再用Ringer’s溶液将每个浓度稀释到目标浓度的方法。此外,由于本实验中的样品采集后立即进行测定,因此未考察样品长期放置稳定性。
本实验所建立的用于检测透析液中人参皂苷Rg1含量的LC-MS/MS方法具有简单快速、灵敏准确、重现性好的特点,可用于测定微透析实验中探针体外及体内回收率,并比较两者间的差异。
微透析方法中,对采集的透析液浓度进行校正、得到脑间质液中药物的真实浓度是实验的关键环节。目前探针回收率的测定有多种方法,可分为体内和体外两类方法。本研究根据给药后大鼠脑透析液中药物浓度范围及对两种探针回收率的预估,分别选择3个浓度对探针进行体内和体外考察。
影响探针回收率的因素较多,除了受灌流液流速的影响外,还与药物透过探针的曲折度有关,药物透过越曲折,其透过探针的量越少,回收率越低。因此,考察体内回收率时由于探针处于脑组织中,理论上其回收率应较体外回收率低。然而,本研究发现探针对Rg1的体外回收率较低,而体内回收率明显高于体外回收率,分析原因可能为:药物透过浓度较高的探针至组织中后,会受组织中微脉管运输及代谢的作用继续向周围扩散,且药物代谢速率及微脉管转运速率越快,药物扩散速率越快,与探针内浓度差越大,从而促进药物继续透过探针进入组织内[13],而体外不存在该作用。此外,探针所处环境温度也与其回收率有关,温度越高,回收率越大,因此体内较高的温度有利于提高探针回收率。综上所述,以上原因可能导致体外回收率较体内回收率低。
由于体内回收率的实验过程更接近在体透析过程,更适于药代动力学研究。本实验证明了Rg1的体外回收率与体内回收率差异有显著性,在今后校正脑透析液中Rg1浓度时,将采用体内回收率的实验结果。同时本实验发现探针对Rg1的体内回收率在9 h内较稳定,因此,在考察脑内Rg1浓度时,可直接采取各时间点回收率的平均值进行校正,而不需对每个时间点采用不同的回收率分别进行校正。
综上所述,本实验建立了灵敏度高、准确性好的LC-MS/MS方法,用于测定透析液中Rg1浓度,基于该方法我们考察并比较了探针体外回收率以及大鼠体内回收率间的差异。因此,本实验的研究可为今后准确测定给药后各脑区中透析液中Rg1浓度,并通过回收率校正得到脑内真实浓度奠定基础,具有一定的研究意义。
(致谢:本课题是在卫生部北京医院临床药理室完成的,感谢史爱欣主任为本课题提供的实验平台以及对所遇到困难的耐心解答,同时感谢李可欣、薛薇等老师对本实验的帮助与大力支持。)
| [1] | Cheng Y,Shen L H,Zhang J T.Anti-amnestic and anti-aging effects of ginsenoside Rg1 and Rb1 and its mechanism of action[J].Acta Pharmacol Sin,2005,26(2): 143-9. |
| [2] | 宿延丽,宿艳霞,宿武林.人参有效成分及其复方研究进展[J].人参研究,2008,20(2): 7-11. Su Y L,Su Y X,Su W L. Advances of active ingredients of ginseng and its compound research[J].Ginseng Res,2008,20(2): 7-11. |
| [3] | Rudakewich M,Ba F,Benishin C G.Neurotrophic and neuroprotective actions of ginsenosides Rb(1) and Rg(1)[J].Planta Med,2001,67(6): 533-7. |
| [4] | Wang B,He L,Cui B,et al.Protection of ginsenoside Rg1 on central nerve cell damage and the influence on neuron apoptosis[J].Pak J Pharm Sci,2014,27(6 Suppl): 2035-40. |
| [5] | 彭小松,陈晓春,黄俊山,等.人参皂苷Rg1对Aβ(25-35)诱导大鼠海马神经元tau蛋白异常磷酸化的影响[J].中国药理学通报,2005,31(3): 299-305. Peng X S,Chen X C,Huang J S,et al. The effects of Ginsenoside Rg1 on A beta(25-35) induced tau protein abnormal phosphorylation in rat hippocampal neurons[J]. Chin Pharmacol Bull,2005,31(3):299-305. |
| [6] | Wang Y,Kan H,Yin Y,et al.Protective effects of ginsenoside Rg1 on chronic restraint stress induced learning and memory impairments in male mice[J].Pharmacol Biochem Behav,2014,120: 73-81. |
| [7] | Fang F,Chen X,Huang T,et al.Multi-faced neuroprotective effects of Ginsenoside Rg1 in an Alzheimer mouse model[J].Biochim Biophys Acta,2012,1822(2): 286-92. |
| [8] | Shi C,Zheng D,Fang L,et al.Ginsenoside Rg1 promotes nonamyloidgenic cleavage of APP via estrogen receptor signaling to MAPK/ERK and PI3K/Akt[J].Biochim Biophys Acta,2012,1820(4): 453-60. |
| [9] | Yang L,Zhang J,Zheng K,et al.Long-term ginsenoside Rg1 supplementation improves age-related cognitive decline by promoting synaptic plasticity associated protein expression in C57BL/6J mice[J].J Gerontol A Biol Sci Med Sci,2014,69(3): 282-94. |
| [10] | 陈云波,张大鹏,冯 梅,等.人参皂苷Rg1对Aβ(25-35)诱导的神经细胞核因子-κB活化的影响[J].中国药理学通报,2007,23(5): 612-7. Chen Y B,Zhang D P,Feng M,et al. The effects of Ginsenoside Rg1 on the activation of nerve nuclear factor kappa B induced by Abeta(25-35)[J].Chin Pharmacol Bull,2007,23(5): 612-7. |
| [11] | Nirogi R,Ajjala D R,Kandikere V,et al.LC-MS/MS method for the quantification of almotriptan in dialysates: application to rat brain and blood microdialysis study[J].J Pharm Biomed Anal,2013,81-82: 160-7. |
| [12] | Bundgaard C,Jrgensen M,Mrk A.An integrated microdialysis rat model for multiple pharmacokinetic/pharmacodynamic investigations of serotonergic agents[J].J Pharmacol Tox Met,2007,55(2): 214-23. |
| [13] | Menacherry S,Hubert W,Justice J B. In vivo calibration of microdialysis probes for exogenous compounds[J]. Anal Chem,1992,64(6) 577-83. |

