


2. 济南大学山东省医学科学院医学与生命科学学院, 山东济南 250062;
3. 中国药科大学, 江苏南京 211198
2. School of Medicine and Life Sciences, University of Jinan-Shandong Academy of Medical Sciences, Jinan 250062, China;
3. China Pharmaceutical University, Nanjing 211198, China
糖尿病(diabetes mellitus,DM)的发病率和死亡率呈逐年上升趋势,心血管并发症是DM患者死亡的主要原因。Wnt/β-catenin信号通路作为一条保守的信号传导通路广泛存在于各生物体中,参与调控细胞增殖、迁移、分化等细胞发育过程。近年来研究表明,Wnt/β-catenin信号通路参与主动脉内皮细胞生长和分化[1],在心血管疾病中起重要作用[2]。此外,Wnt/β-catenin信号通路的异常可能引起代谢综合征[3]。沉默信息调节因子1(silent informationregulator1,SIRT1)为哺乳动物Sirtuins家族成员之一,是一种依赖于烟酰胺腺嘌呤二核苷酸(NAD+)的去乙酰化酶,成人组织中广泛表达。研究显示[4, 5],SIRT1通过去乙酰化相关因子调节作用Wnt/β-catenin在内的多个细胞信号通路,参与血管内皮细胞的保护作用,但在糖尿病主动脉病变过程中的作用仍不清楚。本文通过检测Wnt/β-catenin信号通路相关蛋白及SIRT1在2型糖尿病大鼠主动脉中的表达变化,探讨SIRT1对该信号通路在DM主动脉中的表达调节作用,为糖尿病主动脉病变的治疗提供理论基础。
1 材料与方法 1.1 实验动物及模型建立健康♂ SD大鼠50只,SPF级,体质量150~180 g,购自山东鲁抗医药股份有限公司实验动物中心。大鼠适应性喂养1周后,按体重均衡的原则随机分为正常对照组(A)10只,糖尿病模型组(B)40只。 A组始终饲以普通饮食,B组采用高脂流质(猪油30%,胆固醇2.5%,脱氧胆酸钠1% ,常规饲料66.5%)灌胃,两组动物均自由饮水。5周后,B组大鼠禁食12 h,颈静脉窦取血检测血清总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)等生化指标,确定形成高脂模型,诱导出大鼠胰岛素抵抗(insulin resistance,IR)状态,联合链脲菌素造模。B组大鼠一次性腹腔注射 1 % 链脲菌素(30 mg·kg-1,pH=4.5柠檬酸-柠檬酸三钠缓冲液,4 ℃配制,现配现用),A组正常大鼠注射同体积柠檬酸-柠檬酸三钠缓冲液。造模后72 h尾静脉采血检测空腹血糖值(fasting blood glucose,FBG),以FBG≥11.1 mmol·L-1,胰岛素敏感指数降低,认为糖尿病大鼠模型成功。B组造模成功大鼠随机分为2、4、8和12周模型组,继续高脂饮食灌胃。A组继续以普通饲料喂养4周。
1.2 材料与试剂链脲佐菌素、戊巴比妥钠(美国Sigma公司);血糖试纸(强生中国医疗器材有限公司);TG试剂盒、TC试剂盒、低密度脂蛋白-胆固醇(low density lipoprotein- cholesterol,LDL-C)试剂盒、高密度脂蛋白-胆固醇(high density lipoprotein- cholesterol,HDL-C)试剂盒(四川迈克生物科技股份有限公司);胰岛素(insulin,INS)试剂盒(Lengton 生物上海公司);生物素标记山羊抗兔IgG/小鼠IgG二抗试剂盒(北京中杉金桥生物技术有限公司);Western blot一抗、二抗去除液、Western blot细胞裂解液、Western blot转膜液、BCA蛋白浓度测定试剂盒(增强型)、SDS-PAGE凝胶配制试剂盒和SDS-PAGE电泳液均购自碧云天生物技术研究所;ProSieve Color ptrotein makers(美国Lonza Rockland公司);PVDF膜(0.45 μm;美国SERVA公司);增强型化学发光试剂(美国Millipore公司);所用单克隆抗体为:Wnt2(美国Epitomics公司),β-catenin(美国Cell Signaling Technology公司),TCF4(英国Abcam公司),sFRP2(美国Cell Signaling Technology公司),β-actin(美国Ambobio公司);PCR引物(中国BioSune);逆转录试剂盒(美国ThermoFisher公司)。
1.3 空腹血糖及胰岛素检测高脂灌胃5 周后,大鼠一次性腹腔注射链脲菌素后72 h,禁食12 h,颈静脉窦取血,离心分离血清,检测空腹血糖及胰岛素(fasting insulin,FINS)水平,计算胰岛素敏感指数(insulin sensitive index,ISI),检测胰岛素敏感性变化,公式为 ISI=ln[1/(FINS×FBG)]。
1.4 标本收集造模结束后,各模型组大鼠高脂灌胃,分别喂养至实验设定的2、4、8和12周。大鼠麻醉,仰位固定,开胸,腹主动脉取血,5 ml/只,3 000 r·min-1离心10 min,取上清,分装,-20 ℃保存待测。生化仪检测TC、TG、HDL-C、LDL-C水平。迅速取出主动脉,用预冷生理盐水洗净,滤纸吸干,剔除血管周围脂肪组织,分为两部分:一部分用4%多聚甲醛固定,经脱水、透明、包埋,制成主动脉组织石蜡块;另一部分置于EP管,于液氮中保存待用。
1.5 HE染色取正常对照组及各时间点模型组主动脉组织,制作石蜡切片,常规脱蜡至水,苏木精染色10 min,流水稍洗,体积分数1%的盐酸酒精分化,流水冲洗数分钟,伊红染色5 min,流水稍洗,梯度酒精常规脱水,中性树胶封片。Eclipse TE 2000-S 免疫荧光显微镜拍照(日本Nikon),观察主动脉组织病理结构的改变。
1.6 Western blot取正常组及各模型组大鼠主动脉组织,制备组织匀浆,每20 mg组织加入100~200 μL含1 mmol·L-1 PMSF的裂解液,4 ℃下14 000×g离心10 min,取匀浆上清,用BCA蛋白浓度测定试剂盒测定总蛋白浓度。20~50 μg总蛋白上样量以浓度为8 %的凝胶电泳进行分离。冰浴下恒流(300 mA)湿法转膜2 h,体积分数5 %的脱脂奶粉封闭1 h后与相应一抗4 ℃共孵育过夜。TBS-T洗液洗涤,与辣根过氧化物标记的二抗共孵育,用增强型化学发光试剂进行显色,并利用灰度分析软件定量分析。
1.7 逆转录-聚合酶链式反应(RT-PCR)取各组主动脉组织100~150 mg,均匀粉碎后按 TRIzol 提取程序(说明书)提取组织总RNA;按AMV逆转录试剂盒操作说明进行逆转录后,4℃保存。各目的基因的扩增引物序列,如Tab 1所示;扩增条件: 94℃预变性3 min,然后94 ℃变性30 s,55 ℃ 变性30 s,72 ℃ 延伸60 s,共 35个循环,最后72 ℃延伸5 min,快速冷却至4℃保存。2%琼脂糖凝胶电泳后,凝胶成像仪观察,用 BandScan 5.0软件测定条带灰度值,将mRNA、分别与β-actin mRNA 灰度值的比值作为观察指标,进行统计学分析。
| Gene | Forward primers(sense/antisense 5′-3′) | Reverse primers (sense/antisense 5′-3′) |
| Wnt2 | GGCCTTTGTTTACGCCATCTC | TCCTTCCAGCTCTGTTGTTG |
| β-Catenin | CGAGGACTCAATACCATTCC | AGCCGTTTCTTGTAGTCCTG |
| TCF4 | GCCTCTCATCACGTACAGCA | GGATGGGGGATTTGTCCTAC |
| SIRT1 | TTGGTACCAAGATGGCGGACGAGGTGGCGC | GCTCGAGTTATGATTTGTCTGATGGATAGTT |
| sFRP2 | CCAGAAAGTAGTGACCGG | GAGCAGAGTGAGCAGAGG |
| β-actin | TCACCCACACTGTGCCCCATCTACGA | CAGCGGAACCGCTCATTG-CCAATGG |
应用SPSS19.0统计软件进行数据处理,数据以x±s表示,组间差异比较采用方差分析及 t检验。
2 结果 2.1 大鼠模型建立情况实验期间,正常对照组大 鼠状态良好、健壮、皮毛油亮有光泽,自主活动正常,对外界反应灵敏,无死亡。与正常对照组大鼠相比较,DM组大鼠逐渐消瘦,精神萎靡,皮毛无光泽,腥臊臭味加重等;且随着时间延长,多饮、多食、多尿和消瘦表现加重,大鼠生存状态越来越差,造模成功大鼠36只,成功率为90%。
2.2 造模后大鼠体重变化及FBG、FINS、ISI情况注射STZ造模72 h后,正常对照组大鼠体重增加,糖尿病组大鼠糖尿病模型组大鼠与对照组大鼠比较血清FBG、FINS明显升高,ISI下降,差异有统计学意义(P<0.01),表明2型糖尿病大鼠造模成功。见Tab 2。
| (x±s,n=6) | |||||
| Group | n | ΔBW/g | FBG/mmol·L-1 | FINS/mU·L-1 | ISI |
| Control | 10 | 29.360±2.336 | 5.776±0.267 | 19.712±0.836 | -4.735±0.465 |
| DM Model | 36 | -3.552±0.426** | 32.150±0.997** | 29.545±1.342* | -6.856±0.761** |
| ΔBW=Body Weight(after 2 wks) - Body Weight(before);*P<0.05,**P<0.01 vs control | |||||
与正常对照组比较,模型组大鼠血清中FBG、TG、TC、LDL-C明显升高(P<0.05)。而4、8周模型组与2周DM模型组相比较,大鼠血清TG含量略有升高,HDL-C略有降低,二者之间比较差异无统计学意义(P>0.05),8周和12周DM模型组各生化指标变化不大;FBG、TC、LDL-C继续升高,差异有统计学意义(P<0.05)。见Tab 3。
| (x±s,n=6) | ||||||
| Group | n | FBG/mmol·L-1 | TG/mmol·L-1 | TC/mmol·L-1 | HDL-C/mmol·L-1 | LDL-C/mmol·L-1 |
| Control | 10 | 5.776±0.2671 | 1.107±0.023 | 2.151±0.225 | 0.638±0.077 | 0.117±0.021 |
| 2 week DM | 9 | 30.612±4.375** | 1.211±0.076** | 2.323±0.167* | 0.555±0.109* | 0.178±0.029** |
| 4 week DM | 9 | 34.078±6.715**△ | 1.299±0.098** | 2.776±0.096**△ | 0.506±0.023* | 0.221±0.016**△ |
| 8 week DM | 9 | 36.676±6.112**△ | 1.374±0.097** | 2.998±0.116**△ | 0.499±0.036* | 0.240±0.009**△ |
| 12 week DM | 9 | 36.118±5.733**△ | 1.394±0.108** | 3.332±0.109**△ | 0.421±0.034*△ | 0.249±0.015**△ |
| *P<0.05,**P<0.01 vs control;△P<0.05 vs 2 week DM | ||||||
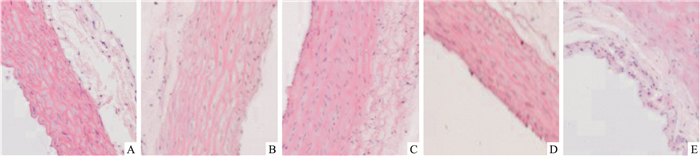
正常对照组大鼠主动脉内皮细胞形态正常,内皮细胞排列整齐,细胞核均匀分布,无变性、坏死等病理结构改变。DM组大鼠主动脉内皮细胞,胞质丰富,细胞核由正常的圆形或椭圆形不同程度的出现变为长杆状,排列紊乱,8周和12周DM大鼠内皮细胞出现局部的细胞变性、细胞空泡化,甚至坏死(Fig 1)。
|
| Fig 1 HE staining of aorta of DM rats(×400) A:Control group;B:2 wk DM;C:4 wk DM;D: 8wk DM;E:12wk DM |
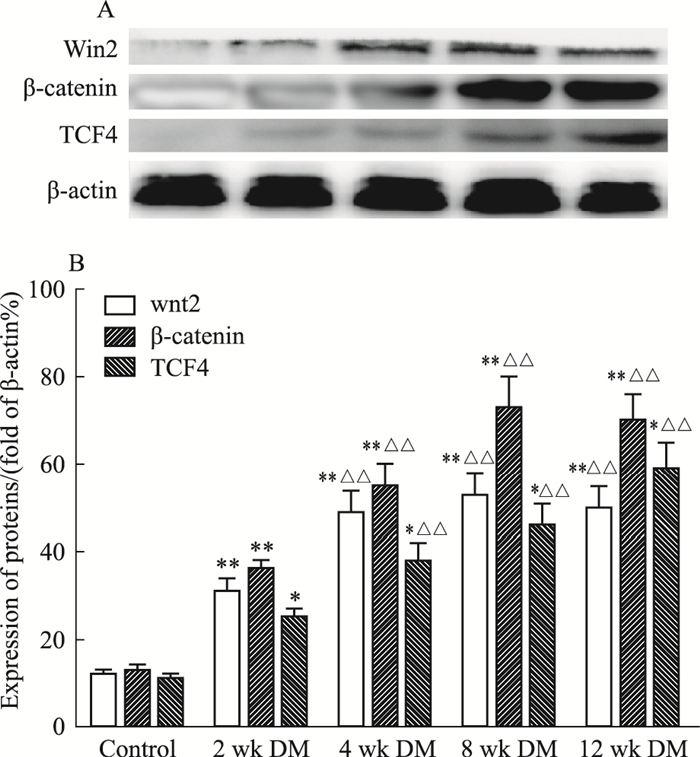
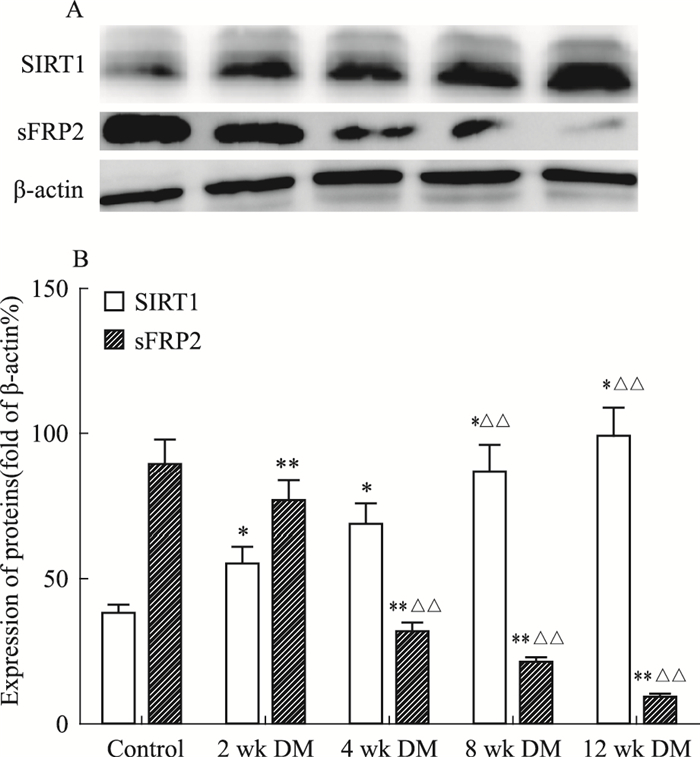
Westem blot实验结果表明,糖尿病组大鼠相对于正常对照组主动脉Wnt2和β-catenin的表达在2周及4周明显增加(P<0.01),4周后维持在较高水平,8周及12周相关蛋白表达变化差异没有显著性(P>0.05);糖尿病大鼠从2周到12周过程中,TCF4、SIRT1蛋白表达与正常对照组相比表现为持续的增加(P<0.05),sFRP2蛋白的表达在持续的降低(P<0.01)(Fig 2、3)。
|
| Fig 2 The protein levels of Wnt2, β-catenin and TCF4 in total protein extracts of aorta from control and DM rats analyzed by Western blot( x±s,n=9) A:Representative Western blot analysis of the time-dependent changes of protein levels;B:Bar graph shows quantification of protein levels(fold of net intensity of bands with β-actin).*P<0.05, **P<0.01 vs control group;△△P<0.01 vs 2 wk DM group |
|
| Fig 3 The protein levels of SIRT1 and sFRP2 in total protein extracts of aorta from control and DM rats analyzed by Western blot( x±s, n=9) A:Representative Western blot analysis of the time-dependent changes of protein levels;B:Bar graph shows quantification of protein levels (fold of net intensity of bands with β-actin).*P<0.05,**P <0.01 vs control group;△△P<0.01 vs 2 wk DM group |
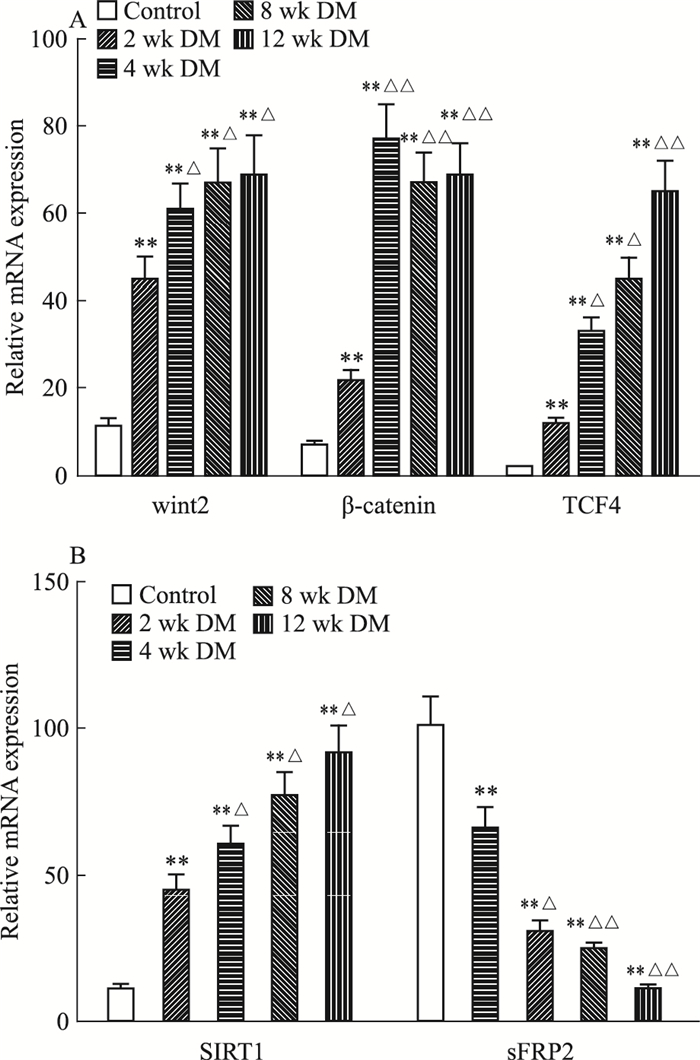
正常组大鼠主动脉组织细胞有一定量的Wnt2、β-catenin、TCF4及SIRT1 mRNA的表达,但表达量不随时间的变化而变化(P>0.05),而sFRP2 mRNA始终维持在较高的转录水平。与正常组相比,各糖尿病组大鼠主动脉组织中Wnt2,β-catenin mRNA明显增高(P<0.01),且各模型组中,2周和4周组mRNA表达持续增加,8周和12周组维持在高表达水平,二者之间差异没有显著性(P>0.05);与此同时,各模型组中SIRT1和TCF4 mRNA的表达持续增高,sFRP2 mRNA表达水平持续降低,各组别之间差异也具有显著性(P<0.05)。见Fig 4。
|
| Fig 4 The mRNA expression of Wnt/β-catenin signaling, SIRT1 andsFRP2 in total RNA extracts of aortic tissue from control and DM rats using qRT-PCR( x±s,n=9) Bar graph shows quantification of mRNA expression(2-ΔΔCt).A:Quantitative analysis of Wnt/β-catenin signaling mRNA expression;B:Quantitative analysis of SIRT1 and sFRP2 mRNA expression.**P<0.01 vs control group;△P<0.05,△△P<0.01 vs 2 wk DM group |
糖尿病可引起机体多个脏器的损害,主动脉等大血管疾病是2型糖尿病致死或致残的主要原因。糖尿病主动脉内皮细胞病变的发病机制及相关信号通路的研究也较少,探索血管内皮功能异常的病理生理机制,并有效改善血管内皮功能,可能是防治2型糖尿病心血管事件的靶点。
本实验采用了高脂饮食联合链脲佐菌素建模方法[6],建立2型DM大鼠模型,与正常对照组相比,DM大鼠血清TC、TG、LDL-C值有明显升高,并呈现持续的高血糖,胰岛素抵抗出现,糖尿病状态形成。本研究中,DM大鼠FBG明显升高,体重明显低于正常对照组,DM大鼠主动脉出现局灶性内皮细胞空泡变性、甚至坏死,表明DM大鼠主动脉出现不同程度的大血管损伤。
Wnt/β-catenin信号通路在大血管损伤中的作用也被广泛关注[7]。Dabernat等[8]研究Wnt/β-catenin信号通路的异常会引起糖代谢的异常,增加2型糖尿病的风险,参与高糖介导的肾上皮细胞转分化过程[9]。Xi等[10]在对1型糖尿病大鼠模型的研究中发现,DM状态下,大鼠心肌Wnt/β-catenin信号通路被激活。因此,我们推测Wnt/β-catenin信号通路可能在DM主动脉损伤中起重要作用。
SIRT1可以通过调节FOXOs、NF-κB、AMPK等相关信号通路,对多种心血管疾病的病理生理过程产生重要影响,发挥保护心肌、舒张血管、抑制动脉粥样硬化等作用[6]。Takeda等[11]认为,在单核-巨噬细胞中,SIRTl失活条件下,mTOR通路介导NF-κB信号激活,进而诱发动脉粥样硬化发生。Yang等[12]研究发现,Sirtl过表达时,去乙酰化并激活LKB1,随后AMPK的去磷酸化水平升高,进而正向调节细胞寿命和能量平衡,从而保护主动脉血管内皮细胞功能,降低了动脉粥样硬化的发生。另有研究[13]显示,肝缺血-再灌注损伤中,SIRT1通过调节抑制Wnt信号通路,减少氧化损伤和细胞凋亡来保护肝细胞。而Zhou等[14]在研究间充质干细胞时发现,SIRT1可以通过调节sFRP2的表达来调节Wnt/β-catenin信号通路。但是,SIRT1在心血管系统对Wnt/β-catenin信号通路的调节还不清楚。
Wnt/β-catenin信号通路转导过程中,Wnt蛋白与细胞膜上的跨膜受体结合,促使β-catenin降解复合体轴蛋白/结肠腺瘤样息肉蛋白/糖原合成酶激酶3β(Axin/APC/GSK-3β)解聚而失活,抑制β-catenin的磷酸化及降解,促进β-catenin发生核转移,与核内转录因子TCF/LEF结合,激活下游靶基因启动基因转录[15]。本研究中Western blot及RT-PCR结果表明2周和4周DM大鼠心肌Wnt2的表达增加,促进β-catenin发生核转移,核内转录因子TCF4的表达增加,显示Wnt/β-catenin信号通路的激活;与此同时,早期DM大鼠主动脉内皮细胞的空泡变性、晚期甚至出现坏死等病变。而SIRT1表达持续增加,Wnt/β-catenin信号通路内源性抑制剂sFRP2在DM早期高表达,持续期表达下降;可能是因为在DM早期,主动脉组织中Wnt/β-catenin信号通路的迅速激活,体内广泛存在的SIRT1合成增加,直接调节sFRP2抑制Wnt/β-catenin信号通路的β-catenin的表达;高血糖状态持续,Wnt/β-catenin信号通路持续激活状态,sFRP2则随之降低。而SIRT1如何作用于sFRP2而发挥作用的,还需要进一步研究。
糖尿病主动脉病变是糖尿病心血管严重并发症的重要组成部分,明确其发生发展机制,进而阻滞其发展成为研究热点。本实验揭示Wnt/β-catenin信号通路的激活与SIRT1的调节作用,共同参与DM主动脉的损伤过程,我们将进一步研究二者在DM主动脉病变发展过程中的作用机制,以期为糖尿病主动脉病变的治疗找到新的靶点。
(致谢:本实验全部由山东省医学科学院药物研究所药理学实验室牟艳玲老师课题组独立完成,感谢我的导师牟艳玲老师在实验设计思路上提出的建议和意见及实验技术上给予的指导。)
| [1] | Zhuang Y, Mao J Q, Yu M, et al.Hyperlipidemia induces vascular smooth muscle cell proliferation involving Wnt/β-catenin signaling[J].Cell Biol Int, 2016, 40(2):121-30. |
| [2] | Xi X H, Wang Y, Li J, et al.Activation of Wnt/β-catenin/GSK3β signaling during the development of diabetic cardiomyopathy[J].Cardiovasc Pathol, 2015, 24(3):179-86. |
| [3] | Singh R, Smith E, Fathzadeh M, et al.Rare nonconservative LRP6 mutations are associated with metabolic syndrome[J].Hum Mutat, 2013, 34(9):1221-5. |
| [4] | Wang W R, Liu E Q, Zhang J Y, et al.Activation of PPAR alpha by fenofibrate inhibits apoptosis in vascular adventitial fibroblasts partly through SIRT1-mediated deacetylation of FoxO1[J].Exp Cell Res, 2015, 338(1):54-63. |
| [5] | Kim Y H, Bae J U, Lee S J, et al.SIRT1 attenuates PAF-induced MMP-2 production via down-regulation of PAF receptor expression in vascular smooth muscle cells[J].Vascul Pharmacol, 2015, 72:35-42. |
| [6] | Rhee K J, Lee C G, Kim S W, et al.Extract of Ginkgo Biloba Ameliorates streptozotocin-induced type 1 diabetes mellitus and high-fat diet-induced type 2 diabetes mellitus in mice[J].Int J Med Sci, 2015, 12(12):987-94. |
| [7] | Blankesteijn W M, Hermans K.Wnt signaling in atherosclerosis[J].Eur J Pharmacol, 2015, 763(Part A):122-30. |
| [8] | Dabernat S, Secrest P, Peuchant E, et al.Lack of beta-catenin in early life induces abnormal glucose homeostasis in mice[J].Diabetologia, 2009, 52(8):1608-17. |
| [9] | 闫喆, 姚芳, 张丽萍, 等.厄贝沙坦对高糖诱导肾小管上皮细胞转分化中Wnt/β-catenin信号途径表达的影响[J].中国药理学通报, 2009, 25(12):1630-4.Yan Z, Yao F, Zhang L P, et al.Modulation of Wnt/β-catenin signaling pathway byirbesartan in high glucose induced tubular epithelial mesenchymal transition[J].Chin Pharmacol Bull, 2009, 25(12):1630-4. |
| [10] | 席晓慧, 王福文, 王燕, 等.早期糖尿病大鼠心肌Wnt/β-catenin信号通路的变化[J].中国药理学通报, 2015, 31(3):363-6.Xi X H, Wang F W, Wang Y, et al.Alteration of Wnt/β-catenin signaling pathway in early diabetic rats'myocardium[J].Chin Pharmacol Bull, 2015, 31(3):363-6. |
| [11] | Takeda W A, Kitada M, Kanasaki K, et al.SIRT1 in activation induces inflammation through the dysregulation of autophagy in human THP-1 cells[J].Biochem Biophys Res Commun, 2012, 427(1):191-6. |
| [12] | Yang Z, Kahn B B, Shi H, et al.Macrophage alpha1 AMP-activated protein kinase(alpha1 AMPK) antagonizes fatty acid-induced inflammation through SIRT1[J].J Biol Chem, 2010, 285(25):19051-9. |
| [13] | Liu B, Zhang R, Tao G, et al.Augmented wnt-signaling as a therapeutic tool to prevent ischemia and reperfusion injury in liver:preclinical studies in a mouse model[J].Liver Transpl, 2015, 21(12):1533-42. |
| [14] | Zhou Y, Zhou Z, Zhang W, et al.SIRT1 inhibits adipogenesis and promotes myogenic differentiation in C3H10T1/2 pluripotent cells by regulating Wnt signaling[J].Cell Biosci, 2015, 5:61. |
| [15] | Dawson K, Aflaki M, Nattel S.Role of the wnt-frizzled system in cardiac pathophysiology:a rapidly developing, poorly understood area with enormous potential[J].J Physiol, 2013, 591(6):1409-32. |

