


2. 湖南医药学院附属第一医院呼吸内科, 湖南 怀化 418000;
3. 南华大学附属第一医院呼吸内科, 湖南 衡阳 421001
2. Dept of Respiration, the First Affiliated Hospital, Hunan University of Medicine, Huaihua Hunan 418000, China;
3. Dept of Respiration, the First Affiliated Hospital, University of South China, Hengyang Hunan 421001, China
肺纤维化是各种不同病因引起的间质性肺疾病的最终结局,以肺间质内单核/巨噬细胞等炎症细胞浸润、成纤维细胞异常增殖和胶原蛋白过量沉积为特征,迄今尚无有效的临床治疗方法,预后极差,死亡率高,严重危害人类健康,因而迫切需要开发有效治疗或逆转肺纤维化的药物[1]。尽管肺纤维化的发病机制尚未完全阐明,但多种炎症因子在其发生和发展中发挥着关键作用[2]。白介素-17(interleukin-17,IL-17)是由 Th17 细胞产生的一种重要促炎症细胞因子,参与介导了多种炎症反应和自身免疫性疾病的发生发展[3, 4]。研究表明,IL-17可促进心肌、肝脏及肾脏等组织纤维化[5, 6, 7],向气管内注射大剂量 IL-17 可诱发肺纤维化[8]。我们前期研究也发现,IL-17 在肺纤维化大鼠中表达增高[9]。这些结果提示IL-17与组织纤维化密切相关,阻断IL-17表达可望成为分子治疗新的靶点。IL-17 单克隆抗体(monoclonal antibody,mAb)已被尝试用于银屑病、克劳恩病及强直性脊柱炎等自身免疫性疾病的治疗,并显示出较好的效果[10, 11]。新近研究报道,IL-17 中和抗体能减少成纤维细胞过度增殖,并明显改善肺纤维化小鼠的肺功能[12, 13],但其作用机制仍不清楚。为此,本研究采用气管内注射博莱霉素构建大鼠肺纤维化模型,观察 IL-17mAb 对大鼠肺纤维化病理改变、核因子-κB(nuclear factor-κB,NF-κB)、炎症因子和胶原蛋白表达的影响,探索 IL-17mAb 对肺纤维化大鼠的保护作用及其相关机制,为其应用于肺纤维化的治疗提供理论基础和实验依据。
1 材料与方法 1.1 实验动物与药品75只清洁级♂ SD大鼠,8~10周龄,体质量为(283±13) g,由南华大学实验动物学部提供,实验动物使用许可证号:SYKK(湘)2010-0006,随机分笼于SPF级环境中,常规颗粒饲料饲养。博莱霉素A5为天津太和制药有限公司产品(批号070501)。RNA提取试剂TRIzol、PVDF膜购自美国Invitrogen公司。逆转录试剂盒为美国Promega公司出品。兔抗大鼠IL-17单克隆抗体、非特异性IgG、兔抗大鼠NF-κB p65、Ⅰ型胶原(collagen type Ⅰ,Col Ⅰ)、Ⅲ型胶原(collagen type Ⅲ,Col Ⅲ)、β-actin抗体购于Santa Cruz公司。ELISA检测试剂盒为美国R&D公司产品。
1.2 模型制备与分组给药随机将75只 ♂ SD大鼠分为正常对照组、假手术组、模型组、非特异性IgG组、IL-17 mAb组,各组15只。后4组予以100 g·L-1水合氯醛(3 mL·kg-1)腹腔注射麻醉大鼠后,切开颈正中部,使气管充分暴露,其中模型组、非特异性IgG组、IL-17 mAb组用溶解了博莱霉素A5(5 mg·kg-1)的生理盐水0.2 mL一次性向气管内注射,而假手术组给予等体积生理盐水气管内注入,直立大鼠并旋转,以使药液在肺内均匀分布。造模后d 7、14、21,非特异性IgG组尾静脉注射非特异性IgG(200 μg·kg-1),IL-17 mAb组尾静脉注射IL-17 mAb(200 μg·kg-1),正常对照组、假手术组、模型组则尾静脉注射等量生理盐水。d 28,麻醉大鼠后无菌开胸,以心脏采血法采集血液3 mL,离心并提取血清,保存于-20℃冰箱内,用于测定Ⅰ型前胶原羧基端前肽(procollagen type 1 carboxyterminal propeptide,PICP)、Ⅲ型前胶原氨基端前肽(procollagen type Ⅲ aminoterminal propeptide,PIIINP)浓度。然后行颈动脉放血将全部大鼠处死,截取右肺组织,冻存于-70℃液氮中,以供双抗体夹心酶联免疫吸附法(enzyme linked immunosorbent assay,ELISA)、Western blot和荧光实时定量PCR检测。再使用0.1 mol·L-1中性缓和福尔马林经主支气管注入左肺内,使胸膜展开后,再固定于0.1 mol·L-1中性福尔马林中至少24 h,石蜡包埋,切片,用于肺组织病理学检查。
1.3 肺组织病理学改变将左肺石蜡切片后,行常规苏木精-伊红(hematoxylin-eosin,HE)染色及Masson 染色,参照 Szapiel等[14]方法,采用HE染色在光镜下评定肺组织肺泡炎症程度:0分:无肺组织炎;1分:轻度肺组织炎,仅局部或近胸膜部有炎性细胞浸润,面积在 20%以内;2分:中度肺组织炎,面积在20%~50%之间;3分:重度肺组织炎,面积达50%以上。采用Masson染色于光镜下评定肺组织纤维化程度:0分:无肺纤维化;1分:轻度肺纤维化,病变面积未超过全肺 20%;2分:中度肺纤维化,病变面积达到全肺 20%~50%;3分:重度肺纤维化,病变面积在50%以上,肺泡结构破坏。
1.4 Western blot按照试剂盒(美国ProMab公司)的说明书提取右肺组织细胞核蛋白和细胞蛋白,并测定蛋白浓度。常规制备SDS-PAGE凝胶,上样、电泳并转膜,室温下用5%脱脂牛奶封闭4 h,再分别滴加1 ∶500稀释的兔抗大鼠NF-κB p65、Col Ⅰ、Col Ⅲ、β-actin一抗,于4℃条件下反应过夜,洗膜后加入1 ∶2 500稀释的辣根过氧化物酶标记的山羊抗兔IgG,室温下孵育1h,ECL显色、暗室曝光,利用Labwork凝胶图像分析系统扫描胶片后得出目的蛋白(NF-κB p65、Col Ⅰ、Col Ⅲ)灰度值,目的蛋白表达水平=NF-κB p65、Col Ⅰ、Col Ⅲ灰度值/β-actin灰度值。
1.5 荧光实时定量PCR使用TRIzol试剂提取肺组织样本中总RNA,并用无RNase水溶解后,每个样本利用紫外分光光度计测定总RNA的A260/280比值,结果均在1.8~2.0之间,达到实验要求。取2 μg总RNA,然后用逆转录试剂盒合成cDNA。引物序列由上海生工生物技术有限公司参照文献[15]合成,Col Ⅰ引物序列:上游5′-CTTGGCTCCTGCTCTACCTC-3′,下游5′-CAACGGCCAGAACTTAAGCCCA-3′,扩增产物长度为114 bp; Col Ⅲ引物序列:上游5′-GGTGCAGCTCAGTTGCTTGAAT-3′,下游5′-GTTCTTGGTGCAGTGTTATGTAATG-3’,扩增产物长度145 bp;β-actin引物序列:上游5′-CTGATCATGTCAAACTTAGCTCAA-3′,下游5′-TACTGTGGTGTGTCG TTCCAGTGG-3′,扩增产物长度为136 bp。取10 μL的cDNA进行PCR循环,条件:94℃预变性3 min,94℃变性40 s,62℃复性40s,60℃延伸60 s,共40个循环。经溶解曲线分析PCR反应产物为单独的双链DNA。以β-actin为内参照,采用ΔΔCt值法定量Col Ⅰ、Col Ⅲ mRNA的表达。
1.6 ELISA取适量右肺组织,进行充分匀浆后,离心并提取上清液,由专人按照ELISA试剂盒提供的方法分别测定上清液IL-17、IL-6、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)含量以及血清PICP、PIIINP浓度。
1.7 统计学处理 采用SPSS 13.0统计软件分析全部资料,实验数据以 ± s表示,采用单因素方差分析比较多组均数以及q检验进行两两之间比较。
± s表示,采用单因素方差分析比较多组均数以及q检验进行两两之间比较。
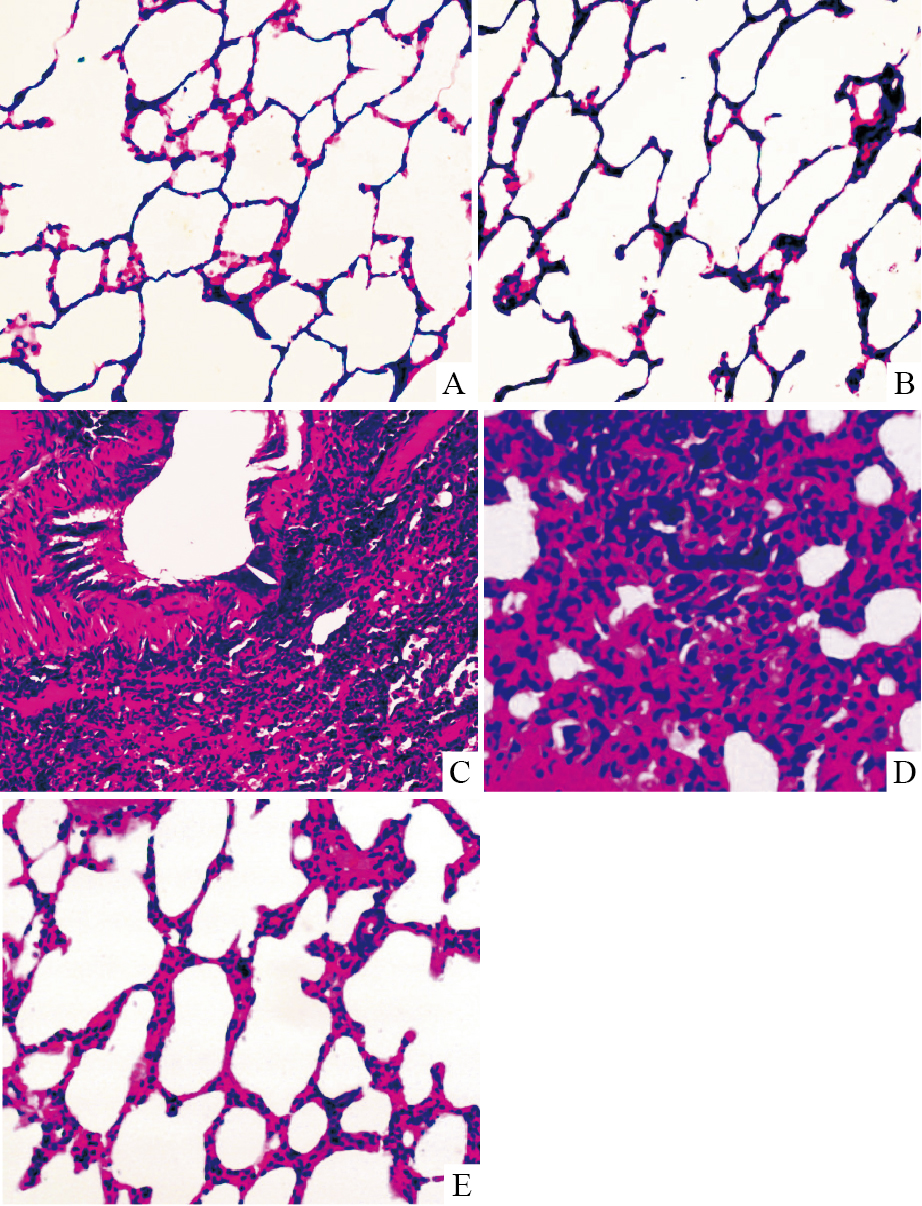
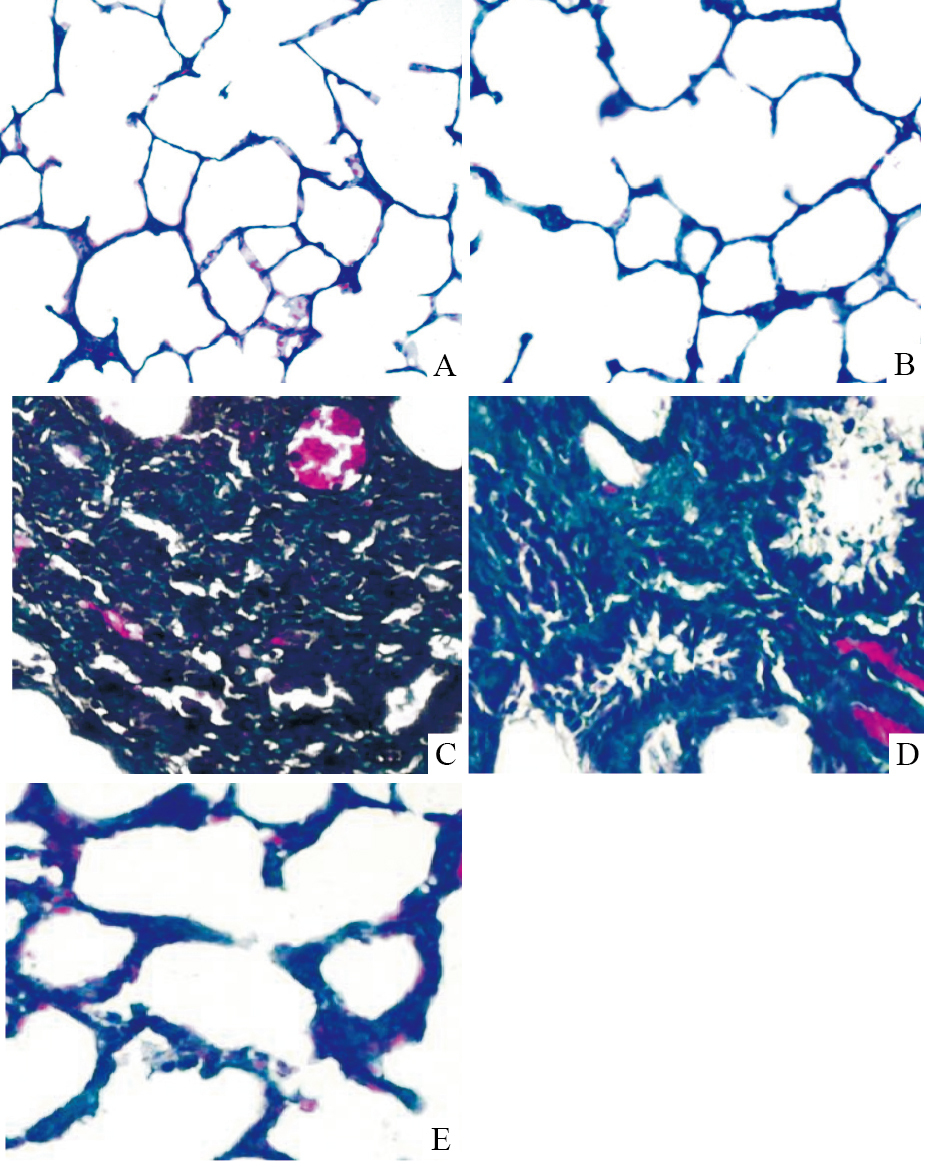
实验过程中,各组大鼠无死亡。正常对照组、假手术组大鼠肺组织无炎症细胞浸润及纤维化发生,肺泡结构清晰;模型组、非特异性IgG组HE染色可见较多的巨噬细胞等炎症细胞浸润,大量成纤维细胞增生,肺泡间隔明显增厚,部分肺泡腔被纤维组织占据,肺泡壁被破坏,Masson染色可见大量蓝色胶原沉积于肺间质内,广泛纤维化形成;IL-17mAb组的上述病理变化明显减轻(Fig1、2)。并且IL-17mAb组肺泡炎与肺纤维化评分较模型组及非特异性IgG组明显降低(P < 0.01),而非特异性IgG组与模型组相比无差异(P>0.05),见Tab1。
|
| Fig 1 Effect of IL-17mAb on inflammation of lung tissues (HE×200) A: Normal control group; B: Sham operated group; C: Model group; D: Non-specific IgG group; E: IL-17 mAb group |
|
| Fig 2 Effect of IL-17mAb on fibrosis of lung tissues (Masson×200) A: Normal control group; B: Sham operated group; C: Model group; D: Non-specific IgG group; E: IL-17 mAb group |
( ± s,n=15) ± s,n=15) |
||
| Group | Alveolitis(Scores) | Pulmonary fibrosis(Scores) |
| Model | 1.51±0.35 | 2.21±0.42 |
| Non-specific IgG | 1.42±0.32 | 2.11±0.39 |
| IL-17 mAb | 0.75±0.14** | 1.38±0.27** |
| **P < 0.01 vs model group or non-specific IgG group | ||
为了探讨IL-17mAb是否通过抑制炎症反应和胶原合成而保护肺纤维化大鼠,应用ELISA测定各组大鼠肺组织IL-17、IL-6、TNF-α含量及血清PICP、PIIINP浓度。结果显示,与正常对照组、假手术组相比,模型组和非特异性IgG组肺组织IL-17、IL-6、TNF-α含量及血清PICP、PIIINP浓度明显增加(P < 0.01),但IL-17 mAb组上述指标较模型组、非特异性IgG组明显减少(P < 0.01)。然而,假手术组与正常对照组以及非特异性IgG组与模型组比较,差异无显著性(P>0.05),见Tab2。
( ± s,n=15) ± s,n=15) |
|||||
| Group | IL-17/μg·L-1 | IL-6/μg·L-1 | TNF-α/μg·L-1 | PICP/μg·L-1 | PIIINP/ng·L-1 |
| Normal control | 43.45±4.68 | 54.27±4.76 | 31.42±3.43 | 7.11±1.48 | 85.73±10.11 |
| Sham operation | 45.13±4.45 | 56.08±4.65 | 32.81±3.65 | 7.23±1.61 | 87.12±10.67 |
| Model | 92.67±9.72** | 128.06±10.21** | 65.39±5.82** | 34.07±5.62** | 182.05±15.06** |
| Non-specific IgG | 88.54±9.65** | 122.74±10.33** | 62.71±5.68** | 31.85±6.15** | 173.83±14.85** |
| IL-17mAb | 51.08±6.33## | 62.15±6.29## | 35.76±3.68## | 16.95±4.23## | 118.87±13.35## |
| **P < 0.01 vs normal control group or sham operated group;##P < 0.01 vs model group or non-specific IgG group | |||||
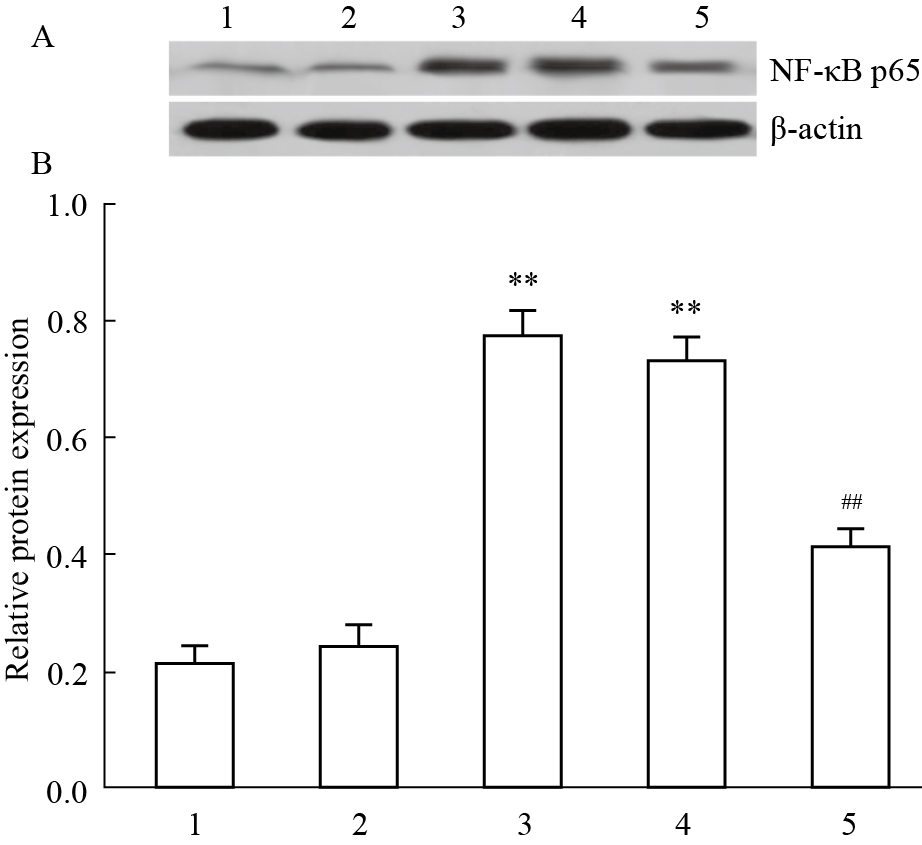
通过Western blot检测各组肺组织中胞核NF-κB p65蛋白的表达,以进一步明确IL-17 mAb抑制肺纤维化大鼠炎症反应的机制。如Fig3所示,模型组、非特异性IgG组胞核NF-κB p65蛋白表达水平较正常对照组、假手术组升高(P < 0.01),尾静脉注射IL-17mAb治疗后,胞核NF-κB p65蛋白表达水平较模型组、非特异性IgG组下降(P < 0.01),但非特异性IgG组与模型组及假手术组与正常对照组之间差异无显著性(P>0.05)。
|
| Fig 3 Expression of NF-κB p65 in the pulmonary tissues nucleus among groups A:Western blot results; B: NF-κB p65 protein expression in the nucleus.1: Normal control group; 2: Sham operated group; 3: Model group; 4: Non-specific IgG group; 5: IL-17 mAb group.**P < 0.01 vs normal control group or sham operated group;##P < 0.01 vs model group or non-specific IgG group |
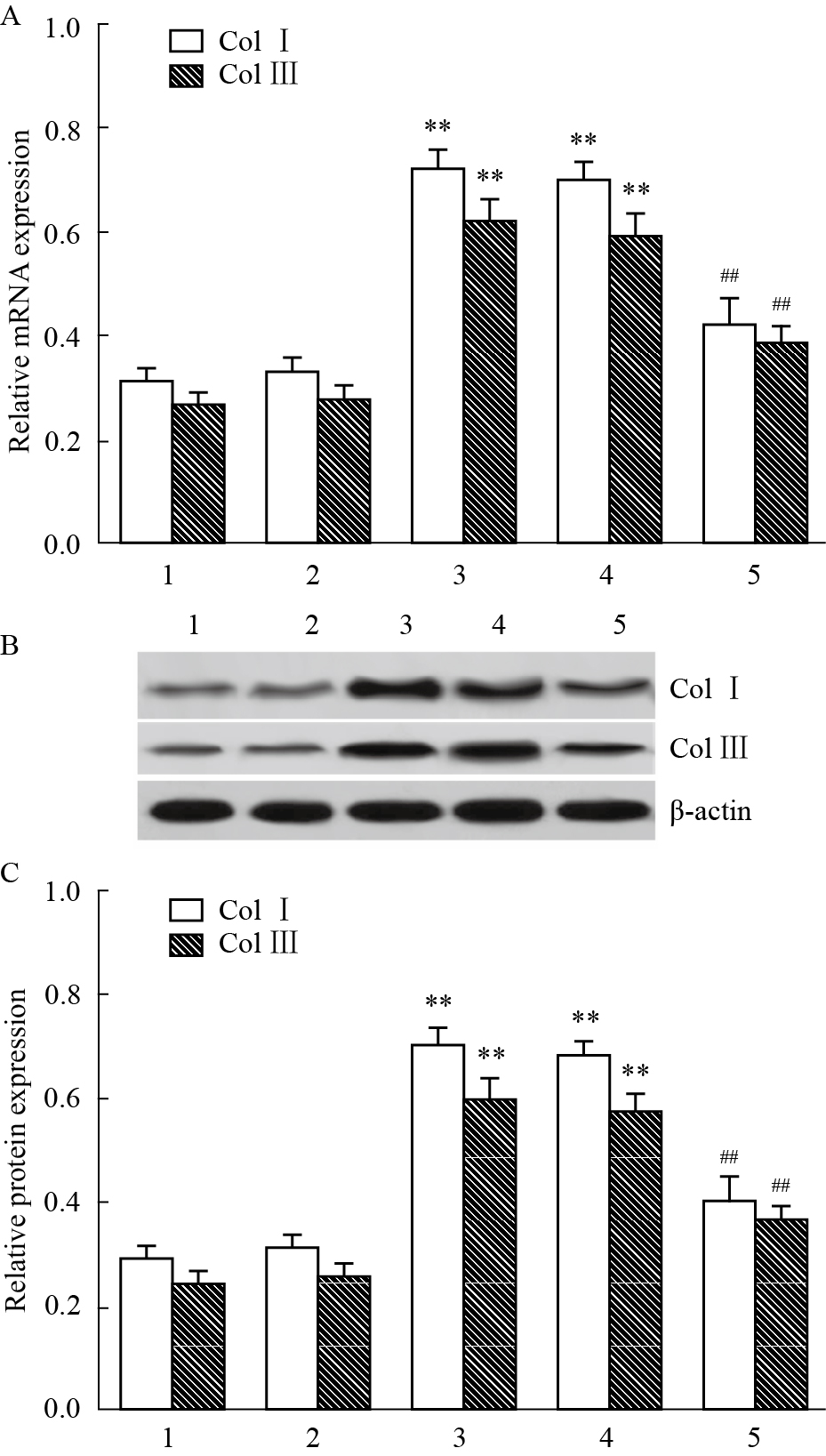
利用荧光实时定量PCR和Western blot检测各组肺组织中ColⅠ、ColⅢ mRNA和蛋白表达,进一步证实IL-17mAb通过抑制胶原蛋白合成而抗肺纤维化。结果表明,与正常对照组、假手术组比较,模型组和非特异性IgG组肺组织Col Ⅰ、Col Ⅲ mRNA和蛋白表达水平明显升高(P < 0.01),经IL-17 mAb治疗后,肺组织Col Ⅰ、Col Ⅲ mRNA和蛋白表达水平较模型组和非特异性IgG组明显下降(P < 0.01),但非特异性IgG组与模型组以及假手术组与正常对照组相比无区别(P>0.05),见Fig4。
|
| Fig 4 Expression of Col Ⅰ and Col Ⅲ in the pulmonary tissues among groups A: Col Ⅰ and Col Ⅲ mRNA expression;B: Western blot results;C: Col Ⅰ and Col Ⅲ protein expression.1: Normal control group; 2: Sham operated group; 3: Model group; 4: Non-specific IgG group; 5: IL-17 mAb group.**P < 0.01 vs normal control group or sham operated group;##P < 0.01 vs model group or non-specific IgG group |
肺纤维化是肺泡不断损伤、成纤维细胞增殖及细胞外基质(extracellular matrix,ECM)大量沉积致使肺组织持续破坏,过度修复,最终大量胶原沉积于肺间质的一类疾病,是肺损伤、免疫反应、炎症反应和纤维生成4个要素的综合结果。目前,临床治疗以激素和免疫抑制剂为主,但效果较差,且不良反应大,限制了其应用[1 ,16] 。过度炎症反应已被证实在肺纤维化形成中起重要作用[17],IL-17 作为一种强效的促炎症因子在多种纤维化疾病中表达增高[18],阻断 IL-17 介导的炎症反应已成为治疗纤维化疾病的新途径。实验发现,中和IL-17活性能预防小鼠肺损伤后肺纤维化的发生[19]。本实验结果显示,行气管切开术后的假手术组与正常对照组肺组织内均无肺泡炎症与纤维化改变,两组无统计学差异,完全可以排除手术损伤本身以及气管内灌注生理盐水的影响。模型组及非特异性IgG组肺组织炎症与纤维化明显,符合肺纤维化模型标准。此外,IL-17 mAb组肺泡炎与肺纤维化评分比模型组和非特异性IgG组明显降低,与文献报道一致[13 ,19],说明 IL-17 mAb 通过特异性抑制IL-17的活性,从而减少巨噬细胞等炎症细胞的趋化聚集,减轻博莱霉素所致急性肺损伤后的炎症反应,抑制肺组织的过度修复,减少胶原纤维沉积,进而改善肺纤维化,提示 IL-17 mAb 对博莱霉素所致大鼠肺纤维化具有良好的治疗效果。然而,非特异性IgG组与模型组相比无区别,进一步证实了非特异性IgG无此阻断作用。
肺损伤后炎症细胞的浸润、活化导致促炎细胞因子的异常表达与肺纤维化的病理生理过程密切相关[9]。Wilson等[8]发现,博莱霉素诱导的肺纤维化是由 IL-17所介导的多种炎症细胞因子共同作用的结果,肺损伤后Th17细胞分泌大量的IL-17可刺激并诱导成纤维细胞、巨噬细胞和上皮细胞产生IL-6、TNF-α、IL-1等多种促炎介质,协同且放大加强TNF-α致炎效应,从而介导炎症反应,最终导致肺纤维化。这表明IL-17、IL-6、TNF-α都是引起肺纤维化的关键促炎介质,抑制这些介质的产生可明显改善肺纤维化[20, 21]。本研究结果显示,经过IL-17 mAb治疗后,大鼠肺组织IL-17、IL-6、TNF-α含量较模型组和非特异性IgG组明显减少,说明抑制促炎介质的分泌是IL-17 mAb抗肺纤维化的主要机制之一。NF-κB是炎症反应中重要的转录调节因子,通常以p50-p65异二聚体的形式与其抑制性蛋白IκB结合形成复合体,呈失活状态存在于静息细胞质里。当细胞外信号刺激细胞后,激活IκB激酶,将IκB磷酸化,随即与NF-κB解离,游离的NF-κB迅速移位入胞核,与核内TNF-α、IL-6、IL-8基因中特异性κB 序列结合,强烈诱导TNF-α、IL-6等释放[22, 23]。研究发现,IL-17能够通过NF-κВ信号通路促进成纤维细胞、上皮细胞分泌IL-6、IL-8以及上调TNF-α表达[24, 25]。故本实验通过Western blot检测肺组织胞核NF-κB p65表达,进一步证实IL-17 mAb是否通过调控NF-κB减少这些促炎介质的表达,结果显示,与模型组和非特异性IgG组比较,IL-17 mAb处理组胞核NF-κB p65表达水平降低,提示IL-17 mAb通过下调NF-κB表达,减少促炎介质的释放,抑制肺组织炎症反应而抗肺纤维化。
Col Ⅰ、Col Ⅲ主要由成纤维细胞及转化后的肌成纤维细胞合成和分泌,是ECM的主要成分,它们过量聚积是肺纤维化的特征性病理改变[26, 27]。当刺激因素作用于肺成纤维细胞后,能促进其合成Col Ⅰ、Col Ⅲ,增加ECM积聚,诱发肺纤维化,而IL-17抗体能减少肺成纤维细胞过度增殖及分泌羟脯氨酸[12]。本研究显示,大鼠经IL-17 mAb处理后,肺组织Col Ⅰ、Col Ⅲ表达水平较模型组和非特异性IgG组明显减少,提示抑制肺成纤维细胞增殖而降低Col Ⅰ、Col Ⅲ合成可能是IL-17 mAb抗肺纤维化的重要机制之一。PICP、PIIINP分别是合成Col Ⅰ、Col Ⅲ的前体多肽,它们随着Col Ⅰ、Col Ⅲ合成的增多而增加,故能良好反映Col Ⅰ、Col Ⅲ的含量,可用于间接评价纤维化程度[15]。本研究检测了大鼠血清PICP、PIIINP浓度,进一步证实IL-17 mAb的这种作用,结果发现各组PICP、PIIINP的浓度变化同Col Ⅰ、Col Ⅲ的变化趋势相同,证明IL-17 mAb通过降低肺组织胶原蛋白合成抑制大鼠肺纤维化。
综上所述,IL-17 mAb对大鼠肺纤维化具有保护作用,其机制可能与下调NF-κB表达,抑制肺组织炎症反应以及减少胶原蛋白合成有关,但其作用机制仍有待更深一步探讨。
(致谢: 本实验在侗医药研究湖南省重点实验室和南华大学附属第一医院临床医学研究所完成,感谢张平教授及各位老师的指导和帮助。)
| [1] | Cottin V, Crestani B, Valeyre D, et al. Diagnosis and management of idiopathic pulmonary fibrosis: French practical guidelines[J]. Eur Respir Rev, 2014, 23(132):193-214. |
| [2] | Wollin L, Wex E, Pautsch A, et al. Mode of action of nintedanib in the treatment of idiopathic pulmonary fibrosis[J]. Eur Respir J, 2015,45(5):1434-45. |
| [3] | Shabgah A G, Fattahi E, Shahneh F Z. Interleukin-17 in human inflammatory diseases[J]. Postepy Dermatol Alergol, 2014, 31(4):256-61. |
| [4] | Jin W, Dong C. IL-17 cytokines in immunity and inflammation[J]. Emerg Microbes Infect, 2013, 2(9):e60. |
| [5] | Xie Y, Li M, Wang X, et al. In vivo delivery of adenoviral vector containing interleukin-17 receptor a reduces cardiac remodeling and improves myocardial function in viral myocarditis leading to dilated cardiomyopathy [J]. PLoS One, 2013, 8(8):e72158. |
| [6] | Amara S, Lopez K, Banan B, et al. Synergistic effect of pro-inflammatory TNF-α and IL-17 in periostin mediated collagen deposition: potential role in liver fibrosis [J]. Mol Immunol, 2015, 64(1):26-35. |
| [7] | Peng X, Xiao Z, Zhang J, et al. IL-17A produced by both γδ T and Th17 cells promotes renal fibrosis via RANTES-mediated leukocyte infiltration after renal obstruction[J]. J Pathol, 2015, 235(1):79-89. |
| [8] | Wilson M S, Madala S K, Ramalingam T R, et al. Bleomycin and IL-1beta-mediated pulmonary fibrosis is IL-17A dependent[J]. J Exp Med,2010, 207(3):535-52. |
| [9] | 刘理静,钱 红,张 平,等. 大黄素对肺纤维化大鼠的保护作用及部分机制研究[J].中国药理学通报,2015,31(2): 266-72. Liu L J, Qian H, Zhang P, et al. Protective effect of emodin on rats with pulmonary fibrosis and its partial mechanisms[J]. Chin Pharmacol Bull, 2015, 31(2): 266-72. |
| [10] | Xiong H Z, Gu J Y, He Z G, et al. Efficacy and safety of secukinumab in the treatment of moderate to severe plaque psoriasis: a meta-analysis of randomized controlled trials[J]. Int J Clin Exp Med, 2015, 8(3):3156-72. |
| [11] | Baeten D, Baraliakos X, Braun J,et al. Anti-interleukin-17A monoclonal antibody secukinumab in treatment of ankylosing spondylitis: a randomised, double-blind, placebo-controlled trial[J]. Lancet,2013, 382(9906):1705-13. |
| [12] | 张 明,黄成亮,王文军,等. IL-17A抗体对成纤维细胞增殖及分泌羟脯氨酸的影响[J]. 免疫学杂志, 2014, 30(11):962-5. Zhang M, Huang C L,Wang W J, et al. The effect of IL-17A antibody on proliferation and hydroxyproline secretion of fibroblasts[J]. Immunol J, 2014, 30(11):962-5. |
| [13] | 刘 虹,李 辙,吕晓希,等. 中和IL-17A活性改善肺纤维化小鼠肺功能[J]. 航天医学与医学工程,2013, 26(1):38-42. Liu H, Li Z,Lyu X X, et al. Neutralization of IL-17A to improve lung functions of pulmonary fibrosis in mice[J]. Space Med Med Eng, 2013, 26(1):38-42. |
| [14] | Szapiel S V, Elson N A, Fulmer J D, et al. Bleomycin-induce dinterstitial pulmonary disease in the nude, athymic mouse[J]. Am Rev Respir Dis, 1979, 120(4): 893-9. |
| [15] | 刘理静,于小华,张 平. 白藜芦醇通过TGF-β1/ADAMTS-1信号通路抑制肺纤维化[J]. 中国药理学通报, 2013, 29(3): 425-31Liu L J, Yu X H, Zhang P. Resveratrol inhibits pulmonary fibrosis through TGF-β1/ADAMTS-1 signaling pathway[J]. Chin Pharmacol Bull, 2013, 29(3): 425-31. |
| [16] | 郭 刚,王久存,史 颖,等. 参麦开肺散对NIH/3T3成纤维细胞增殖及胶原合成的影响[J].解放军医药杂志, 2015, 27(2):24-8.Guo G, Wang J C, Shi Y, et al. Effect of Shenmaikaifei powder on the proliferation and collagen synthesis of NIH/3T3 fibroblasts[J]. Med Pharm J Chin PLA,2015, 27(2):24-8. |
| [17] | Lee A S, Mira-Avendano I, Ryu J H, et al. The burden of idiopathic pulmonary fibrosis: an unmet public health need[J]. Respir Med, 2014, 108(7):955-67. |
| [18] | Tan Z, Qian X, Jiang R,et al. IL-17A plays a critical role in the pathogenesis of liver fibrosis through hepatic stellate cell activation [J]. J Immunol, 2013, 191(4):1835-44. |
| [19] | 米 粟,李 辙,刘 虹,等.阻断 IL-17A 活化 p50 NF-κB 抑制小鼠肺损伤引起的肺纤维化[J]. 药学学报, 2012, 47(6): 739-44.Mi S, Li Z, Liu H, et al. Blocking IL-17A protects against lung injury-induced pulmonary fibrosis through promoting the activation of p50 NF-κB[J]. Acta Pharm Sin, 2012, 47(6): 739-44. |
| [20] | You H, Wei L, Sun W L, et al. The green tea extract epigallocatechin-3-gallate inhibits irradiation-induced pulmonary fibrosis in adult rats[J]. Int J Mol Med, 2014, 34(1):92-102. |
| [21] | 黄成亮, 李艳艳, 范贤明, 等. IL-17A 促进博来霉素诱导的肺纤维化大鼠肺组织的炎症形成[J]. 细胞与分子免疫学杂志, 2014, 30(4):366-70.Huang C L, Li Y Y, Fan X M, et al. IL-17A promotes pulmonary inflammation in rats with pulmonary fibrosis induced by bleomycin[J]. Chin J Cell Mol Immunol, 2014, 30(4):366-70. |
| [22] | 钱 红,刘理静. IL-17单克隆抗体对病毒性心肌炎小鼠的保护作用[J]. 细胞与分子免疫学杂志, 2014,30(5):509-12. Qian H, Liu L J. Protective effect and mechanism of IL-17 monoclonal antibody on mice with viral myocarditis[J].Chin J Cell Mol Immunol,2014,30(5):509-12. |
| [23] | Metelev V G, Kubareva E A, Oretskaya T S, et al. Regulation of activity of transcription factor NF-κB by synthetic oligonucleotides[J]. Biochemistry (Mosc), 2013, 78(8):867-78. |
| [24] | 郭江燕,高梓珊,姜姝姝,等.IL-17和NF-κB通路与类风湿性关节炎的相关性研究 [J]. 长春中医药大学学报,2015, 31(1):192-4. Guo J Y, Gao Z S, Jiang S S, et al. Study progress of IL-17 and NF-kappa B pathway in RA[J]. J Changchun Univ Chin Med,2015,31(1):192-4. |
| [25] | Gu C, Wu L, Li X. IL-17 family: cytokines, receptors and signaling [J]. Cytokine, 2013, 64(2):477-85. |
| [26] | Guo T, Lok K Y, Yu C, et al. Lung fibrosis: drug screening and disease biomarker identification with a lung slice culture model and subtracted cDNA library[J]. Altern Lab Anim, 2014, 42(4):235-43. |
| [27] | 刘理静, 钱 红. 上调miR-21表达促进肺成纤维细胞增殖和胶原蛋白合成[J]. 细胞与分子免疫学杂志, 2015, 31(7):918-22.Liu L J, Qian H. Up-regulation of miR-21 promotes cell proliferation and collagen synthesis in pulmonary fibroblasts[J]. Chin J Cell Mol Immunol, 2015, 31(7):918-22. |

